Ammine
Ammine
Sintesi delle ammine
Reazioni delle ammine
Alcalodi
Ammine
Composti organici dell’azoto N
Sono classificate come primarie, secondarie,
tertiarie
CH3
CH3
CH3—NH2 CH3—NH CH3—N — CH3
1°
2°
3°
Nomenclatura
IUPAC amminoalcano
CH3CH2NH2
amminoetano
(etilammina)
NH2
Comune alchilammina
CH3—NH —CH3
N-metilamminometano
(dimetilammina)
NH 2
|
CH3CHCH3
2-amminopropano
(isopropilammina)
anilina
Ammine eterocicliche
Struttura delle ammine
L’atomo di azoto è ibridato sp3
I tre gruppi ed il doppietto non condiviso danno luogo ad una
geometria tetraedrica.
Se si considerano solo i tre gruppi la forma che l’ammina assume è
trigonale piramidale.
Una parziale carica negativa è nella regione del doppietto non
condiviso.
Non è possibile risolvere le ammine enantiomeriche che sono chirali
all’azoto perchè si interconvertono rapidamente.
I Sali di ammonio quaternari possono essere risolti negli
enantiomeri.
Proprietà fisiche delle ammine
Le ammine primarie e secondarie possono
formare legami idrogeno fra loro e con
l’acqua.
Le ammine terziarie non possono formare
legami idrogeno fra loro ma solo con
l’acqua.
A peso molecolare paragonabile le ammine
terziarie hanno punti di ebollizione più bassi
delle ammine primarie e secondarie
Preparatione delle Ammine
Reazioni di riduzione
Trasposizione
Reazioni di sostituzione nucleofila
– Preparazione di ammine primarie, secondarie
e terziarie per riduzione di nitrili, ossime ed
ammidi.
La riduzione di nitrili ed ossime porta ad ammine
primarie mentre quella delle ammidi può dare
ammine primarie, secondarie e terziarie.
Preparazione di ammine aromatiche per
riduzione di nitrocomposti.
Preparazione delle ammine primarie per
trasposizione di Curtius
Preparazione delle ammine per
alchilazione dell’amminiaca.
Il metodo è limitato perchè avviene alchilazione multipla.
Un eccesso di ammoniaca minimizza l’alchilazione multipla.
Sintesi di Gabriel delle ammine primarie
•Il primo stadio consiste nell’alchilazione della
potassio ftalimmide
• La reazione della N-alchilftalimmide con idrazina
in etanolo bollente porta all’ammina
Reazione delle Ammine
Reazione come basi: formazione di sali
Formazione di ammidi
Alchilazione
Reazione con acido nitroso
Agiscono come basi deboli in acqua
CH3NH2 + H2O
CH3NH3+ + OH–
idrossido di
metilammonio
La neutralizzazione con acidi porta al sale di ammonio
CH3NH2 + HCl
CH3NH3+ Cl–
cloruro di metilammonio
La basicità relativa delle ammine può essere
paragonata in termini di pKa dei rispettivi acidi
coniugati. Maggiore è il pKa, più basica è l’ammina
–
Le ammine primarie sono più basiche
dell’ammoniaca in quanto il gruppo alchilico
elettrodonatore stabilizza il catione alchilammonio.
In fase gassosa la basicità delle metilammine
aumenta passando dall’ammina primaria alla
terziaria in quanto aumenta la stabilizzazione dello
ione ammonio.
In soluzione acquosa la trimetillammina è meno
basica della dimetil- e metilammina.
Lo ione alchilammonio in acqua è solvatato e stabilizzato dai
legami idrogeno dei suoi idrogeni con l’acqua. Lo ione
trimetilammonio ha un solo idrogeno per formare legame con
l’acqua e pertanto è meno solvatato e quindi stabilizzato
rispetto al dimetilammonio.
Basicità delle arilammine
– Le arilammine sono meno basiche delle corrispondenti
cicloesilammine.
– La coppia di elettroni non condivisa dell’azoto è
delocalizzata alle posizioni orto e para dell’anello ed è
quindi meno disponibile per la protonazione.
La protonazione dell’anilina è anche sfavorita perchè lo ione
anilinio nonè così stabilizzato per risonanza come l’anilina.
DHo per la protonazione dell’anilina è maggiore del DHo per la
protonazione della cicloesilammina.
Basicità delle ammine eterocicliche
Il doppietto elettronico conferisce carattere nucleofilo
O
RCCl + R'2NH + HO–
O
RCNR'2 + H2O
+ Cl–
I cloruri acilici reagiscono con le ammine
primarie e secondarie per dare le ammidi
Reazione delle ammine con acido nitroso
RNH
2
ArNH
2
HONO
o
0 C
HONO
o
0 C
R 2NH
or
ArNHR
+
R N N
alkyl diazonium salt
unstable
+
Ar N N
Nu
+ R
N2
+ Ar Nu
aryl diazonium salt
stable at low temp.
R
HONO
o
0 C
Ar
R
N
R
N
or
N
N
O
O
Nitrosamines
NR 2
HONO
o
0 C
N
O
+
N2
NR 2
Aromatic C-nitroso compound
•Le ammine primarie alifatiche subiscono
diazotazione con acido nitroso
•Il sale di diazonio è instabile e si decompone
per dare un carbocatione
•Il carbocatione reagisce per dare alcheni,
alcooli e alogenuri.
La reazione delle arilammine primarie con acido
nitroso porta a sali di arendiazonio relativamente
stabili. La reazione avviene attraverso la formazione
di N-nitrosoammine intermedie.
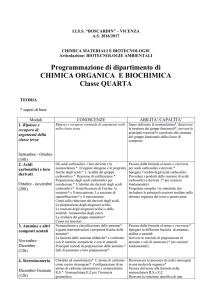
I Sali di arildiazonio possono reagire con diversi nucleofili
HO
N N
an azo dye
OH
I
KI
H 2O
Phenol
heat
+
CN
N N
Cl
CuCN
CuCl
CuBr
H 3 PO 2
1. HBF 4
2. heat
Br
H
F
Alcaloidi
Composti fisiologicamente attivi contenenti
azoto
Ottenuti da piante e funghi
Usati come anestetici, antidepressivi,
stimolanti
NICOTINA
ATROPINA
COCAINA
MORFINA
CODEINA
EROINA
SEROTONINA
CHININA
PAPAVERINA
A. LISERGICO
LSD
CAFFEINA
TEOBROMINA
TEOFILLINA
Analisi spettroscopica
Spettri infrarossi
– Le ammine primarie e secondarie hanno vibrazioni
N-H stretching nella regione 3300-3555 cm -1
Spettri 1H NMR
Le ammine primarie e secondarie hanno larghi
picchi N-H fra 0.5-5 ppm
I protoni N-H scambiano con D2O scomparendo
dallo spettro
I protoni sui carboni adiacenti all’azoto sono fra
2.2-2.9 ppm
Spettri 13C NMR
– I carbonsi legati all’azoto mostrano segnali a campi bassi
fra d 20 e 70
– L’effetto deschermante dell’azoto diminuisce con la
distanza