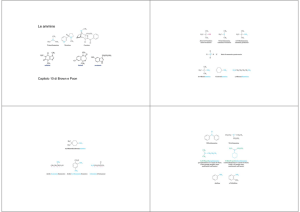
Ammine
p.e
Nelle ammine gli orbitali dell’azoto sono ibridati sp3. Il lone pair che abita
uno dei quattro orbitali conferisce carattere basico alle ammine.
I gruppi alchilici legati all’azoto, per effetto induttivo positivo, aumentano la
densità di carica nell’orbitale atomico.
H3C
N
H
CH3
Se i gruppi legati all’azoto sono diversi tra loro
enantiomeri?
i due enantiomeri teorici si interconvertono molto rapidamente a causa
dell'inversione piramidale ed i racemi non sono risolvibili.
C2H5
C2H5
H N
H
H5C2
N
C2H5
H5C2
H
N
C2H5
Carattere nucleofilo dell’azoto amminico
La nucleofilia dell’azoto del gruppo funzionale delle ammine è influenzata dalla
natura dei gruppi alchilici o aromatici legati all’azoto. Nelle ammine alifatiche,
aumentando il numero dei gruppi alchilici aumenta la densità elettronica
nell’orbitale atomico dell’azoto e quindi il carattere nucleofilo.
NH2
La presenza di un radicale aromatico, a causa della delocalizzazione
dei due elettroni dell’azoto nell’orbitale p dell’anello, rende le ammine
meno nucleofile.
Kb = 4.4 • 10-4
N
CH3
H
CH 3
Kb = 4.7 • 10-4
N
H
H+
H
H
CH3
Kb = 5.4 • 10-5
N
H 3C
C H3
H+
H+
H
H
H
N
N
N
CH3
CH3
H
H
CH3
H3 C
CH3
CH 3
CH3
• Gli acidi coniugati delle ammine alchiliche semplici hanno
pKa 9.5-11, le loro soluzioni pH 11-12.
N
H
Kb = 4,2 • 10-10
H
benzenammina
N
H
Kb = 5,5 • 10-4
H
cicloesanammina
Riconoscimento delle ammine
1. Ricerca del carattere basico
2. Saggio di Hinsberg
3. Saggio di diazotazione e copulazione
4. Formazione di senfoli
5. Metodo dell’anidride 3-nitroftalica
6. Saggio con acetone e nitroprussiato sodico
7. Saggio con acetaldeide e nitroprussiato sodico
8. Formazione di composti colorati con la lignina
9. Trattamento con acido nitroso
10. Formazione di carbilammine
Riconoscimento delle ammine
Ricerca del carattere basico
A. Una goccia della sostanza in esame viene posta su un cartina al rosso congo
preventivamente azzurrata con HCl 0,1 N e si verifica l’arrossamento della
cartina.
B. Una soluzione di metilarancio resa acida per aggiunta di HCl 2N reagisce con la
sostanza in esame dando luogo al viraggio dell’indicatore che passa dal rosso
al giallo.
Riconoscimento delle ammine
2. Saggio di Hinsberg
Il saggio permette di differenziare tra loro le ammine 1°, 2° e 3°. Le prime due
reagiscono con il cloruro di tosile in presenza di NaOH (reazione di Schotten Baumann) per dare le p-toluensolfonammidi sostituite, l’ammina 3° non reagisce.
Solfonammide
acida
Solfonammide
neutra
Riconoscimento delle ammine
2. Saggio di Hinsberg
Separazione della miscela costituita da ammine 1°, 2° e 3°.
Questa miscela viene trattata con cloruro di tosile in ambiente alcalino e
estratta con etere: si ottengono due fasi (alcalina ed eterea).
Nella fase alcalina rimane la solfonammide (1°) e da essa si può
riottenere l’ammina 1° per idrolisi.
Nella fase eterea sono contenute la solfonammide 2° e l’ammina 3°;
quest’ultima a contatto con una soluzione di acidi passa nella fase
acquosa acida, da cui per successiva alcalinizzazione si ottiene
nuovamente l’ammina libera.
Nella fase eterea rimane la solfonammide (2°) che, per evaporazione del
solvente e successiva idrolisi, restituisce l’ammina 2°.
Riconoscimento delle ammine
3. Saggio di diazotazione e copulazione
E’ un saggio specifico per le ammine 1° aromatiche ed è basato sulla formazione
del sale di diazonio ad opera di NaNO2 in ambiente acido (H2SO4 conc.) tra 0 e 5 °C e
sulla successiva copulazione con β-naftolo in ambiente basico (NaOH) con formazione
del colorante azoico rosso.
Reazione di diazotazione
Reazione di copulazione
NaOH
Riconoscimento delle ammine
4. Formazione di senfoli
E’ un saggio specifico per le ammine 1° alifatiche che reagiscono con CS2
formando un ditiocarbammato, in presenza di AgNO3 si trasforma in sale
d’argento. Due molecole di sale perdono poi H2S e Ag2S (pp nero) dando luogo
alla formazione dell’isosolfocianato o senfolo, riconoscibile per l’odore di senape.
S
RCH2NH2 + CS2
AgNO3
R-H2C-HN
Sditiocarbammato
+ H3N+-CH2-R
S
+ NO3- + H3N+-CH2-R
R-H2C-HN
SAg
S
2
R-H2C-HN
SAg
2 R-CH2-N=C=S + Ag2S + H2S
isosolfocianato
o senfolo
nero
Riconoscimento delle ammine
5. Metodo dell’anidride 3-nitroftalica
Consente di separare tra loro le ammine 1°, 2° e 3°. Le ammine 1° e 2°
reagiscono in ambiente anidro, a caldo in solvente inerte, con anidride 3-nitroftalica
dando i corrispondenti acidi ftalammici, le ammine 3° non reagiscono.
O
O
CONHR
R-NH2 +
COOH
150 °C
O
COOH
O
O 2N
NR
-H2O
CONHR
NO2
NO2
O
NO2
3-nitroftalimmide
O
O
O
OH
NRR'
R-NH- R' +
O
+
NRR'
OH
NO2
O
NO2
O
O2N
O
Riconoscimento delle ammine
5. Metodo dell’anidride 3-Nitroftalica
Separazione di una miscela costituita da ammine 1°, 2° e 3°.
Trattando con HCl il prodotto, ottenuto dalla reazione precedente, esso scioglie solo
l’ammina 3°.
Nello strato acido acquoso passerà quindi tutta l’ammina 3° mentre il residuo
contenente i due acidi ftalammici viene riscaldato a 150 °C per ottenere la 3nitroftalimmide N-alchil sostituita.
A questo punto si tratta il residuo con NaHCO3 che scioglie solo l’acido ftalammico
proveniente dall’ammina 2°, mentre la ftalimmide proveniente dall’ammina 1°
rimane nel residuo.
Riconoscimento delle ammine
6. Saggio con acetone e nitroprussiato sodico
Na2[Fe(CN)5NO] o pentacianonitrosilferrato (III)
Saggio specifico per le ammine alifatiche 1° e 2°
7. Saggio con acetaldeide e nitroprussiato sodico
(in ambiente basico per NaHCO3)
Saggio specifico per le ammine alifatiche 1° e 2°
Trattando la soluzione di ammina con sodio nitroprussiato e acetaldeide (Saggio di
Simon) o acetone (Saggio di Rimini) si sviluppa una colorazione specifica.
A 1 mL di nitroprussiato sodico (0.13 M in MeOH/acqua 1:1) si aggiunge 1 mL di
acqua, 0.2 mL di acetone e circa 30 mg di ammina (primaria o secondaria).
Acetaldeide
Acetone
rosso-bruna per ammine primarie e blu per secondarie
rosso intenso per ammine primarie e secondarie
Riconoscimento delle ammine
8. Formazione di composti colorati con la lignina
Saggio specifico per le ammine 1° e 2°
Solubilizzate in C2H5OH e poste sulla carta di giornale bagnata
di HCl 6N danno una colorazione giallo-arancione.
Ammine 1° e 2° aromatiche: la colorazione compare
immediatamente.
Ammine 1° e 2° alifatiche: la colorazione compare solo
dopo riscaldamento.
Ammine 3°: non reagiscono.
Riconoscimento delle ammine
9. Trattamento con acido nitroso
E’ il metodo che permette di stabilire se l’ammina è alifatica o aromatica se
è 1° , 2° o 3°.
A. Ammine 1° alifatiche
Le ammine 1° reagiscono con HNO2 a freddo con formazione di alcool 1° e
sviluppo di N2.
RCH2NH2 + HNO2 -> RCH2OH + N2á + H2O
B. Ammine 1° aromatiche
reagendo a freddo con HNO2 non sviluppano azoto ma si formano i sali di
diazonio che possono essere messi in evidenza mediante reazione di
copulazione.
ArNH2 + HNO2 -> Ar-N≡N+ + H2O
A temperature elevate, invece, si ottiene il fenolo corrispondente.
Nel primo stadio della reazione (protonazione dell’acido
nitroso) si forma l’elettrofilo (il catione nitrosile)
HO N
O
H+
H
O N
H
O
N
O
N
catione nitrosile
O
Nel secondo stadio, il nucleofilo catione nitrosile attacca l’ammina. Per
eliminazione di una molecola di acqua si forma uno ione diazonio instabile
che, in ambiente acquoso, elimina azoto molecolare e si converte nel
corrispondente alcool.
Ammina primaria alifatica
H
R N
O
N
H
O
R N N
H
H
H
O
R N N
H
O
H
H
R N N
ione diazonio
H2O
H+
R OH
N2
Le ammine aromatiche primarie reagiscono con l’acido nitroso in ambiente
acido per dare sali di diazonio, stabili a bassa temperatura (tra 0 e 5° C).
NH2
NaNO2 (H+)
in acqua a 0°C
N
N
N
N
Riconoscimento delle ammine
9. Trattamento con acido nitroso
C. Ammine 2° alifatiche e aromatiche
Le ammine 2° reagiscono con HNO2 per dare gli N-nitrosoderivati, poco solubili
in H2O.
RR’NH + HO-N=O -> RR’N-N=O + H2O
D. Ammine 3° alifatiche non reagiscono.
E. Ammine 3° aromatiche
Tali ammine aventi la posizione para libera reagiscono con HNO2 formando un
p-nitroso-derivato che per trattamento con NaOH dà una colorazione verde.
Ar-N(CH3)2 + O=N-OH
HCl
ON
+
NH(CH3)2 + Cl- + H2O
NaOH
verde
ON
N(CH3)2
+ NaCl +
H2O
Esempio: Solfatiazolo
saggio del colorante azoico
Riconoscimento delle ammine
10. Formazione di carbilammine
Le ammine 1° alifatiche e aromatiche reagiscono con il CHCl3 in ambiente
alcalino (KOH) dando le carbilammine (isonitrile) riconoscibili per l’odore
tipico tra l’agliaceo e pesce marcio.
Ar
NH2
+ CHCl3 + 3KOH
Ar N
C
+ 3KCl + 3H2O
Meccanismo con formazione di diclorocarbene
Cl
Cl
HO:
H C
H
R
Cl
CCl2
N:
H
C
Cl
H
R
N+
H
Cl
Cl
:CCl2 + Cl-
elettrofilo
Cl
C-
R
Cl
N+
H
CCl
R
N
C
Derivati cristallini delle ammine
1.
2.
3.
4.
5.
6.
7.
8.
Derivati delle ammine primarie e secondarie
Benzammidi
3,5-Dinitrobenzammidi, p-Nitrobenzammidi
Acetammidi
Benzensolfonnamidi e p-Toluensolfonammidi
Ftalimmidi e 3-Nitroftalimmidi
N-Formilderivati
Uree e tiouree sostituite
2,4- Dinitrofenilderivati
Derivati cristallini delle ammine
1. Benzammidi
Reazione di Shotten-Baumann (a freddo con cloruro di benzoile in eccesso)
Ph-CO-Cl + RNH2
Ph-CO-NHR
2. 3,5-Dinitrobenzammidi, p-Nitrobenzammidi
In questo caso la reazione si conduce a caldo con i relativi cloruri degli acidi.
3. Acetammidi
(CH3CO)2O + RNH2 -> CH3CONHR + CH3COOH
4. Benzensolfonnamidi e p-Toluensolfonammidi
R’-C6H4-SO2-Cl + RNH2 → [R’-C6H4-SO2-+NH2R] → R’-C6H4-SO2-NHR
5. Ftalimmidi e 3-Nitroftalimmidi
Reazione analoghe a quelle di riconoscimento
Derivati cristallini delle ammine
6. N-Formilderivati
HCOOH + RNH2 → HCOO- + RNH3+ → HCOHNR + H2O
7. Uree e tiouree sostituite
OAr-N=C=O + R-NH2
Ar-N
Ar = -Ph (fenilisocianato)
Ar = α-naftile (α naftil isocianato)
+
Ar-N-
NH2R
O
+
O
Ar-HN
NH2R
NHR
urea sostituita
8. 2,4- Dinitrofenilderivati
Cl
NO2
Cl +NH2R
NO2
RH 2N+
R-NH2 +
NO2
NO2
NO2
NO2 + Cl-
Derivati cristallini delle ammine
Derivati delle ammine terziarie (solo sali!)
R3NH+X-
1. Cloridrati e Bromidrati
O 2N
2. Picrati
NO2
OH · NR3
3. Stifnati
NO2
OH
4. 3,5-Dinitrobenzoati
O2N
NO2
5. Sali ammonici quaternari
OH · NR3
7. Picrolonati
H3C
H3C
N
N
OH
NO2
NO2
NR3
O2N
NO2
COOH · NR3