1. La f.e.m o forza elettromotrice è indice della tendenza della reazione ad avvenire fino al raggiungimento
dell’equilibrio, più elevata è la f.e.m e:
a. più il sistema è vicino dall’equilibrio
b. più il sistema è vicino al punto equivalente
c. più distante è il sistema dall’equilibrio
2. Quanti elettroni sono scambiati nella reazione redox: 2Fe + O2(g) + 4H3O+ = 2Fe2+ + 6H2O
a. 2
b. 3
c. 4
3. Una certa coppia redox si ossida se:
a. il suo E0 è negativo
b. il suo E0 è positivo
c. il suo E0 è minore di quello della coppia redox con cui reagisce
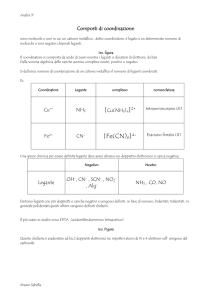
4. Quale relazione è solitamente verificata nel caso delle reazioni di complessamento che portano alla
formazione di complessi del tipo ML, ML2, ..., MLn?
a. K1 < K2 < ... < Kn
b. 1 < 2 < ... < n
c. 1 > 2 > ... > n
5. Il valore di K ', costante condizionale di complessamento, è sempre...
a. >> K
b. << K
c. K
6. Quale delle seguenti affermazioni riguardanti le reazioni di complessamento sono solitamente vere?
a. se L è una base di Lewis, non può essere anche una base di Brønsted
b. leganti polidentati hanno un’elevata cinetica di complessamento
c. i complessi poli-dentati sono più-stabili dei mono-dentati
7. nel caso di una pila al catodo avviene:
a. il processo di riduzione
b. il processo di ossidazione
c. non si può dire, dipende dalle coppie redox in questione
8. nel caso di una pila il flusso di elettroni fluisce
a. dal catodo verso l’anodo
b. dall’anodo verso il catodo
c. non si può dire a priori dipende sempre e comunque dalle coppie redox presenti
9. nel caso di una pila la corrente fluisce
d. dal catodo verso l’anodo
e. dall’anodo verso il catodo
f. non si può dire a priori dipende sempre e comunque dalle coppie redox presenti
10. le reazioni redox sono caratterizzate perchè
a. vengono scambiati protoni come nelle reazioni acido base
b. vengono scambiati elettroni come nelle reazioni acido base
a. esiste almeno una specie che si ossida ed una che si riduce
11. La costante di equilibrio rappresenta:
a. Il decorso termodinamico di una reazione chimica
b. Il decorso termodinamico di una reazione di complessamento
1
c. La velocità di formazione di un complesso metallico
12. L’energia libera di reazione rappresenta
a. L’energia dello stato di transizione, se piccola la reazione è favorita
b. La differenza energetica tra gli stati fondamentali di reagenti e prodotti
c. La differenza energetica tra gli stati fondamentali di reagenti e prodotti, se piccola la reazione è
favorita
13. l'EDTA è un legante polidentato:
a. che dà complessi a geometria di coordinazione bipiramidale a base quadrata
b. con 4 gruppi azotati in grado di coordinare un centro metallico
c. In grado di legare un centro metallico con due gruppi azoto
14. Il (NH3)2Cl2Pt è un complesso utilizzato come agente chemioterapico che:
a. Esiste in due isomeri cis e trans entrambi attivi nella terapia antitumorale
b. assume geometria tetraedrica
c. assume geometria quadrato planare
15. l’acido ossalico è un legante in grado di complessare in maniera stabile molti centri metallici perché:
a. è un legante tridentato
b. è un agente chelante
c. è un agente sequestrante
16. Nei complessi metallici, la formazione dei legami metallo-legante è dovuta a :
a. legame dativo da parte del legante che mette a disposizione un orbitale libero
b. legame dativo da parte del legante che mette a disposizione un doppietto elettronico
c. Legame dativo da parte del metallo che mette a disposizione gli elettroni di un orbitale occupato
17. Dal punto di vista formale gli equilibri di complessamente sono equilibri acido base perché:
a. I centri metallici sono considerati acidi di Lewis in grado di accettare un doppietto elettronico
b. I centri metallici sono considerati basi di Lewis in grado di cedere un doppietto elettronico
c. I centri metallici sono considerati acidi di Lewis in grado di cedere un doppietto elettronico
18. Negli isomeri geometrici di complessi a geometria bipiramidale a base quadrata l’isomero facciale è
caratterizzato da:
a. 4 leganti L in posizione equatoriale, 2 leganti L’ in posizione assiale
b. 2 leganti L in posizione equatoriale and 1 assiale, 2 leganti L’ in posizione equatoriale ed uno
assiale
c. 3 leganti L in posizione equatoriale, 2 leganti L’ in posizione assiale ed uno equatoriale
19. La costante di complessamente globale di un complesso del tipo ML2:
a. È la somma delle costanti di formazione parziali dei singoli stadi
b. È il prodotto delle costanti di formazione parziali dei singoli stadi
c. È il rapporto delle costanti di formazione parziali dei singoli stadi
20. L’artrite reumatoide viene curata con farmaci a base di:
a. Cromo picolinato che stimola l’assorbimento del glucosio da parte delle cellule
b. Con l’aurotioglucosio (solganol) a base di complessi di oro a geometria lineare
c. Con complessi di Tc(V) complessato con mercaptoacetiltriglicina .
21. la frazione di legante attiva ad un determinato valore di pH definisce:
a. la concentrazione di legante complessivamente presente in soluzione
b. la concentrazione di legante presente come forma complessata e/o libera
c. la concentrazione di legante presente come forma protonata e/o libera
22. Tanto maggiore è la frazione di legante presente in forma "attiva" ( )
2
a. tanto più la reazione di complessamento è spostata verso i prodotti.
b. tanto più la reazione di complessamento è spostata verso i reagenti.
c. tanto meno la reazione di complessamento è spostata verso i prodotti
23. se la costante condizionale K' per un complesso ML assume un valore 106 vuol dire:
a. ho la formazione di un complesso stabile
b. non ho la formazione di nessun complesso
c. è possibile che il complesso si formi, ma la reazione non è molto favorita
24. la costante condizionale K' per un complesso ML:
a. è il rapporto tra KML ed L (frazione di legante attiva)
b. è il prodotto tra KML ed M (frazione di legante attiva)
c. è il prodotto tra KML ed [H+]
25. Poiché per i leganti basici L cresce al crescere del pH:
a. il pH basico favorisce la reazione di complessamento
b. il pH basico sfavorisce la reazione di complessamento
c. non si può dire, dipende dalla costante formale
sia nullo a pH acidi vuol dire:
26. il fatto che
a. che la reazione di complessamento non avviene
b. che la reazione di complessamento avviene
c. non si può dire, dipende da quanto è grande la
27. In generale per un complesso
a. minore è
e tanto minore potrà essere il pH a cui la mia reazione è spostata a destra
e tanto maggiore potrà essere il pH a cui la mia reazione è spostata a destra
b. maggiore è
e tanto minore potrà essere il pH a cui la mia reazione è spostata a destra
c. maggiore è
28. Per un catione metallico il pH acido "limite" è :
a. il valore sotto al quale la reazione tra ione metallico e legante non avviene efficacemente
b. il valore sopra il quale la reazione tra ione metallico e legante non avviene efficacemente
c. il valore sotto al quale la reazione tra ione metallico e legante avviene efficacemente
29. Gli agenti terapeutici contenenti metalli usati in medicina devono avere:
a. leganti molto stabili e difficilmente spostabili
b. leganti poco molto stabili e facilmente spostabili
c. leganti non molto stabili e facilmente spostabili
30. Le tetracicline sono:
a. un vasto gruppo di farmaci chemioterapici
b. un vasto gruppo di farmaci antibatterici
c. un vasto gruppo di farmaci antiacidi.
31. Lo ione ossalato dà un complesso con il ferro:
a. monodentato
b. bidentato
c. tridentato
32. Il cis-platino è un complesso del platino ed ha geometria:
a. tetraedrica
b. planare quadrata
c. trigonale planare
3
33. Nella teoria del campo cristallino:
a. Gli orbitale a minore energia sono quelli che puntano verso gli assi dei leganti
b. Gli orbitale a minore energia sono quelli che evitano di porsi sugli assi dei leganti
c. Non permette di descrivere le proprietà magnetiche e spettroscopiche dei complessi
34. Per quale ragione l'EDTA non può essere conservato in recipienti di vetro?
a. perché dà reazione a-cido-base col vetro
b. perché dà reazione di precipitazione col vetro
c. perché dà reazione di complessamento col vetro
35. In generale tanto maggiore è la costante di formazione
di un complesso e:
a. tanto maggiore dovrà essere il pH a cui potrò effettuare la titolazione
b. tanto minore potrà essere il pH a cui potrò effettuare la titolazione
c. non si può dire, dipende dalla costante formale
36. la maggiore stabilità di complessi chelati è dovuta :
a. ad un maggiore contributo entalpico
b. ad un minore contributo entalpico
c. ad un maggiore contributo entropico
37. quali tra queste coppie di reagenti daranno un complesso più stabile
a. Fe3+/CN
b. Fe2+/CO
c. Pt2+/CO
38. L’EDTA è un legante :
a. esadentato
b. contemporaneamente bidentato e tetradentato
c. ha due gruppi ossigeno e quattro azoto che possono legare
39. nei complessi a basso spin gli elettroni:
a. sono tutti accoppiati prima di occupare un orbitale a più elevata energia
b. possono occupare orbitali sia di legame che di antilegame senza ordine di priorità
c. hanno spin paralleli negli orbitali a più bassa energia
40. i fattori che influenzano maggiormente gli equilibri di complessamento sono:
a. effetti del campo cristallino
b. il carattere acido‐basico di leganti e cationi
c. il rapporto carica raggio degli ioni.
41. Il saturnismo è una malattia dovuta:
a. all'esposizione professionale od accidentale al piombo
b. all'esposizione professionale od accidentale al rame
c. all'esposizione professionale od accidentale all’alluminio
42. lo zucchero di Saturno è un complesso di poimbo con
a. saccarosio.
b. glucosio.
c. acetato
43. l’avvelenamento da metalli pesanti avviene perchè:
a. l’organismo umano non ha dei meccanismi specifici per l’escrezione di ioni metallici
b. l’organismo umano ha dei meccanismi specifici per l’escrezione solo dei metallici non essenziali
c. l’organismo umano produce ioni metallici in maniera endogena
4
44. la relazione
esprime
a. la frazione di legante attiva nel caso di un equilibrio competitivo tra leganti L ed F
b. la frazione di metallo attiva nel caso di un equilibrio competitivo tra leganti L ed F
c. la frazione di metallo attiva nel caso di un equilibrio competitivo acido base
45. Nel caso di una reazione competitiva di un legante ausiliario F la reazione di complessamento ML
a. È favorita al diminuire della concentrazione di M
b. È favorita al diminuire della concentrazione di L
c. È favorita al diminuire della concentrazione di F
46. Nel caso di una reazione competitiva di un legante ausiliario F la reazione di complessamento ML
a. È favorita al diminuire della costante di stabilità
b. È favorita al diminuire della costante di stabilità
c. È favorita all’aumentare costante di stabilità
47. La b‐talassemia è una malattia genetica che può essere controllata
a. Impiegando una terapia chelante
b. Effettuando regolari trasfusioni di sangue
c. Somministrando quando serve il farmaco Deferasirox
48. I farmaci chelanti utilizzati nelle terapie sperimentali per l’Alzheimer:
g. Devono causare la precipitazione e necrotizzazione della proteina b‐amiloide
h. Devono poter attraversare la barriera emato‐encefalica
i. devono formare complessi forti con ferro, rame e zinco
49. I complessi utilizzati nella diagnostica clinica devono :
d. Essere molto attivi al fine di vedere delle immagini accettabili
e. Avere una piccola reattività chimica
f. Devono essere complessi molto stabili
50. I complessi utilizzati nella terapia chemioterapica devono in genere
c. Essere molto attivi al fine di legarsi velocemente a tutti i tessuti
g. Devono avere una certa labilità chimica
h. Devono essere complessi molto stabili
5