SOC Chirurgia Generale
Azienda Ospedaliero - Universitaria
S. Maria della Misericordia – UDINE
Direttore Roberto Petri
Resezione segmentaria
duodeno – digiunale
videolaparoscopica per GIST
A. Rosignoli, G. Petrin, E. Sattin, V. Durastante, M. Zuccolo, R. Petri
Padova, 12 dicembre 2008
Definizione/Epidemiologia
• I
GIST
sono
i
più
comuni
tumori
mesenchimali gastrointestinali
• Stessa distribuzione tra i sessi
• Maggiore incidenza nella 7° decade di vita
Localizzazione
• Stomaco 45-65%
(> corpo e antro)
• Piccolo intestino 15-25%
• Colon-retto 5-10%
• Esofago 5-10%
• Duodeno 3-5%
(> digiuno)
(> retto)
Aspetti macroscopici
• Tumori singoli intramurali
– Endofitici (spesso ulcerati)
– Esofitici
Istologia
• Cellule fusate
• Cellule epitelioidi
• Forme miste
• CD117/c-kit+ (90%)
• CD34+ (70 – 80%)
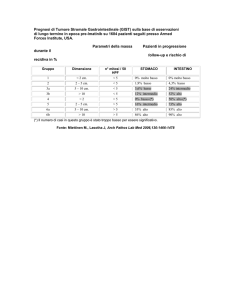
Categorie di rischio
Fletcher et al. 2002
Rischio
Dimensione tumore
Conta mitotica
Rischio molto basso
<2 cm
<5 / 50 HPF
Rischio basso
2-5 cm
< 5 / 50 HPF
<5 cm
6-10 / 50 HPF
5-10 cm
< 5 / 50 HPF
>5 cm
> 5 / 50 HPF
>10 cm
Qualsiasi
Rischio intermedio
Rischio alto
HPF = High-power fields (campi ad alto ingrandimento).
Presentazione clinica
• Asintomatici
• Sanguinamento GI
• Dolori addominali
• Massa addominale
• Sintomi e segni specifici per sito:
– disfagia (esofago-cardias)
– occlusione intestinale (piccolo intestino)
– ittero ostruttivo (duodeno)
– tenesmo (retto)
– emoperitoneo (rottura intrap.)
Diagnosi
• Endoscopia
Compressione ab estrinseco da lesione sub mucosa
• TC
I scelta nelle masse che improntano la mucosa GI con biopsia –
–
–
–
–
Dimensioni
Sede
Morfologia (parete vascolarizzata, centro necrotico, morfologia irregolare disomogenea)
Metastasi.
sensibilità riguardo l’infiltrazione delle strutture adiacenti
• FDG-PET
sensibilità/specificità. Utile per le metastasi e follow up
• Biopsia percutanea
– NO nei primitivi (rischio di rottura/disseminazione neoplasia),
– SI in fase avanzata e/o metastatica (terapia con Imatinib)
Terapia
La chirurgia rimane il trattamento di
scelta del GIST primitivo non metastatico
• Resezioni cuneiformi o segmentali
Margine libero 2 - 3cm
• Resezione“En bloc ”
Se infiltrazione strutture adiacenti
Non è richiesta linfoadenectomia (rara disseminazione linfatica)
Manipolazione cauta ( rischio di rottura e dissem. intraperitoneale)
Ann Surg 244:176,2006
Trattamento
videolaparoscopico
Selezione appropriata dei casi per la natura
friabile della pseudocapsula ed il potenziale
rischio di rottura durante la manipolazione
Terapia medica
Terapia molecolare mirata con gli
inibitori della tirosinchinasi (Imatinib)
• Regressione dei GIST metastatici
• Downsize dei primitivi
Management multidisciplinare tra oncologo e chirurgo
N Engl J Med 344:1052,2001
Recidiva
• Più frequente in base a:
– Organo d’origine (tenue)
– Stato margini resezione
– Rottura tumore (pre o intra operatoria)
• Recidiva
o
metastasi
20-50%
(nonostante
intervento chirurgico radicale)
• Recidiva
recidiva
>
entro 2 aa dall’intervento (più frequente
locale
seguita
dalle
Mx
intraaddominali,
raramente a distanza in fegato, polmone, ossa)
Sopravvivenza
A 5 aa: 30 – 65%
Follow up
Indagini strumentali (TC – TC PET)
• < 3 aa ogni 3 mesi
• 3 – 4 aa ogni 4 mesi
• 5 aa ogni 6 mesi
• > 5 aa ogni anno
Abominal mass suspicious for GIST
Unresectable or borderline resectable
or wide metastatic disease
resectable
Operative path
biopsy
(+) GIST
Non GIST:
Appropriate
tumor /CA Rx
(+) GIST
Early close follow up with
exam and CT csan (3-5 years)
Consider PET in addiction
to CT scan
Imatinib
Recurrence (?)
Resectable: consider
re-resection
response
No response
3-6months
Stop Imatinib
resection
Adv Surg 39: 193, 0052
Non-GIST
Appropriate
Tumor/CA RX
Consider palliative resection / other tier
therapy / consider clinical trial
Caso clinico
E.R. M 1938
• APR: K mammella, melanoma spalla, K prostata.
• APP: In corso di follow – up reperto TC:
“neoformazione solida di
circa 1cm di Ø tra corpo/coda pancreas e parete post. antro gastrico”.
• EGDS:
“Gastrite cronica atrofica + iperplasia rigenerativa e metaplasia
intestinale incompleta”.
• PET – TC:
Focalità di 1cm a livello di corpo – coda del pancreas sul
margine anteriore aderente alla parete post. dell’antro gastrico (SUV=6.4).
CONCLUSIONE: Lesione ad elevato gradiente metabolico da riferirsi in
prima ipotesi a lesione “mali moris”
ER – 14.11.2006
ER – 14.11.2006
ER – 14.11.2006
Caso clinico
E.R. M 1938
INTERVENTO CHIRURGICO
• DIAGNOSI INTRAOPERATORIA: Neoformazione intramurale I ansa digiunale
• DESCRIZIONE INTERVENTO: Resezione duodeno – digiunale in VL.
ESAME ISTOLOGICO
Sarcoma stromale GI/GIST, kit+, di basso grado (< 5cm, mitosi < 5/50 HPF),
margini liberi da neoplasia
FOLLOW - UP
Cadenza semestrale (esami ematochimici, TC torace – addome).
Attualmente (luglio 2008), libero da malattia
GIST - Casistica operatoria
(maggio 2004 – dicembre 2008)
VL
Stomaco
Primitivo
Stomaco
Recidivo
Tenue
Primitivo
TOTALE
3
OPEN
8
1
4
2
18