STOMACO: NEOPLASIE
Sede: n
n
n
Antro e piccola curva Grande curva Corpo-­‐fondo Tumori primi8vi vs. secondari (con8guità) Epiteliali vs. mesenchimali Benigni vs. maligni STOMACO: NEOPLASIE
Epiteliali benigne esofi8che = Polipi Lesioni rilevate sul piano mucoso, neoplas8che e non (pseudopolipi) Macroscopicamente possono essere: • sessili (cupoliformi, a larga base di impianto) • peduncola8 (fungiformi, con testa piu’ ampia del peduncolo). Tra$azione con il grosso intes0no Carcinoma gastrico
Epidemiologia"
n Prevalenza:
tendenza alla riduzione nei
paesi Occidentali"
n Aree geografiche ad alto rischio:
Giappone, Cina, Cile, Brasile, Colombia,
Islanda, Yugoslavia, Spagna."
Carcinoma gastrico
Patogenesi"
n
n
n
n
Familiarità neoplastica"
Gruppo sanguigno A"
Secrezione di un tipo specifico di Pepsinogeno"
Fattori ambientali (Helicobacter pylorii) e dieta"
ð
ð
ð
ð
Nitrosamine (Nitrati – nitriti)"
Basso apporto di verdura, insalata, frutta fresca"
Basso apporto di grassi e proteine animali"
Elevato apporto di sale e carboidrati complessi"
Condizioni e lesioni precancerose"
n Anemia
perniciosa"
n Gastroresezioni parziali"
n Gastriti croniche atrofiche"
n Lesioni precancerose:"
ð Metaplasia
intestinale (completa ed
incompleta)"
ð Displasia di alto grado"
Displasia gastrica"
n Neoplasia
non invasiva"
n E’ la lesione istologica più ad alto
rischio di evoluzione in carcinoma
invasivo"
n La sua presenza impone il controllo
periodico endoscopico e bioptico del
paziente"
n Può insorgere su epiteli nativi o su
epiteli metaplastici"
Displasia gastrica"
n
Alterazioni citologiche"
ð
ð
ð
ð
n
Alterazioni della maturazione cellulare "
Aumentato rapporto N/C"
Polimorfismo, polistratificazione ed ipercromia nucleare"
Presenza di macronucleoli"
Graduazione: basso e alto grado"
ð
ð
Lesioni indefinite per displasia"
Lesioni sospette per carcinoma infiltrante"
Early gastric cancer"
n Adenocarcinoma
gastrico la cui
infiltrazione non supera la sottomucosa."
n Tendenza a crescere radialmente
(superficialmente)"
n Prognosi più favorevole (80% a 5 anni)"
n Bassa frequenza di metastasi
linfonodali (4% e 17% per le forme
mucose e sottomucose rispettivamente)"
Carcinoma gastrico avanzato"
Adenocarcinoma che infiltra la muscolatura
propria"
n Sedi: prepilorico, antro-pilorico, piccola curva"
n Forme macroscopiche:"
n
Ulcerato"
ð Vegetante"
ð Infiltrante (“linite plastica”)"
ð
n
Modalità di infiltrazione:"
ð
Espansivo o infiltrativo"
Carcinoma gastrico avanzato"
n
Tipo istologico (sec. Laurén):"
ð
Tipo intestinale: "
•
•
•
•
ð
paesi ad alto rischio"
secondario a fattori ambientali"
tipo espansivo"
associato a gastrite atrofico-metaplasica."
Tipo diffuso:"
•
•
•
•
•
età di insorgenza inferiore"
minore variabilità geografica"
nei paesi a basso rischio"
non associato a gastrite"
basso tasso di sopravvivenza."
Citocheratine
Carcinoma gastrico avanzato"
n Altri
istotipi"
ð Adenocarcinoma
mucoide o colloide"
ð Adenocarcinoma epatoide"
ð Coriocarcinoma"
ð Tumori con differenziazione neuroendocrina"
"
Carcinoma gastrico avanzato"
n Diffusione
del carcinoma"
ð Locale
(esofago, duodeno)"
ð Linfatica (grande e piccola curva)"
ð Ematica: fegato, polmoni, surreni e ovaie
(tumore di Kruckenberg)"
n Grado
istologico"
§ Stadiazione: T.N.M."
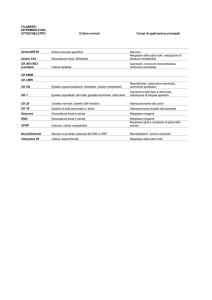
Tumori Stromali Gastro-Intestinali
GIST
•
•
•
Neoplasie dello stroma proprio
(dell’apparato gastro-enterico)
Distinte da altre comuni neoplasie
mesenchimali (angiomi, lipomi, etc.)
Rare (0,5-2%) rispetto alle neoplasie
epiteliali del medesimo distretto
GIST
•
•
•
•
•
Aggressività biologica incerta (“Tumor”)
Origine da cellule interstiziali di Cajal
Derivate dalla mutazione del gene c-kit
Amplificazione del recettore tirosinkinasico CD117 (o PDGFRα)
Sensibili a terapia con anti-recettori
specifici
GIST
Caratteri macroscopici “distintivi”
•
•
•
•
•
noduli circoscritti
crescita espansiva, lobulata
sede profonda
consistenza “carnosa”
colorito grigio-roseo, traslucido
GIST
Caratteri istologici “distintivi”
•
•
•
cellularità fusata, monomorfa
architettura fascicolata
storiforme
a palizzata
frequenti alterazioni regressive
(necrosi, emorragia, jalinosi, calciosi)
GIST
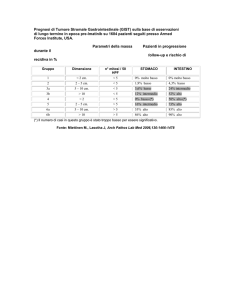
n
Parametri prognostici istologici
➙
indice mitotico
intermedio
➙
➙
➙
< 2/10 HPF Basso rischio
3-5/10 HPF Rischio
> 5/10 HPF Alto rischio
infiltrazione della mucosa
necrosi massiva “tumorale”
estensione / metastasi ad altri visceri
Newman PL, et al. J Pathol 1991; 164: 107-117
GIST
Fattori Prognostico-Predittivi
§ Dimensioni
§ Sede
(stomaco < colon < tenue)
§ Indice mitotico
§ Completa resezione (margini liberi)
§ Rottura intraoperatoria del tumore
§ Status di c-Kit
• Prognosi favorevole (mutazioni puntiformi ed
inserzioni di esone 11)
• Prognosi intermedia (assenza di mutazioni)
• Prognosi sfavorevole (mutazioni di esone 9 o
delezioni di esone 11)
GIST
Classi di Rischio
§ Very
low risk
§ Low risk
§ Intermediate risk
§ High risk
GIST
Sopravvivenza globale secondo
la categoria di rischio
Modified AFIP(A)
1.0
Cumulative survival
Very high
+
0.8
Very high-censored
High
+
0.6
High-censored
Intermediate
+
0.4
Intermediate-censored
Low
+
0.2
0
0
100
200
Time (months)
AFIP, Armed Forces Institute of Pathology.
Adapted with permission from Goh BKP et al. Ann Surg Oncol. 2008;15:2153-2163.
Low-censored
Proportion Recurrence-Free
Parametri prognostico-predittivi Status di c-Kit
1.0
KIT exon 11 PM/INS (n=32)
0.8
Other KIT exon 11 deletion (n=17)
PDGFRA mutation (n=8)
0.6
No mutation (n=29)
0.4
KIT exon 11 DEL557/8 (n=35)
0.2
KIT exon 9 mutation (n=4)
P<0.001
0.0
0
1
2
3
4
5
6
7
Years After Resection
DeMatteo RP et al. Cancer. 2008;112:608-615.
8
9
10
CD117
CD34