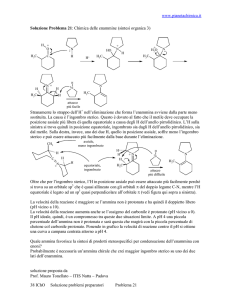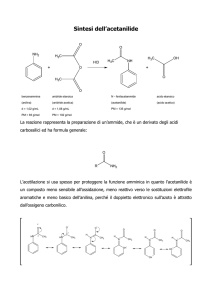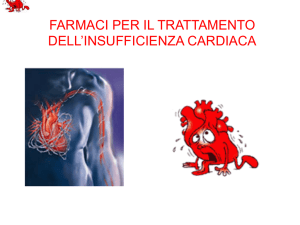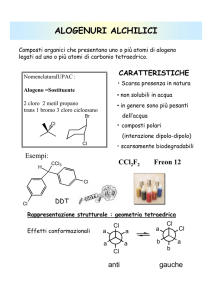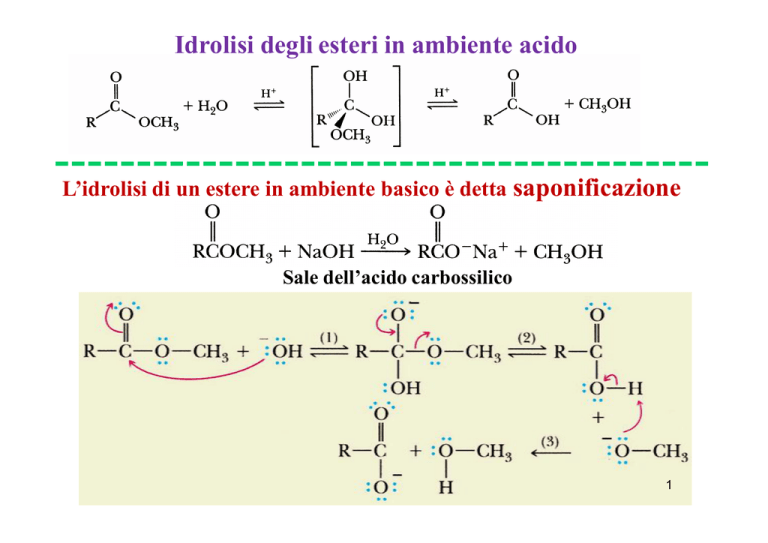
Idrolisi degli esteri in ambiente acido
L’idrolisi di un estere in ambiente basico è detta saponificazione
Sale dell’acido carbossilico
1
Saponificazione – Idrolisi basica degli esteri
1) attacco nucleofilo di HO- sul carbonile e formazione
dell'intermnedio tetraedrico
O
H3C
O -
-
C OCH3 + HO
H3C
C
OCH3
OH
2) fuoriuscita del gruppo alcossi e ripristino del gruppo
carbonilico
O O
H3C C OCH3
H3C C OH
+ OCH3
OH
3) stadio irreversibile perchè la reazione è spostata verso
l'acido e la base più debole
O
H3C
C
O-H
specie più forti
+ OCH3
O
-
H3C C O + CH3OH
specie più deboli
2
Idrolisi di altri derivati degli acidi carbossilici
Si riforma l’acido carbossilico
Cloruro di etanoile
Anidride acetica
2-Fenil-butanammide
La idrolisi delle ammidi non decorre in ambiente neutro, ma
occorre un ambiente acido o basico
3
cloruri degli acidi
O
H3C C Cl
H2O
O
-
OH
H3C C Cl
H3C C Cl
OH2
+
H3C C
OH
OH
Anidridi
O
H3C C
O
-HCl
H3C C
O
O
2 H3C C OH
+ H2O
O
Ammidi
HCl
O
calore
O
+ H3C C OH + NH4 Cl
H3C C NH2 + H2O
NaOH
calore
Esteri
H2SO4
O
H3C C O-Na+ + NH3
O
H3C C OH + CH3OH
O
H3C C OCH3+ H2O
NaOH
O
H3C C O-Na+ + CH3OH
4
Preparazione di derivati di acidi: Formazione di un estere
Reazione con alcoli
Cloruri degli acidi
Anidridi
5
Reazione con ammoniaca ed ammine: Formazione di ammidi
Da Cloruri degli acidi
1
2
3
6
Reazione con ammoniaca ed ammine: Formazione di ammidi
Da Anidridi degli acidi
Da Esteri
7
Reattività decrescente
Reattività dei derivati degli acidi carbossilici ed
interconversioni
8
O
H3C C Cl
SOCl2
O
O
H3C C O C CH3
O
H3C C OH
O
H3C C OCH3
H+
O
H3C C NH2
O
H3C C O
9
-
Riduzione degli esteri
Alcoli primari
1. LiAlH4
Riduzione delle ammidi
Ammine
10
Gli esteri reagiscono con i reattivi di
Grignard
Alcoli
1)
2)
11