Funzionalità del fegato,
normale e patologica
E’ il più voluminoso organo viscerale (~1,5 kg), situato nella parte alta e destra
dell’addome, subito sotto il diaframma;
Conserva le sue dimensioni → capacità di autorigenerarsi;
Molto irrorato (a riposo circa 1,5 L di sangue/minuto); costituito da EPATOCITI e da
pochi altri tipi cellulari.
Funzioni di sintesi
Riguarda la maggior parte delle proteine plasmatiche (albumina, globuline (ad eccezione delle
immunoglobuline)), dei fattori della coagulazione, (protrombina), dei composti azotati non
proteici (urea, purine, pirimidine, eparina ecc.).
Interviene nel metabolismo di quasi tutte le sostanze organiche:
metabolismo glucidico: mantiene l’omeostasi glucidica, regolando gluconeogenesi,
glicogenesi, glicogenolisi;
metabolismo lipidico: sintesi di trigliceridi, di acidi grassi, di lipoproteine, con formazione di
corpi chetonici, scissione dei trigliceridi, sintesi ed escrezione di colesterolo, fissazione,
formazione e scissione dei fosfolipidi;
metabolismo di vitamine e degli acidi biliari;
metabolismo dei pigmenti biliari (bilirubina);
Funzioni di accumulo
Costituisce la sede di deposito di glicogeno, dei trigliceridi, degli acidi grassi, dei fosfolipidi, del
colesterolo, delle proteine plasmatiche, delle vitamine idro- e liposolubili, dei fattori ematopoietici
come ferro, rame, acido folico e vitamina B12.
Funzioni cataboliche
Attraverso reazioni di ossidazione, riduzione, idrolisi, decarbossilazione e ossidrilazione, il fegato
catabolizza
sostanze
endogene
come
l’insulina,
il
glucagone,
gli
estrogeni,
gli
ormoni
gastrointestinali e detossifica da sostanze esogene, dannose per l’organismo, come prodotti chimici
inquinanti e farmaci.
Funzioni di escrezione
Coniugando composti, sia esogeni che endogeni, con molecole come l’acido glucuronico
(prodotto solo dagli epatociti), la glicina, l’acido solforico, l’acido acetico e la taurina, ne
consente l’escrezione.
Svolge, inoltre, l’importante funzione esocrina di produzione ed escrezione della bile, costituita
da pigmenti biliari, acidi biliari, colesterolo, fosfolipidi - soprattutto lecitina- ioni inorganici e
proteine in limitata quantità.
In considerazione di tale varietà di funzioni, reputando, quindi, onerosa una richiesta di
tutti i test disponibili, dispersiva ai fini di una diagnosi, in presenza di una malattia epatica
accertata o sospetta il clinico selezionerà i test essenziali (di primo livello), indicativi
delle funzioni fondamentali:
Bilirubina, diretta e indiretta
Enzimi (AST/ALT, ALP, γ-GT, LDH)
Proteine plasmatiche (albumina e globuline)
Fattori della coagulazione
Queste indagini biochimiche possono aiutare nella differenziazione delle seguenti diagnosi:
Ostruzione biliare
Danno acuto epatocellulare
Malattia epatica cronica
La funzionalità epatica è mantenuta fino a che rimane attivo anche solo il 10% del parenchima
epatico.
a) Marcatori di citolisi: fuoriuscita di componenti intracellulari
Es.: Enzimi plasmatici (AST, ALT, γ-GT , LDH)
b) Marcatori di colestasi: valutazione della incapacità di secrezione
Es.: ALP, γ-GT, Bilirubina
c) Marcatori di coniugazione: metabolismo di bilirubina e dei sali biliari
Es.: Bilirubina totale, diretta, indiretta....
d) Marcatori di Protidosintesi
Es.: Proteine plasmatiche, fattori della coagulazione (tempo di Quick), pseudocolinesterasi
e) Altri marcatori di danno
Es.: Ammoniemia, Transferrina, Ceruloplasmina, Alfa-fetoproteina, ecc ecc
N.B. Nessuna delle indagini di laboratorio descritte è in grado, DA SOLA, di
valutare la funzionalità epatica in maniera completa
I risultati di questi test di primo livello indirizzeranno verso esami più specialistici (in
caso di epatite, ricerca di marcatori del virus, in caso di cirrosi biliare indagini
immunologiche) ecc…
Possono essere necessari test di funzionalità specifica, ad es., per la valutazione pre-
operatoria della funzionalità epatica, fondamentale per tutti i pazienti con
indicazione all'intervento chirurgico, soprattutto se si tratta di pazienti affetti da cirrosi
epatica. In questi ultimi, il rischio di sviluppare complicanze, anche fatali, post-
operatorie è elevato.
Es.: Capacità di biotrasformazione: clearance di xenobiotici (Clearance dell’antipirina, del
galattosio, verde di indocianina etc…)
MARCATORI DI CITOLISI
Rivedere Lezione sugli ENZIMI!!!!!!!!
Indicatori di danno/necrosi epatocellulare
Le transaminasi sono enzimi che si trovano soprattutto nelle cellule del fegato. I loro livelli
nel sangue sono utili per valutare il corretto funzionamento del fegato, ma possono
anche riflettere lo stato di salute del cuore e dei muscoli scheletrici.
Negli esami di routine si misurano:
transaminasi AST (o GOT), che riguarda anche il cuore e muscoli
transaminasi ALT (o GPT), che riguarda soprattutto il fegato
AST: aspartico amino transferasi o GOT: glutammico ossalacetico transaminasi
ALT: alanina amino transferasi GPT: glutammico piruvato transaminasi
INDICI SENSIBILI DI NECROSI EPATOCELLARE
Gli aumenti maggiori si hanno nel danno epatico acuto virale o tossico
ALT(o GPT): è un enzima citoplasmatico, anch’esso ubiquitario, ma presente nel
fegato in quantità maggiori che negli altri tessuti. Il suo aumento nel siero avviene
quindi solo nelle epatopatie.
AST(o GOT): è un enzima principalmente legato ai mitocondri (80%), ubiquitario
(miocardio ad elevatissima concentrazione, rene, eritrociti, cervello, muscolo), può
aumentare oltre che nelle epatopatie a causa della lisi cellulare, anche in altre
condizioni patologiche (infarto del miocardio).
AST e ALT aumentano, principalmente, per necrosi dell’epatocita ma, anche
se in maniera minore, per danneggiamento funzionale cellulare .
AST e ALT sono indicatori sensibili, capaci di evidenziare presenza di lesioni
epatiche anche in pazienti asintomatici.
ALT
Dosaggio: siero
Note preanalitiche: evitare emolisi (attività negli eritrociti maggiore di quella
plasmatica), stabilità buona a temp. amb.
Intervallo di Riferimento: adulti (dipende dai metodi) 10-40 UI/l
(interferenze da farmaci epatotossici)
AST
Dosaggio: siero
Note preanalitiche: evitare emolisi (attività negli eritrociti circa 6 volte superiore di quella
plasmatica), stabilità buona a temp. amb.
Intervallo di Riferimento: adulti (dipende dai metodi) 10-37 UI/l
ALT /AST
Molto elevato (10-20 volte, con Interv. di Riferim.: 0,7-1,4) sono indici di epatite acuta
(virale o da farmaci o autoimmune)
Altri marcatori di necrosi sono γ-GT e LDH…….
…….rivedersi la lezione sugli enzimi!!!!!!!
Marcatori di colestasi
COLESTASI: In medicina la colestasi è una stasi con flusso retrogrado della bile verso il
sangue, per incapacità alla secrezione verso il letto biliare o per aumentata pressione a
valle. UNA CONDIZIONE IN CUI LA BILE NON PUÒ FLUIRE DAL FEGATO AL DUODENO.
Le due distinzioni principali della colestasi sono:
TIPO OSTRUTTIVO, dove c'è un blocco fisico nel sistema duttale come può accadere
a causa di calcoli o tumori
TIPO METABOLICO, dove ci sono alterazioni nella formazione della bile che possono
essere causate da difetti genetici od acquisiti (come effetto collaterale di
trattamenti medici).
Fisiologicamente….
Nella colestasi intraepatica l'ostruzione biliare è interna al fegato, mentre
nella colestasi extraepatica il blocco è situato all'esterno dell'organo.
La Fosfatasi Alcalina (ALP/AP) è un enzima presente in diversi tessuti del corpo.
In particolare, essa si trova nelle ossa e nelle cellule del fegato che formano i dotti biliari
(i canalicoli, che trasportano la bile all’intestino dove è necessaria per la digestione dei
grassi). Sebbene in concentrazioni inferiori, la AP è presente anche nelle cellule
intestinali e nella placenta. Tutte queste parti del corpo producono forme diverse di
fosfatasi alcalina, che sono definite isoenzimi. La AP è presente anche nel sangue, ma a
livelli bassi; in caso di malattie del fegato o delle ossa essa può aumentare.
L’esame è usato per evidenziare malattie del fegato (soprattutto delle vie biliari, insieme
a dosaggio di
bilirubina, transaminasi AST e ALT) e delle ossa, per seguirne la
progressione o per valutare l’efficacia di un eventuale trattamento terapeutico.
Aumenta in due condizioni fisiologiche:
• bambini (per l’accrescimento osseo)
• gravidanza (isoenzima circolante di origine placentare)
Aumenta:
• In ogni forma di ostruzione delle vie biliari (da ostruzione dei canalicoli intraepatici,
es.: cirrosi biliare primitiva, fino all’ostruzione del dotto comune es.: calcolosi biliare).
• A causa di farmaci epatotossici
• Nelle epatopatie
In presenza di un aumento di dubbia origine, si deve valutare anche la presenza
CONTEMPORANEA di aumento della γ-GT, che è più specifico per la patologia epatica.
La γ-GLUTAMIL-TRANSPEPTIDASI (γ-GT o GGT) è un parametro di stasi biliare (influenzato
in particolare dall’assunzione di alcool). E’ un enzima glicoproteico, legato alla
membrana plasmatica e coinvolto nel metabolismo del glutatione.
Aumenta:
• per danno epatocellulare, ma soprattutto la colestasi può contribuire ad aumentare
la GGT sierica
• fortemente negli alcolisti, perché l’alcol etilico ne stimola la sintesi epatica
• per induzione da farmaci (rifampicina, antiepilettici)
Uso preminente nello screening e nel follow-up di alcolisti sottoposti a terapia. Si ritiene
un parametro più sensibile e più specifico di patologia epatica della fosfatasi alcalina.
Dosaggio: siero
Note preanalitiche: buona stabilità
Intervallo di Riferimento (dipende dai metodi): Uomini: 10-50 U/L; Donne a 8-31 UI/l
Marcatori di coniugazione
Metabolismo della bilirubina e iperbilirubinemia
La bilirubina è un prodotto del catabolismo dell'emoglobina; è un pigmento di
colore giallo-rossastro;
Proviene per l’80% dalla distruzione di globuli rossi senescenti nel SRE e per il 15% dal
catabolismo di emoproteine sieriche (mioglobina, citocromi, catalasi) e per il 5% da
eritropoiesi inefficace;
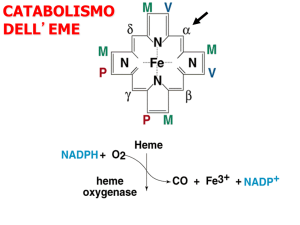
L'emoglobina contenuta nei GR viene catabolizzata e l'eme che viene liberato
viene convertita in biliverdina, grazie all’eme-ossigenasi, con distacco del ferro e
della globina:
HO-1
BVR
Bilirubina
EME
Biliverdina
La biliverdina diventa bilirubina grazie all’enzima biliverdina-reduttasi. Questa è la
bilirubina non coniugata (o indiretta), è insolubile e quindi per essere trasportata
all'interno del sangue deve essere legata ad una proteina sierica prodotta dal
fegato, l'albumina.
All’interno delle cellule epatiche si distacca dall'albumina e viene coniugata, nel
reticolo endoplasmatico, con acido glucuronico con formazione della bilirubina
diretta o coniugata (solubile).
La bilirubina coniugata è secreta nei canalicoli biliari; nella bile è sotto forma di
micelle miste con acidi biliari.
Acido glucuronico
Idrofobica e tossica, la bilirubina circola nel plasma legata all’albumina;
Uptake a livello membrana basolaterale degli epatociti mediante meccanismo carrier
mediato;
Proteine di legame citosoliche (ligandine) portano la bilirubina al reticolo endoplasmico
dove viene coniugata con acido uridindifosfato-glicuronico (UDP-glucuronato) dall’enzima
UDP-glucuroniltransferasi (UGT) con formazione di bilirubina mono-(BMG) e di-(BDG)
glucuronide; questo processo rende la bilirubina idrosolubile e quindi pronta per la
escrezione nella bile;
BMG e BDG dirette verso la membrana apicale canalicolare e trasportate nel canalicolo
biliare da una pompa di esporto ATP-dipendente. La proteina responsabile si chiama MRP2
(multidrug resistance protein 2);
L’80% della bilirubina è escreta come BDG, il 20% come BMG solo tracce come UCB (non
coniugata);
BDG e BMG sono deconiugate da enzimi batterici nell’ileo e nel colon e convertiti in
tetrapirroli privi di colore (urobilinogeno). Il 20% dell’ urobilinogeno è riassorbito ed eliminato
nelle urine e nella bile.
Valori di riferimento nel siero:
Bilirubina Totale: 0,3 -1,1 mg/dl
Bilirubina Indiretta (non coniugata): 0,3-1 mg/dl
Bilirubina Diretta (coniugata): 0 - 0,4 mg/dl
La bilirubina non coniugata (indiretta) è così fortemente legata all’albumina che nel
plasma non è presente in forma libera: quindi, in condizioni normali, NON PASSA
NELLE URINE. Avendo, inoltre, alta affinità per i lipidi di membrana, un suo aumento
causa alterazioni della funzionalità delle membrane cellulari, soprattutto del sistema
nervoso.
Al contrario, la bilirubina coniugata (diretta) è relativamente solubile in acqua ed un
suo aumento porta ad elevate concentrazioni nelle urine, che avranno un’intensa
colorazione giallo-marrone.
Ittero
L’ittero è inequivocabilmente evidente su base clinica quando la concentrazione
plasmatica di bilirubina supera la soglia di 2.5-3 mg/dl.
L’ittero in seguito a situazioni di iperbilirubinemia si verifica come conseguenza di una
delle seguenti condizioni:
Iperproduzione della bilirubina nell’organismo ed incapacità della cellula epatica
di captare, coniugare ed eliminare il pigmento. Aumento della bilirubina indiretta;
Non aumento della produzione di bilirubina, ma difetto funzionale dell’epatocita
(alterazione dei meccanismi di captazione, coniugazione). Aumento della
bilirubina diretta ed indiretta (es.: Sindrome di Gilbert, uso di farmaci epatotossici..);
Incapacità di escrezione della bilirubina attraverso le vie biliari dovuta ad ostacolo
meccanico intra o extra epatico. Aumento della bilirubina diretta (ostruzione da
calcoli, neoplasie, epatite virale, etc..).
Classificazione (storica) degli itteri:
Pre-epatico: Ittero emolitico. Nell’ittero emolitico la bilirubina in eccesso e’
quella indiretta (legata all’albumina) che non è escreta nelle urine
(bilirubinuria ridotta/assente).
Epatico: Ittero epatocellulare. Nell’ittero epatocellulare la bilirubina
circolante è in gran parte nella forma glucuronata (diretta) idrosolubile e
quindi si ha bilirubinuria più o meno accentuata.
Post-epatico: Ittero ostruttivo. Nell’ittero ostruttivo si ha un aumento in
circolo di bilirubina glucuronata (diretta) e quindi elevata bilirubinuria.
ITTERO NEONATALE
Marcatori di protidosintesi
Rivedere Lezione sull’Elettroforesi!!!!!!!!
Proteine plasmatiche
La maggior parte delle proteine plasmatiche è sintetizzata dal fegato, cui compete
anche la fase catabolica degli aa (attraverso reazioni di transaminazione,
deaminazione dell’aa e successiva trasformazione dello ione ammonio, tossico, in
urea, poi escreta dai reni)
Le proteine plasmatiche hanno caratteristiche velocità di migrazione durante
l’elettroforesi : si possono, così, facilmente separare ALBUMINA, GLOBULINE ALFA1,
ALFA2 e BETA, fibrinogeno, gamma-globuline
Elettroforesi delle proteine sieriche
L’albumina è sintetizzata dalle cellule parenchimali del fegato, ha una vita media di
20 giorni, è responsabile del mantenimento della pressione oncotica e del trasporto
di numerose sostanze (bilirubina, acidi grassi liberi, cortisolo, ormoni tiroidei, calcio,
farmaci).
I valori di riferimento sono 35-55 g/l
In caso di valori alterati, si può avere:
Iperalbuminemia (rara) in genere per disidratazione
Ipoalbuminemia (al di sotto di 3 g/dl), dovuta a varie cause
Ipoalbuminemia
Perdita da sindrome nefrosica, perdita da ustioni o dermatiti, perdita dal tubo
digerente per lesioni della mucosa
Apporto inadeguato di proteine (vomito, diarrea, malassorbimento, pancreatiti, coliti,
enteriti, etc..)
Diminuita sintesi epatica (si ritiene comunque che il fattore che influenza in modo
significativo l’albuminemia nelle malattie epatiche croniche non è la funzione
epatocellulare ma la ritenzione idrica) eventualmente associata a diminuita
alimentazione, ascite, malassorbimento)
Aumentato catabolismo (ipertiroidismo, traumi, sindrome di Cushing)
In alcune condizioni fisiologiche (gravidanza, lattazione)
Infiammazione acuta e cronica con necrosi tissutale
Le globuline sono un gruppo eterogeneo di proteine, distinte, nel tracciato
elettroforetico, in alfa, beta e gamma;
La loro concentrazione fisiologica è 20-35 g/l;
Durante la cirrosi epatica si può avere iperglobulinemia, di grado variabile, dovuta a
stimolazione del SRE.
Le alfa-globuline non rivestono particolare importanza nella diagnosi di malattie
epatiche, eccetto l’alfa1-antitripsina, proteina con attività antiproteasica (anti-tripsina,
anti-plasmina); essa risulta ridotta o assente nelle cirrosi ad eziologia ignota o nell’ittero
colestatico giovanile.
Alfa1 globuline
Valori riferimento: 0,2-0,4 g/dl
Se aumenta:
›
malattie infiammatorie croniche, malattie infettive, infarto cardiaco, assunzione pillola
contraccettiva, gravidanza
Se diminuisce:
›
malattie epatiche gravi, una malattia ereditaria rara chiamata enfisema congenito,
malattie renali
Alfa2 globuline
Valori riferimento: 0,4-0,8 g/dl
Se aumenta:
›
malattie renali, malattie infiammatorie croniche e acute, infezioni, infarto cardiaco,
sindrome di Down, diabete, alcuni tumori maligni
Se diminuisce:
›
malattie epatiche gravi, diabete, ipertiroidismo, rottura dei globuli rossi (emolisi), artrite
reumatoide
Beta globuline
Valori riferimento:0,6-1 g/dl
Se aumenta:
›
anemia da carenza di ferro, alcuni casi di mieloma multiplo, ipercolesterolemia (elevati
livelli di colesterolo nel sangue), gravidanza
Se diminuisce:
›
malnutrizione, cirrosi
Gamma globuline
Valori riferimento: 0,9-1,4 g/dl
Se aumenta:
›
alcune malattie del sistema immunitario dette gammopatie (MGUS), mieloma multiplo,
malattie epatiche croniche (epatite, cirrosi), infezioni, alcuni tumori, artrite reumatoide,
lupus
Se diminuisce:
›
alcune malattie ereditarie del sistema immunitario
Fattori della coagulazione
Fibrinogeno (Fattore I)
Proteina sintetizzata dal fegato, solubile, che si trasforma in fibrina, prodotto insolubile e
fibroso, ad opera della trombina. La sua concentrazione fisiologica è tra 200-400 mg/dl,
che diminuisce in caso di epatopatie croniche, comportando alterazione della
coagulazione.
Trombina (Fattore IIa)
Enzima, sintetizzato dal fegato, che trasforma il fibrinogeno in fibrina. Circola nel plasma
come protrombina (Fattore II, un’alfa2-globulina). La sua formazione è dipendente dalla
vitamina K.
Il tempo di Quick o di protrombina (PT) è molto utilizzato in epatologia: è una misura
dell’attività di alcuni fattori di coagulazione, prodotti dal fegato, e viene spesso
utilizzata come indicatore dell’attività di sintesi del fegato.
Infatti, il fegato sintetizza molti fattori della coagulazione, in particolare quelli vitamina K
dipendenti.
Il procedimento di Quick misura la velocità della conversione della protrombina
(fattore II) in trombina (fattore IIa) in presenza di tromboplastina (fattore III), calcio,
fibrinogeno (fattore I) ed altri fattori della coagulazione (V, VII, X), a 37°C; a sua volta la
trombina converte il fibrinogeno in fibrina. La protrombina ed i fattori VII e X necessitano
della vitamina K per la loro attivazione.
Valori di Riferimento: 11-15 secondi
Altri marcatori di danno
METABOLISMO AMINOACIDI E CICLO DELL’UREA
Un uomo normale di 70 kg elimina circa 10-20 g di azoto al giorno (provenienti
dall’alimentazione o da aminoacidi non riutilizzabili) attraverso lo schema:
AA → L-glutammato → NH3 → ciclo di Krebs → Urea
L’NH3 liberata dagli AA, a causa della sua tossicità, deve essere rapidamente
allontanata dall’organismo (es.: come urea o glutammina) (AMMONIEMIA).
L’Urea nel sangue è generalmente indice di funzionalità renale (nella valutazione dei
valori aumentati), ma diminuisce in seguito ad una grave insufficienza epatica o in
soggetti con alimentazione povera di proteine.
Si può avere uremia normale anche con alterazione dell’80-90% del parenchima
epatico (dato poco utile in diagnostica epatologica).
Valori di riferimento dell’urea: 11-50 mg/dl
Ammoniemia: parametro di alterato metabolismo proteico.
I valori di riferimento sono: 20-80 μg/dl
L’ammoniemia è utile in caso di sospetta encefalopatia epatica (sindrome
caratterizzata da alterazioni neurologiche conseguenti a grave insufficienza della
funzionalità epatica e/o cortocircuiti venosi fra vena porta e circolo sistemico).
Il danno cerebrale sarebbe conseguente all’accumulo di sostanze tossiche
(ammoniaca) assorbite dall’intestino e non metabolizzate dal fegato adeguatamente.
Carboidrati
Il fegato presiede al’omeostasi del glucosio nel sangue, attraverso il mantenimento
dell’equilibrio tra i meccanismi di glicogenesi, glicogenolisi, glicolisi, gluconeogenesi.
Tali reazioni sono controllate da ormoni pancreatici (insulina, glucagone, da GH e da
catecolamine.
Nelle gravi epatopatie si po’ verificare ipoglicemia, mentre nell’epatite cronica si può
manifestare un’iperglicemia.
Lipidi
Il fegato è determinante nella regolazione del metabolismo lipidico, svolgendo sia
funzioni di sintesi che cataboliche.
Un eccesso di afflusso di acidi grassi può determinare steatosi epatica.