IDENTIFICAZIONE DEI
COMPOSTI CARBONILICI
C O
Generalità
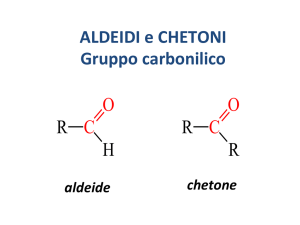
Il gruppo carbonilico, caratteristico delle aldeidi e dei chetoni è polare,
in quanto la nube elettronica del legame CO è attirata dall'atomo di
ossigeno più elettronegativo.
Le proprietà chimiche delle aldeidi e dei chetoni sono molto simili,
tuttavia la sostituzione di uno dei due radicali legati al carbonile dei
chetoni con un atomo di H (aldeidi), porta a differenze radicali nel
comportamento chimico.
R
R
C O
C O
H
R
aldeidi
chetoni
Le aldeidi si ossidano più facilmente ad acidi rispetto ai chetoni (si
ossidano molto difficilmente) e sono più reattive anche nei confronti
dell'attacco nucleofilo.
Addizione nucleofila
La reazione tipica dei composti carbonilici è l’addizione nucleofila, il cui
meccanismo può essere così schematizzato:
C O +
R'
-
R
R
O
C
:Nu
R'
Nu
R
H2O
- OH
-
OH
C
R'
Nu
Questa reazione è catalizzata dagli acidi, che protonando l'ossigeno
carbonilico, stabilizzano la carica positiva sul carbonio.
In alcuni casi, in particolare in presenza di deboli nucleofili, la reazione
può essere catalizzata dalle basi. In tal modo la base può trasformare il
reattivo in un nucleofilo più forte per estrazione di un protone (R-NH2 a
R-NH-).
Aldeidi
Stato fisico
R
C O
H
Benché siano composti polari non possono dare
legami idrogeno, per cui hanno punti di fusione
(p.f.) più bassi rispetto agli acidi corrispondenti.
Sono generalmente caratterizzate da un odore
gradevole.
Aldeidi
Solubilità
R
C O
H
Le aldeidi inferiori sono molto solubili in acqua, a
causa dei legami idrogeno che intercorrono fra le
molecole di soluto e di solvente.
Reazioni di identificazione
a) Formazione di ossime
-
O
R
R
C O +
: NH2OH
C +
H
N
R'
OH
H
R'
+
OH2
R
C
N:
R'
H
- H2O
H
R
C
R'
N
+
OH
OH
R
H
C
N
R'
- H+
+
H
OH
C
N
R
OH
R'
OH
La reazione avviene in due stadi:
1. attacco nucleofilo dell'idrossilammina al carbonio carbonilico;
2. disidratazione dell'addotto con idrossilammina (catalizzata dagli
acidi).
La formazione di ossime può anche essere catalizzata da basi (in
genere si usa piridina).
Reazioni di identificazione
b) Formazione di 2,4-dinitrofenilidrazoni
Consiste nel trattare la sostanza con una soluzione di 2,4dinitrofenilidrazina in acido acetico. Si ha un precipitato di colore dal
giallo al rosso.
NO2
NO2
R
O2N
NH NH2 +
C O
R'
- H2O
R
O2N
NH N C
R'
pp giallo o arancio
La reazione non viene condotta con idrazina in quanto questa
molecola ha due atomi di azoto nucleofilo che possono reagire con
due molecole di composto carbonilico, portando alla formazione delle
azine, prodotti di più difficile cristallizzazione.
c) Reazione di Fehling
Questa reazione è data delle aldeidi
alifatiche, dagli -ossichetoni e dagli
zuccheri riducenti.
R
O
H
+
2 Cu++ + 4 OH-
R
O +
HO
2 H2O + Cu2O rosso mattone
d) Reazione di Tollens
La reazione viene data dalle aldeidi, dagli -ossichetoni,
dagli zuccheri riducenti, dai poliidrossifenoli, dagli
amminofenoli e da altri composti riducenti.
Il reattivo di Tollens è costituito da una soluzione acquosa
di nitrato d’argento ammoniacale, che si prepara al
momento dell’uso mescolando AgNO3, insieme a NaOH e
NH4OH
d) Reazione di Tollens
2 AgNO3 + 2 NaOH
Ag2O + 2 NaNO3+ H2O
2 [Ag(NH3)2]+ OH-
Ag2O + 4 NH3+ H2O
rid.
2 Ag + 4 NH3+ H2O
R
2 [Ag(NH3)2]OH +
C O
H
R COOH + 2 Ag
+ 4 NH3 + H2O
e) Reazione con dimedone
Il dimedone (5,5-dimetilcicloesan-1,3-dione) è un reattivo specifico
per le aldeidi.
La reazione consiste in una condensazione fra due molecole di
dimedone e una di aldeide, che porta alla formazione di un solido che
può essere impiegato anche come derivato cristallino delle aldeidi.
O
O
R
+
2
O
C O
H
H2O
R
C
H
O
OO
Esecuzione pratica del saggio:
50 mg di aldeide solubilizzati in etanolo vengono fatti reagire con 5 gocce di
una soluzione al 5% di dimedone in etanolo. Il saggio è positivo se entro 5'
si osserva la formazione di un precipitato bianco.
Derivati cristallini dei composti carbonilici
Azometine o Basi di Schiff
Sono i prodotti che derivano dalla reazione dei composti
carbonilici con le ammine.
Non sempre è conveniente sintetizzarle per il
riconoscimento, in quanto sono derivati bassofondenti e
sono solubili negli stessi solventi dei prodotti di partenza.
H3CO
H3CO
+
H
HO
CHO + H2N
NO2
HO
C
H
N
NO2
Derivati cristallini dei composti carbonilici
Derivati idrazonici (vd reazioni di riconoscimento)
I derivati idrazonici vengono generalmente cristallizzati da
etanolo.
Oltre ai derivati ottenuti con la 2,4-dinitrofenilidrazina si
possono utilizzare anche quelli ottenuti con fenilidrazina e
p-nitrofenilidrazina.
Derivati cristallini dei composti carbonilici
Derivati con semicarbazide e tiosemicarbazide
R
C O
R'
+
O
H2N NH C NH2
R
C N
O
NH C NH2
R'
Esecuzione pratica del saggio:
Per l'ottenimento dei semicarbazoni si opera come per i derivati idrazonici.
I tiosemicarbazoni si ottengono facendo reagire una soluzione di 0,2 g di
tiosemicarbazide in 2 ml di acqua con una soluzione dell'aldeide in acqua,
alcool o acido acetico. Si lascia riposare per una notte e quindi si scalda a
bagnomaria per 1h e si lascia raffreddare. Si forma un precipitato che si filtra e
si cristallizza da acqua, alcool o da miscela idroalcolica.