Aldeidi e chetoni
Brosolo e Not
Gruppo funzionale
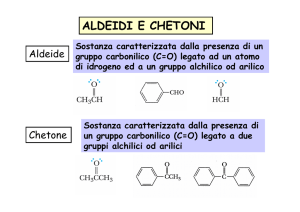
Aldeidi e chetoni sono composti contenenti entrambi il gruppo carbonile C=O, che è
molto polarizzato.
Struttura molecola
Nelle aldeidi il carbonile è legato a un idrogeno e al carbonio di un radicale
alchilico R (o arilico Ar).
Nei chetoni il carbonile è legato a due atomi di carbonio di gruppi alchilici (o
arilici).
Nomenclatura
Il nome degli aldeidi si ottiene aggiungendo al nome dell'idrocarburo corrispondente la
desinenza —ale.
Il nome dei chetoni si ottiene aggiungendo al nome dell'idrocarburo corrispondente la
desinenza —one.
Esempi di molecole
Le due aldeidi più comuni della serie alifatica sono il metanale HCHO (aldeide formica)
e l'etanale CH3—CHO (acetaldeide). Il metanale è un gas, di odore pungente, usato
come germicida e disinfettante, solubile in acqua (la sua soluzione acquosa è la
cosiddetta formalina). L'etanale è usato, tra l'altro, per la preparazione di acido
acetico e delle resine fenoliche e ureiche.
Un esempio di chetone è il fruttosio C6H12O6. E' importante nella nutrizione umana e
animale, spesso usato come dolcificante e nell'industria alimentare di dolci e
panificati. In natura si presenta, solido o in soluzione liquida, nella maggior
parte dei frutti zuccherini e dei loro relativi succhi, quindi nel miele, e in
percentuale più
bassa, in diversi vegetali, ad esempio la barbabietola da zucchero o
la canna da zucchero. Il fruttosio è il più dolce tra tutti i tipi di zuccheri.
Proprietà chimiche
A causa della differenza di elettronegatività tra carbonio e ossigeno, il doppio legame
C=O è polare con una parziale carica negativa sull’ossigeno e una parziale carica
positiva sul carbonio. Nelle reazioni dei gruppi carbonilici, il carbonio si
comporta da elettrofilo e da acido di Lewis mentre l’ossigeno da nucleofilo e da
base di Lewis.
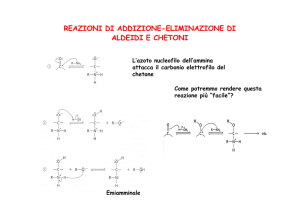
Poiché i gruppi carbonilici delle aldeidi e dei chetoni interagiscono con le molecole
d’acqua mediante la formazione di legami idrogeno, le aldeidi e i chetoni a basso
peso molecolare sono più solubili in acqua rispetto ai composti non polari di peso
molecolare paragonabile.
Proprietà fisiche
A causa della polarità del gruppo carbonilico, le aldeidi e i chetoni sono composti
polari e allo stato liquido mostrano interazioni dipolo-dipolo. Per questo motivo
hanno punti di ebollizione più alti dei composti non polari di peso molecolare
paragonabile.
Reazioni
Le aldeidi si ottengono per ossidazione di un alcol primario, per esempio con anidride
cromica (CrO3) in presenza di piridina, oppure dai cloruri degli acidi
corrispondenti per riduzione catalitica.
I chetoni si ottengono per ossidazione di un alcol secondario con CrO3, oppure dagli
alchini per addizione di acqua.
1. Reazioni di addizione nucleofila:
Addizione di H2 (riduzione). Le aldeidi danno alcoli primari, i chetoni danno alcoli
secondari. La riduzione si effettua per riscaldamento con un riducente, come
l’idruro di litio e alluminio (LiAlH4) o l’idruro di sodio e boro (NaBH4). In
questi casi, lo ione idruro (H–) funge da nucleofilo. Un altro possibile processo
di riduzione è l’idrogenazione catalitica:
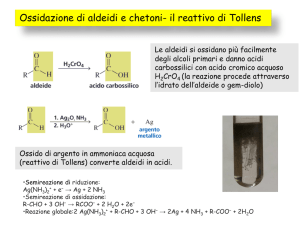
2. Reazioni di ossidazione:
Le aldeidi si ossidano facilmente ad acidi carbossilici; i chetoni, invece, si ossidano
solo in condizioni drastiche (ossidanti energici a caldo), con rottura di un legame
carbonio – carbonio e formazioni di acidi carbossilici con catena più corta. Per
esempio, il bicromato di potassio ossida l’etanale ad acido etanoico, ma non
ossida l’acetone.
3. Reazioni di condensazione:
Due molecole di aldeidi o due molecole di chetoni possono dare luogo a condensazione
aldolica con formazione rispettivamente di un’idrossialdeide o di un
idrossichetone: