Composti carbonilici
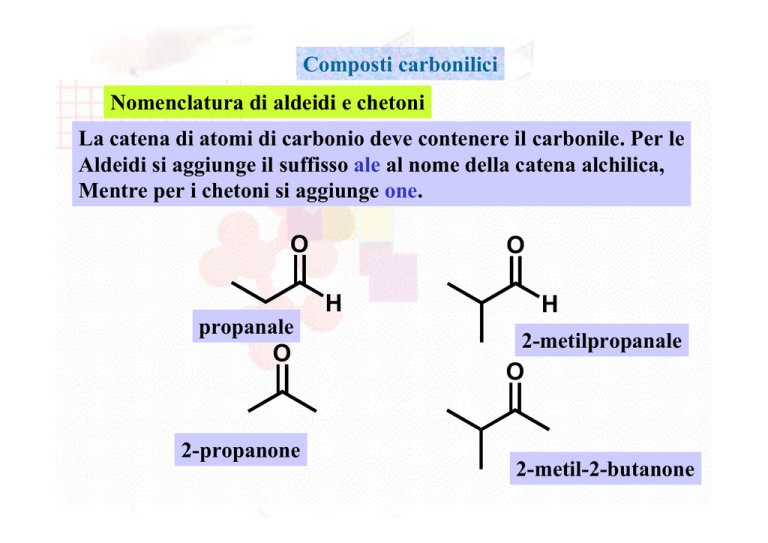
Nomenclatura di aldeidi e chetoni
La catena di atomi di carbonio deve contenere il carbonile. Per le
Aldeidi si aggiunge il suffisso ale al nome della catena alchilica,
Mentre per i chetoni si aggiunge one.
O
O
H
propanale
O
2-propanone
H
2-metilpropanale
O
2-metil-2-butanone
Composti carbonilici
Quando un chetone è un sostituente in catena si riferisce ad esso
come gruppo osso.
O
O
5
1 H
esanale
5-ossoesanale
Mentre quando l’aldeide è il sostituente di un anello ci si riferisce
ad essa come carbaldeide
O
H
cicloesancarbaldeide
Composti carbonilici
Se il gruppo carbonilico viene considerato il sostituente in una catena
ci si riferisce come gruppo acilico ed il nome è formato dal suffisso il.
Alcuni esempi…
O
O
H
Me
formil
acetil
O
benzoil
Struttura di un carbonile
O
O
H
H
cinnamaldeide
benzaldeide
O
C6H13
O
Vitamina K
O
canfora
CHO
O
OMe
OH
vanillina
carvone
O
jasmone
Composti carbonilici
I composti carbonili sono elettrofilici
O
O
O
δ
δ
Più reattiva un aldeide o un chetone??
Composti carbonilici
Nu:
Nu:
Le aldeidi sono più reattive perché i sostituenti alchilici
sono gruppi donatori che diminuiscono la parziale carica
positiva sul carbonio carbonilico. La minore reattività dei
chetoni deriva anche da un maggior ingombro sterico.
Composti carbonilici
Reazioni di aldeidi e chetoni
Un meccanismo generale
O
H2Nu
Due possibilità….
Nu
Me
+
H2O
Me
Me
O
Me
O
Nu
HO
Me
Nu
Me
Composti carbonilici
Reazioni di aldeidi e chetoni
Idratazione dei composti carbonili…il nucleofilo è l’acqua
O
O
Me
Me
H2O
O
Me
H
O
Me
H
O
Me
H
HO
Me
Me
H
O
Me
Composti carbonilici
Reazioni di aldeidi e chetoni
Reazione con HCN, formazione di cianidrine
O
O
Me
Me
CN-
HO
Me
Me
CN
Me
Me
CN
Composti carbonilici
Reazioni di aldeidi e chetoni
O
Reazione con alcoli:
formazione di acetali
e chetali
H
Me
Me
O
Me
O
+
Me
ROH
ROH
Me
Me
H
H
HO
Me
R
O
Me
H
HO
emiacetale
Me
Me
OR
Ma la reazione di
Equilibrio può…..
Composti carbonilici
H
HO
Me
+
H
Me
OR
O
Me
H
Me
OR
O
R
Me
Me
ROH
RO
Me
Me
OR
RO
Me
R
O
Me
H
Si forma un chetale (acetale se si fa reagire
un aldeide)
Composti carbonilici
O
Esempi….
H
MeOH/H+
HOCH2CH2OH/H+
O
O
CH3CH2OH/H+
Composti carbonilici
Addizione di ammine
O
O
Me
Me
Me
Me
NH2R
H
N
R
H
O
Me
H
Me
NR
HO
Me
H
Me
NR
Ancora una volta le reazioni sono di equilibrio.
La reazione prosegue…
Composti carbonilici
H
HO
Me
H
H
H+
Me
NR
Me
Me
NR
O
H
Me
Me
N R
H
Me
Me
N
R
Un immina
Composti carbonilici
Esempi……
O
NH2CH2CH3
Me
Me
NH2
O
Me
Me
O
Me
NH2OH
Me
Composti carbonilici
Riduzioni di aldeidi e chetoni.
O
LiH3AlO
Me
Me
Me
H
H
Li
H Al
Me
H
H
HO
Na H
H B
H
Me
H
Me
H
Me
Me
O
NaH3BO
Me
H
Me
Immine nelle trasformazioni Biologiche
Il meccanismo della Visione
O
retinale
Enzima
H
H
N2H
H
O
N
H
O
opsina
rodopsina
Luce
N
H
rodopsina
rodopsina
N
H
rodopsina
Coenzimi ed ammine . Il piridossale
O
O
R
NH2
NH2
O
OH
HO
N
Me
+
OH
R
O
N
O
OH
OH
R
R
N
OH
HO
N
Me
OH
HO
H O
H
OH
N
OH
HO
N
Me
Me
Coenzimi ed ammine . Il piridossale
O
OH
R
NH2
OHC
OH
HO
N
Me
Ossidazioni e riduzioni:
O
H H O
NH2
N
O
O P O
H
O
O
riduzione
H
H
OH HO
NH2
O
NAD
O
H
H
OH HO
O
N
ossidazione
H
H
NH2
N
H
H
OH HO
H
N
N
H
N
O
O P O
H
N
O P O
O
NH2
O P O
O
N
N
H
O
N
H
H
OH HO
NADH
H
Ossidazioni e riduzioni:
O
H3C
Enzima
H OH
H3C
COOH
COOH
H H O
NH2
H3C
N
R
COOH
O
H
H
R N
O
H2N
H
riduzione
O
H3C
H3C
N
H3C
FAD
N
NH
NH
N
N
CH2
H
OH
H
OH
H
OH
H2C
O
O P O
O
O P O
O
O
H3C
O
ossidazione
NH2
N
N
N
H
O
N
H
H
OH HO
N
N
CH2 H
H
OH
H
OH
H
OH
H2C
O
O P O
O
O P O
O
H
FADH
O
NH2
N
N
N
H
O
N
H
H
OH HO
H
Ossidazioni e riduzioni:
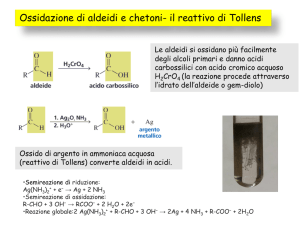
Le aldeidi si ossidano facilmente
O
R
O
H
H
R
O
O
O
H
Ag(NH3)2 OH
Come avvengono le ossidazioni?
O
Metodi di ossidazione .Cromo
Ossidazione alcoli
HO
O
R
R
L’ossidazione ad alcoli è un processo che coinvolge due elettroni.
Si possono ottenere anche acidi.
+ 3e-
Cr+3
1.10V
Cr2O72- + 14H+ + 6e-
Cr+3
1.33V
Cr+3
1.19V
Cr
-
+6
+
HCrO4 + 7H + 3e-
Ossidazione in acqua!
Condizione diluite portano alla presenza di dicromato…
Meccanismo ossidazione: Reazione a stadi
R2CHOH + Cr+6
R2CHOH + Cr+4
.
R CH-OH + Cr
2
+6
R2CHOH + Cr+5
R2C=O + Cr+4
.
R CH-OH + Cr
2
+3
R2C=O + Cr+5
R2C=O + Cr+3
L’ossidazione comincia con la formazione di un estere cromico.
Lo stadio che sposta l’equilibrio è la formazione del Cr+4.
Come avviene la reazione? Si possono proporre dei meccanismi?
R
R
R
O
CrO3H
O
R
H
H 2O
O
R
OH
Cr
R
O
O
H
H
HO
H
R
O
OH
OH
Cr
O
R
H
H
OH
O
R
Cr
O
R
H
OH
O
MnO2
Il biossido di Manganese è un ossidante potente, capace di ossidare
alcoli a Chetoni.
Di norma è impiegato per alcoli allilici, o benzilici (aromatici).
Il metodo di preparazione influenza le proprietà ossidanti
MnO2
O
O Mn
OH
OH
O
HO
Mn
HO
OH
O Mn
OH