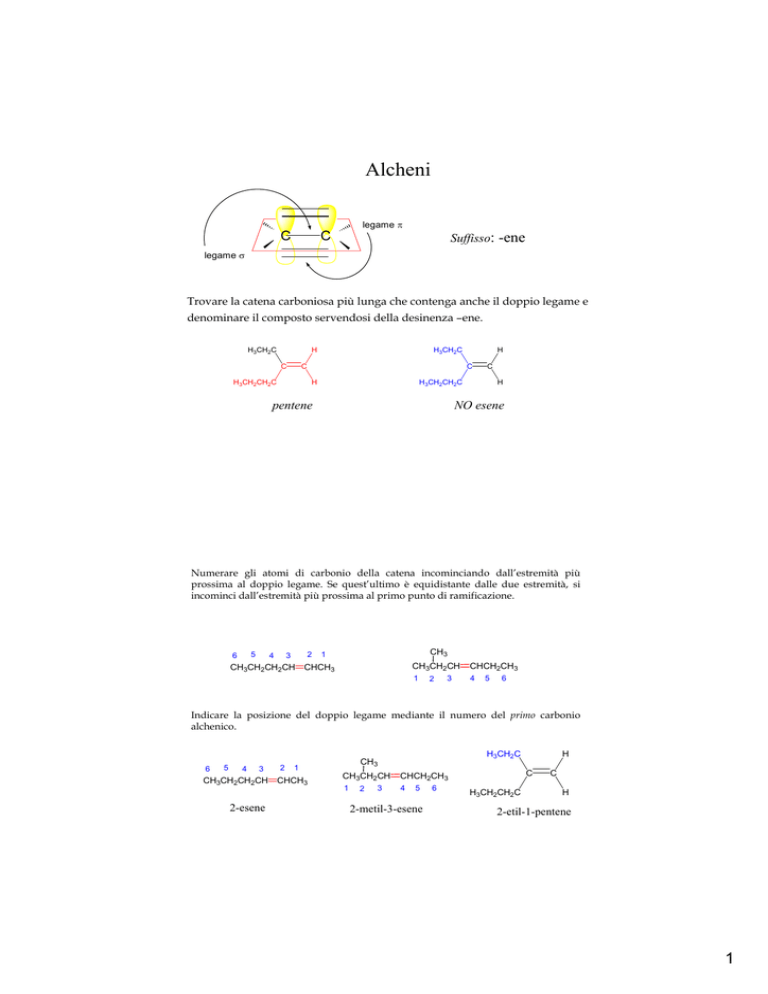
Alcheni
C
legame π
C
Suffisso: -ene
legame σ
Trovare la catena carboniosa più lunga che contenga anche il doppio legame e
denominare il composto servendosi della desinenza –ene.
H3CH2C
C
H
H3CH2C
H
H3CH2CH2C
C
H
C
H3CH2CH2C
pentene
C
H
NO esene
Numerare gli atomi di carbonio della catena incominciando dall’estremità più
prossima al doppio legame. Se quest’ultimo è equidistante dalle due estremità, si
incominci dall’estremità più prossima al primo punto di ramificazione.
5
6
4
2
3
CH3
1
CH3CH2CH2CH CHCH3
CH3CH2CH
CHCH2CH3
1
4
2
3
5
6
Indicare la posizione del doppio legame mediante il numero del primo carbonio
alchenico.
6
5
4
3
2
1
CH3CH2CH2CH CHCH3
2-esene
H3CH2C
CH3
CH3CH2CH
CHCH2CH3
1
4
2
3
5
2-metil-3-esene
6
H
C
H3CH2CH2C
C
H
2-etil-1-pentene
1
In maniera simile si denominano i cicloalcheni, non esistendo però in essi il punto
di inizio di una catena, si denominano in modo che il doppio legame si trovi tra
C1 e C2 e che il primo sostituente abbia il più piccolo numero possibile.
H3C
H3C
1-metilcicloesene
CH3
1,5-dimetilciclopentene
CH2=
CH2=CH-
metilene
vinile
CH2=CH-CH2allile
Isomeria cis-trans negli alcheni
H3C
H
CH3
H
cis-2-butene
H3C
H
H
CH3
trans-2-butene
Cl
H
H
H
H
Cl
Cl
Cl
trans-1,2-dicloroetene
L'isomeria cis-trans può verificarsi ogni qual volta
entrambi gli atomi di carbonio del doppio legame
siano congiunti con due gruppi differenti. Se, però, uno di
tali atomi di carbonio è legato a due gruppi
identici, l'isomeria cis-trans non è possibile.
cis-1,2-dicloroetene
2
Regole di successione: notazione E, Z
ATLA
ALTA
ASSAB
ATLA
BASSA
BASSA
ASSAB
ALTA
Z
E
Il sistema di nomenclatura E, Z si basa su regole di successione che assegnano la priorità ai gruppi
sostituenti congiunti con un doppio legame. Se i gruppi a priorità più alta presenti sull'uno e sull'altro
carbonio si trovano dalla stessa parte del doppio legame, l'alchene si designa Z ( = insieme). Se
i gruppi a priorità più alta si trovano da parti opposte l'alchene si designa E (= opposto).
H
alta
CH3
H3C
Cl
Cl alta
H
alta
alta
H3C
(Z)-2-cloro-butene
CH3
(E)-2-cloro-butene
Assegnate la configurazione E, Z ai seguenti alcheni:
H3C
CH2OH
H3CH2C
Cl
CH2CH3
H3CO
Cl
CH2CH2CH3
Z
E
H3C
COOH
CH2OH
Z
H
CN
H3C
CH2NH2
E
3
Gli alcheni si comportano da nucleofili. Il doppio legame carbonio-carbonio è ricco di elettroni e può
donarne una coppia ad un elettrofilo nel corso di una reazione di addizione elettrofila.
Addizione di HX (acidi alogenidrici) agli alcheni
H3C
H
H
δ+
H
+
H3C
H3C
H
H3C
H
2-metilpropene
H
H3C
H
carbocatione intermedio
l'elettrofilo H+ è attaccato dagli elettroni
π del doppio legame e si forma un nuovo legame semplice
C-H. Ciò lascia sull'altro atomo di carbonio una carica +
(carbocatione) e un orbitale p vuoto.
H
Br
Br -
H3C
δ−
Br
H
il carbocatione intermedio è esso stesso
un elettrofilo in grado di accettare
una coppia di elettroni dal nucleofilo ione bromuro,
formando così un legame C-Br
e, di conseguenza un prodotto di addizione neutro.
Regola di Markovnikov: nell’addizionarsi di HX ad un alchene H si lega al carbonio che
reca il minor numero di sostituenti ed X al carbonio che reca il maggior numero di
sostituenti.
Quale prodotto vi attendereste dalla reazione fra l’HCl e l’1-metilcicloesene?
Due alchili sul carbonio 1
1
2
H 3C
un alchile sul carbonio 2
H
1-metilcicloesene
Secondo la regola di Markovnikov l’idrogeno dovrebbe addizionarsi al carbonio del doppio legame
che reca un alchile e il cloro a quello che ne reca due.
+
H3C
H
1-metilcicloesene
δ+
H
Cl -
δ−
Cl
H
H3C
H
carbocatione intermedio
Cl
H3C
H
H
1-cloro-1-metilcicloesano
4
Quale prodotto vi attendereste dalla reazione fra l’HBr e il 2-pentene?
H3CH2C
CH3
un alchile sulcarbonio 2
un alchile sul carbonio 3
H
H
Essendo le estremità del doppio legame caratterizzate da una sostituzione della stessa entità,
il prodotto è una miscela.
H
Br
H3CH2C
H3CH2C
H
CH3
+
H
CH3
δ+
δ−
H
Br
H
H3CH2C
H
CH3
H
H
carbocatione 2°
H
H
H
CH3
H3CH2C
H
Br
CH
H3CH2C
H
3
H
H
carbocatione 2°
Dato che nelle reazioni di addizione elettrofila si invocano come intermedi i carbocationi, una
versione alternativa della regola di Markovnikov è che, nell’addizione di HX all’alchene, tende
a formarsi di preferenza come intermedio il carbocatione maggiormente sostituito.
H
R
R
R
C
più stabile
R
C
R
R
terziario
H
>
secondario
H
H
C
H
>
primario
C
H
>
metile
meno stabile
La stabilità dei carbocationi aumenta con l’aumentare del numero dei sostituenti: i
carbocationi maggiormente sostituiti sono più stabili.
5
Durante la reazione di HX con un alchene possono aver luogo trasposizioni strutturali.
H
CH3
H
CH3
H
H
+
H
CH3
H
CH3
H
H
Cl
H
H
trasposizione
H
di idruro
H
CH3
H
3-metil-1-butene
H
carbocatione 2°
Il carbocatione intermedio secondario
formatosi per protonazione del 3-metil1-butene si riordina (traspone) nel più
stabile carbocatione terziario mediante
uno spostamento di idruro.
CH3
H
carbocatione 3°
Cl
H
Cl
CH3
H
H
CH3
H
H
Cl
CH3
CH3
H
Cl
H
H
H
2-cloro-3-metilbutano
H
2-cloro-2-metilbutano
N.B. la trasposizione del carbocatione può anche avvenire mediante spostamento di un gruppo
alchilico insieme con la sua coppia di elettroni. Vedi esempio successivo
Quali prodotti sono sintetizzati dalla reazione fra l’HBr e il 3,3-dimetilbutene? Quale
avrà maggiore stabilità?
H
CH3
H
CH3
H
CH3
+
H
CH3
H
CH3
H
CH3
Br
H
trasposizione
H
CH3
di metiluro H
H
3,3-dimetil-1-butene
CH3
H
H
carbocatione 2°
carbocatione 3°
Br
H
Br
CH3
H
CH3
H
CH3
Br
CH3
H
2-bromo-3,3-dimetilbutano
H
CH3
H
CH3
H
Br
H
CH3
2-bromo-2,3-dimetilbutano
+ Stabile
6
Quali prodotti sono sintetizzati dalla reazione fra l’HBr e l’1-metil-1-vinilciclobutano?
Quale avrà maggiore stabilità?
CH3
CH3
H+
H
C
CH2
CH3
Br-
H
C
Br
CH
CH3
CH3
i carbocationi possono riarrangiarsi anche attraverso un'espansione d'anello,
un altro shift-1,2.
CH3
CH3
Br
BrCH3
CH3
l'espansione ad anello porta ad un carbocatione più stabile e alla
formazione di un anello a cinque termini con minore tensione
angolare dell'anello a quattro termini.
Stereochimica delle reazioni di addizione elettrofila di acidi alogenidrici agli alcheni
Quando un reagente che non presenta carboni asimmetrici subisce una reazione che porta alla
sintesi di un prodotto con un carbonio asimmetrico, il prodotto sarà una miscela
Cl racemica.
H
Cl
H
H
H
H
H3CH2C
(S)
Cl
H
CH3
H3CH2C
H3CH2C
CH3
+
H
CH3
H3CH2C
(R)
Cl
Se una reazione porta alla formazione di un carbonio asimmetrico in un composto che già ne
presenta uno, si formerà una coppia di diastereoisomeri.
diastereoisomeri
Br
H
Cl
C
H
Cl
Cl
Br
H
H
C
H
C
H3C
(R)-3-cloro-1-butene
H
H
H3C
C
C
H
CH3
+
H
H3C
C
C
Br
CH3
(2R,3R)-2-bromo-3-clorobutano (2S,3R)-2-bromo-3-clorobutano
7
Se, come risultato di una reazione di addizione che passa attraverso un intermedio
carbocationico, si creano due carboni asimmetrici, si ottengono come prodotti della reazione
quattro stereoisomeri.
CH2CH3
CH2CH3
H3CH2C
+ H
Br
Br
CH3
H3C
H
C
*C
CH2CH3
*
CH3
CH3
3-bromo-3,4-dimetilesano
(Z)-3,4-dimetil-3-esene
Formule prospettiche degli stereoisomeri del prodotto
H3C
H
H3CH2C
CH2CH3
C
C
H3CH2C
Br
Br
H3C
CH3
C
CH3
C
H
CH2CH3
H3CH2C
H3C
Br
C
H3C
CH3
C
H
CH2CH3
H
H3CH2C
C
CH2CH3
C
CH3
Br
Proiezioni di Fisher degli stereoisomeri del prodotto
CH2CH3
CH2CH3
H3C
Br
Br
CH3
H3C
H3C
H
H
CH3
H
CH2CH3
CH2CH3
CH2CH3
CH2CH3
Br
CH3
CH2CH3
Br
H3C
CH3
H
CH2CH3
Prevedete i prodotti delle seguenti reazioni
…da svolgere!
A
+
HCl
+
B
HBr
CH2
C
+
KI
H3PO4
N.B. Anche HI si addiziona agli alcheni
ma anziché servirsi direttamente di HI
conviene generare HI nella miscela
reattiva mescolando acido fosforico e
ioduro di potassio.
8
Da quali alcheni partireste per preparare i seguenti alogenuri alchilici?
…da svolgere!
a) bromociclopentano;
b) 1-iodo-1-etilcicloesano;
c) 1-cloro-1-metilciclopentano;
d) 2-iodo-2-metilpropano.
Addizione degli alogeni agli alcheni
H3 C
H
H3 C
H
+
δ+
Br
δ−
Br
H3 C
H3 C
H
Br
2-metilpropene
la coppia di elettroni del doppio legame attacca il bromo
polarizzato positivamente formando
uno ione bromonio ciclico a tre termini
H
Br -
Br
H
H3 C
H
H3 C
Br
lo ione bromuro reagisce con questo intermedio
a ponte dal lato opposto a quello occupato dallo
ione bromonio (addizione anti)
per dare il dibroalcano.
In che senso la formazione dello ione bromonio giustifica la stereochimica anti dell’addizione
all’alchene? In un simile intermedio si può immaginare che l’atomo di bromo “schermi” una
faccia della molecola, sicché l’attacco dello ione bromuro – nello stadio successivo – potrebbe
avvenire solo sull’altra faccia fornendo il prodotto anti.
9
Se in seguito ad una reazione di addizione che presenta come intermedio uno ione alonio ciclico si
formano due carboni asimmetrici, si formerà un’unica coppia di enantiomeri.
Br
H3C
CH2CH3
(R)
H3C
Br
CH2CH3
C
+
C
Br
CH2CH3
Br
H
Br
C
(R)
H
H
+
C
H
H
H
H3C
Br
C
Br
CH2CH3
H
(S)
cis-2-pentene
C
H3C
C
(S)
H
Br
Dal cis-2-pentene si formano gli enantiomeri (2R,3R)-2,3-dibromopentano e (2S,3S)-2,3-dibromopentano
Br
H3C
H3C
Br
H
C
+
C
Br
H3C
Br
H
C
H
H
(S)
CH2CH3
+
CH2CH3
CH2CH3
C
Br
C
H
H
(R)
Br
H
Br
trans-2-pentene
(S)
C
H3C
C
CH2CH3
(R)
H
Br
Dal trans-2-pentene si formano gli enantiomeri (2R,3S)-2,3-dibromopentano e (2S,3R)-2,3-dibromopentano
L’alogenazione degli alcheni è una reazione stereospecifica. Una reazione si definisce stereospecifica quando
ognuno dei due specifici stereoisomeri del materiale di partenza fornisce un determinato stereoisomero del
prodotto.
L’alogenazione del 2-butene determina la sintesi di prodotti in cui ciascuno dei due atomi di carbonio asimmetrici
lega a sè gli stessi quattro sostituenti.
H3 C
CH 3
+
H
δ+
Cl
δ−
Cl
H3 C
H
H
CH3
Cl
Cl -
H
Cl
CH3
H3 C
H
H
Cl
H3 C
+
Cl
H
Cl
CH 3
H
cis-2-butene
ENANTIOMERI
L’alogenazione del cis-2-butene fornisce due enantiomeri.
H3 C
H
+
H
δ+
Cl
δ−
Cl
CH 3
H3 C
H
H
Cl
Cl -
CH 3
Cl
H3C
H
H
H3 C
CH3
Cl
+
Cl
H
H
Cl
CH3
trans-2-butene
singolo composto meso achirale
L’alogenazione del trans-2-butene fornisce un composto meso achirale.
Per disegnare i prodotti dell’alogenazione:
- Addizionate Cl2 in modo anti sui due lati del doppio legame, lasciando tutti gli altri gruppi nella loro
orientazione originale. Disegnate i prodotti in modo che un determinato atomo di Cl si trovi al di sopra del piano
in un prodotto e al di sotto nell’altro.
10
Disegnate tutti gli stereosomeri che si formano nella seguente reazione:
CH3
(R)
+
Br
Br
CH3
CH3
Br
δ+
Br
δ−
Br
(R)
(R)
(R)
(R)
Br
CH3
CH3
Br-
(R)
Br
+
(S)
(S)
Br
Br
Br
Br
Sintesi di aloidrine
H
CH3
+
H3C
H
Br
Br
H2O
H
CH3
H
CH3
H3C
H
H3C
H
O
H
H
2-butene
Br -
la reazione dell'alchene con una molecola di
bromo fornisce un intermedio a carattere di
ione bromonio.
Br
CH3
H
H
H3C
OH
+
HBr
3-bromo-2-butanolo
l'acqua si comporta da nucleofilo impiegando
una coppia di elettroni solitaria per
aprire lo ione bromonio e formare un legame con il carbonio.
Donando i suoi elettroni, l'ossigeno acquista una carica +.
La perdita di un protone da parte dell'ossigeno fornisce poi
HBr e la bromoidrina.
11
Addizione di acqua agli alcheni (idratazione)
H
H
H
CH3
H
CH2CH3
+
H2O
H
H2O
H
CH3
H
CH3
H
CH2CH3
H
CH2CH3
O
H
H
2-metil-1-butene
La reazione dell'alchene con
acqua è catalizzata da acidi.
Essa fornisce un intermedio a carattere carbocationico.
L'addizione di acqua segue la regola di Markovnikov.
Base
H
H
H
CH3
CH2CH3
OH
Quali sono le coppie di alcheni che, tramite una reazione di idratazione acido
catalizzata, formano come prodotto principale ognuno dei seguenti alcoli?
CH3
a.
H3C
C
CH2CH2CH3
OH
CH3
H3C
H+
CHCH2CH3
C
CH3
H3C
C
CHCH2CH3
H
O
CH3
H2C
C
H+
CH2CH2CH3
H
H2C
CH2CH2CH3
H
H2C
CHCH2CH3
CH3
C
H
H
H3C
CH2CH2CH3
C
CHCH2CH
3
OH H
H
H
H
H2C
CH3
C
CH2CH2CH3
OH
O
O
H
H
CH3
C
C
O
H
H
CH3
CH3
H3C
H
12
CH3
b.
OH
H
H
CH2
H
H+
CH2
CH2
CH2
H
OH
O
O
H
H
H
H
H O
CH3
H+
CH3
CH3
CH3
H
OH
O
H
H
H
H
Ossidazione di un alchene a glicole
H
CH3
+
(H3C)2HC
Alcuni metalli di transizione nei loro stati di ossidazione più alti, particolarmente
il Mn (VII), sono efficaci agenti ossidanti e convertono l'alchene in glicole. Un
glicole o diolo vicinale è un composto con gruppi ossidrilici su carboni adiacenti.
KMnO4
CH2CH3
H
CH3
(H3C)2HC
CH2CH3
O
H
CH3
(H3C)2HC
CH2CH3
O
O
O
O
Mn
O
O
H
H2O
CH3
(H3C)2HC
CH2CH3
HO
+
MnO2
OH
Mn
O
L'ossidazione di un alchene è una reazione stereoselettiva:
essa porta ad un addizione sin di gruppi -OH al doppio legame C-C.
In un'addizione sin entrambi i gruppi sono addizionati dallo stesso lato o faccia del doppio legame.
13
Quali prodotti sono sintetizzati dalla reazione fra OsO4 e il ciclopentene?
+
Il tetrossido di osmio reagisce con gli alcheni fornendo con alte rese gli
1,2-dioli. Anche in questo caso prende corpo un intermedio ciclico che si
scinde, poi,a dare il diolo cis.
OsO4
H2O
O
O
O
HO
O
OsO2
OH
Os
Os
O
O
+
O
O
Essendo un'addizione sin, l'ossidazione si può realizzare su entrambe le facce della molecola. Ne segue che possono
essere sintetizzati entrambi i prodotti cis:
oppure
HO
OH
HO
OH
14












