Le basi del calcolo statistico
equilibrio statistico di N particelle su n stati possibili:
• descrizione del sistema: individuare gli stati possibili (microstati),
mediante i relativi numeri quantici
• calcolare l’energia Ei dell’i-esimo stato
• calcolare la degenerazione gi dell’i-esimo stato
• calcolare la probabilità di una certa partizione, cioè in quanti modi
si possono disporre Ni particelle sugli n stati conservando l’energia totale a
disposizione (probabilità di una certa partizione di stati)
• ipotesi: tutti i microstati accessibili sono egualmente probabili
Esempio: microstati accessibili a particelle di
massa m in una scatola cubica di lato L
1
( p x2 p 2y p z2 ) ; H ( x, y, z ) E ( x, y, z )
2m
H
Microstati e macrostati
L
( x, y , z ) sen( k x x ) sen( k y y ) sen( k z z )
π
π
π
m x ; k y m y ; kz mz
L
L
L
1
1
2
2
3
3
2
3
1
3
1
2
3
2
3
1
2
1
6
6
E6
N6
5
E5
N5
2
2
2
1
4
E4
N4
1
1
3
1
3
1
3
1
1
3
3
E3
N3
1
2
2
2
1
2
2
2
1
3
2
E2
N2
1
1
2
1
2
1
2
1
1
3
livello energetico: Ei
1
E1
N1
1
1
1
degenerazione : gi
i
mz
gi
kx
2 2
E
( k x k 2y k z2 )
2m
E
π 2 2
2
(
m
x
2
2mL
m 2y
mz2 )
E Eo (mx2 m2y mz2 )
numeri quantici: mx my
numero di occupazione: Ni
mz
1
mx my
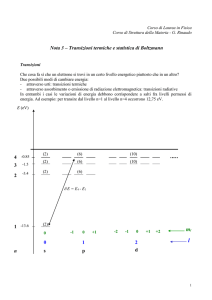
Livelli energetici
Esempio: un “gas” di elettroni in un cubo di lato 10-6 m
E o
π 2 (c) 2
2mc2 L2
10 (2 10 7 eVm ) 2
2 0,5 106 eV 1012 m 2
E1= Eo (1+1+1)=3Eo = 1,2 10-6 eV
E2= Eo (4+1+1)=6Eo = 2,4 10-6 eV
E3= Eo (4+4+1)=9Eo = 3,6 10-6 eV
E4= Eo (9+1+1)=11Eo = 4,4 10-6 eV
E5= Eo (4+4+4)=12Eo = 4,8 10-6 eV
E6= Eo (9+4+1)=14Eo = 5,6 10-6 eV
4 10 7 eV
conteggio statistico secondo Boltzmann
Esempio:
probabilità della partizione
Wi= numero di modi in cui si possono
disporre Ni particelle sul livello i
N ( N 1)( N 2)( N 3)
N!
W1
4!
N1! ( N N1 )!
W2
( N N1 )!
N
g2 2
N 2!( N N1 N 2 )!
N
gi i
W N! i
N i!
si cerca il massimo di lnW con i vincoli
sul numero totale N di particelle e
l’energia totale E (massimo vincolato):
ln W ln N ! i Ni ln gi i Ni !
i N i N
i Ni Ei E
N1=4
N2=3
N3=5
N4=3
N5=4
N6=2
1
1
2
2
3
3
2
3
3
1
1
2
3
2
1
3
2
1
6
6
E6
N6
5
E5
N5
2
2
2
1
4
E4
N4
1
1
3
1
3
1
3
1
1
3
3
E3
N3
1
2
2
2
1
2
2
2
1
3
2
E2
N2
1
1
2
1
2
1
2
1
1
3
1
E1
N1
1
1
1
mz
gi
i
1
mx my
metodo dei “moltiplicatori di Lagrange”
Statistica di Boltzmann
formula di Stirling:
lnx! = x lnx - x
d ln Wi
dN
dNi Ei
dNi 0
i
dN
dN
dN
i
i
i
i
d ln Wi
1
ln g i (ln N i N i
1)
dN i
Ni
ln g i ln N i Ei 0 ; ln
N i Cgi e
gi
fattore di
“spazio delle fasi”
Ni
E i
gi
Ei
ha le dimensioni
dell’inverso di una energia
=1/ kBT
fBol (E,T) = e-E/kT
funzione di distribuzione
di Boltzmann
Ni Cgi f Bz ( E i , T )
Esempio: distribuzione sui livelli
rotazionali di molecole HCl a T=300K
Statistica di
Boltzmann
Erot=Brot l(l+1) con Brot=1,3 meV
kBT=26 meV; gl=2l+1
l
gl
Erot
fBlz(Erot,T)
1,2
gl fBlz
(meV)
0
1
2
3
4
5
6
7
8
1
3
5
7
9
11
13
15
17
0
2,6
7,8
15,6
26
39
55
73
94
1
fBz
1
0,90
0,74
0,55
0,37
0,22
0,12
0,06
0,03
funzione
funzionedidipartizione
partizioneZ:
Z:
1
2,7
3,7
3,8
3,3
2,5
1,6
0,9
0,5
(Z=20)
(Z
20)
0,8
0,6
0,4
0,2
0
0
20
40
60
E (meV)
Z i g i f Bz ( E i , T )
probabilità di occupazione dello stato:
g i f Bz ( E i , T )
Pi
Z
80
100
120
g nel caso di distribuzione “continua” di energia,
ad esempio energia cinetica E=p2/2m
spazio delle fasi
gi g(E)
cella elementare dello spazio delle fasi:
dx dy dz dpx dpy dpz = h3
numero di celle elementari con energia fra E ed E+dE:
g ( E )dE
dxdydz dp x dp y dp z
h3
g ( E )dE
V 4
2
p
dp
3
h
4V 2m3
h
per l’elettrone (due stati di spin):
3
4V 2m3
h
3
E dE
E dE
g ( E )dE
8V 2m3
h
3
E dE
g ( E )dE
8V 2m3
E dE
h3
py
pymax
in ciascuna
banda, E si
calcola a
partire dal
fondo della
banda e g(E) va
a zero alla cima
della banda
per p>pxmax lo spazio delle fasi
disponibile si riduce
progressivamente fino a
diventare un punto per p=pmax
pmax
E3max
g(E)
pxmax
px
E3min
terza banda
E2max
g(E)
3,5
3
E2min
Emax=10 eV
2,5
g(E)
spazio delle fasi nella
banda di energia
seconda banda
2
E1max
g(E)
E1min
1,5
1
0,5
0
0
2
4 E (eV) 6
8
10
prima banda
distribuzione
di Boltzmann
1.2
fBz
1
300 K
0.8
g
0.6
0.4
dNBz(E)/dE
dNBz(E,T) =
g(E) fBz(E,T) dE
0.2
0
0
20
40
60
80
100
80
100
E (meV)
1.2
fBz
1
100 K
0.8
g
0.6
0.4
(la cima della banda
capita a energie molto
maggiori delle energie
termiche)
dNBz (E)/dE
0.2
0
0
20
40
60
E (meV)
Statistiche quantistiche:
indistinguibilità classica e quantistica
z
x2, y2, z2,
px2, py2, pz2
x1, y1, z1,
px1, py1, pz1
y
x
z
m(x2, y2, z2 )
n(x1, y1, z1 )
y
indistinguibilità classica: le due particelle sono
identiche, lo stato in cui la particella “rossa” ha
coordinate (x1, y1, z1, px1, py1, pz1 ) e la particella
“verde” ha coordinate (x2, y2, z2, px2, py2, pz2 ) è
equivalente allo stato con le particelle scambiate
indistinguibilità quantistica: le due particelle sono
identiche, lo stato in cui la particella di coordinate (x1,
y1, z1) ha funzione d’onda n e la particella di
coordinate (x2, y2, z2) ha funzione d’onda m e lo stato
con le particelle scambiate vanno considerati entrambi
e sommati o sottratti a seconda del tipo di particella
Fermioni: (r1,r 2 )
x
Bosoni:
1
( m (r1 ) n (r2 ) m (r2 ) n (r1 ))
2
1
(r1,r 2)
( m (r1 ) n (r2 ) m (r2 ) n (r1 ))
2
In quanti modi si possono disporre 2 particelle identiche in 3 celle?
Boltzmann
P
mx= 1
my= 1
mz= 2
a
b
a
b
ab
Q
mx= 1
my= 2
mz= 1
b
a
a
b
ab
Bose
R
mx= 2
my= 1
mz= 1
mx= 1
my= 1
mz= 2
Q
mx= 1
my= 2
mz= 1
R
mx= 2
my= 1
mz= 1
P
mx= 1
my= 1
mz= 2
Q
mx= 1
my= 2
mz= 1
R
mx= 2
my= 1
mz= 1
b
a
b
a
ab
N
gi i
9
per Boltzmann:
Ni ! 2
indistinguibilità
classica e
quantistica
P
Fermi
1
( P (a) Q (b) P (b) Q (a)) 1 (a, b)
2
1
2 (a, b) ( P (a) R (b) P (b) R (a)) 2 (a, b)
2
1
3 (a, b) ( Q (a) R (b) Q (b) R (a)) 3 (a, b)
2
4 (a, b) P (a) P (b)
1 ( a, b)
5 (a, b) Q (a) Q (b)
6 (a, b) R (a) R (b)
6 modi
1
( P (a) Q (b) P (b) Q (a))
2
1
( P (a) R (b) P (b) R (a))
2
1
( Q (a) R (b) Q (b) R (a))
2
3 modi
Statistica di
Fermi - Dirac
P
mx= 1
my= 2
mz= 3
Q
mx= 1
my= 3
mz= 2
R
mx= 2
my= 1
mz= 3
S
mx= 2
my= 3
mz= 1
mx= 3
my= 2
mz= 1
Ni particelle in gi celle:
Ni “celle piene”,
(gi-Ni ) “celle vuote”
g i ( gi 1) ( gi N i 1)
g i!
Wi
Ni !
N i !( gi N i )!
g i!
d ln W
ln W i ln
;
Ei 0
N i !( gi N i )!
dN i
ln N i ln( gi N i ) Ei 0
g Ni
ln i
Ei
Ni
;
gi
1 e Ei
Ni
Ni
gi
gi
; Ni
e Ei 1
e( Ei E F ) / k BT 1
T
U
mx=3
my= 1
mz= 2
Statistica di Fermi Dirac
elettroni in una banda non piena
dN ( E )
g (E)
dE
e ( E E F ) / k BT 1
g(E)
fF(E,T)
T=0K
dN ( E )
g ( E ) f F( E , T )
dE
1
f F( E , T ) ( E E ) / k T
F
B 1
e
g(E)
fF(E,T)
T >> 0 K
l’integrale sull’energia di dN/dE è
pari al numero totale N di elettroni:
N
g ( E )dE
e( E E F ) / k BT 1
8V 2m3
h3
0
a T=0 K:
L’energia di Fermi
E dE
e( E E F ) / k B T 1
0
N
8π 2m3
n
V
h3
EF
E dE
16π 2m3
0
h2 3n
EF
8m π
3h3
3/ 2
EF
2/3
Esempio: il rame ha circa un elettrone libero per atomo, densità di circa 9
g/cm3 e numero di massa A=63
N mole g
6 1023 9 g 1023
1
n
N Av A d
3 mole g
3
3
63g cm
cm
cm
cm 3
N
4π 2 (c )2 3n
EF
8mc2 π
2/3
4 10 (2 105 eV cm )2 3
8 0,5 106 eV
10 1045 cm 2 10eV
Energie di
Fermi
metallo
EF (eV)
TF (K)
Li
4,7
5,5104
Na
3,1
3,7104
TF = EF /kB
K
2,1
2,4104
kB 910-5eV K-1
Cu
7,0
8,2104
Ag
5,5
6,4104
Au
5,5
6,4104
Energia media a 0 K:
EF
C
E 3 / 2dE
2 5/ 2
EF
3
5
0
ET 0K E
EF
2 3/ 2
F
5
EF
1/ 2
C E
dE
3
0
<E>
Statistica di
Bose - Einstein
Ni particelle in gi celle:
in quanti modi si
possono mettere gi-1
“separatori” fra le Ni
particelle
P
Q
mx= 1
my= 2
mz= 3
mx= 1
my= 3
mz= 2
R
mx= 2
my= 1
mz= 3
S
mx= 2
my= 3
mz= 1
T
mx= 3
my= 2
mz= 1
U
mx=3
my= 1
mz= 2
tutte le possibili permutazioni di Ni+gi-1 oggetti
( N g i 1)!
Wi i
N i ! ( gi 1)!
ln N i ln( N i g i 1) Ei 0
ln
Ni g i
Ei
Ni
gi
Ni E / k T
i
B 1
e
;
gi
1 e Ei
Ni
nel continuo:
dN ( E )
g ( E ) f BE ( E , T ) ;
dE
distribuzione di B.E.
g
; N i Ei
i 1
e
dN ( E )
g(E)
E / k T
B 1
dE
e
1
f BE ( E , T ) E / k T
B 1
e
funzione di distribuzione di B.E.
Per i fotoni non c’è la conservazione
del numero totale = 0
dN ( E )
g(E)
E /k T
B 1
dE
e
gas di
fotoni
termine di spazio delle fasi per i fotoni:
g ( E )dE 2
dxdydz dp x dp y dp z
h3
due stati di polarizzazione
8πV
h3
p 2 dp
8πV
(hc)3
E 2 dE
120
100
distribuzione in energia:
dn( E )
8π
E2
dE
(hc)3 e E / k BT 1
dnBE
80
g
60
fBE
40
20
spettro di “corpo nero”
0
0
d ( )
8π
h 3
d
c 3 e h / k BT 1
50
100
150
energia (meV)
200
250
distribuzione in energia secondo Bose (Planck):
dn( E )
1
8πE 2
1
g (E)
dE
e E / k BT 1 (hc)3 e E / k BT 1
confronto fra le
statistiche di Bose
e di Boltzmann
2
dn( E )
8
π
E
E
/
k
T
B
secondo Boltzmann (Wien):
g (E) e
e E / k BT
dE
(hc)3
120
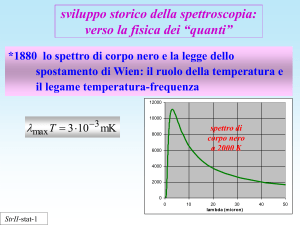
legge di Wien dello
“spostamento”
max T 3 103 mK
fBE
100
dnBz
80
dnBE
60
legge di Wien:
d ( )
3e f ( / T )
d
g
40
fBz
20
0
legge di Rayleigh-Jeans
0
50
100
150
energia (meV)
200
250
confronto fra le
statistiche di Bose
e di Boltzmann
12000
secondo
Planck
10000
8000
spettro di
corpo nero
a 2000 K
6000
secondo
Wien
4000
2000
0
0
10
20
30
lambda (micron)
40
50