IL RUOLO DEGLI OPPIOIDI NELLA
TERAPIA FARMACOLOGICA DEL
DOLORE NEUROPATICO
Stefano Tamburin
Università di Verona, Dipartimento di Scienze
Neurologiche e della Visione, Sezione di
Neurologia Riabilitativa
U.O. Neurologia, Clinica Pederzoli,
Peschiera del Garda (VR)
Terapia del Dolore Neuropatico:
possibili siti d’azione dei farmaci
Inibizione canali Na+
Inibizione canali Ca++
Riduzione trasmissione glutamatergica
Potenziamento trasmissione GABAergica
Potenziamento sistemi inibitori discendenti
Modulatori della sensibilizzazione periferica
SNP
Na++
CBZ
OXC
PHT
TPM
LTG
Modulatori della
Lidocaina
sensibilità
Mexiletina
periferica
TCAs
Midollo
Spinale
JJ Pain
Pain Symp
Symp Manag
Manag 2003;
2003; 25
25 (Suppl5
(Suppl5 ):): S18-S30
S18-S30
Modulatori della sensibilizzazione centrale
Sensibilizzazione centrale
Midollo
Spinale
++ GBP/PGB, LVT, OXC, LTG
Ca++
NMDA
GABA
Ketamina
Destrometorfano
Memantina
Oppioidi
CBZ/OXC
GBP/PGB
LTG
TGB
VPA
JJ Pain
Pain Symp
Symp Manag
Manag 2003;
2003; 25
25 (Suppl5
(Suppl5 ):): S18-S30
S18-S30
Modulatori delle vie inibitorie discendenti
Cervello
TCAs
SSRIs
SNRIs
Tramadolo
Oppioidi
Vie discendenti inibitorie
Noradrenalina
Serotonina
Oppioidi endogeni
Midollo
Spinale
JJ Pain
Pain Symp
Symp Manag
Manag 2003;
2003; 25
25 (Suppl5
(Suppl5 ):): S18-S30
S18-S30
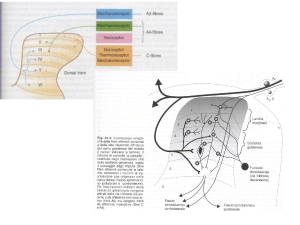
Tecniche antalgiche e livelli d’azione
ENCEFALO
Talamo
NEURONE
NEURONE DI
DI
TERZO
ORDINE
TERZO ORDINE
TECNICHE
TECNICHE E
E
FARMACI
FARMACI
AD
AD
AZIONE
AZIONE SINAPTICA
SINAPTICA
TECNICHE E FARMACI
AD AZIONE CENTRALE
Analgesici azione centrale (oppioidi)
Antidepressivi, Neurolettici
Anticonvulsivanti
Elettrostimolazione (D.B.S.)
((oppioidi)
oppioidi)
NEURONE
NEURONE DI
DI
SECONDO
SECONDO ORDINE
ORDINE
TECNICHE
TECNICHE E
E FARMACI
FARMACI
AD
AD AZIONE
AZIONE
SULLA
SULLA CONDUZIONE
CONDUZIONE
Anestetici
Anestetici,, Anticonvulsivanti
Anticonvulsivanti,,
Elettrostimolazione
Elettrostimolazione (SCS
(SCS))
FARMACI
FARMACI E
E TECNICHE
TECNICHE
AD
AD AZIONE
AZIONE LOCALE
LOCALE
Anestetici
Anestetici topici
topici
Antiinfiammatori
Antiinfiammatori non
non steroidei
steroidei
Elettrostimolazione
Elettrostimolazione (T.E.N.S.)
(T.E.N.S.)
RECETTORE
RECETTORE
MIDOLLO
NEURONE
NEURONE DI
DI
PRIMO
ORDINE
PRIMO ORDINE
Antidepressivi: meccanismo d’azione
Effetto sui sistemi discendenti (5HT, NA)
Riduzione di ansia e depressione
Proprietà anestetiche locali (TCA)
Antidepressivi più recenti
SNaRI
NaSSA
NaRI
Inibitori del reuptake di Venlafaxina
serotonina e noradrenalina Duloxetina
Antidepressivi
noradrenergici e
serotoninergici specifici
Mirtazapina
Inibitori del reuptake di
noradrenalina
Reboxetina
Antiepilettici: meccanismo d’azione
Canali
Na+
Canali Ca++
Recettori GABA
Metabolismo GABA
Recettori glutammato (NMDA)
Fenitoina
Carbamazepina
Lamotrigina
Valproato
Etosuccimide
Gabapentin
Pregabalin
Barbiturici
Benzodiazepine
Gabapentin
Pregabalin
Vigabatrin
Valproato
Felbamato
Topiramato
Carbamazepina
Oppioidi: meccanismo d’azione
Azione su recettori mu, delta, kappa spinali
con riduzione Ca++ pres ed aumento K posts
(vie inibitorie discendenti)
Azione sovraspinale sul dolore
(tronco e sistema limbico)
TRAMADOLO
Oppioide
Inibizione reuptake NA-5HT
RECETTORI OPPIOIDI
Dinorfine
Encefaline
µ1
Analgesia
Sopraspinale
• Euforia
µ2
•
•Bradicardia
•Depressione
respiratoria
κ
•Analgesia
Spinale
•Sedazione
•Miosi
β-Endorfine
δ
σ
Disforia
Allucinazioni
Analgesia
spinale
15603
ASA
ASA ++ clopidogrel
clopidogrel
vs
vs ASA
ASA
7329
1252
1252
perindopril
perindopril vs
vs
placebo
placebo
419
419
ximelagatran
ximelagatran vs
vs
warfarine
warfarine
237
237
66
66
cabergoline
cabergoline vs
vs
levodopa
levodopa
duloxetine
duloxetine vs
vs
placebo
placebo
cannabis
cannabis vs
vs
placebo
placebo
Necessità di meta-analisi
Gabapentin - Pregabalina
In particolare:
Neuropatia diabetica
Nevralgia posterpetica
Wiffen
Wiffen et
et al.,
al., 2006
2006
Carbamazepina ed Oxcarbazepina
Authors' conclusions
Wiffen
Wiffen et
et al.,
al., 2006
2006
There is evidence to show that CBZ is effective
but trials are small
Antidepressivi
• Antidepressants (TCA, SNRI) are effective for the
treatment of NP
• The best evidence for amitriptyline
• Only limited data for the effectiveness of SSRIs
Opioid agonists
Eisenberger
et al.,
al., 2005
2005
Intermediate-term
of
Intermediate-term studies
studies ->
-> significant
significant efficacy
efficacy Eisenberger
of opioids
opioidset
Adverse
Adverse events
events of
of opioids
opioids common
common but
but not
not life-threatening
life-threatening
Further
Further RCTs
RCTs to
to establish
establish long-term
long-term efficacy,
efficacy, safety
safety and
and effects
effects on
on QoL
QoL
Tramadol for neuropathic pain
Hollingshead
Hollingshead et
et al.,
al., 2006
2006
• Positive trials of oxycodone in diabetic PN and PHN (Gimbel et al.,
2003; Watson et al., 1998, 2003)
• Positive trial of methadone in mixed types of NP (Morley et al., 2003)
• Positive trial of morphine in PHN (Raja et al., 2002)
• Short and intermediate-term studies: opioids can reduce dynamic
mechanical allodynia and perhaps cold allodynia in peripheral NP
• These findings are clinically relevant
Finnerup et al., 2006
Raccomandazioni EBM – Linee guida
una recente revisione sistematica
Finnerup
Finnerup NB,
NB, Otto
Otto M,
M, McQuay
McQuay HJ,
HJ, Jensen
Jensen TS,
TS, Sindrup
Sindrup SH,
SH, Pain
Pain 2005
2005
le conclusioni di una task force EFNS
Attal
Attal N,
N, Cruccu
Cruccu G,
G, Haanpaa
Haanpaa M,
M, Hansson
Hansson P,
P, Jensen
Jensen TS,
TS, McQuay
McQuay H,
H,
Nurmikko
Nurmikko T,
T, Sampaio
Sampaio C,
C, Sindrup
Sindrup S,
S, Wiffen
Wiffen P
P
un libro Cochrane su EBN
Cruccu
Cruccu G,
G, Attal
Attal N,
N, Taylor
Taylor R
R
NNT
Number
Needed to
Treat
Responders
Responders ==
VAS
VAS reduction
reduction
at
at least
least 50%
50%
Max
-40%
Max 30
30-40%
Finnerup
Finnerup et
et al.
al. 2005
2005
NNH Number Needed to Harm
Finnerup
Finnerup et
et al.
al. 2005
2005
Canadian Pain Society guidelines
1st
TCA
2nd
3rd
Gabapentin or Pregabalin
Topical Lidocaine*
SNRI
Tramadol
or
CR Opioid Analgesic
Add additional
agents
sequentially if
partial but
inadequate pain
relief ‡
Fourth Line Agents †
* 5% gel or cream - useful for focal neuropathy such as postherpetic neuralgia. Lidocaine
patch not available in Canada.
† e.g. Cannabinoids, methadone, lamotrigine, topiramate, valproic acid.
‡ Do not add SNRI to TCA
SNRI: serotonin/noradrenaline reuptake inhibitor; TCA: tricyclic antidepressant; CR: controlled-release
J. Pain Res. Manage. 12:13-21, 2007
Linee Guida EFNS sul trattamento
farmacologico del dolore neuropatico
Affidabilità dell’Evidenza
Radice del campione x
Qualità (Jadad’s 2-5)
Guadagno Effettivo
guadagno netto con il preparato attivo
(% responders meno % dropouts)
meno
guadagno netto con il placebo
(% responders meno % dropouts)
Cruccu
Cruccu et
et al.,
al., 2006
2006
Affidabilità dell’evidenza nel dolore neuropatico
Pregabalin/GBP
Pregabalin/GBP
opioids
opioids
SNRI
SNRI
TCA
TCA
lamotrigine
lamotrigine
lidocaine
lidocaine
valproate
valproate
AED-SCB
AED-SCB
topiramate
topiramate
NS
NS
capsaicin
capsaicin
NS
NS
mexiletine
mexiletine
NS
NS
NMDA-ant
NMDA-ant
NS
NS
00
10
10
20
20
30
30
40
40
50
50
60
60
70
70
80
80
90
90
100
100
Diagrammi di Affidabilità/Efficacia
100
100
Low
Low Reliability
Reliability
Effective Gain
Gain
Effective
75
75
BEST
BEST
High
High efficacy
efficacy
50
50
WORST
WORST
25
25
High
High Reliability
Reliability
Low
Low efficacy
efficacy
00
00
25
25
50
50
Reliability
Reliability
75
75
100
100
Peripheral Neuropathic Pain
100
100
90
90
Effective Gain
Gain
Effective
80
80
Preg/GBP
Preg/GBP
SNRI
SNRI
TCA
TCA
Opioids
Opioids
Valproate
Valproate
AED-SCB
AED-SCB
Lamotrigine
Lamotrigine
Capsaicin
Capsaicin
Mexiletine
Mexiletine
NMDA
NMDA
Topiramate
Topiramate
70
70
60
60
50
50
40
40
30
30
20
20
10
10
00
00
10
10 20
20 30
30 40
40 50
50 60
60 70
70 80
80 90
90 100
100
Reliability
Reliability
Central Pain
100
100
90
90
Effective Gain
Gain
Effective
80
80
70
70
60
60
Pregabalin
Pregabalin
Amitriptyline
Amitriptyline
Cannabis
Cannabis
Valproate
Valproate
CBZ
CBZ
Lamotrigine
Lamotrigine
50
50
40
40
30
30
20
20
10
10
00
00
25
25
50
50
Reliability
Reliability
75
75
100
100
Condizioni meno studiate, più resistenti
Post-surgical pain
2 positive / 2 negative
Phantom limb
2 positive / 4 negative
HIV-neuropathy
1 positive / 8 negative
Brachial plexus-avulsion
1 negative
Post-stroke
2 positive / 2 negative
Spinal Cord Injury
2 positive / 3 negative
Number and outcome
of RCTs:
positive / negative
Condizioni meno studiate, più resistenti
30
30
Effective Gain
Gain
Effective
20
20
Preg/GBP
Preg/GBP
SNRI
SNRI
TCA
TCA
Opioids
Opioids
Valproate
Valproate
AED-SCB
AED-SCB
Lamotrigine
Lamotrigine
Capsaicin
Capsaicin
Mexiletine
Mexiletine
NMDA
NMDA
Topiramate
Topiramate
10
10
00
-10
-10
-20
-20
00
10
10 20
20 30
30 40
40 50
50 60
60 70
70 80
80 90
90 100
100
Reliability
Reliability
… or better…
Qualità di Vita, Umore, Sonno
GBP/Pregabalin
GBP/Pregabalin
8
duloxetine
duloxetine
1
cannabis
cannabis
2
opioids
opioids 4
1
Positive
Positive
Negative
Negative
lidocaine
lidocaine 1
00
10
10
20
20
30
30
40
40
50
50
60
60
70
70
80
80
90
90
100
100
Controindicazioni-Sicurezza
CBZ
Rash cutaneo ed anemia aplastica. Enzimi epatici ed
emocromo devono essere controllati almeno 3 volte all’anno.
LTG
Reazioni allergiche potenzialmente gravi fino al 10% dei
pazienti. Per minimizzarli occorre titolazione lentissima (25
mg ogni 2 settimane), che comporta 16-32 settimane per
raggiungere i dosaggi analgesici (200-400 mg/die).
TCA
Le tipiche controindicazioni sono glaucoma ed ipertrofia
prostatica. La possibile associazione tra triciclici e morte
cardiaca improvvisa è stata documentata solo con dosaggi
elevati fino a 300 mg/die (Ray et al. 2004). Si raccomanda
cautela nei pazienti anziani con fattori di rischio CV
Farmaci ad alta
evidenza
Farmaci inefficaci o con
insufficiente evidenza
Pregabalina/GBP
Pregabalina/GBP
Periferico
Periferico ee Centrale
Centrale
Fentanyl
Fentanyl cerotto
cerotto
Nessun
Nessun trial
trial ufficiale
ufficiale
TCA
TCA
Periferico
Periferico ee Centrale
Centrale
Topiramato
Topiramato
Inefficace
Inefficace nel
nel Periferico
Periferico
Oppioidi
Oppioidi
Periferico
Periferico
SSRI
SSRI
Inefficaci
Inefficaci nel
nel Periferico
Periferico
Cannabinoidi
Cannabinoidi
Centrale
Centrale
Antagonisti
Antagonisti NMDA
NMDA
Inefficaci
Inefficaci nel
nel Periferico
Periferico
SNRI
SNRI
Periferico
Periferico
Mexiletina
Mexiletina
Inefficace
Inefficace in
in tutto
tutto
AED-SCB
AED-SCB
Nevralgia
Nevralgia trigemino
trigemino
Capsaicina
Capsaicina
Insufficiente
Insufficiente evidenza
evidenza
Politerapia
Epilessia: 30%
Ipertensione: 40%
Malattia di Parkinson: 80-90%
Dolore: ???
Farmacocinetica vs Farmacodinamica
Possibili associazioni nel dolore neuropatico
Antiepilettici
Antidepressivi
(CBZ, GBP,
PGB, LTG)
(TCA, SNRI)
Anestetici
e terapie locali
Oppioidi e
tramadolo
Altre terapie
da
da Romanò,
Romanò, 2006;
2006; modificato
modificato
Dolore Misto
NOCICETTIVO
NEUROPATICO
MISTO
Radiculopatie
Sindromi compressive di nervi
Dolore oncologico
Neuropatie ischemiche
Complex Regional Pain Syndrome
Possibili associazioni nel dolore misto
Antidepressivi
Antiepilettici
Oppioidi e
tramadolo
(TCA, SNRI)
(CBZ, GBP,
PGB, LTG)
Altre terapie
Anestetici
e terapie locali
FANS, COX-2
Cortisonici
Miorilassanti
da
da Romanò,
Romanò, 2006;
2006; modificato
modificato
RECETTORI OPPIOIDI
Dinorfine
Encefaline
µ1
Analgesia
Sopraspinale
• Euforia
µ2
•
•Bradicardia
•Depressione
respiratoria
κ
•Analgesia
Spinale
•Sedazione
•Miosi
β-Endorfine
δ
σ
Disforia
Allucinazioni
Analgesia
spinale
Activity of Opioid Agonists, Agonist-Antagonists, and
Antagonists at Opioid Receptors
Agent
Mu
•
•
•
•
•
•
•
•
Morphine
Oxycodone
Methadone
Buprenorphine
Fentanyl/sulfentanyl
Idromorphone
Pentazocine
Naloxone
Ag
Ag
Ag
pAg
Ag
Ag
Ant
Ant
Receptor Type
Kappa
Sigma
Ag
Ag
Ag
Unknown
Ag
Ant
Ag = Agonist, Ant = Antagonist, pAg = Partial Agonist
Ag
Ant
Short-acting Agents
Long-acting Agents
• Codeine
• Methadone
• Hydromorphone
• Morphine
• Oxycodone
• Morphine CR
• Oxycodone CR
• Tramadol
• Fentanyl transdermal
Moderate opioids
Strong opioids
• Codeine
• Hydromorphone
• Tramadol
• Morphine
• Oxycodone
• Methadone
• Fentanyl
Problems with chronic
use of opioids
• Tolerance
• Physical dependence
• Pseudoaddiction
• Addiction
Tolerance
• A physiologic state resulting from regular use of a drug in
which an increased dosage is needed to produce the
same effect or a reduced effect is observed with a
constant dose
• Occurs to both analgesic and adverse effects
• Hyperalgesia: diminished drug effect over time due to
ongoing drug exposure, i.e.: takes higher dose to get
relief
• Does NOT imply or cause addiction
• Production of anti-opioids (CCK)
• Mu receptor desensitization
• NMDA receptor activation
Physical Dependence
• Physiologic changes expected to occur with ongoing
exposure to opioids (similar changes occur with other
medications, e.g.: beta blockers, anti-depressants, etc.)
• Signs/symptoms of opioid withdrawal: tachycardia, nausea,
vomiting, diarrhea, rhinorrhea, lacrimation, yawning, anxiety
• Avoid withdrawal syndrome by tapering dose by 50% every
2-3 days
• Does NOT imply or cause addiction
Pseudoaddiction
• Describes aberrant behaviors occurring as a result of
under-treated pain:
– “clock-watching”
– aggressive complaining
– requesting specific drugs
– unsanctioned dose escalation
• Behaviors resolve when effectively treated
• May inappropriately stigmatize patients
Addiction
• Psychological dependence on a drug
• Fundamental features include:
¾ Loss of control over use
¾ Preoccupation with obtaining opioids despite adequate pain control
(craving)
¾ Continued use despite adverse consequences
• Behaviors more likely to be related to addiction:
¾ Prescription forgery
¾ Stealing or “borrowing” drugs
¾ Multiple episodes of prescription “loss”
¾ Concurrent abuse of related illicit drugs
¾ Selling prescription drugs
The neurobiology of opiate addiction
• Coinvolge sistema DA-ergico mesolimbico, nucleo
accumbens ed altre aree limbiche
• Fenomeno complesso meno studiato rispetto alla
dipendenza da psicostimolanti, plurifattoriale
¾ Predisposizione genetica
¾ Fattori socio-ambientali
¾ Profilo psicologico e patologie psichiatriche
¾ Periodo della vita in cui viene somministrato il
farmaco (soprattutto adolescenza)
•
•
Abuso/dipendenza solo in una piccola percentuale di pazienti
La percentuale può essere ulteriormente ridotta con un’attenta anamnesi volta ad
identificare precedenti o intercorrenti problemi di alcolismo o abuso/dipendenza da
farmaci.
Effetti collaterali degli oppioidi
• Stipsi: mediato da recettori mu a livello enterico
• Ritenzione urinaria
• Nausea e vomito: mediato da recettori tronco
• Prurito, flushing: mediato da recettori tronco con rilascio istamina
• Depressione respiratoria, aritmia: mediato da recettori tronco (mu)
• Sedazione: effetto sovraspinale (kappa)
• Confusione, allucinazioni: effetti sovraspinali (sigma)
• Ipogonadismo e calo libido: effetto ipotalamico
• Effetti di tipo neuropsicologico: segnalati in pazienti oncologici
• Effetto immunosoppressivo: descritto, soprattutto per morfina e
fentanly ma anche dolore non trattato agisce da immunosoppressore
Strategie per ridurre gli effetti collaterali
¾La tolleranza agli effetti collaterali è più precoce
che per l’effetto analgesico
¾Il profilo degli effetti collaterali è variabile per i
singoli farmaci
Aumentare con piccoli incrementi il dosaggio
Ruotare gli oppioidi
Valutare l’eventuale sospensione del farmaco
(drug holiday)
Scala equianalgesica degli oppioidi
mcg/ora
/ora
mcg
mcg/ora
mcg/ora
/ora
mcg
mcg/ora
http://www.simg.it/default2.asp?active_page_id=739
http://www.simg.it/default2.asp?active_page_id=739
http://www.hopkinskimmelcancercenter.org/
specialtycenters/hop.cfm?facilityid=27
http://www.hopkinskimmelcancercenter.org/specialtycenters/hop.cfm?facilityid=27
TRAMADOLO
• Emivita: 5-6 ore
• Metabolismo epatico, eliminazione renale
• Effetto tetto per dosi giornaliere di 400-600 mg
• Interagisce con CBZ che ne aumenta il metabolismo
CODEINA
• Buona disponibilità per os
• Metabolismo epatico: 10% demetilata a morfina
• Dosi abituali: 30-60 mg per os ogni 4-6 ore
• Effetto tetto per dosi giornaliere di 360 mg
• In vendita in formulazioni combinate con altri analgesici
MORFINA
• Metabolismo epatico, conversione a morfina-6-glicuronide
• Eliminazione renale
• Molecola idrofila: supera lentamente BEE
• Dose iniziale: 5-10 mg ogni 4 ore; dose nel DN: 60-300 mg/die
• Non presenta effetto tetto
• Interazione con BDZ, TCA e ranitidina
METADONE
• Agonista mu, kappa ed antagonista NMDA
• Buona disponibilità per os, lunga emivita plasmatica
• Metabolismo epatico, eliminazione renale e biliare
• Molecola lipofila: supera facilmente BEE
• Dose iniziale: 5 mg per os ogni 8 ore, dose nel DN: 20-30 mg/die
• Non presenta effetto tetto
OSSICODONE
• Agonista mu, kappa
• Metabolismo epatico, eliminazione renale
• Buona disponibilità per os con emivita di 2-3 ore
• Esiste in formulazione a rilascio prolungato
• Effetto analgesico dura 5-6 ore
• Dose iniziale: 10 mg ogni 12 ore; dose nel DN: 40-120 mg/die
• Non presenta effetto tetto
IDROMORFONE
• Buona disponibilità per os
• Metabolismo epatico
• Esiste in formulazione a rilascio prolungato
FENTANYL
• Agonista mu, metabolismo epatico
• Elevata rapidità d’azione (30’’ ev) ma breve durata (30-60’)
• Alta lipofilia: supera velocemente BEE
• Formulazione transmucosale (lollipop) e cerotto transdermico
• Monitorare la fase di induzione (possibile sottodosaggio nelle prime 24
ore o sovradosaggio nelle ore successive)
• Dose iniziale: cerotto 25 mcg/ora; dose nel DN: 25-100 mg/ora
BUPRENORFINA
• Agonista parziale mu, kappa
• Metabolismo ed escrezione epatica
• Formulazione transmucosale (lollipop) e cerotto transdermico con
problematiche analoghe al fentanyl
• Effetto tetto per dosi > 4 mg/die
Recommendations for using opioids in chronic noncancer pain
¾La terapia con oppioidi va presa in considerazione nel DN se
altre terapie sono inadeguate dopo un ragionevole periodo di
tempo
Utilizzare oppioidi in politerapia nel DN, soprattutto se
oppioidi forti
¾Scopo della terapia è la riduzione del dolore ed il miglioramento
della qualità della vita e dello stato funzionale
Valutare dolore (VAS), QoL, stato funzionale prima e dopo
la terapia (eventuale diario tenuto dal paziente)
Bilanciare miglioramento di queste variabili ed eventuali
effetti collaterali
Kalso, European Journal of Pain, 2003
Recommendations for using opioids in chronic noncancer pain
¾Chi prescrive il farmaco deve essere informato sullo status
psicosociale del paziente e sul rischio di dipendenza
Kalso, European Journal of Pain, 2003
Recommendations for using opioids in chronic noncancer pain
¾L’utilizzo di formulazioni a rilascio prolungato ad orari regolari è
preferibile
Evitare farmaci a breve durata d’azione (indicati per trattare
‘breakthrough pain’)
Evitare cerotti transdermici perchè l’assorbimento può
essere irregolare con rischio di sotto- o sovra-dosaggio
Kalso, European Journal of Pain, 2003
Recommendations for using opioids in chronic noncancer pain
¾Monitorare il trattamento
Efficacia su dolore, QoL, stato funzionale (diario
autocompilato dal paziente)
Effetti collaterali
Utilizzo di altri farmaci
Individualizzare obiettivi del trattamento
¾Il trattamento con oppioidi non va considerato una terapia da
continuare per tutta la vita
Kalso, European Journal of Pain, 2003
Recommendations for using opioids in chronic noncancer pain
¾ Chiarire al paziente obiettivi ed effetti collaterali della terapia
Alcuni Autori consigliano un ‘contratto’ per sottolineare
l’importanza del coinvolgimento del paziente
Kalso, European Journal of Pain, 2003