Controllo
Neuroendocrino del
Comportamento
Alimentare
Augusto Innocenti
Dottore in Biologia
Perfezionamento in Biochimica e Biologia Molecolare
Phd in Neurobiologia e Neurofisiologia
La regolazione del peso corporeo è frutto di un
processo omeostatico, ovvero di un equilibrio
dinamico caratterizzato da un tentativo di
bilanciamento fra l’introito calorico e il
dispendio energetico.
1
I soggetti in sovrappeso, dopo un periodo di
dieta rigida o di un calo ponderale repentino,
tendono a riportarsi alla condizione precedente.
Studi eseguiti negli atleti olimpici hanno
evidenziato che la perdita di tessuto adiposo
ottenuta dopo un intenso programma
d'allenamento è reversibile dopo la fine delle
gare.
Anche i risultati ottenuti con l’uso di
anabolizzanti sono completamente cancellati e
riportati allo stato iniziale una volta interrotto il
trattamento.
2
Questo equilibrio viene mantenuto grazie al
controllo del bilancio energetico attraverso una
complessa regolazione neuroendocrina del
comportamento alimentare sia a breve che a
lungo termine.
La notevole complessità di questo sistema
necessita, per la fondamentale importanza delle
sue funzioni, di una stretta interrelazione di
diversi segnali, spesso ridondanti, provenienti sia
dal cervello che dagli organi periferici.
3
La ridondanza di questi sistemi è spiegata dalla
necessità di rendere questi parametri meno
vulnerabili di fronte a qualsiasi agente esterno od
interno al sistema che tenti di modificarne
l'assetto primitivo o più in generale l'equilibrio.
Perché mangiamo?
Aspetto Fisiologico = Bisogno di Nutrienti
Aspetto Edonistico = Piacere (-endorfine)
4
Perché mangiamo?
Aspetto Fisiologico = Bisogno di Nutrienti
Aspetto Edonistico = Piacere
Appetito
desiderio di assumere un particolare tipo di cibo
non sempre connesso a un suo reale bisogno e la
cui ingestione si accompagna a sensazione di
piacere.
Fame
sensazione che spinge un individuo a ingerire del
cibo senza alcuna predilezione ed è solitamente
accompagnata a sensazione di sofferenza e
malessere.
5
Sazietà
Fa riferimento a due distinti momenti che si
susseguono a distanza dal pasto:
Fase precoce (satiation) che termina con la
cessazione del pasto dovuta essenzialmente alla
quantità di cibo ingerito
Fase tardiva postprandiale (satiety)
caratterizzata dall'assenza di fame.
Il cibo induce sazietà
6
I meccanismi che regolano la seconda fase sono
profondamente
diversi
da
quelli
che
accompagnano la prima fase e implicano
l'intervento di sistemi integrati di controllo situati
a livello del sistema nervoso centrale.
Regolazione a breve termine
Fame e Sazietà
Regola l’assunzione di cibo
Regolazione a lungo termine
Bilancio energetico e peso
Mantenuto nel corso degli anni
7
Regolazione a breve
termine
8
Sistema di controllo = Ipotalamo
Feedback = Asse Ipotalamo-Enterico
Vago e [Nutrienti]
Sistemi Integrativi = Aree Emotive e Associative
Immediatamente dopo il pasto
9
Tra un pasto e l’altro
Quantità di cibo
Intervallo tra i pasti
10
L’assunzione del cibo
innesca quindi una serie di
segnali che innescano a
livello
cerebrale
la
sensazione di sazietà.
IPOTALAMO
Il centro di controllo
11
Già da tempo è noto il coinvolgimento
dell’ipotalamo
nella
regolazione
del
comportamento alimentare.
Complessa interazione di segnali regolata da due
sistemi
distinti
che
pur
controllando
rispettivamente la fame e la sazietà,
interagiscono
fisiologicamente
ed
anatomicamente tra loro.
PVH
N. Paraventricolari
LHA
Area Laterale
DMH Area DorsoMediale
VMH Area VentroMediale
ARC
N. Arcuato
3V III Ventricolo
12
PVN N. Paraventricolari LH Area Laterale
DMH Area DorsoMediale ARC N. Arcuato
VMH Area VentroMediale OC Chiasma Ottico
I segnali fisiologici che innescano l’assunzione di
cibo
(appetito,
ricerca,
scelta),
sono
qualitativamente differenti rispetto a quelli che la
fanno cessare.
In particolare nel secolo scorso fu sviluppato un
modello a due centri:
Ipotalamo Laterale = Fame
Ipotalamo Ventromediale = Sazietà.
13
Lesione dell’Ipotalamo Laterale
determina:
inibizione nell’assunzione di cibo
anomalie comportamentali:
motilità incongrua rispetto alla ricerca del cibo
ridotta attenzione verso stimoli esterni.
Iperattivazione dell’Ipotalamo Laterale
induce:
Comportamento di ricerca del cibo
Iperfagia
14
Lesione dell’Ipotalamo Ventromediale
induce:
Iperfagia
Obesità
Stimolazione dell’Ipotalamo Ventromediale
induce:
Soppressione del comportamento alimentare
15
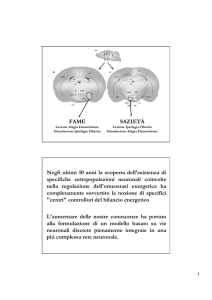
Negli ultimi 10 anni la scoperta dell'esistenza di
specifiche sottopopolazioni neuronali coinvolte
nella regolazione dell'omeostasi energetica ha
completamente sovvertito la nozione di specifici
"centri" controllori del bilancio energetico
L’aumentare delle nostre conoscenze ha portato
alla formulazione di un modello basato su vie
neuronali discrete pienamente integrate in una
più complessa rete neuronale.
Lo studio anatomo-funzionale di tale rete
continua a mostrare una complessità crescente
coinvolgendo molte altre strutture cerebrali:
la corteccia frontale
l'amigdala
le strutture troncomesencefaliche
il talamo.
16
Nella rete neuronale emergente L’ARC stà
assumendo una valenza primaria nel controllo del
comportamento alimentare.
Due popolazioni di Neuroni:
NPY Oressigeni coesprimono NPY e AgoutiRelated Protein (AgRP)
POMC Anoressigeni che coesprimono la proopiomelanocortina (POMC) e il Cocaine and
Amphetamine-Regulated Transcript (CART).
17
I neuroni in esso contenuti possiedono recettori
per una serie di ormoni coinvolti nella
regolazione dell'introito alimentare, quali la
leptina, i glicocorticoidi, gli estrogeni, il
progesterone, l'ormone della crescita, la ghrelina
e la barriera emato-encefalica in questa parte del
cervello (Eminenza Mediana) è liberamente
permeabile a queste molecole segnale.
18
L’ARC è inoltre in stretta connessione anatomica
e fisiologica attraverso vie neuronali con le altre
aree ipotalamiche coinvolte nella regolazione
del comportamento alimentare:
PVN
DMH
VMH
LH
L’EM è permeabile anche a glucosio ed insulina
e già da tempo è noto che nell’ipotalamo
esistono neuroni sensibili ai livelli ematici di
glucosio e di insulina, in particolare nei:
PVN
LH
ARC
19
Inoltre è stato dimostrato che l’ipotalamo è
sensibile anche alla [acidi grassi], infatti la
somministrazione intra-cerebro-ventriculare di
acido oleico nel topo riduce l'assunzione di cibo
attraverso l'inibizione dei neuroni NPY
inibendo
la
produzione
di
tale
neurotrasmettitore.
L’ARC
mantiene
neuroanatomiche con:
anche
connessioni
l’Area Postrema (AP) mesencefalica, altro
sensore cerebrale della concentrazione ematica
di nutrienti ed ormoni dove la BEE lascia
permeare le molecole di nutrienti ed ormoni.
Il Nucleo del Tratto Solitario (NTS) del Midollo
Allungato che raccoglie le terminazioni nervose
dei nervi faciale, glossossofaringeo e Vago
20
Pertanto il nucleo ARC può essere considerato
un complesso sensore metabolico che riceve e
integra a livello centrale le informazione
metaboliche ed endocrine dalla periferia circa lo
stato energetico del corpo, e controlla le altre
aree ipotalamiche coinvolte nella regolazione di
fame e sazietà.
21
Neuropeptide Y NPY
La sintesi e le secrezione di NPY
dall'ipotalamo aumenta in risposta al digiuno,
all'esercizio fisico, al deficit di insulina o di
leptina.
Il sistema neuronale NPYergico avverte e
risponde ad un'ampia serie di segnali
metabolici e ormonali che vengono modificati
dal decremento delle riserve energetiche.
Neuropeptide Y NPY
Nei ratti
Somministrazione i.c.v. acuta
Aumento dell’introito alimentare
Somministrazione i.c.v. cronica
Iperfagia
Incremento ponderale
Riduzione del dispendio energetico.
22
Neuropeptide Y NPY
La somministrazione i.c.v. di NPY induce un
aumento di:
Insulinemia
Liposintesi nel fegato e del tessuto adiposo
Aumento della sensibilità all'insulina
Attività della lipoprotein lipasi.
Neuropeptide Y NPY
La massima concentrazione di NPY nei PVN è
stata osservata prima e durante i pasti,
confermando un suo ruolo nell’induzione
dell’assunzione alimentare.
Il digiuno si è dimostrato il principale
stimolatore dell’espressione di NPY negli
animali.
23
Neuropeptide Y NPY
I topi knockout per NPY risultano avere un
peso corporeo normale e mostrano variazioni
ponderali simili a quelle degli animali di
controllo sia in condizioni di iper-alimentazione
sia in condizioni di digiuno.
Attivazione di vie oressanti alternative, al fine di
preservare l’integrità allo stimolo della fame,
evolutivamente fondamentale per la
sopravvivenza.
Agouti Related Protein (AgRP)
I neuroni che secernono NPY co-esprimono
anche la Agouti Related Protein (AgRP)
dotata di considerevoli azioni oressigene
NPY-indipendenti.
AgRP determina un aumento dell’introito
alimentare agendo come antagonista
endogeno dei recettori per melanocortina
MC3 e MC4, inibendo così l’azione
anoressizzante di alpha-MSH (ormone
stimolante i melanociti).
24
Agouti Related Protein (AgRP)
La somministrazione i.c.v. acuta di AgRP
nei roditori determina un incremento
dell’introito calorico per sei giorni
Il trattamento cronico determina
importante aumento di peso
un
Rispetto al NPY, l'effetto del AgRP è
minore, ma più prolungato
I neuroni NPY/AgRP rappresentano il
bersaglio più importante dei segnali
oressanti e anoressanti centrali e periferici.
In particolare, essi sono inibiti da leptina,
peptide YY (PYY) e insulina e attivati dal
peptide oressante ghrelina.
25
Pro-opiomelanocortina (POMC)
Il gene della POMC è espresso in diversi
tessuti quali ipotalamo, ipofisi, sistema
immunitario e pelle.
Nell’ipotalamo la POMC è espressa in
particolare nell’ARC
Pro-opiomelanocortina (POMC)
Precursore di molecole biologicamente
attive:
, , e MSH (Melanocortina)
ACTH (Adrenocorticotropina)
endorfine
Lipotrofine
26
Pro-opiomelanocortina (POMC)
MSH è un potente inibitore dell’introito
calorico che agisce attraverso i recettori MC3
e MC4.
Negli animali, la somministrazione centrale
di MSH inibisce l’assunzione di cibo e
riduce il peso corporeo.
Pro-opiomelanocortina (POMC)
I topi knockout per la POMC mostrano un
fenotipo obeso e iperfagico e presentano
un’ipoplasia surrenalica e un’alterazione
della pigmentazione cutanea.
Somministrazione cronica giornaliera di
alpha-MSH inverte questi effetti e determina
un rapido calo ponderale.
27
Pro-opiomelanocortina (POMC)
Nell’uomo, la somministrazione cronica
intranasale di un frammento sintetico di
MSH (MSH/ACTH 4-10) determina una
lieve ma persistente riduzione del grasso
corporeo.
Cocaine and amphetamine-regulated
transcript (CART)
Somministrazione endogena di cannabinoidi e
oppioidi aumentano l’appetito e l’introito
calorico attraverso l’attivazione del recettore
CB1.
CB1 è coespresso con CART e MSH nelle aree
ipotalamiche centrali coinvolte nel controllo
del comportamento alimentare.
28
Cocaine and amphetamine-regulated
transcript (CART)
CART è coespresso in neuroni della POMC
nel ARC ed è direttamente modulato da
leptina.
E’ anche espresso nel
PVN
LH
DMH
NTS
Cocaine and amphetamine-regulated
transcript (CART)
L’iniezione i.c.v. di CART è seguita da una
riduzione dell’introito alimentare perfino
quando co-somministrato con NPY insieme a:
diminuzione della [insulina] plasmatica
diminuzione della [leptina] plasmatica
incremento dell’ossidazione lipidica
29
Orexine
Orexina A (OXA) e B (OXB) sono due peptidi
espressi principalmente nel LH e dati recenti
mostrano la presenza di immunoreattività per
OXA anche a livello viscerale.
Nell’uomo, i livelli
aumentano durante
plasmatici
di
OXA
Digiuno
Ipoglicemia
30
Orexine
In condizioni di digiuno, la OXA:
inibisce la motilità gastrointestinale
inibisce la risposta vagale alla colecistochinina
è coinvolta nella modulazione della secrezione
di insulina e glucagone.
I livelli plasmatici di OXA sono risultati essere
ridotti nell’obesità
Orexine
I topi knockout per le orexine sono narcolettici,
indicando che questi peptidi sembrerebbero
partecipare non solo al controllo dell’omeostasi
tra appetito e peso, ma anche al controllo del
sonno.
31
32
Asse Ipotalamo-Enterico
Il Feedback
Ghrelina
Peptide, isolato nello stomaco, ma espresso
anche da altri tessuti, come pancreas, rene,
testicoli e placenta, e, a livello centrale, da
ipofisi e ipotalamo, in particolare nei ARC e
PVN.
33
Ghrelina
Esercita diverse attività biologiche quali
stimolazione della secrezione di GH, PRL e
ACTH, modulazione dell’asse gonadico,
influenza sul sonno e comportamento, controllo
di motilità e secrezione acida dello stomaco,
effetti cardiovascolari e di modulazione della
proliferazione cellulare.
Ghrelina
34
Ghrelina
Fin dalla sua scoperta, è chiaramente emerso il
ruolo della ghrelina nella regolazione dell’introito
calorico e della spesa energetica, essendo il più
potente ormone periferico oressigeno ad oggi
conosciuto.
Ghrelina
Nell’uomo, i livelli della ghrelina sono aumentati
dal digiuno e dalla restrizione calorica e
diminuiti dall’ingestione di cibo.
Nei roditori la ghrelina stimola l’introito di cibo
in modo dose-dipendente, e, in seguito a
somministrazione
prolungata,
causa
un
aumento di peso, principalmente dovuto
all’incremento della massa grassa corporea.
35
Ghrelina
La ghrelina possiede effetti oressanti e
adipogenici anche dopo somministrazione
sistemica.
L’efficacia di ghrelin come agente oressante
dopo somministrazione periferica si può
spiegare alla luce del suo trasporto attraverso la
barriera ematoencefalica, in direzione sanguecervello.
Ghrelina
La ghrelina nei ratti aumenta l’espressione di
AgRP e NPY sia dopo somministrazione acuta
che cronica.
NPY sembrerebbe mediare un effetto oressante
acuto di ghrelina
AgRP sembrerebbe essere coinvolto in effetti di
più lunga durata
36
Ghrelina
Oltre all’aumento dell’appetito e dell’introito
calorico, l’aumento della massa grassa indotto
dalla ghrelina potrebbe anche essere mediato
da una inibizione dell’ossidazione del grasso
cellulare.
La regolazione da parte della ghrelina
dell’omeostasi energetica viene mediata da
fibre efferenti ed afferenti del nervo vago.
Colecistochinina (CCK)
Presente sia nel sistema nervosa centrale che
nelle cellule endocrine del duodeno e del
digiuno è rilasciata in circolo in presenza di
cibo nel lume intestinale.
Contrazione della colecisti
Secrezione esocrina pancreatica
Riempimento e secrezione acida dello stomaco
Stimola la motilità intestinale
Riduzione dell'introito alimentare nel pasto
37
Colecistochinina (CCK)
Sino a ora sono stati identificati due recettori
del CCK (A e B).
Il recettore di tipo A è più espresso nei tessuti
periferici includendo in essi anche il pancreas,
lo sfintere pilorico e le fibre nervose vagali
afferenti, ma è presente anche in strutture del
CNS.
Il recettore di tipo B è ampiamente distribuito a
livello del SNC.
Colecistochinina (CCK)
Il blocco dei recettori CCK di tipo A, ma non di
tipo B, si oppone all'effetto saziante della
somministrazione esogena di CCK portando
inoltre, nel ratto, a un aumento dell'introito
alimentare basale a causa di un'inibizione
dell'azione della CCK endogena.
38
Colecistochinina (CCK)
Somministrazione periferica di CCK promuove
il senso di sazietà indirettamente attraverso
l'inibizione dello svuotamento gastrico, che a
sua volta attiva i segnali vagali afferenti, o
direttamente, agendo su specifici recettori
presenti sui neuroni delle vie vagali afferenti al
SNC.
Colecistochinina (CCK)
Entrambi questi meccanismi richiedono
l'integrità del nervo vago ed in particolare di
quelle fibre vagali responsive al CCK che
terminano a livello del NTS
39
Insulina
L’insulina è il principale ormone regolatore
della glicemia e gioca un ruolo fondamentale
nel controllo dell’appetito.
Nel cervello sono espressi recettori per
l’insulina, in particolare livello di ipotalamo,
ippocampo e della corteccia cerebrale.
L’insulina attraversa barriera emato-encefalica
L’insulina inibisce l’appetito a livello del SNC.
Insulina
Somministrata direttamente a livello centrale:
Soppressione dell’introito di cibo
Inibizione della gluconeogenesi a livello
epatico tramite un segnale a livello ipotalamico.
40
Insulina
Delezione selettiva dei recettori a livello SNC:
Iperfagia
Obesità
Insulino-resistenza
41
Peptide YY (PYY)
Il Peptide YY (PYY) è un peptide membro della
famiglia NPY e secreto dalle cellule-L del
piccolo e grande intestino, incluso il retto e
mostra effetti anoressanti.
Esercita il suo effetto modulatorio sull'introito
di cibo agendo sui recettori Y2 a livello
ipotalamico, e, di conseguenza, sopprimendo
l'effetto oressante di NPY.
Peptide YY (PYY)
PYY non riduce l'introito calorico nei topi
knockout per Y2
Nell' uomo la somministrazione di PYY è
seguita da una riduzione del 30% del totale dei
nutrienti ingeriti rispetto al placebo ed è
accompagnata da una sensazione di sazietà.
42
Peptide YY (PYY)
I livelli plasmatici di PYY aumentano dopo
l'ingestione di cibo.
Negli obesi i livelli plasmatici a digiuno di PYY
sono più bassi e mostrano un incremento più
lento e ritardato dopo il pasto.
Peptide YY (PYY)
PYY sembra contrastare l'azione della ghrelina
sia a livello delle afferenze vagali sia a livello
ipotalamico, in particolare nell'ARC.
PYY è coinvolto quindi sia nel controllo a breve
che a lungo termine del peso.
43
Leptina
Leptina è un peptide espresso e secreto dal
tessuto adiposo bianco, in modo proporzionale
alla massa di grasso corporeo.
Leptina aumenta alcune ore prima dei pasti nei
roditori
e
dopo
diversi
giorni
di
iperalimentazione negli uomini, mentre si
riduce in corso di digiuno.
Leptina
44
Leptina
Svolge la sua attività principale a livello
centrale, in particolare nell’ARC e nel PVN,
attraverso l’attivazione di specifici recettori
chiamati OB-Rb.
Nello specifico inibisce i neuroni NPY e AgRP,
portando a una riduzione dell’introito di cibo.
Ghrelina-Leptina
45
Leptina
I topi knockout per leptina o per il recettore di
leptina sono obesi, iperfagici e iperinsulinemici
Nell’uomo mutazioni che portano al difetto di
leptina sono rara causa di obesità che si
normalizza durante terapia sostitutiva.
Nell’uomo l’obesità è fortemente associata ad
alti livelli plasmatici di leptina, suggerendo
invece una condizione di leptina-resistenza.
Leptina
La secrezione di leptina è regolata da diversi
segnali metabolici e ormonali il rilascio gastrico
di leptina è anche stimolato in modo
consistente dall’attivazione delle afferenze
vagali, suggerendo così che questo ormone sia
coinvolto non solo nel mantenimento a lungo
termine del bilancio del peso ma anche nella
fase cefalica della digestione.
46
Adiponectina
Adiponectina
è
un
peptide
prodotto
esclusivamente dagli adipociti che dimostra
un’omologia strutturale con la famiglia delle
citochine TNF caratterizzate dall’avere un
effetto negativo sul bilancio energetico
I livelli di adiponectina non seguono ritmi
circadiani e sembrano non essere influenzate
all’alimentazione. Tuttavia, adiponectina è
correlata negativamente con il BMI.
Adiponectina
L’evidenza di livelli di adiponectina più bassi
nei soggetti diabetici obesi che nei soggetti
obesi non diabetici, suggerisce un ruolo
importante di adiponectina nello sviluppo
dell’insulino-resistenza.
47
Glucagon-like-peptide-1 (GLP-1)
Il GLP-1 è un peptide derivato dallo stesso
precursore del glucagone, espresso e secreto
dalle cellule endocrine-L della mucosa
intestinale a livello dell’ileo e del colon.
GLP-1 mostra diverse attività, tra cui la capacità
di aumentare la secrezione di insulina e di
sopprimere quella di glucagone nella fase
postprandiale.
Glucagon-like-peptide-1 (GLP-1)
Negli animali e nell’uomo GLP-1 rallenta lo
svuotamento gastrico e quindi attenua la
risposta insulinica indotta dal cibo.
Oltre a tali effetti endocrino-metabolici, studi
recenti hanno mostrato che GLP-1 sarebbe in
grado di inibire anche l’appetito e di ridurre
l’introito di cibo.
48
Glucagon-like-peptide-1 (GLP-1)
Somministrazione centrale di GLP-1 inibisce
l’introito di cibo e acqua con un effetto
specifico ma anche antagonizzando l’effetto
oressante di NPY.
Questo effetto è dose-dipendente e prolungato
nel tempo.
Amilina
Amilina è un peptide sintetizzato neitessuti
periferici, co-secreto con l’insulina.
Amilina modula la regolazione dell'introito di
cibo agendo attraverso recettori specifici e
anche attraverso i recettori D2 per la dopamina
nel SNC.
La somministrazione di amilina, anche in
condizioni di digiuno, inibisce l'introito di cibo
e lo svuotamento gastrico.
49
Resistina
Resistina è secreta dal tessuto adiposo ed
esercita la propria attività su diversi tessuti
periferici, come il fegato e il muscolo.
Sembra possedere effetti inversi rispetto
all’adiponectina; infatti, livelli più alti possono
aumentare l’insulino-resistenza.
50
51
52
53
54
55
56