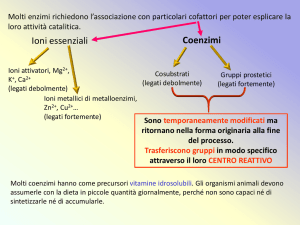
In enzimologia con il termine cofattore si intende una piccola molecola di
natura non proteica o uno ione metallico che si associa all'enzima e ne
rende possibile l'attività catalitica tipica dell'enzima stesso. La maggior
parte degli enzimi che richiedono il legame a cofattori, infatti, perde ogni
funzionalità in caso di assenza del cofattore stesso.
I COENZIMI
Sulla base della loro natura chimica, i cofattori sono suddivisi in
• metalli e
• coenzimi (intesi come piccole molecole organiche
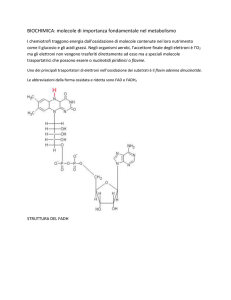
I COENZIMI DINUCLEOTIDICI: NAD+ E FAD
NAD e FAD sono i coenzimi delle deidrogenasi, la classe di enzimi che
catalizza le reazioni di ossido-riduzione. Entrambi sono dinucleotidi contenenti
AMP. I due mononucleotidi sono uniti da un legame fosfoanidridico.
(Nicotinammide adenina dinucleotide ossidato)
Flavina adenin dinucleotide
Il flavin-mononucleotide (FMN) è anche presente come gruppo
prostetico (parte non proteica essenziale alla funzione) nel 1° complesso
della catena respiratoria.
Il NAD, nicotinamide adenindinucleotide è un derivato dell’acido nicotinico detto anche niacina,
vitamina PP o vitamina B3. e funge da coenzima nelle reazioni di ossidoriduzione biologiche
Di grande importanza è anche la forma fosforilata del NAD, indicata come NADP .
La niacina si trova nella carne, nelle uova e nel lievito
Il NAD+, ed il suo analogo fosforilato NADP+ (sono le forme ossidate), possono essere ridotte a
NADH e NADPH
Acido nicotinico
o niacina
Nicotinammide
Il NAD+ è il coenzima nelle reazioni di ossidazione dei gruppi alcolici ad aldeidici e dei
gruppi aldeidici a carbossilici (esempi nella glicolisi e ciclo di Krebs).
Il MECCANISMO di ossidoriduzione è:
Il NADH trasporta 2 elettroni e 1 H+. (cioè uno ione idruro H-)
Il secondo H+ liberato dall’ossidazione del substrato è libero nel mezzo.
H
H
Ricorda!!
Nicotinammide
ossidata NAD+
H2
Nicotinammide
ridotta NADH
Quando un composto si
ossida cede gli e ad uno
che si riduce e il NAD è
molto spesso colui che
cede o acquista gli e nelle
reazioni biochimiche
nelle cellule gli enzimi catalizzano reazioni redox utilizzando dei
trasportatori di e- : NAD+ , NADP+ , FMN e FAD
NAD+: nicotinamide adenin dinucleotide
gruppo
reattivo
H
O
C
O
C H2 O
O P O-
H
+
O
H
OH
OH
O P OO
2H+ + 2e-
H
C H2 O
H
H
N
H
N
esterificato con
gruppo fosforico nel
NADP+
H
+ H+
H
OH
OH
N H2
N
C H2 O
H
adenina
H
H
O
N
OH
-
P O
O P O-
H
OH
O
N H2
N
C H2 O
O
N H2
N
O
C
N H2
N
H
O
H H
H
N
H
H
OH
OH
N
N
+
NAD +
SH2
NADH + S + H
+
NADP +
SH2
NADPH + S + H
substrato
ridotto
+
+
(1)
(2)
substrato
ossidato
nell’ossidazione di un substrato il NAD+ accetta un protone e due elettroni
= uno ione idruro e uno ione idrogeno viene rilasciato in soluzione
[NAD+ ]
= valore elevato reazione (1) favorita ossidazioni cataboliche
prodotti finali poveri di E
[NADH]
[NADP+ ]
[NADPH]
= valore basso reazione (2) sfavorita riduzioni anaboliche
prodotti finali macromolecole
es. enzimi: ossidoriduttasi o deidrogenasi
+
NAD + CH3 CH2 OH
NADH + CH3 CHO + H
la reazione è catalizzata dall’enzima alcol deidrogenasi
+
Ricorda l’ossidazione di un
alcol porta ad un aldeide e
riduce il NAD+
L’’addizione di uno ione idruro a un anello piridinico è alla base di molti processi riduttivi
in ambiente biologico
Il NAD+è in grado di ossidare alcoli a composti carbonilici mediante formale addizione di un idruro
La reazione avviene in posizione 4 poiché il processo avviene all’’interno di un sito attivo enzimatico, ma il processo è
del tutto analogo a quanto visto in precedenza.
Il NADP+ differisce dal NAD+ per la presenza di un gruppo fosfato sul
carbonio 2 del riboso che porta l’adenina.
Il NADPH è il donatore di elettroni nelle biosintesi riduttive
O
C H3
N
H
NH
O
C H3
N
C H3
N
N
R
H
NH
+ 2H+ +2eC H3
N
O
C H3
C H3
forma ossidata
NH
N
O
OH
H C
OH
H C
OH
FAD:
flavin adenin
dinucleotide
C H2
N
C H3
N
N
N
N
-O P O C H
2
O
O
H
H
H
H
OH
O
N
N
C H2
N
O P O
O
FADH2
C H3
N H2
O
OH
O
forma ridotta
FAD
La riduzione avviene come scambio di
atomi di H da un substrato riducente
C H2
H C
O
R
N
N
N
FMN:
flavin
mononucleotide
H C
OH
H C
OH
H C
OH
C H2
O
O P O
OH
O