Neoplasie del testicolo
II Università degli Studi di Napoli - Sede di Caserta – A.A. 2007-2008
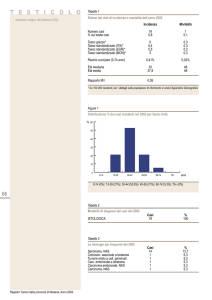
EPIDEMIOLOGIA
Rappresenta la neoplasia più comune nei
maschi di età compresa tra i 20 ed i 35 anni
Bassa mortalità
Alto indice di curabilità
CAUSE E FATTORI DI RISCHIO
Precedenti neoplasie testicolari
Criptorchidismo
Sindrome di Klinefelter
Familiarità
Atrofia testicolare
ISTOPATOLOGIA
Neoplasie germinali (95%) Neoplasie non germinali (5%)
Seminoma
Tipico
Spermatocitico
Con sinciziotrofoblasti
Anaplastico
Non seminoma
Carcinoma embrionale
Tumore del sacco vitellino
Corioncarcinoma
Teratoma
Delle cellule interstiziali (di
Leydig)
Delle cellule di Sertoli
Androblastoma
Stromali (fibromi, sarcomi, mesoteliomi, linfomi)
Forme miste
costituite da seminoma e non
seminoma o da vari tipi di non
seminoma
Seminoma classico (cellule uniformi con nuclei centrali, ben delineati.
I rari spazi chiari rappresentano aree di depositi di glicogeno) (H&E, ×50)
Seminoma con cellule giganti sinciziotrofoblasti.
Questo pattern istologico si può osservare nei seminomi HCG+ . I setti
fibrovascolari con infiltrati linfoidi sono un tipico riscontro nei seminomi
(H&E, ×25)
Seminoma spermatocitico. Distinto istologicamente dal
seminoma classico per la relativa mancanza di setti fibrovascolari,
infiltrato linfoide, e marcata variabilità del volume cellulare
(H&E, ×100)
Carcinoma embrionale. Confrontato con il seminoma classico
si nota il pleiomorfismo cellulare e nucleare ed il pattern sinciziale
(perdita dei confini cellulari) (H&E, ×50)
Tumore a cellule germinali misto, con elementi di
seminoma e carcinoma embrionale. Si noti la presenza di setti
fibrovascolari con infiltrato linfoide (tipici del seminoma
classico) e isole di carcinoma embrionale. (H&E, ×25)
Teratoma Immaturo. Si noti la differenziazione
primitiva in senso neurale (H&E, ×25)
Coriocarcinoma. I due tipi di cellule necessari per fare diagnosi sono presenti
Cellule sinciziotrofoblastiche (cellule giganti con nuclei ipercromatici
e abbondante citoplasma eosinofilo) sono presenti nel quadrante sup. dx.
Citotrofblasti (sheets of cells with single nuclei and abundant clear cytoplasm)
Sono presenti nella parte centrale della foto. Hemorrhagic infiltrate at the
bottom of the photomicrograph is common in choriocarcinoma. (H&E, ×25)
Yolk Sac Tumor, pattern microcistico. (H&E, ×25)
SEGNI E SINTOMI
Paziente asintomatico
Presenza di tumefazione scrotale
Inguino-orchidinia
Idrocele
Algie lombari e/o addominali
Stipsi e/o sintomatologia urinaria
Nausea, vomito
Dolore toracico e/o tosse
Linfoadenopatia sovraclaveare o addominale
Ginecomastia e pigmentazione del capezzolo
(corioncarcinoma o tumori a cellule del Sertoli)
Segni di virilizzazione (tumori a cellule del Leydig)
ESAMI DIAGNOSTICI
Palpazione bimanuale della gonade
Ecografia gonadica
Dosaggio di : α-FP, β-HCG, LDH, fosfatasi alcalina
NO AGOASPIRATO
α-FP : è elevata nel 65-70% dei carcinomi embrionali, teratomi e
nei tumori del sacco vitellino. Tempo di dimezzamento < 5
giorni
β-HCG : è elevata sia nei non-seminomi che nei seminomi come
la variante sinciziotrofoblastica. Tempo di dimezzamento < 1
giorno
STADIAZIONE
STADIAZIONE
Preoperatoria
RX torace
Ecografia addomino-pelvica
Postoperatoria
TAC total body
Dosaggio dei biomarcatori
TRATTAMENTO
Chirurgia
Chemioterapia
Radioterapia
CHIRURGIA
Orchifunilectomia preceduta da clampaggio con
pinza vascolare del funicolo spermatico: rappresenta il
primo tempo diagnostico-terapeutico
Prima e dopo l’intervento si deve effettuare il dosaggio
dei biomarcatori e valutarne il tempo di dimezzamento
Linfoadenectomia retroperitoneale: viene eseguita
solo dopo l’orchiectomia al fine di conoscere l’istotipo.
Trova indicazione in tutti i tumori ad eccezione del
seminoma puro e del corioncarcinoma puro.
SEMINOMA PURO - STADIO I
(Tis-4, N0, M0)
Orchiectomia inguinale radicale seguita da :
Vigile attesa o
RT sui linfonodi paraaortici ed eventualmente
estesa agli iliaci omolaterali o
2 cicli di CT con Carboplatino o PEB
SEMINOMA PURO - STADIO II
anyT No Mo S1-3; anyT N1-3 M0 Sx; any T N+ M0 S0-1
Orchiectomia inguinale radicale seguita da :
Metastasi ai lnf retroperitoneali < 5 cm (N2) → RT
a campi estesi sui lnf paraaortici ed iliaci omolaterali
Metastasi ai lnf retroperitoneali > 5 cm (N3) → RT
→ 3-4 cicli di PEB → RT in caso di mancata RC
SEMINOMA PURO - STADIO III
any T any N M+ Sx-3
Orchiectomia inguinale radicale seguita da :
Poli-CT
Nei pazienti con malattia bulky dopo CT
NB: il consolidamento della risposta con RT o CH
sembra predisporre ad un medesimo rischio
di ricaduta
Distribution of retroperitoneal nodal metastases
in an early-stage nonseminoma germ cell tumor.
NON SEMINOMA - STADIO I
(Tis-4, N0, M0)
Orchiectomia inguinale radicale seguita da :
Linfoadenectomia retroperitoneale con tecnica
“nerve sparing”
Vigile attesa per 3-5 anni con l’avvio di 3 cicli di
PEB in caso di innalzamento dei marcatori e/o
evidenza strumentale di metastasi
3-4 cicli di CT immediata per i pazienti ad alto
rischio (invasione linfatica o vascolare, ca embrionale e
assenza di yolk sac elements)
NON SEMINOMA - STADIO II
anyT No Mo S1-3; anyT N1-3 M0 Sx; any T N+ M0 S0-1
Orchiectomia inguinale radicale seguita da :
Linfoadenopatie < 3 cm → linfoadenectomia
Linfoadenopatie > 3 cm → 3 cicli di PEB seguiti
da intervento chirurgico per le masse residue
CT adiuvante in pazienti con :
- dissezione linfonodale incompleta
- persistente elevazione dei biomarcatori
- linfonodi coinvolti > 6 con dimensioni > 2 cm
NON SEMINOMA - STADIO III
any T any N M+ Sx-3
A buona prognosi :
sorveglianza in coloro che hanno ottenuto una RC
3 cicli di PEB
resezione chirurgica in caso di residuo di malattia
Teratoma maturo o immaturo carcinoma
niente
altri 2 cicli di PEB
NON SEMINOMA - STADIO III
A cattiva prognosi : 4 cicli di PEB