Metabolismo: visione generale
•
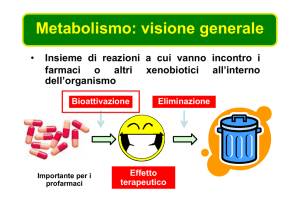
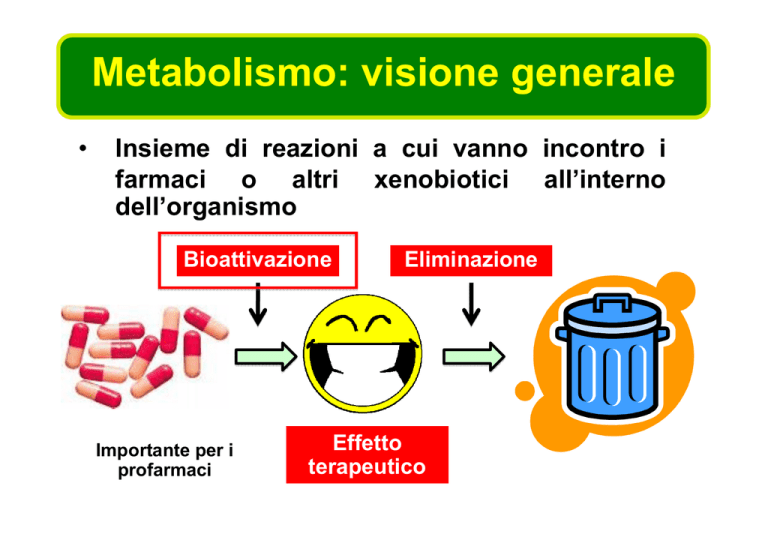
Insieme di reazioni a cui vanno incontro i
farmaci o altri xenobiotici all’interno
dell’organismo
Bioattivazione
Importante per i
profarmaci
Eliminazione
Effetto
terapeutico
Profarmaci: famciclovir
N
N
H2N
N
Aldehyde oxidase
Esterase / hydrolysis
N
O
N
HN
H2N
N
N
HO
AcO
AcO
Famciclovir
Antiviral (Herpes etc)
Pro-drug
HO
Penciclovir
Profarmaci: L-DOPA
H
COOH
NH2
NH2
L-DOPA
decarbossilasi
OH
OH
HO
L-DOPA
HO
dopamina
Metabolismo: visione generale
•
Insieme di reazioni a cui vanno incontro i
farmaci o altri xenobiotici all’interno
dell’organismo
Bioattivazione
Es.: paracetamolo
Effetto
Tossico
Metabolismo del paracetamolo
Metabolismo: visione generale
•
Insieme di reazioni a cui vanno incontro i
farmaci o altri xenobiotici all’interno
dell’organismo
Eliminazione
Es.: etanolo
Effetto
Tossico
Metabolismo: visione generale
•
Insieme di reazioni a cui vanno incontro i
farmaci o altri xenobiotici all’interno
dell’organismo
Bioattivazione
Es.: rifampicina,
fenitoina
Eliminazione
Mancato
effetto
terapeutico
Metabolismo: visione generale
•
Insieme di reazioni a cui vanno incontro i
farmaci o altri xenobiotici all’interno
dell’organismo
•
Generalmente dopo metabolismo i farmaci
sono piu’ polari e piu’ idrosolubili
•
Le sedi principali per il metabolismo sono
fegato, tratto gastrointestinale, reni, polmoni
(anche altre sedi)
•
La conversione metabolica avviene di solito
per via enzimatica (reazioni di fase I e II)
Reazioni di fase I
•
Hanno la finalita’ di inserire o mettere in
evidenza nel substrato gruppi funzionali di
legami (funzionalizzazione)
Ossidazione
Riduzione
Idrolisi
Citocromo P450-dipendenti
Citocromo P450-indipendenti
Citocromo P450
•
NADPH
NADP
O2
RH
H2O
R-OH
0
5
4
P-
R
tt
u
ed
i
s
a
Superfamiglia di emoproteine
enzimatiche identificate con la
sigla CYP seguita da un
numero
(famiglia),
lettera
(sottofamiglia) e un numero
(singolo gene)
Es. CYP3A4, CYP3A5
•
Localizzato
prevalentemente
nel reticolo endoplasmatico del
fegato (frazione microsomiale)
•
Specificita’, velocita’ e affinita’
diverse per vari substrati a
seconda del sottotipo CYP
Reazioni di fase I
•
Hanno la finalita’ di inserire o mettere in
evidenza nel substrato gruppi funzionali di
legami (funzionalizzazione)
Ossidazione
Riduzione
Idrolisi
Citocromo P450-dipendenti
Citocromo P450-indipendenti
Esempi
Alcol e aldeide deidrogenasi
Xantina ossidasi
Monoamminossidasi
Reazioni di fase I
•
Hanno la finalita’ di inserire o mettere in
evidenza nel substrato gruppi funzionali di
legami (funzionalizzazione)
Ossidazione
Riduzione
Idrolisi
Esempio
Acetilcolinoesterasi (AChE)
Reazioni di fase II
•
Usano i gruppi funzionali come “terminale”
per la coniugazione con molecole diverse
Acetilazione
Metilazione
Coniugazione con glutatione
Coniugazione con aminoacidi
Coniugazione con glucuronato
•
Prevedono il consumo di energia, fornita
direttamente o indirettamente dall’ATP
Fasi del metabolismo dei farmaci
Alcuni farmaci subiscono solo
il metabolismo di fase II
Farmaco
FASE I
Ossidazione
Riduzione e/o
idrolisi
FASE II
Prodotti di
coniugazione
(Solitamente Inattivo)
Il farmaco può risultare attivato, immodificato,
o nella maggior parte dei casi, inattivo
Avvengono prevalentemente nel fegato (poi reni e polmoni)
Entrambi gli stadi (fase I e fase II) sono responsabili
generalmente di una riduzione della liposolubilità del farmaco
e quindi aumentano la velocità di eliminazione renale
Fasi del metabolismo dei farmaci
Fasi del metabolismo dei farmaci
Coniugazione con acido
glucuronico
(Fase II)
morfina
(Fase I)
N-demetilazione
Fasi del metabolismo dei farmaci
Metabolismo dei farmaci:
microflora intestinale
• Per farmaci assunti per os la flora microbica imtestinale
puo’ essere rilevante (potenzialita’ biotrasformativa ≥
fegato)
• Biotrasformazioni da flora intestinale essenzialmente di
tipo riduttivo (ambiente anaerobico)
• Flora intestinale potenzialmente coinvolta nel ricircolo
enteroepatico
Fattori che modificano il
metabolismo di xenobiotici
Specie
Differenze tra organismi nell’abilita’ a metabolizzare
particolari sostanze sono alla base di tossicita’ selettiva
(es. Malation)
Età e sesso
In generale feti, neonati e anziani hanno una capacità
limitata per la trasformazione di xenobiotici rispetto agli
adulti. Es. cloranfenicolo, etanolo
Variabilità
genetica
Ad es. reazioni di acetilazione (fase II) e’ influenzata da
fenotipo “lento” o “rapido”. Es. isoniazide.
Nutrizione e Scarsa nutrizione e malattie (es. epatite) influiscono
malattie
negativamente sul metabolismo di xenobiotici.
Esposizione Precedente o simultanea esposizione ad un xenobiotico
ad altre
puo’ portare a inibizione o induzione enzimatica (es. DDT,
sostanze
alcool, fumo di sigaretta)
Dose
Puo’ influire la natura della biotrasformazione (dose
soglia per la tossicità). Es. paracetamolo
Eliminazione: visione generale
• Descrive quella serie di processi che sono alla
base della rimozione di xenobiotici assorbiti
attraverso l’escrezione e/o biotrasformazione
PRINCIPALI
RENALE
FECALE
SECONDARIE
POLMONARE
CUTANEA
SALIVARE
LACRIMALE
MAMMARIA
Escrezione renale
• La funzione principale dei reni e’ l’escrezione di composti
di
scarto
e/o
riassorbimento)
tossici
(filtrazione,
secrezione,
• 130 ml/min vengono filtrati a livello glomerulare (> 150 L
al giorno!!!!) 99% normalmente riassorbito
• Proteine plasmatiche (e farmaci legati ad esse) non
attraversano di norma i filtri glomerulari
• L’eliminazione di farmaci acidi e’ favorita alcalinizzando
le urine (e ostacolata acidificando le urine)
Escrezione renale
Escrezione renale
Escrezione renale
Escrezione fecale
• Il fegato svolge due diverse importanti funzioni sui
farmaci nell’organismo: metabolismo ed escrezione
• Farmaci incapaci di passare la membrana cellulare
vengono trasportati molto efficientemente nella cellula
epatica da vari sistemi di trasporto
• L’escrezione dei farmaci nella bile e’ favorita da due
caratteristiche fisiche: polarita’ e peso molecolare
• L’escrezione biliare puo’ avere particolare importanza
per farmaci assunti per os (effetto di primo passaggio)
Escrezione fecale
• Una volta escreto nella
bile,
viene
un
farmaco
non
necessariamente
eliminato
(ricircolo
enteroepatico)
Cinetiche di eliminazione
Cinetiche di I ordine
La quantita’ di xenobiotico eliminata
per unita’ di tempo e’ una percentuale
Le cinetiche di I ordine indicano in
genere
che
dall’organismo
avviene
l’eliminazione
per
lo
tramite meccanismi diffusionali
trasportatori non saturati.
piu’
o
L’eliminazione della maggiorparte degli
xenobiotici segue una cinetica di I
ordine.
100
% di xenobiotico
da eliminare
costante di quella che rimane da
eliminare.
0
Tempo
Cinetiche di eliminazione
Cinetiche di ordine 0
La quantita’ di xenobiotico eliminata
Le cinetiche di ordine 0 indicano che
l’eliminazione dall’organismo si basa
su
processi
metabolici
escrezione attivi saturati.
e/o
di
Al di sotto di concentrazioni saturanti le
cinetiche di eliminazione di ordine 0
possono seguire andamenti di I ordine.
100
% di xenobiotico
da eliminare
per unita’ di tempo e’ costante (flusso
indipendente dalla concentrazione).
0
Tempo
Comparison
• First Order Elimination
• Zero Order Elimination
– [drug] decreases
exponentially w/ time
– [drug] decreases linearly
with time
– Rate of elimination is
proportional to [drug]
– Rate of elimination is
constant
– Plot of log [drug] or
ln[drug] vs. time are
linear
– Rate of elimination is
independent of [drug]
– t 1/2 is constant
regardless of [drug]
– No true t 1/2
Emivita (t1/2)
• L’intervallo
di
tempo
necessario
affinche’
concentrazione plasmatica si riduca del 50%
la
• E’ indipendente dai valori di concentrazione iniziale di
xenobiotico
• Fornisce una misura dell’efficienza dei processi di
eliminazione dell’organismo nei confronti di un dato
xenobiotico
• Dipende da stato funzionale degli organi o sistemi
dell’individuo
xenobiotico
preposti
all’eliminazione
di
un
dato
Emivita (t1/2)
• Solitamente farmaci con elevato Vd hanno una emivita
lunga
• Alterazioni dei valori di emivita richiedono correzioni del
regime terapeutico
Half-Life
• C = Co e - kt
• C/Co = 0.5 for half of the original amount
• 0.5 = e – k t
• ln 0.5 = -k t ½
• -0.693 = -k t ½
• t 1/2 = 0.693 / k
N° di t½
0
1
2
3
4
5
6
7
8
9
10
Frazione di xenobiotico
rimanente
100%
50%
25%
12.5%
6.25%
3.125%
1.56%
0.78%
0.39%
0.195%
0.0975%
*** Sono neccessarie 10 emivite per eliminare il 99,9%***
Clearance
• Puo’ essere definito come il volume di sangue
virtualmente ripulito nell’unita’ di tempo dai processi
di eliminazione
• Clearance d’organo e clearance totale
• Puo’ essere influenzata da vari fattori (es. malattie,
presenza di altre sostanze, legame alle proteine, grado
di ionizzazione, eta’)
• Per farmaci eliminati per via renale, la loro clearance
puo’ essere uguale, maggiore o minore di 130 ml/min
Somministrazioni ripetute e
stato stazionario
Condizione di equilibrio, raggiunta in corso di
somministrazioni ripetute di farmaco, in cui la
quantità di farmaco assorbito è uguale alla
quantità di farmaco eliminato
Effetto
Tossico
Effetto
terapeutico
Somministrazioni ripetute e
stato stazionario
Condizione di equilibrio, raggiunta in corso di
somministrazioni ripetute di farmaco, in cui la
quantità di farmaco assorbito è uguale alla
quantità di farmaco eliminato
Nel caso di un trattamento con una dose
costante di farmaco lo stato stazionario si
raggiunge in un
intervallo di tempo
corrispondente a 4-5 emivite
Loading dose(s)
Loading dose
Cp
time
Loading Dose
Dose = Cp(Target) x Vd
Principali parametri
farmacocinetici
Cmax: concentrazione massima
Tmax: tempo per raggiungere la Cmax
AUC: area sotto la curva
F%: biodisponibilità
T½: tempo necessario perché la concentrazione
plasmatica si riduca della metà
Vd: volume di distribuzione
Cl: clearance