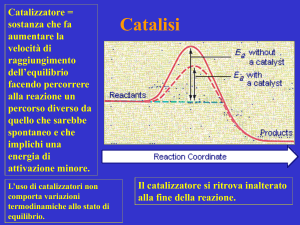
Chimica Verde e Catalisi
Chimica Metallorganica e Catalisi
Green Chemistry e Catalisi
Dario Duca
Dipartimento di Fisica e Chimica dell’Università di Palermo
Chimica Metallorganica e Catalisi, A.A. 2015 – 2016
Chimica Metallorganica e Catalisi
Dipartimento di Fisica e Chimica dell’Università di Palermo
Chimica Verde e Catalisi
Indice
Chimica Verde e Catalisi
Chimica Verde
Catalisi: uno Sguardo d’Insieme
Catalysis: Concepts and Green Applications
Lecture slides for Chapter 1: Introduction to
catalysis, green chemistry, and sustainable
development.
Most of the graphics here were drawn using
PowerPoint and Chemdraw (version Ultra 9.0).
Feel free to modify and/or add your own
pyrotechnics.
Please send any feedback to
[email protected]
Catalysis/ Rothenberg, ISBN 978-3-527-31824-7.
Chimica Metallorganica e Catalisi
www.catalysisbook.org
Dipartimento di Fisica e Chimica dell’Università di Palermo
Chimica Verde e Catalisi
Chimica Verde
Indice
Chimica Verde e Catalisi
Chimica Verde
Catalisi: uno Sguardo d’Insieme
Chimica Metallorganica e Catalisi
Dipartimento di Fisica e Chimica dell’Università di Palermo
Chimica Verde e Catalisi
Chimica Verde
Produzione Sostenibile
The big picture
I Sustainable Development: “...
Meets the needs of the current
generation without sacrificing the
ability to meet the needs of future
generations...”;
I perché la produzione possa essere
considerata sostenibile bisogna, in
ambito chimico, rispettare alcuni punti
cardine (Green Chemistry) di
seguito riassunti:
Strategic goal
Sustainable
development
Practical approaches
Operational tools
Green
chemistry
Catalysis
Green
engineering
Waste
management
Industrial
ecology
Process
intensification
Renewable
energy
Monitoring tools
Life-cycle
assessment
• prevenire, piuttosto che trattare, rifiuti;
E-factor,
atom economy
• progettare metodi sintetici
atomisticamente efficienti;
Catalysis/ Rothenberg, ISBN 978-3-527-31824-7.
Chimica Metallorganica e Catalisi
www.catalysisbook.org
Dipartimento di Fisica e Chimica dell’Università di Palermo
Chimica Verde e Catalisi
Chimica Verde
Produzione Sostenibile
The big picture
• scegliere vie sintetiche che usino,
quando possibile, composti non
tossici;
Strategic goal
• progettare nuovi prodotti che
preservino le funzionalità, riducendo
la tossicità;
• minimizzare l’impiego di reagenti e
solventi;
Sustainable
development
Practical approaches
Operational tools
Green
chemistry
Catalysis
Green
engineering
Waste
management
Industrial
ecology
Process
intensification
Renewable
energy
Monitoring tools
Life-cycle
assessment
• progettare processi che minimizzino
l’uso di risorse energetiche;
E-factor,
atom economy
Catalysis/ Rothenberg, ISBN 978-3-527-31824-7.
Chimica Metallorganica e Catalisi
www.catalysisbook.org
Dipartimento di Fisica e Chimica dell’Università di Palermo
Chimica Verde e Catalisi
Chimica Verde
Produzione Sostenibile
The big picture
• usare, quando possibile, materiali di
partenza rinnovabili;
• evitare non necessari processi
preliminari e/o paralleli;
• rimpiazzare processi stechiometrici
con processi catalitici;
Strategic goal
Sustainable
development
Practical approaches
Operational tools
Green
chemistry
Catalysis
Green
engineering
Waste
management
Industrial
ecology
Process
intensification
Renewable
energy
Monitoring tools
Life-cycle
assessment
E-factor,
atom economy
Catalysis/ Rothenberg, ISBN 978-3-527-31824-7.
Chimica Metallorganica e Catalisi
www.catalysisbook.org
Dipartimento di Fisica e Chimica dell’Università di Palermo
Chimica Verde e Catalisi
Chimica Verde
Produzione Sostenibile
The big picture
• progettare nuovi prodotti
bio-degradabili;
Strategic goal
• sviluppare metodi real-time ed on-line
di analisi e monitoring di processo;
• scegliere feed-stock e progettare
processi che minimizzino le possibilità
di incidenti
Sustainable
development
Practical approaches
Operational tools
Green
chemistry
Catalysis
Green
engineering
Waste
management
Industrial
ecology
Process
intensification
Renewable
energy
Monitoring tools
Life-cycle
assessment
E-factor,
atom economy
Catalysis/ Rothenberg, ISBN 978-3-527-31824-7.
Chimica Metallorganica e Catalisi
www.catalysisbook.org
Dipartimento di Fisica e Chimica dell’Università di Palermo
Chimica Verde e Catalisi
Chimica Verde
REACH: EU
Directive on the Registration, Evaluation,
The drivers of green chemistry
and Assessment of Chemicals
Economic benefit
Lower
capital investment
Lower
operating costs
Societal pressure
Government legislation
Improved
public image
Safer
and smaller plants
Pollution control
Less
hazardous materials
Green chemistry
High fines for waste
Producer
responsibility
Catalysis/
Rothenberg, opinione
ISBN 978-3-527-31824-7.
iniziative
di governo,
pubblica e beneficiwww.catalysisbook.org
economici guidano la
green-chemistry
Chimica Metallorganica e Catalisi
Dipartimento di Fisica e Chimica dell’Università di Palermo
Chimica Verde e Catalisi
Chimica Verde
E-factor e Atom Economy
Al di là dei proclami dei produttori, è possibile introdurre parametri obiettivi che
definiscano la sostenibilità di un processo:
I conversione dei reagenti (c);
I selettività dei prodotti (si );
I quantità complessiva di un dato prodotto c·si in un tempo di riferimento;
I i tre punti di sopra si riassumono nel termine: efficienza del processo (della
reazione) in considerazione;
I questa può, fra l’altro, essere stimata con l’E-factor (Enviromental Factor)
Chimica Metallorganica e Catalisi
Dipartimento di Fisica e Chimica dell’Università di Palermo
Chimica Verde e Catalisi
Chimica Verde
E-factor e Atom Economy
I il parametro E-factor (R.A. Sheldon, 1994) è così definito: E-factor =
Kgwaste
Kgproduct
I nella tabella l’E-factor è messo in relazione alla produzione di diversi settori
industriali:
I waste è tutto ciò che non sia product;
I i parametri E-factor ed atom economy (B. Trost, 1991) sono comparabili ma l’uno
fa riferimento alle masse coinvolte l’altro alle specie elementari in gioco;
I reazioni a più step e con “passaggi stechiometrici” aumentano il valore
dell’E-factor
Chimica Metallorganica e Catalisi
Dipartimento di Fisica e Chimica dell’Università di Palermo
Chimica Verde e Catalisi
Chimica Verde
Attività, Selettività, E-factor e Atom Economy
I come esempio, consideriamo un processo specifico:
Oxidation of diphenylmethanol to benzophenone
stoichiometric reagents
+ 2CrO3 + 3H2SO4
3
OH
diphenyl methanol
3
+ 2Cr2(SO4)3 + 6H2O
waste
O
benzophenone
I per un caso ideale (mai realistico) con selettività 100%, il parametro E-factor è:
Catalysis/ Rothenberg, ISBN 978-3-527-31824-7.
www.catalysisbook.org
I nel passato, considerato il passaggio diretto da difenilmetanolo
a benzofenone, il processo era considerato pulito
Chimica Metallorganica e Catalisi
Dipartimento di Fisica e Chimica dell’Università di Palermo
Chimica Verde e Catalisi
Chimica Verde
Environmental Quotient (EQ)
I si consideri ancora che esistono good waste e bad waste;
I in riferimento a ciò, un altro parametro utile alla valutazione di un processo è il
quoziente di rischio (hazard quotient) Q;
I questo è il rapporto fra livello di esposizione ad una sostanza potenzialmente
pericolosa e il livello di esposizione tollerabile alla stessa sostanza:
I e il quoziente ambientale (environmental quotient) EQ:
EQ = E-factor · Q
Chimica Metallorganica e Catalisi
Dipartimento di Fisica e Chimica dell’Università di Palermo
Chimica Verde e Catalisi
Chimica Verde
Green Processes: Celle a Combustibile
I nella valutazione di un processo bisogna considerare i diversi fattori in gioco:
Relative efficiency of various engine types
100
90
80
70
% Efficiency
50
Costs of
obtaining
hydrogen
50
40
30
20
10
Gas
electric
Diesel
electric
Microturbine
Hydrogen
fuel cell
I ad es. all’efficenza delle celle a combustibile, in relazione ad altri apparati
per laCatalysis/
produzione
di energia elettrica, si potrebbe
anche associare l’assenza
Rothenberg, ISBN 978-3-527-31824-7.
www.catalysisbook.org
di emissioni nocive tuttavia l’idrogeno ha attualmente origine da combustibili
fossili e in misura minore da biomasse e acqua (quindi ha un costo alto)
I al di là di ciò è anche pericoloso (da trasportare e stoccare)
Chimica Metallorganica e Catalisi
Dipartimento di Fisica e Chimica dell’Università di Palermo
Chimica Verde e Catalisi
Chimica Verde
Green Processes: Produzione dell’Epossipropano
I un altro processo del quale si può valutare l’opportunità di realizzazione è quello
che riguarda la produzione (secondo lo schema classico — 40% della
produzione mondiale) di ossido di propilene (bulk chemistry );
I l’uso dell’ossido di propilene è alla base della produzione di glicoli, ad es. 1,2
propandiolo o 1,2,3 propantriolo;
The traditional propene oxide route
OH
+ HOCl
propylene oxide
chlorohydrin
propylene
O
O + HCl
Cl
+ HCl + NaOH
O
+ NaCl + H2O
I nella valutazione del processo va anche considerata la pericolosità ambientale
di molecole reagenti coinvolte, anche in step di reazione intermedi);
I altri processi apparentemente convenienti coinvolgono l’addizione di Br2 ,
HCN o HF a doppi legami di idrocarburi insaturi
Catalysis/ Rothenberg, ISBN 978-3-527-31824-7.
Chimica Metallorganica e Catalisi
www.catalysisbook.org
Dipartimento di Fisica e Chimica dell’Università di Palermo
Chimica Verde e Catalisi
Chimica Verde
Green Processes: Produzione dell’Epossipropano
The SMPO process
+ CH2=CH2
Zeolite
ethylbenzene
+ O2
OOH
ethylbenzene hydroperoxide
+
Ti/SiO2
+
OOH
O
OH
Alumina
+ H2O
OH
styrene
Catalytic oxidation of propene
I il processo styrene monomer propene oxide (SMPO) è usato dalla SHELL
Mo catalyst
O
OH
OOH
+
OCH3
+
e dalla Lyondell;
MTBE
t-butyl hydroperoxide
I i vantaggi del processo sono però fortemente condizionati dal mercato dello
stirene
Catalysis/ Rothenberg, ISBN 978-3-527-31824-7.
Chimica Metallorganica e Catalisi
www.catalysisbook.org
Dipartimento di Fisica e Chimica dell’Università di Palermo
+ O2
OOH
Chimica Verde e Catalisi
ethylbenzene hydroperoxide
Chimica Verde
Ti/SiO2
+
+
OOH
O
OH
Green Processes: Produzione dell’Epossipropano
Alumina
+ H2O
OH
styrene
Catalytic oxidation of propene
+
OOH
Mo catalyst
t-butyl hydroperoxide
O
+
OH
OCH3
MTBE
I il processo ARCO/Oxirane coinvolge l’ossidazione dell’isobutene e origina come
Catalysis/ Rothenberg,
ISBNil978-3-527-31824-7.
sotto prodotto
t-butanolo, usato come additivo perwww.catalysisbook.org
carburanti e materiale di
partenza per la sintesi del metil-t-butil-etere (MTBE); quest’ultimo tuttavia è stato
bandito nei paesi EU e in USA;
I come ossidante, in linea di principio, si potrebbe usare N2 O che come
sotto-prodotto darebbe N2 ma sebbene N2 O sia un gas serra, e quindi la sua
eliminazione (il suo utilizzo) sia auspicabile, è di difficile reperibilià
Chimica Metallorganica e Catalisi
Dipartimento di Fisica e Chimica dell’Università di Palermo
Chimica Verde e Catalisi
Chimica Verde
Life-Cycle Assessment (LCA)
I nel progettare un prodotto "sostenibile" è utile lo studio del suo ciclo di vita,
dall’ottimizzazione d’impiego del prodotto stesso alla scelta delle materie prime e
del tipo di energia da utilizzare nella loro trasformazione, attraverso la
valutazione dell’impatto ambientale con l’apporto di eventuali correttivi alla
produzione e alla gestione della stessa:
The four stages of life-cycle assessment
Life-cycle
assessment
Stage 1
Defining
the scope
Stage 2
Stage 3
Inventory
analysis
Chimica Metallorganica e Catalisi
Catalysis/ Rothenberg, ISBN 978-3-527-31824-7.
Impact
analysis
Stage 4
Improvement
analysis
Dipartimento
di Fisica e Chimica dell’Università di Palermo
www.catalysisbook.org
Chimica Verde e Catalisi
Chimica Verde
Life-Cycle Assessment (LCA)
The four stages of life-cycle assessment
Life-cycle
assessment
Stage 1
Defining
the scope
Stage 2
Stage 3
Inventory
analysis
Impact
analysis
Stage 4
Improvement
analysis
I STAGE1: valutazione e confronto di possibili prodotti utili ad uno stesso scopo
(valutazione dei modi — per scegliere i più convenienti — di produzione,
distribuzione ed uso di una merce);
I STAGE2: inventario degli interventi sull’ambiente e sulla capacità di reperimento
delle materie prime (valutazione del carico/discarico di materie ed energia
mediante l’utilizzo di bilanci di massa e di energia);
I STAGE3: valutazione dell’impatto ambientale (riscaldamento globale, piogge
acide, effetti sulla qualità dell’aria, effetti sullo strato di ozono, effetto serra);
I STAGE4: valutazione di nuove tecnologie e strategie per migliorare processi
e prodotti (green-chemistry, catalisi industriale)
Catalysis/ Rothenberg, ISBN 978-3-527-31824-7.
Chimica Metallorganica e Catalisi
www.catalysisbook.org
Dipartimento di Fisica e Chimica dell’Università di Palermo
Chimica Verde e Catalisi
Catalisi: uno Sguardo d’Insieme
Indice
Chimica Verde e Catalisi
Chimica Verde
Catalisi: uno Sguardo d’Insieme
Chimica Metallorganica e Catalisi
Dipartimento di Fisica e Chimica dell’Università di Palermo
Chimica Verde e Catalisi
Catalisi: uno Sguardo d’Insieme
Ruolo della Catalisi in una Produzione Sostenibile
I il catalizzatore è una specie chimica che accelera un reazione
Different types of catalysts
H
F
F
B
F
homogeneous acid catalysts
CO2H
N
H
L-proline (organocatalyst)
enzyme (biocatalyst)
zeolite (crystalline
aluminosilicate)
OMe
P
Rh
P
OMe
(R,R)-DiPAMP-Rh (organometallic complex)
copper-zinc crystallites on silica
I “... In fact, as far as chemistry is concerned, catalysis is the key to
Catalysis/ Rothenberg, ISBN 978-3-527-31824-7.
www.catalysisbook.org
sustainability...”
(R.A. Sheldon, 2000)
Chimica Metallorganica e Catalisi
Dipartimento di Fisica e Chimica dell’Università di Palermo
Chimica Verde e Catalisi
Catalisi: uno Sguardo d’Insieme
Alcuni Richiami sulla Catalisi
I il catalizzatore:
• è una specie chimica in grado di accelerare (cambiare meccanismo a) una
reazione;
• sebbene in maniera modesta, è (ciclicamente) modificato nel corso della stessa
reazione;
I i principi di base coinvolti nella catalisi – sia essa inorganica, organica,
organometallica o biologica in fase omogenea o eterogenea – sono analoghi;
I è possibile trovare un linguaggio comune allo studio dei diversi aspetti della
catalisi
Chimica Metallorganica e Catalisi
Dipartimento di Fisica e Chimica dell’Università di Palermo
Chimica Verde e Catalisi
Catalisi: uno Sguardo d’Insieme
Alcuni Richiami sulla Catalisi
I i parametri TON (TurnOver Number) e TOF (TurnOver Frequency) sono introdotti
per valutare “obiettivamente” l’attività (assoluta e relativa) di un processo:
• in catalisi omogenea:
n
TON = A→B
n
o TOF = TON
n
time
χ
? il parametro TON in catalisi omogenea è valutato considerando la conversione
prima della disattivazione delle molecole di catalizzatore;
• in catalisi eterogenea:
n
TON = A→B
n
o TOF = TON
σ
time
χ
? i parametri TON e TOF in catalisi eterogenea sono valutati rispetto al numero di
siti catalitici e talvolta vengono riferiti ai grammi di catalizzatore usato: il “TOF”
così definito è anche chiamato “specific rate”;
• in catalisi enzimatica:
n
o TOF = TON
TON = nA/ n
time
? i parametri TON e TOF in catalisi enzimatica sono riferiti al numero di
molecole di enzima complessate da molecole da trasformare rispetto
al numero totale di molecole di enzima
Chimica Metallorganica e Catalisi
Dipartimento di Fisica e Chimica dell’Università di Palermo
Chimica Verde e Catalisi
Catalisi: uno Sguardo d’Insieme
Alcuni Richiami sulla Catalisi
I il catalizzatore può aprire nuove vie alla produzione selettiva di numerose specie
chimiche – ciò avviene attraverso il coinvolgimento della:
• chemoselettività: di due o più vie sintetiche una è quella privileggiata;
• regioselettività: interviene quando una reazione che potenzialmente produce
diverse modifiche sulla stessa molecola è invece orientata verso uno solo dei
possibili prodotti;
• diastereoselettività: interviene quando la reazione è orientata verso la
produzione di uno dei possibili diastereomeri (caso particolare del punto
precedente);
• enantioselettività: interviene quando la reazione è orientata verso la
produzione di uno dei possibili enantiomeri (caso particolare del punto
precedente)
Chimica Metallorganica e Catalisi
Dipartimento di Fisica e Chimica dell’Università di Palermo
Chimica Verde e Catalisi
Catalisi: uno Sguardo d’Insieme
Selettività in Catalisi
I di seguito sono riportati alcuni esempi di selettività in presenza di catalizzatori:
Examples of chemo- and diastereoselectivity
α-pinene oxide diastereomers
O
O
+ O2
CrCl3
+
+
O
verbenone
α-pinene
Regioselectivity
+ CO + H2
Rh complex
O
C5H11
O
+
C5H11
nonanal
iso-nonanal
Enantioselectivity
MeO
MeO
N
+ H2
Ir complex
prochiral imine
Catalysis/ Rothenberg, ISBN 978-3-527-31824-7.
Chimica Metallorganica e Catalisi
MeO
*
NH
+
(R)-enantiomer
*
NH
(S)-enantiomer
www.catalysisbook.org
Dipartimento di Fisica e Chimica dell’Università di Palermo
Chimica Verde e Catalisi
Catalisi: uno Sguardo d’Insieme
Esempi di Reazioni Catalitiche in Fase Omogenea
I la trans-esterificazione dei trigliceridi in ambiente basico (catalizzatore basico) è
una reazione particolarmente veloce:
Base-catalysed transesterification of triglycerides
R2
R1
O
O
O
+ 3MeOH
R3
O
O
triglycerides
O
OH–
catalyst
OH
R1COOMe
OH + R2COOMe
OH
glycerol
R3COOMe
fatty acid methyl esters
(FAME)
used as biodiesel
I il TON di questa reazione è ∼1000
• della trans-esterificazione non sono chiaramente evidenziati gli step elementari coinvolti
Chimica Metallorganica e Catalisi
Dipartimento di Fisica e Chimica dell’Università di Palermo
Chimica Verde e Catalisi
Catalisi: uno Sguardo d’Insieme
Figure
Esempi
di1.11
Reazioni Catalitiche in Fase Omogenea
I la reazione di Heck è un cross-coupling catalitico fra alcheni e aril-alogenuri su
catalizzatori (organometallici) di Pd che cambiano nel corso della reazione:
2x Ligand
Pd0L4
base:HX
Ligand
base
R
L
Pd L
L
L
Pd H
X
Ar X
base
Ar X
R
catalyst
Ligand
Ar
L
R
L
Ar
Pd
L X
Pd
X
Ar
L
Pd
R
Ar
X
Ar
R
base:HX
R
Ligand
I la reazione è stata scoperta da Heck e Mizoroki nel 1968;
I dalla scoperta è molto utilizzata in chimica organica: sono coinvolti diversi
intermedi catalitici (che mostrano proprietà diverse al cambio dei leganti
sul Pd) – alla fine del ciclo, il catalizzatore di partenza è tuttavia ripristinato
(e pronto per un nuovo ciclo catalitico)
Chimica Metallorganica e Catalisi
Dipartimento di Fisica e Chimica dell’Università di Palermo
Chimica Verde e Catalisi
Catalisi: uno Sguardo d’Insieme
Esempi di Reazioni Catalitiche in Fase Omogenea
I l’utilizzo di opportuni leganti nei catalizzatori omogenei può aumentare sia
l’attività sia la selettività dei processi “verdi” in cui sono impiegati;
I per rendere più “verde” un processo, i reagenti possono essere scelti fra i
materiali rinnovabili o di facile reperimento come nel caso della
co-polimerizzazione dell’ossido di limonene e della CO2 :
I il limonene ha una produzione di ≈ 150 · 103 tpa mentre la CO2 è
abbondante, non tossica e poco cara
Chimica Metallorganica e Catalisi
Dipartimento di Fisica e Chimica dell’Università di Palermo
Chimica Verde e Catalisi
Catalisi: uno Sguardo d’Insieme
Esempi di Reazioni Catalitiche
Figure 1.13 in Fase Eterogenea
I l’impiego della catalisi eterogenea è
estremamente vasto:
metal crystallite
CH3CH2CH3
CH3CH=CH2
oxide support
• i primi e più importanti impieghi riguardavano
l’uso di sistemi gas/solido nella petrolchimica
e nell’industria dei derivati della bulk
chemistry (classic heterogeneous
catalysis):
? l’idrogenazione del propene su metalli del
gruppo del Ni (gruppo 10) rappresenta un
importante esempio di catalisi eterogenea;
? per il processo rappresentato vale il principio
di microreversibilità (microscopic reversibility )
Chimica Metallorganica e Catalisi
H
H3C
H
H3C
CH3
H
CH2
H
H
H3C
H3C
CH2
H
H2
H
H3C
CH2
CH2 H
H
H
Catalysis/ Rothenberg,
ISBN
Dipartimento
di 978-3-527-31824-7.
Fisica e Chimica dell’Università di Palermoww
Chimica Verde e Catalisi
Catalisi: uno Sguardo d’Insieme
Figure 1.13 in Fase Eterogenea
Esempi di Reazioni Catalitiche
metal crystallite
CH3CH2CH3
CH3CH=CH2
oxide support
H
I il principio di microreversibilità, applicato
all’idrogenazione del propene, suggerirebbe
la possibilità di ottenere propene – materiale
di partenza nella sintesi del poli-propilene e di
altri polimeri – da propano, per
deidrogenazione;
H3C
H
H3C
CH3
H
H
H
H3C
H3C
CH2
H
CH2
H2
H
H3C
Chimica Metallorganica e Catalisi
CH2
CH2 H
H
H
Catalysis/ Rothenberg,
ISBN
Dipartimento
di 978-3-527-31824-7.
Fisica e Chimica dell’Università di Palermoww
Chimica Verde e Catalisi
Catalisi: uno Sguardo d’Insieme
Figure 1.13 in Fase Eterogenea
Esempi di Reazioni Catalitiche
metal crystallite
CH3CH2CH3
CH3CH=CH2
oxide support
I l’idrogenazione industriale delle olefine di
origine vegetale su catalizzatori di Ni data al
1927 (Margarine Unie) ed è un
importantissimo processo industriale;
I la Margarine Unie consociata alla Lever Bros.
Co. ha portato alla Unilever, quest’ultima nel
2007 è stata quotata 37 Ge
H
H3C
CH2
H
H
H3C
H3C
CH2
H
CH2
H2
H
H3C
Chimica Metallorganica e Catalisi
H
H3C
CH3
H
CH2 H
H
H
Catalysis/ Rothenberg,
ISBN
Dipartimento
di 978-3-527-31824-7.
Fisica e Chimica dell’Università di Palermoww
Chimica Verde e Catalisi
Catalisi: uno Sguardo d’Insieme
1.14
EsempiFigure
di Reazioni
Catalitiche in Fase Eterogenea
I catalizzatori industriali eterogenei di notevole interesse sono le zeoliti (silicaliti
modificate ad es. per la presenza di Al o Ti):
OH
Y-zeolite
geraniol
OH +
!-cyclogeraniol
OH
"-cyclogeraniol
H
Zeolite Y
Lewis acid
OH
Lewis acid
OH
H
I l’impiego della zeolite Y nella ciclizzazione del geraniolo coinvolge la
presenza sia di siti di Brønsted sia di siti di Lewis:
Catalysis/ Rothenberg, ISBN 978-3-527-31824-7.
Chimica Metallorganica e Catalisi
www.catalysisbook.org
Dipartimento di Fisica e Chimica dell’Università di Palermo
Chimica Verde e Catalisi
Catalisi: uno Sguardo d’Insieme
Bio-Catalisi
I la bio-catalisi può essere collocata, in prima battutta, in una posizione di mezzo
fra la catalisi eterogenea e quella omogenea;
I nella bio-catalisi i processi con più di 1000 cicli per secondo sono abbastanza
comuni – ciò và comparato ai 100 - 10000 cicli per ora caratteristici dei processi
catalitici eterogenei ed omogenei;
I l’attività dei bio-catalizzaztori è però solo un aspetto delle loro peculiarità;
I la selettività verso un reagente e/o verso un prodotto è invece l’aspetto più
interessante:
• in particolare, l’enantioselettività – che in genere governa sia l’attività
farmacologica sia le proprietà organolettiche di numerose sostanze – è una
caratteristica che viene sfruttata dall’industria farmaceutica ed alimentare
Chimica Metallorganica e Catalisi
Dipartimento di Fisica e Chimica dell’Università di Palermo
Chimica Verde e Catalisi
Catalisi: uno Sguardo d’Insieme
Bio-Catalisi
I le condizioni d’uso dei bio-catalizzatori sono generalmente molto convenienti
(diretti nella loro attività e mild) mentre possono essere supportati/dispersi su
mezzi di diversa natura ed anche ottimizzati:
N
acrylonitrile
+ H2O
Rhodococcus
(nitrile hydratase)
NH2
O
acrylamide
I nonostante la bio-catalisi sia un NKOTB, l’industria chimica la comincia ad usare
con sempre maggior frequenza;
I l’acrilammide è per esempio prodotta – utilizzando un biocatalizzatore – in
quantità pari a ∼ 10000 tpa e ∼ 50000 tpa in Giappone e nel mondo,
rispettivamente;
I le cellule batteriche sono immobilizzate in un gel poliacrilammidico
mantenuto a pH 8.0 - 8.5 in un sistema semi-batch con una
concentrazione del substrato <3%
Chimica Metallorganica e Catalisi
Dipartimento di Fisica e Chimica dell’Università di Palermo
Chimica Verde e Catalisi
Catalisi: uno Sguardo d’Insieme
Bio-Catalisi
Figure 1.16
E. coli cell
OH
I l’ingegneria genetica ha dato un notevole
impulso alla bio-catalisi;
I un esempio sull’impiego di una modificazione
batterica a fini catalitici si ha in un processo
relativo alla sintesi dell’acido adipico, utile alla
produzione del nylon 6.6;
I l’acido adipico è oggi prodotto principalmente
da C6 H6 (∼ 2.2 Mtpa)
I il processo è efficiente ma il C6 H6 è
cancerogeno e origina da combustibili fossili
(non rinnovabili), richiedendo anche
condizioni di temperatura e pressione
drastiche oltreché l’impiego di HNO3
H2O3PO
H
OH
OH
OH OH
Ni/Al2O3
D-glucose
HO
HO
CO2H
CO2H O
O2
900 KPa
Co, 160 oC
OH
O
O
OH
OH
OH
O
H2O3PO
OH
OH
OH
HO2C
CO2H
+
OH
OH
conc.
HNO3
CO2H
O
O
OH
OH
Cu, NH4NO3
catechol
cis,cismuconic
acid
CO2H
O
HO
OH
O
Adipic acid
Catalysis/ Rothenberg, ISBN 978-3-527-31824-7.
Chimica Metallorganica e Catalisi
OH O
OH
O
H2
5000 KPa
www.catalysisb
Dipartimento di Fisica e Chimica dell’Università di Palermo
Chimica Verde e Catalisi
Catalisi: uno Sguardo d’Insieme
Figure 1.16
Bio-Catalisi
E. coli cell
OH
• la via bio-sintetica è più complessa ma
avviene all’interno del “microreattore” E. Coli;
• il D-glucosio è poco costoso (200e/ton)
rinnovabile e non pericoloso
D-glucose
HO
HO
CO2H
CO2H O
Co, 160 oC
OH
O
O
OH
OH
OH
O
H2O3PO
OH
OH
OH
HO2C
CO2H
+
OH
OH
conc.
HNO3
CO2H
O
O
O2
900 KPa
OH
OH
Cu, NH4NO3
catechol
cis,cismuconic
acid
CO2H
O
HO
OH
O
Adipic acid
Catalysis/ Rothenberg, ISBN 978-3-527-31824-7.
Chimica Metallorganica e Catalisi
H
OH
OH OH
Ni/Al2O3
• il processo avviene a 37◦ C e pressione
ambiente ;
H2O3PO
OH
H2
5000 KPa
I nel 2002, Frost “costruì” un Escherichia Coli
mutato, capace d’iniziare un processo che
portava all’ottenimento di acido adipico dalla
digestione di D-glucosio:
OH O
OH
O
www.catalysisb
Dipartimento di Fisica e Chimica dell’Università di Palermo
Chimica Verde e Catalisi
Catalisi: uno Sguardo d’Insieme
Figure 1.16
Bio-Catalisi
E. coli cell
OH
OH O
OH
O
H2O3PO
H
OH
H2
5000 KPa
OH
OH OH
Ni/Al2O3
D-glucose
HO
HO
CO2H
CO2H O
Co, 160 oC
I il processo bio-catalitico, ad oggi, non ha
sostituito quello “classico” – il benzene è
infatti largamente disponibile, i
bio-catalizzatori sono molto costosi e
l’industria pesante è lenta al rinnovamento
OH
O
O
OH
OH
OH
O
H2O3PO
OH
OH
OH
HO2C
CO2H
+
OH
OH
conc.
HNO3
CO2H
O
O
O2
900 KPa
OH
OH
Cu, NH4NO3
catechol
cis,cismuconic
acid
CO2H
O
HO
OH
O
Adipic acid
Catalysis/ Rothenberg, ISBN 978-3-527-31824-7.
Chimica Metallorganica e Catalisi
www.catalysisb
Dipartimento di Fisica e Chimica dell’Università di Palermo
Chimica Verde e Catalisi
Catalisi: uno Sguardo d’Insieme
1.17
Processi Stechiometrici e Analoghi Catalitici
I nella reazione di Ulmann due radicali arilici vengono convertiti in un di-arile:
I
2
+ Cu
R
aryl iodide
Δ
+ CuI2
R
R
biaryl
I sono però usati aril-iodo derivati che sono molto inquinanti;
I inoltre, una tonnelata di iodo-arile contiene 620 kg di iodio – inutile nel bilancio
complessivo del processo – e solo ∼ 380 kg di residuo arilico (E-factor basso);
I con la formazione di CuI2 anche il rame viene trasformato in un prodotto di
scarto
Chimica Metallorganica e Catalisi
Dipartimento di Fisica e Chimica dell’Università di Palermo
Chimica Verde e Catalisi
Catalisi: uno Sguardo d’Insieme
Processi
Stechiometrici e Analoghi Catalitici
Figure 1.18
I con la combinazione di due processi stechiometrici:
X
+ Pd0
2
Δ
aryl halide
biaryl
PdIIX2 + H2
Pd0 + 2HX
Pd0
X
PdII
2
+ PdIIX2
R
R
R
+ H2
R
R
+ 2HX
R
where X = Cl, Br, I
I si ottiene invece un ciclo catalitico con il Pd che prima si ossida e poi si riduce;
I il Pd è un metallo molto più costoso del Cu ma può essere riutilizzato in cicli
successivi, non trasformandosi in un prodotto finale (di scarto)
Chimica Metallorganica e Catalisi
Dipartimento di Fisica e Chimica dell’Università di Palermo
Chimica Verde e Catalisi
Catalisi: uno Sguardo d’Insieme
Figure 1.19
Processi Stechiometrici e Analoghi Catalitici
I si può aumentare l’E-factor della sintesi
diarilica partendo da specie che non
rilasciano gruppi secondari;
I il primo processo sarebbe ideale ma è
molto difficile da realizzare;
I il secondo processo – accopiamento
ossidativo – è invece realizzabile
(massima resa attuale 80%) sebbene
occorra una seconda reazione in fase
omogenea per ripristinare il catalizzatore;
I l’accoppiamento ossidativo è più
complesso di come rappresentato ma
formalmente molto semplice (vedi
riquadro)
Chimica Metallorganica e Catalisi
+
benzene
2
benzyne
+ 1/2O2
biphenyl
Pd0
2
+ PdIICl2
PdII
AcOH
+ PdIIH2 + 2Cl-
PdIIH2 + 2Cl- + 1/2O2
Co(OAc)3
AcOH
+ H2O
PdCl2 + 2H2O
Dipartimento di Fisica e Chimica dell’Università di Palermo
Catalysis/ Rothenberg, ISBN 978-3-527-31824-7.
www.ca
Chimica Verde e Catalisi
Catalisi: uno Sguardo d’Insieme
Figure 1.20
Processo BHC per la Produzione di Ibuprofene
O
O
O
AlCl3
1
2
2-methylpropylbenzene
NaOEt
I il processo del consorzio BHC (Boots &
Hoechst Celanese Corporation) è stato
messo in produzione nel 1992 dalla BASF
per l’ottenimento dell’ibuprofene (a
destra);
I questo rappresenta un esempio del
possibile (e favorevole) connubio fra
green-chemistry e catalisi
O
1
O
OEt
H3O+
4
H2O
3
OEt
O
2
O
NH2OH
5
O
O
HF
H
N
O
O
Cl
OH
C
6
O
H2
Raney
Nickel
N
7
Pd
OH
CO
COOH
Ibuprofen
Chimica Metallorganica e Catalisi
di Fisica e Chimica dell’Università di Palermo
Catalysis/ Rothenberg,Dipartimento
ISBN 978-3-527-31824-7.
www
Chimica Verde e Catalisi
Catalisi: uno Sguardo d’Insieme
Figure 1.20
Processo BHC per la Produzione di Ibuprofene
O
O
O
AlCl3
I con il processo (riportato a sinistra) si
produce sempre l’antinfiammatorio
ibuprofene (AdvilTM , Motrinr , Nurofen)
con il metodo già brevettato da Boots nel
1962 con una “roundabout synthesis”
stechiometrica;
I il processo Boots come il BHC prevede
l’uso di anidride acetica;
I l’atom-economy del processo Boots è
solo del 40% (per es. l’idrossilamina è
prima introdotta e poi eliminata)
1
2
2-methylpropylbenzene
NaOEt
O
1
O
OEt
H3O+
4
H2O
3
OEt
O
2
O
NH2OH
5
O
O
HF
H
N
O
O
Cl
OH
C
6
O
H2
Raney
Nickel
N
7
Pd
OH
CO
COOH
Ibuprofen
Chimica Metallorganica e Catalisi
di Fisica e Chimica dell’Università di Palermo
Catalysis/ Rothenberg,Dipartimento
ISBN 978-3-527-31824-7.
www
Chimica Verde e Catalisi
Catalisi: uno Sguardo d’Insieme
Figure 1.20
Processo BHC per la Produzione di Ibuprofene
O
O
O
AlCl3
1
I il processo BHC ha un’atom-economy
pari a ∼ 80%;
I il recupero e riciclo dell’acido acetico ha
portato l’atom-economy a ∼ 99%!
I l’uso di HF come catalizzatore e solvente
(con una capacità di riciclaggio del
99.9%) ha ulteriormente ridotto la
capacità d’inquinamento del processo
(eliminando lo smaltimento di sali in
soluzione acquosa)
2
2-methylpropylbenzene
NaOEt
O
1
O
OEt
H3O+
4
H2O
3
OEt
O
2
O
NH2OH
5
O
O
HF
H
N
O
O
Cl
OH
C
6
O
H2
Raney
Nickel
N
7
Pd
OH
CO
COOH
Ibuprofen
Chimica Metallorganica e Catalisi
di Fisica e Chimica dell’Università di Palermo
Catalysis/ Rothenberg,Dipartimento
ISBN 978-3-527-31824-7.
www
Chimica Verde e Catalisi
Catalisi: uno Sguardo d’Insieme
Strumenti
Figured’uso
1.21 nello Studio della Catalisi
I lo studio della catalisi si articola in una gamma di ambiti eccezionalmente vasta:
Activity
testing
Mechanistic
studies
Synthesis tools
Characterisation tools
Modelling tools
Novel
reactor concepts
Spectroscopy
Quantum
mechanics
Parallel
screening
Surface science
Molecular
simulations
Process
intensification
Microscopy
Data mining
Kinetic studies
Process
simulations
• “..... any chemical engineering development that leads to a substantially smaller, cleaner, and more
energy-efficient technology is process intensification.....”
Catalysis/ Rothenberg, ISBN 978-3-527-31824-7.
Chimica Metallorganica e Catalisi
www.catalysisbook.org
Dipartimento di Fisica e Chimica dell’Università di Palermo
Chimica Verde e Catalisi
Catalisi: uno Sguardo d’Insieme
Strumenti d’uso nello Studio della Catalisi
I il work-flow di uno studio catalitico prevede la sintesi del catalizzatore, la sua
caratterizzazione strutturale e cinetica (catalyst-testing) e l’analisi meccanicistica
(anche a livello atomistico del processo);
I nel 1994 la Symyx suggerisce un cambio di paradigma – oggi largamente
accettata anche dall’industria – introducendo la miniaturizzazione e
parallelizzazione di processo;
I in quest’ottica, Claude de Bellefon nel 2000 propose un sistema a pulsi che
permetteva lo studio integrato di proprietà cinetiche e di superficie di catalizzatori
eterogenei usati in sistemi gas/liquido e liquido/liquido mediante tecniche
cromatografiche e/o spettrofotometriche
Chimica Metallorganica e Catalisi
Dipartimento di Fisica e Chimica dell’Università di Palermo
Chimica Verde e Catalisi
Catalisi: uno Sguardo d’Insieme
Figured’uso
1.22 nello Studio della Catalisi
Strumenti
I uno schema dell’apparato di Bellefont è di seguito riportato:
substrates
infrared
flow cell
pump
substrate loop
solvent reservoir
catalyst loop
micromixer
air loop
waste
catalysts
air bubble
substrate pulse
mixed substrate/ catalyst pulse
I nel 1996 sono state introdotte svariate “librerie” di catalizzatori, sintetizzate su
supporti standard con metodologie standard per avere uno strumento
comparativo omogeneo operante su metalli in diversi stati d’ossidazione e
supporti catalitici
Catalysis/ Rothenberg, ISBN 978-3-527-31824-7.
Chimica Metallorganica e Catalisi
www.catalysisbook.org
Dipartimento di Fisica e Chimica dell’Università di Palermo
Chimica Verde e Catalisi
Catalisi: uno Sguardo d’Insieme
Strumenti d’uso nello Studio della Catalisi
I le librerie sono state analizzate sitematicamente riguardo alla loro attività e
selettività in diversi processi catalitici;
I questo tipo d’analisi è stata estesa ai catalizzatori omogenei dopo opportuna
supportazione (eterogenizzazione) e cercando di mantenere (e studiare) il loro
“naturale” comportamento in fase omogenea (borderline-catalyst);
I nella caratterizzazione di un processo catalitico grossolanamente distinguiamo i
tre livelli:
• macroscopico
• mesoscopico
• nanoscopico
Chimica Metallorganica e Catalisi
Dipartimento di Fisica e Chimica dell’Università di Palermo
Chimica Verde e Catalisi
Catalisi: uno Sguardo d’Insieme
Strumenti d’uso nello Studio della Catalisi
I nel primo si ricerca a livello ingegneristico/reattoristico l’ottimizzazione delle
condizioni operative di un processo catalitico;
I nel secondo si possono includere l’analisi delle superfici, gli studi cinetici, le
relazioni composizione/struttura/attività;
I nel terzo si studiano le proprietà di molecole, cluster e atomi cercando di capire
le sequenze di step (a livello molecolare) che caratterizzano un processo
catalitico;
• lo studio del primo livello è fuori dagli scopi del nostro corso;
• quello del secondo livello è trattato nei blocchi CMC-L4, CMC-L5, CMC-L7 –
CMC-L9;
• lo studio del terzo livello è infine analizzato nel blocco di lezioni CMC-L6
Chimica Metallorganica e Catalisi
Dipartimento di Fisica e Chimica dell’Università di Palermo
Chimica Verde e Catalisi
Catalisi: uno Sguardo d’Insieme
Strumenti d’uso nello Studio della Catalisi
• in particolare:
? in CMC-L4 e CMC-L5 sono approfonditi aspetti cinetici e meccanicistici della
catalisi;
? in CMC-L7 si trattano i sistemi omogenei;
? in CMC-L8 si trattano i sistemi eterogenei e si approfondiscono aspetti relativi
alla caratterizzazione delle superfici e delle specie coinvolte nei processi
catalitici per mezzo di tecniche in-situ (operando-conditions) ed ex-situ
? in CMC-L9 vengono analizzati sistemi bio-catalitici – come per i precedenti
sistemi anche per quelli di questo blocco verranno presi in considerazione
esempi di utilizzo industriale
Chimica Metallorganica e Catalisi
Dipartimento di Fisica e Chimica dell’Università di Palermo
Chimica Verde e Catalisi
Catalisi: uno Sguardo d’Insieme
Strumenti d’uso nello Studio della Catalisi
? in CMC-L6 sono infine presentati gli approcci modellistici nello studio della
catalisi; questi – escludendo il modelling della fluido-dinamica di processo e
quello relativo al trasferimento di massa e calore – in maniera grossolana
possono essere raggruppati in tre categorie:
∗ modelling di percorsi di reazione e cicli catalitici;
∗ modelling di cinetiche di processo e performance di reazione;
∗ modelling di relazione struttura-attività, trattate a diversi livelli mediante
opportuni descrittori;
? nello studio modellistico possono essere usati paradigmi classici (deterministici
e/o stocastici) e/o quantistici;
? l’impiego congiunto di descrittori struttura-proprietà-attività e di approcci statistici
– quantitative structure activity relationship (QSAR) quantitative structure
property relationship (QSPR) – e combinatoriali è oggi sempre più diffuso
nello studio della catalisi
Chimica Metallorganica e Catalisi
Dipartimento di Fisica e Chimica dell’Università di Palermo
Appendix
Bibliografia di Base
Libri di Base Suggeriti per il Corso
Gary L. Miessler, Donald A. Tarr;
Chimica Inorganica, IV edizione;
Piccin Nuova Libraria, 2011
Gadi Rothemberg;
Catalysis: Concepts and Green Applications;
Wiley-VCH, 2008
Chimica Metallorganica e Catalisi
Dipartimento di Fisica e Chimica dell’Università di Palermo