Il dolore: riconoscimento, valutazione e
gestione.
Quali farmaci per la terapia del
dolore?
Antonella Goisis MD
Bergamo, 14 maggio 2016
Le premesse
Application of a WHO protocol on medical therapy for oncologic pain in an
internal medicine hospital.
Goisis A1, Gorini M, Ratti R, Luliri P.
Abstract
Pain symptomatology is present in 60% - 80% of patients affected by advanced cancer, but in most cases it is
not adequately treated. Our series, composed of 45 patients affected by cancer in an advanced stage,
demonstrates how the application of common concepts of pharmacotherapy, standardized according to a
sequential scheme proposed by the WHO, makes it possible to reach total control (in 24.4% of our cases) or
only slight residual persistence (in 68.8% of our cases) of pain from cancer, with scarce side effects that are
easily controlled with symptomatic therapy. According to the type of pain, its behavior in relation to the
therapy effected and any previous pharmacologic treatment, the proposed pharmacologic scheme foresees,
as the first step, the use of non-narcotic drugs, eventually associated or substituted with weak narcotics or
finally with strong narcotics. Attention is given to modulation of the administration, to guarantee an
analgesic effect throughout the day, thus preventing the pain. Irrespective of the analgesic scheme
employed, it is more effective if patients affected by chronic oncologic pain (who present an important
emotional component) are treated contemporaneously with anxiolytic and antidepressive drugs and those in
which nerve structures are involved are treated with steroids. In conclusion, pain of an oncologic patient in
an advanced stage can almost always be alleviated or often eliminated by the rigorous application of
therapeutic concepts well known by physicians but for various reasons often neglected in clinical practice.
Tumori. 1989 Oct 31;75(5):470-2.
SICP – FCP
La legge 15 marzo 2010, n. 38
"Disposizioni per garantire l'accesso alle cure palliative
e alla terapia
del dolore"
è stata pubblicata sulla Gazzetta Ufficiale n. 65 del 19
marzo 2010
“ . . . una conquista di civiltà. . . ”
Disposizioni per garantire l’accesso alle cure palliative e alla terapia
del dolore
Art. 1.
(Finalità)
1. La presente legge tutela il diritto del cittadino ad
accedere alle cure palliative e alla terapia del dolore.
Definiamo il dolore...
"Il dolore può essere definito
come una sensazione spiacevole
e un‘ esperienza emotiva dotata
di un tono affettivo negativo,
associata ad un danno tissutale
potenziale o reale e comunque,
descritta in rapporto a tale
danno“
(IASP – International Association for the study of Pain))
Dolore acuto
Il dolore acuto rappresenta un
campanello
d’allarme
sulla
presenza di stimoli pericolosi o
potenzialmente tali nell'ambiente o
nell'organismo stesso.
È un dolore
definire “utile”.
che
potremmo
Prima di essere affrontato e
trattato va capito, interpretato e
inserito
nel
corretto
nesso
eziopatogenetico per un adeguata,
quando possibile, terapia della
patologia causale.
Dolore cronico
•Il dolore cronico, anche se causato da
un evento acuto, si caratterizza nel
tempo come “malattia”, è una malattia
a sé stante, con elementi patogenetici
autonomi, aspetto clinico tipico,
approccio terapeutico definito.
•Persiste
nel
tempo,
genera
depressione, ansia, insonnia e altri
disturbi emotivi.
•Ha un forte impatto sulla vita di
relazione e sugli aspetti psicologici e
sociali; e’ un dolore
“inutile e
potenzialmente dannoso” .
Dolore come malattia
…..la trasformazione da difesa a offesa….
Il Dolore è Fisiologico quando rappresenta una
corretta risposta di adattamento, essenziale per
evitare danni tissutali
Diventa Patologico quando vi è un’alterata risposta
di adattamento ad un insulto tissutale, nervoso o
non nervoso
Mannion & Woolf, The Clinical Journal of Pain, 2000
Circolo vizioso del dolore non trattato
Dolore
Limitazioni sociali
Diminuita
autonomia
Comportamenti
limitanti
Mobilità ridotta
Stato funzionale
alterato
Il dolore cronico..... UNA EPIDEMIA SILENZIOSA
Popolazione italiana colpita da dolore cronico
15 milioni !!!
Dolore non oncologico
87%
Dolore oncologico
13%
Può sembrare artificioso differenziare l’approccio al dolore
dei pazienti oncologici e non oncologici, poiché la sindrome
dolorosa non è caratterizzata da sostanziali differenze dal
punto di vista fisiopatologico.
In realtà, questo approccio è indispensabile poiché, pur
essendo identico l’obiettivo primario di controllare l’intensità
del dolore percepito, gli obiettivi di cura e l’approccio
terapeutico si rivelano assai diversi.
Nel dolore cronico non oncologico, obiettivo prioritario è la
riduzione dell’impatto del dolore sull’autosufficienza e sulle
attività e relazioni quotidiane, in altre parole la riduzione
della disabilità.
Lo stesso risultato è perseguibile nel dolore che si presenta
nella fase iniziale della malattia oncologica, mentre
nell’ambito delle cure palliative, in pazienti destinati a
morire nell’arco di pochi mesi, il tentativo di ridurre la
disabilità è per lo più vano, poiché la capacità di svolgere i
normali atti della vita quotidiana va continuamente
riducendosi a causa della progressione della malattia.
Non è più possibile riferirsi, in questa fase, solo alla qualità
della vita, ma è necessario orientare l’assistenza verso una
qualità della morte.
Risulta indispensabile instaurare un’adeguata relazione di
cura con il malato, ed è essa stessa la prima terapia: un flusso
bidirezionale di informazioni ed esperienze tra due persone
che si aiutano reciprocamente, per raggiungere al meglio un
obiettivo comune.
La relazione di cura inizia con il chiedere al malato se ha
dolore (se aspettiamo che sia lui a dircelo è già troppo tardi) e
con il
credere sempre al dolore che ci segnala !!!
LE CAUSE DEL DOLORE CRONICO
NON ONCOLOGICO
Osteoartrosi
34
Ernia al disco
18
Traumatismi
12
Artrite Reumatoide
8
Emicrania
7
Frattura/deterioramento spinale
6
Danno nervoso
4
Danno Cartilageneo
4
Colpo di frusta
4
Chirurgia
3
0
5
10
15
20
25
30
35
40
Il dolore cronico sconvolge la vita
delle persone
0%
Lavoro Perso
5%
10%
15%
20%
25%
30%
17%
Cambio di Responsabilità al
Lavoro
Cambio di Lavoro
Diagnosi Depressione
Breivik H. et al. Survey of chronic pain in Europe: Prevalence, impact on daily life, and treatment
European Journal of Pain, 2006
28%
20%
22%
Il dolore cronico ha un impatto significativo
sulle attività quotidiane
56%
Dormire
9%
Fare esercizio
23%
Alzarsi
23%
50%
49%
42%
Compiere i lavori domestici
12%
40%
Camminare
7%
Partecipare alle attività
sociali
34%
14%
Meno capace
Non più in grado
24%
Attività sessuale
19%
Mantenere relazioni con
famiglia e amici
22%
5%
0%
10%
20%
30%
Breivik H. et al. Survey of chronic pain in Europe: Prevalence, impact on daily life, and treatment
European Journal of Pain, 2006
40%
50%
60%
THE PAINFUL TRUTH
La gestione del dolore cronico in Europa
La campagna Painful Truth è sponsorizzata da Boston
Scientific
Ltd.
DINNM0060EA
/
NM-114704AA_JAN2013
The Painful Truth Campaign 2013
La campagna “Painful Truth” è stata lanciata
per migliorare la conoscenza dei problemi
affrontati da chi soffre di dolore cronico
non oncologico.
L’obiettivo è migliorare le modalità di
diagnosi e l’accesso a opzioni terapeutiche
innovative e con un buon rapporto costoefficacia.
Importanti associazioni europee si sono
riunite per sostenere questa ricerca e per
incoraggiare tutti a fare qualcosa.
L’indagine “Painful Truth” non solo
approfondisce l’impatto del dolore cronico
sulle vite dei soggetti affetti, ma mette
anche in luce i limiti delle cure
somministrate e le esigenze insoddisfatte
nell’ambito della gestione del dolore.
The Painful Truth Campaign 2013
Interviste nel Maggio 2012 in Francia, Germania,
Italia, Spagna e Regno Unito
1.010 adulti, età 18 - 64 anni, con dolore cronico
(durata ≥6 mesi, escluso dolore oncologico)
Il 57% del campione costituito da donne
The Painful Truth Campaign 2013
L’Europa soffre…
In Europa, il dolore cronico colpisce 1
adulto su 5.
In media, i soggetti convivono con il dolore
cronico per un periodo che arriva fino ai 7
anni.
Il 68% dei partecipanti all’indagine prova
dolore per più di 12 ore al giorno
nonostante le terapie.
Quasi un terzo dei pazienti afferma di
avere ricevuto poche informazioni sulle
nuove opzioni per una gestione migliore
del dolore.
TRATTARE
IL DOLORE
Per impostare una terapia antalgica efficace vi sono tre
criteri guida che permettono
di affrontare la scelta del farmaco in modo razionale.
1 L’introduzione, da parte dell’Organizzazione Mondiale della Sanita’ (OMS),
della “scala” per il trattamento del dolore oncologico ha, in un certo senso,
condizionato anche il trattamento farmacologico del dolore cronico non
oncologico.
La scala OMS, sebbene possa essere vista come un percorso da compiere, e’ in
realta ‘ piu’ un modello di approccio, in cui il farmaco e la sua potenza antalgica
vengono correlati all’intensita’ del dolore; essa rappresenta sostanzialmente un
metodo per rapportarsi al dolore e alla sua intensita’ per la scelta dei farmaci.
2
Una seconda guida alla scelta della
terapia puo’ derivare dalla letteratura e,
quindi, dai lavori scientifici che mostrano
l’efficacia di alcuni farmaci in precise
patologie dolorose. Un esempio e’ dato
dalla nevralgia essenziale del trigemino,
dove tutta la letteratura e’ concorde nel
consigliare l’impiego di carbamazepina e
nel dichiarare il fallimento terapeutico degli
analgesici periferici e centrali.
3
Il terzo criterio che puo’ contribuire a
una scelta terapeutica razionale e’ la
conoscenza dei meccanismi fisiopatologici
che sottendono all’origine del dolore.
Questo percorso e’ in genere applicabile
quando la diagnosi e’ particolarmente
accurata e permette di identificare i
meccanismi periferici e centrali.
La strategia terapeutica che rimane una pietra miliare nel trattamento del
dolore cronico è quella proposta nel 1986 dalla Organizzazione Mondiale
della Sanità, la cosiddetta Analgesic Ladder e alla quale le altre linee-guida
prodotte da varie Agenzie e Società Scientifiche fanno comunque riferimento.
Essa consiste nell’utilizzo di Farmaci Antiinfiammatori Non Steroidei (FANS) e
Paracetamolo nel dolore lieve (farmaci del primo gradino), di “oppioidi per il
dolore lieve-moderato” o “oppioidi deboli” per il dolore lieve-moderato
(farmaci del secondo gradino), associati o meno a farmaci del primo, e
“oppioidi per il dolore moderato-severo” o “oppioidi forti” per il dolore
moderato-severo (farmaci del terzo gradino), associati o meno a farmaci del
primo.
Ciò che caratterizza gli oppioidi del secondo gradino (analogamente ai FANS e
al paracetamolo), è la presenza dell’ effetto-tetto, ossia di un dosaggio
massimale di farmaco oltre il quale peggiora l’indice terapeutico in quanto, in
assenza di effetto terapeutico aggiuntivo, aumentano, per contro, gli effetti
collaterali.
La scala analgesica OMS a tre gradini nella sua formulazione
originale
Trattamento del dolore secondo le linee guida
Dolore
Severo
3
(NRS 7-10)
Dolore
Moderato
(NRS ≤3)
+/- adiuvanti
Il trattamento con oppioidi forti, immediatamente dopo i
Oppioidi deboli
FANS, è efficace e ben tollerato
+/- adiuvanti
Raccomandato dalle
linee guida ESMO,EAPC,SIGOT
2
(NRS 4-6)
Dolore
Lieve
Oppioidi forti
1
Non-oppioidi
+/- adiuvanti
Nel corso degli anni sono state effettuate alcune osservazioni critiche alla
Scala WHO, e la stessa WHO ha identificato del tutto recentemente aree
passibili di ulteriore verifiche scientifiche.
• In primo luogo, se ne è stigmatizzato l’utilizzo schematicamente
“progressivo”: secondo questa prospettiva critica, un paziente che si
presenti con dolore severo, non necessariamente deve “passare”
sequenzialmente attraverso tutti e tre gradini, ma è stato suggerito che
possa assumere farmaci del secondo e terzo gradino fin dall’esordio, a
dosaggi opportuni, in base all’intensità del dolore.
• Un attacco ancora più radicale portato alla strategia nel suo complesso è
rappresentato dall’accusa di essere costruita solo in base all’intensità del
dolore, e non ai meccanismi patogenetici dai quali è provocato. Bisogna
affermare, però, che tale critica non appare del tutto fondata, in quanto la
scala prevede, in ciascun gradino della stessa, il possibile utilizzo di farmaci
adiuvanti, proprio in funzione del meccanismo doloroso sottostante.
Quando utilizzare i fans ?
Nel dolore acuto e cronico, lieve moderato,
di natura infiammatoria
I FANS formano un gruppo assai numeroso di farmaci che, pur avendo
caratteristiche chimiche assai differenti, inducono gli stessi effetti generali:
anti-infiammatorio, analgesico, antipiretico.
I FANS rappresentano il primo livello della scala analgesica proposta dall’OMS.
Un aumento del dosaggio generalmente non produce un corrispondente effetto
analgesico, ma aumenta i rischi di effetti collaterali.
In caso di insoddisfacente risposta antalgica, o comunque in presenza di
un’intensità del dolore molto elevata, è necessario ricorrere all’associazione o alla
sostituzione con un oppiaceo.
Non hanno una provata efficacia nel dolore neuropatico e misto.
Dolore lieve-moderato: i farmaci analgesici
di prima scelta
• Analgesici periferici antinfiammatori: possono essere utilizzati in
fase di valutazione e per brevi periodi in numerose sindromi algiche in
cui prevale un processo infiammatorio. La lunga durata d’azione ne
consiglia la somministrazione giornaliera.
• Paracetamolo: al giusto dosaggio rappresenta l’analgesico di prima
scelta, soprattutto nelle forme di dolore lieve e continuo.
• Paracetamolo-codeina : spesso sottodosato…
• Tramadolo e associazione paracetamolo-tramadolo
Note AIFA, 2009
Un effetto analgesico si ottiene in genere in una
settimana, per un effetto antinfiammatorio completo
(anche dal punto di vista clinico) servono spesso anche 3
settimane. Se trascorso questo tempo non vi sono risultati,
e bene tentare con un altro farmaco.
Nota 66 AIFA G. U. n° 197 del 24-8-2012
• FA N S E C O X I B VA N N O U T I L I Z Z AT I N E L
T R AT TA M E N TO
S I N TO M AT I C O
ALLA
DOSE
MINIMA
EFFICACE
PER
IL
PERIODO PIÙ BREVE POSSIBILE.
•
T U T T I I FA N S S O N O A S S O C I AT I A
TO S S I C I TÀ
GASTROINTESTINALE
G R AV E , C O N R I S C H I O M A G G I O R E P E R
G L I A N Z I A N I E S O N O C O N T R O I N D I C AT I
N E L LO S C O M P E N S O C A R D I A C O G R AV E .
•
I C O X I B S O N O C O N T R O I N D I C AT I
NELLA
C A R D I O PAT I A
ISCHEMICA ,
NELLE
PATO LO G I E
ARTERIOSE
PERIFERICHE,
N E L LO
SCOMPENSO
C A R D I A C O M O D E R ATO E G R AV E .
Quando utilizzare gli analgesici oppiacei?
Nel dolore acuto e cronico moderato-severo
Quando gli analgesici minori sono inefficaci
Quando non è possibile somministrare analgesici minori per
un lungo periodo, per incidenza di effetti collaterali o per la
presenza di patologie concomitanti che ne limitano l’uso
Nelle patologie
scheletrico
degenerative
dell’apparato
Nel dolore neuropatico
Nel dolore post operatorio e in riabilitazione
Nel dolore oncologico
muscolo
Gli oppioidi sono i farmaci di riferimento per il controllo del
dolore cronico moderato-severo
Sicuri
Maneggevoli
Oggi facilmente prescrivibili
Efficaci
WHO 2007; 2G.U. 19 marzo 2010, n. 65
Dolore moderato-grave: i farmaci analgesici
di prima scelta
In pazienti con dolore moderato-grave l’impiego dei farmaci oppiacei e’ fondamentale e deve essere
personalizzato per ciascun paziente .
Tipo di oppiaceo, dosaggio e formulazione dovrebbero essere valutati di volta in volta.
E’ noto come nel dolore cronico la risposta al farmaco oppiaceo sia particolarmente soggettiva, così come
la comparsa di effetti collaterali indesiderati talvolta intollerabili.
La scelta, quindi, deve essere ponderata sia nel periodo di titolazione iniziale, sia nel lungo periodo
della cura.
La terapia con oppiacei dovrebbe costituire una parte di un piano terapeutico complesso, dove si
dovrebbero individuare tutte le altre risorse terapeutiche disponibili, dall’intervento percutaneo miniinvasivo alla riabilitazione, alle terapie comportamentali, al supporto psicologico e altro ancora.
Se nei pazienti in eta’ avanzata ci si puo’ permettere di affidarsi esclusivamente a una terapia con oppiacei
adeguatamente prescritta, nel paziente giovane e socialmente attivo si dovrebbe agire in ogni direzione
possibile.
La collaborazione tra MMG e specialista del dolore e’ auspicabile per poter garantire la continuita’ di
cura e ovviamente il successo terapeutico con il minimo rischio possibile.
Da cosa nasce l’oppiofobia ?
SCARSA conoscenza dei
famaci
PAURA della dipendenza
PAURA della riduzione
della vita
TOLLERANZA
RICETTAZIONE
Continua richieta del
paziente ad adeguare la
dose..... Talvolta, siamo noi
medici gli inadeguati …
Miti da sfatare
Depressione respiratoria
Nausea e vomito
Deficit intellettivi
Alterazioni dell’umore
Stipsi
Alterazione della funzione cardiovascolare
Azione sull’apparato genito-urinario
Effetti neuroendocrini
Prurito
Sindrome da astinenza
CRONISTORIA DEL RISCHIO DI COMPLICANZE E ABUSO
(O ALTRO) NEI PAZIENTI CON DOLORE PERSISTENTE
Nel corso degli anni Settanta era comune pensiero che i pazienti sofferenti di dolore
persistente di natura non oncologica e sottoposti a trattamento con oppiacei,
dovessero inevitabilmente sviluppare dipendenza. Questa convinzione, avvalorata dagli
studi di Kolb (1925) e Rayport (1954), inizio’ a vacillare negli anni Ottanta, quando
alcuni autori evidenziarono che, in presenza di benefici clinici accettabili, i rischi di una
tossicodipendenza in seguito a trattamento con oppiacei erano minimi o pressoche’
nulli. Ipotesi avvalorate dai primi lavori nel 1990 in doppio cieco sul DCNO (Dolore
Cronico Non Oncologico) e in particolare dagli studi di McQuaid (1999) che
affermavano che l’uso medicale degli oppiacei non creava dipendenza qualora fosse
presente dolore.
Infatti, se in situazione di dolore si somministra un oppiaceo, questo si alloca
tutto sui recettori siti nel corno dorsale pronti a modulare l’input doloroso; in
caso contrario l’oppiaceo va a interferire sul sistema dopaminergico a livello del
nucleo accumbens con il rischio di innescare meccanismi che portano alla
tossicodipendenza.
Gli studi piu’ recenti sull’efficacia della terapia con oppiacei nel breve e nel mediolungo termine hanno prodotto evidenze differenti, attribuibili fondamentalmente alla
scarsa numerosita’ della popolazione trattata.
Purtroppo a livello italiano non esistono pubblicazioni sull’argomento, ne e’ presente
un osservatorio nazionale o regionale.
Addiction? Rara nei pazienti con dolore
Out of 11.882 pts treated with opioids,
only 4 cases (0.03%) of documented
addiction in patients without previous
history of addiction …
Autore
Porter et al
Brozovic et al
Schug et al
Sun et al
Perry et al
Pegelow
Ripamonti C et al, Critical Reviews in Oncology/Hematology 2009
Drayer et al. J Pain Sympt Contr 1999
%
4/11882
0.03
0/ 610
0.0
1/ 550
0,2
0/ 538
0.0
0/ >10.000 0.0
1/ 510
0.2
N. pz
Antagonisti degli oppiacei
Naloxone (Narcan) E’ antagonista su tutti i recettori.
Ha una emivita di circa 1-2 ore, l’effetto si ottiene già dopo
1, 2 min. Già a dosi di 1 mg sopprime l’azione degli
oppiacei. Utilizzato nelle sindromi da overdose da oppiacei.
La sua breve emivita rende necessaria la somministrazione
ripetuta, in casi di avvelenamenti gravi.
Naltrexone (Antaxone, Nalorex, Narcoral) Emivita più
lunga, quindi basta una sola somministrazione.
Può essere utilizzato nei tossicodipendenti come misura
preventiva nei confronti di recidive.
LOMBALGIA
La prescrizione precoce di oppioidi non
aumenta il rischio di uso cronico .
La prescrizione precoce di oppioidi non sembra aumentare il rischio di impiego a lungo
termine di questi farmaci nei soggetti con problemi alla schiena. Secondo un recente studio
retrospettivo condotto su 123.000 soggetti, infatti, quelli con dolore lombare che avevano
ricevuto oppioidi entro un mese dalla comparsa dei sintomi presentavano minori probabilità di
fare uso di questi farmaci per più di tre mesi, come confermato dall’autrice Sara Heins della
Johns Hopkins Bloomberg School of Public Health di Baltimora.
Non è comunque possibile individuare le categorie a minor rischio: contrastare rapidamente il
dolore potrebbe di fatto impedire al paziente di sviluppare dolore cronico, ma è anche
possibile che intervenga qualche fattore interferente.
Alcune linee guida, di fatto, sconsigliano la prescrizione di oppioidi per i pazienti con dolore
muscoloscheletrico cronico non grave nelle prime sei settimane susseguenti ad un trauma
diretto.
Prescrivere oppioidi prima di comprendere realmente la ragione alla base del dolore del
paziente potrebbe essere un indicatore di una scarsa qualità assistenziale in generale.
Se un paziente si presenta lamentando dolore e non sono presenti cause evidenti,
probabilmente non è opportuno prescrivere oppioidi prima di effettuare la diagnosi. Lo studio
comunque mette in dubbio le linee guida che sconsigliano la prescrizione precoce di oppioidi
per ridurne il rischio di impiego cronico: i fattori che rientrano nel processo decisionale per la
prescrizione di questi farmaci sono molteplici, ma secondo i ricercatori non sono disponibili
evidenze a supporto dell’attesa di un numero di settimane predeterminato.
Fonte: Inj Prev online 2015
Una buona notizia:
cresce in Italia l’uso di farmaci analgesici oppiacei,
che hanno fatto registrare un aumento del 26% tra il 2012 e il 2014. A segnalarlo è la
relazione sulla legge 38/2010 sulle cure palliative e la terapia del dolore trasmessa al Parlamento
dal Ministero della Salute.
Per quanto riguarda il consumo di farmaci analgesici oppiacei permane un trend di crescita
positivo. In particolare, in alcune regioni quali Valle d’Aosta, Lombardia, la Provincia Autonoma di
Trento, Lazio, Marche, Molise, Puglia e Sardegna, la percentuale di crescita della spesa relativa al
consumo di farmaci oppioidi nel triennio2012–2014 supera il 30%.
A livello nazionale l’incremento della spesa farmaceutica di questa categoria di farmaci, sempre
dal 2012 al 2014, si attesta intorno al 26%.
Alla luce dei dati è dunque ipotizzabile un utilizzo appropriato dei farmaci per la terapia del
dolore.
Tra i risultati più significativi, la relazione sottolinea il trend decrescente del numero di pazienti
deceduti in un reparto ospedaliero per acuti.
Il dato registrato nell’anno 2013 è pari a 44.725 pazienti deceduti con diagnosi primaria o
secondaria di neoplasia nei reparti per acuti rispetto a 47.537 nell’anno 2012.
Misure terapeutiche generali per il controllo
degli effetti collaterali da oppiacei
Ridurre
la dose o sospendere temporaneamente
l’oppiaceo.
Idratare il paziente.
Ridurre le associazioni con farmaci interagenti, ad es.
BDZ, antidepressivi, antiepilettici.
Somministrare farmaci sintomatici ad es. lassativi,
antiemetici.
Cambiare via di somministrazione dell’oppiaceo,
cambiare oppiaceo, cambiare entrambi
(SWITCH =
rotazione).
Rotazione degli oppioidi
Qualora gli effetti collaterali non siano controllabili
adeguatamente ed ostacolino eventuali incrementi delle
dosi per un completo controllo del dolore, è necessario
cambiare il tipo di oppioide, via di somministrazione o
entrambe le cose.
E’ importante rilevare che una buona idratazione che
favorisca la rimozione dei metaboliti attivi della morfina
(M3G e M6G) è spesso sufficiente a controllare i più comuni
effetti collaterali.
Dolore lieve-moderato-grave:
i farmaci “adiuvanti”
Una volta costruito un piano terapeutico con i farmaci analgesici, e’ sicuramente opportuno valutare la
sinergia e la complementarita’ dei cosiddetti farmaci adiuvanti.
CORTICOSTEROIDI
Hanno effetti positivi sull’appetito, l’umore e la cachessia. Sono efficaci nella
compressione di nervi e nella distensione di visceri (4-8 mg di desametasone, 16-32 di metilprednisolone,
20-40 di prednisone per 3/die) e nell’ipertensione endocranica (10-20 mg di desametasone; 40-80 mg di
metilprednisolone iv ogni 6 ore per i primi giorni).
ANTIDEPRESSIVI
Sono utili nel dolore neuropatico. Gli SSRI e i NRI (paroxetina, citalopram, duloxetina,
venlafaxina, ecc.) hanno minori effetti collaterali rispetto ai triciclici (amitriptilina, ecc.), che restano
comunque molto efficaci.
ANTICONVULSIVANTI Sono efficaci nel dolore neuropatico (per esempio gabapentin e pregabalin), anche
in associazione con antidepressivi, soprattutto se il dolore è lancinante tipo scarica elettrica
NEUROLETTICI Hanno effetto ansiolitico e, a basso dosaggio, controllano efficacemente nausea e vomito
da oppioidi in sinergia con altri antiemetici (per esempio aloperidolo).
BIFOSFONATI
Sono utili, nella formulazione iniettabile, nel dolore da metastasi ossee (per esempio
acido zolendronico e pamidronico).
ORMONI Il medrossiprogesterone migliora l’appetito, la forza e la performance. Utile nella cachessia
neoplastica.
D.E.I. (Dolore Episodico Intenso)
• Episodi dolorosi che emergono in una situazione di
dolore ben controllato dalla terapia analgesica cronica
(ad orari fissi).
• E’
caratterizzato da: insorgenza rapida, elevata
intensità, breve durata (durata media di circa 30
minuti).
Breakthrough cancer pain:
D.E.I. (BTcP) : Il trattamento ideale:
Caratteristiche del trattamento ideale del BTcP:1,2
Efficace
Veloce esordio d’azione
Breve durata d’azione
Eventi avversi minimi
Facile da somministrare da parte del
paziente o di chi ne ha cura
1. Zeppetella & Ribeiro. Expert Opin Pharmacother 2003; 2. Simmonds. Oncology 1999
Farmaci per il DEI
Il BTcP può essere trattato con oppioidi orali a rapido rilascio o
con preparazioni di fentanyl transmucosale o intranasale.
In alcuni casi queste formulazioni sono da preferire perché
consentono una più rapida insorgenza dell’analgesia rispetto
alle preparazioni orali a rapido rilascio ed hanno una minor
durata d’azione (raccomandazione positiva forte).
Le formulazioni a rilascio immediato con breve emivita
dovrebbero essere somministrate 20-30 minuti prima di
manovre
considerate
potenzialmente
dolorose
(raccomandazione positiva debole).
Considerazioni
In un recente passato si consigliava una scelta farmacologica empirica, ovvero “per
tentativi”.
Oggi si cerca si attuare scelte piu’ ragionate.
Si e’ stabilito che l’intensita’ del dolore rappresenta un primo criterio di scelta
relativamente alla potenza dei farmaci analgesici a disposizione, cosi come il tipo
di paziente e le sue patologie sottostanti.
Le criticita’ della scelta stanno
nella personalizzazione del farmaco oppiaceo,
nella definizione del giusto dosaggio e
nelle modalità di impiego dei farmaci adiuvanti, che in alcuni casi, modificano il
risultato antalgico in modo sostanziale. Per ultimo
e’ fondamentale che il paziente sia seguito nel tempo all’interno di un piano
di cura preciso e adattabile alle diverse modificazioni della patologia.
Inoltre . . .
Si invia allo specialista algologo il paziente che:
• Non raggiunge o raggiunge parzialmente gli obiettivi prefissati dopo un
periodo di tempo ritenuto adeguato (30-45 giorni).
• Presenta dolore cronico non oncologico in corso di terapia continuativa con
oppiacei per il dolore forte.
• Desidera la visita algologica per sindrome ansiosa giustificata.
• Presenta un quadro clinico che genera nel MMG dubbio/paura/incertezza
per cui il MMG richiede la visita algologica per conferma/supporto.
In caso di dolore non responsivo al trattamento con i farmaci
indicati nella scala OMS, è necessario ricorrere a pratiche
specialistiche specifiche; queste condizioni si presentano nel 520% dei casi.
In alcune patologie particolari (pancreas/trigemino) è necessario
ricorrere a procedure specialistiche che tendono a modulare o
bloccare la trasmissione del dolore con metodiche invasive.
Quindi …..
Percorso assistenziale
Misuro il dolore
Determino il livello
Tratto
Non tratto
Rivaluto
QUALE FARMACO USARE ?
Il più adatto
Con migliore performance nel tempo
Che ci permette di ottenere un painrelief nelle 24
ore con minore incidenza di effetti collaterali
10 REGOLE PER L’USO ANALGESICI
1) Utilizzare la via orale
2) Somministrare a ore fisse
3) Seguire una sequenza nella somministrazione dei
farmaci
4) Individualizzare i trattamenti
5) Dettagliare la posologia
6) Controllare frequentemente i risultati
7) Usare adeguate associazioni farmacologiche
8) Essere a conoscenza delle controindicazioni ed effetti
collaterali
9) Impiegare utilmente i farmaci adiuvanti
10) Non usare mai i farmaci placebo
Gli errori più frequenti
DOSAGGIO
TRAMADOLO 5-10 GOCCE OGNI 12
ORE (il dosaggio per un paziente
adulto è di 50mg – 100 mg ogni 6-8
ore)
EMIVITA ANTALGICA
( attenzione a rispettare le cinetiche
dei farmaci)
SOMMINISTRARE UN OPPIODE CHE
HA UNA EMIVITA DI 6-8 ORE OGNI
12 ORE O UN FARMACO A LENTO
RILASCIO AL BISOGNO (es. codeinaparacetamolo,
tramadoloparacetamolo,
ossicodoneparacetamolo, ossidocone-naloxone,
somministrati al bisogno…)
EFFETTO TETTO
SOLO EFFETTI COLLATERALI E NON
TERAPEUTICI
Gli errori più frequenti
ASSOCIARE OPPIACEI DEBOLI CON OPPIACEI FORTI (esempio classico
tramadolo + morfina)
ASSOCIARE AGONISTI PARZIALI E AGONISTI PURI
rilascio + buprenorfina transdermica)
NON TRATTARE IL BTP(DEI) CON ALTRA MOLECOLA perché già in corso
trattamento con oppiaceo a lento rilascio
INCOMINCIARE NEL PAZIENTE NAIVE UNA TERAPIA ANTALGICA CON
FARMACI PREVISTI PER IL BTP (DEI) (fentanyl transmucoso o per inalazione)
(ossicodone a lento
Gli errori più frequenti
Inizio della terapia con FENTANYL TRANSDERMICO in pazienti che non hanno
mai assunto oppiacei forti
Mancata o errata prescrizione di dose di oppiaceo di soccorso
Scarsa informazione a paziente e familiari
Rivalutazioni intempestive per dolore non controllato, soprattutto in fase iniziale
Errori di dosaggio nella “rotazione” da un oppiaceo ad un altro o da una via di
somministrazione ad un’altra (da os a s.c.)
Mancato o errato utilizzo di farmaci “adiuvanti
Mancata prescrizione di terapia lassativa
Ricorda !
60 MG MORFINA OS/24 ore CORRISPONDONO A :
CEROTTO 25 FENTANYL
CEROTTO 35 BUPRENORFINA
12 MG METADONE
30 MG OSSICODONE
300 MG TRAMADOLO
Dolore cronico.. Quale beneficio dai farmaci ?
Il 68% continua ad avvertire il dolore cronico per
>12 ore nonostante i trattamenti
Il 38% si ritiene mediamente soddisfatto delle
terapie farmacologiche
2 su 10 le definiscono inadeguate e insoddisfacenti
DOLORE TOTALE
L A C O M P L E S S I T À D E L L A M A L AT T I A D O L O R E R E N D E
N E C E S S A R I O U N A P P R O C C I O M U LT I D I M E N S I O N A L E ,
CHE
TENGA
CO N TO
ANCHE
DEI
BISOGNI
PSICOLOGICI, SPIRITUALI E SOCIALI, CHE DEVONO
ESSERE
C O N S I D E R AT I
CON
AT T E N Z I O N E
E
A F F R O N TAT I C O N T E M P O R A N E A M E N T E A L L A C U R A
DEL DOLORE FISICO.
Il dolore totale
Proposte di lettura
1.
Il dolore cronico in Medicina generale, 2010
2.
Libro bianco sul dolore cronico, 2014
3.
Wolkerstorfer A. et al. New approaches to
treating pain. Bioorg Med Chem Lett. 2015 Dec
30.
pii:
S0960-894X(15)30416-9.
doi:
10.1016/j.bmcl.2015.12.103.
4.
The CDC Guideline for Prescribing Opioids for
Chronic Pain, United States, 2016
Trattamento del dolore
L'effetto analgesico è uno degli obiettivi
più importanti del trattamento in termini di
miglioramento della qualità della vita.
Il trattamento farmacologico per il dolore
comprende analgesici non oppioidi, come
salicilati, paracetamolo e FANS, oppiacei e
altre classi di farmaci, tra cui antidepressivi
e anticonvulsivanti.
Wolkerstorfer A. et al. New approaches to treating
pain. Bioorg Med Chem Lett. 2015 Dec 30. pii: S0960894X(15)30416-9. doi: 10.1016/j.bmcl.2015.12.103.
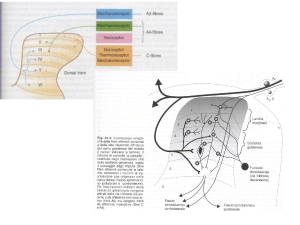
Farmaci oppioidi imitano le azioni di
endorfine interagendo con i recettori
oppioidi nel cervello e nel midollo spinale.
L’attivazione dei recettori mu degli oppioidi
(MOR) nelle vie ascendenti può agire
inibendo i segnali nocicettivi.
L’aumento
dell'effetto
sull’attività
ascendente dei recettori degli oppioidi può
attivare il patway discendente dei percorsi
neurali e produrre sollievo dal dolore.
Tuttavia, gli oppioidi sono associati con un
potenziale di abuso e dipendenza e sono
generalmente indicati nel dolore acuto da
moderato a grave.
Wolkerstorfer A. et al. New approaches to treating
pain. Bioorg Med Chem Lett. 2015 Dec 30. pii: S0960894X(15)30416-9. doi: 10.1016/j.bmcl.2015.12.103.
La classificazione degli analgesici 'non
oppioidi' comprende un insieme di
molecole diverse con effetti analgesici, tra
cui i FANS, modulatori dei canali ionici
voltaggio-dipendenti
(VGCC),
cannabinoidi, antidepressivi e molto altro
ancora.
Farmaci non oppiacei per via orale sono
raccomandati per il dolore acuto da lieve a
moderato e la maggior parte sono
disponibili al banco o su prescrizione
medica.
La terapia con FANS è associata con effetti
collaterali potenzialmente gravi, il rischio
di questi è aumentato in parallelo
all’aumento delle dosi e con l’uso a lungo
termine.
Wolkerstorfer A. et al. New approaches to treating
pain. Bioorg Med Chem Lett. 2015 Dec 30. pii: S0960894X(15)30416-9. doi: 10.1016/j.bmcl.2015.12.103.
Quando la fisiopatologia di una condizione
medica è multimodale, cioè è in relazione a
molteplici cause fisiologiche o mediata
attraverso diverse vie, la strategia ottimale
può essere di utilizzare un farmaco o una
combinazione
di
farmaci
che
contribuiscono con meccanismi multipli
all’azione terapeutica. In tali situazioni, un
razionale approccio multimodale può
anche provocare il minor numero di effetti
negativi.
La maggior parte dei dolori sono
multifattoriali
in
natura a
causa
dell'anatomia e fisiologia di trasmissione
del dolore.
Wolkerstorfer A. et al. New approaches to treating
pain. Bioorg Med Chem Lett. 2015 Dec 30. pii: S0960894X(15)30416-9. doi: 10.1016/j.bmcl.2015.12.103.
Anche il dolore acuto post operatorio risulta sottotrattato
e può succedere che anch’esso cronicizzi. L’utilizzo di nuove tecniche
analgesiche come l’anestesia regionale ha sicuramente migliorato gli
outcome dei pazienti.
Per il dolore neuropatico c’è una vasta gamma di molecole disponibili,
come: farmaci antiepilettici, analgesici oppiacei, antidepressivi triciclici,
inibitori selettivi della ricaptazione della serotonina (SSRI),inibitori della
ricaptazione di serotonina-norepinefrina (SNRI), antagonisti del recettore Nmetil- D-aspartato (NMDA), antagonisti del recettore della colecistochinina,
adenosina, acido lipoico, cannabinoidi, isosorbide dinitrato, dronabinol,
capsaicina, inibitori delle protein chinasi C, inibitori del’aldolaso reduttasi e
modulatori dei recettori VR-1 ma anche combinazioni di alcune classi delle
sopra citate.
Molti di questi composti sono limitati dalla efficacia marginale e da eventi
avversi clinicamente significativi.
Wolkerstorfer A. et al. New approaches to treating pain. Bioorg Med Chem Lett. 2015 Dec 30. pii:
S0960-894X(15)30416-9. doi: 10.1016/j.bmcl.2015.12.103.
I
FANS
includono
molecole
con
caratteristiche differenti; la principale
differenza è in inibitori della COX1 o della
COX2. Questi ultimi sono legati a meno
effetti collaterali visto che non hanno gli
effetti emostatici degli inibitori COX1. I
COX2 sono però collegati ad aumento del
rischio cardiovascolare.
Wolkerstorfer A. et al. New approaches to treating
pain. Bioorg Med Chem Lett. 2015 Dec 30. pii: S0960894X(15)30416-9. doi: 10.1016/j.bmcl.2015.12.103.
Per quanto riguarda gli oppioidi e i loro effetti collaterali negli ultimi anni sono
state sviluppate molecole che consentono il risparmio dell’oppioide .
Ad esempio il tramadolo, agisce come oppioide debole e riduce la trasmissione
degli impulsi di dolore inibendo la ricaptazione di serotonina e noradrenalina, in
modo da indurre un effetto combinato analgesico/adiuvante.
Tapentadolo similmente è un nuovo analgesico che combina un effetto agonista
sui recettori MOR e l'inibizione della ricaptazione della noradrenalina (NRI) in una
singola molecola, e che mostra analgesia potente ed efficace.
Wolkerstorfer A. et al. New approaches to treating pain. Bioorg Med Chem Lett. 2015 Dec 30. pii: S0960894X(15)30416-9. doi: 10.1016/j.bmcl.2015.12.103.
Gli autori continuano la trattazione parlando anche di altri farmaci che ad
esempio agiscono sui canali al sodio, al calcio e al potassio voltaggio dipendenti
e antagonisti selettivi del recettore della CRPC- Calcitonin gene-related peptide e
molecole attive sui recettori dei cannabinoidi, gli anticorpi monoclonali in fase di
sviluppo clinico (es. anti-NGF, anti-IL6 e anti-TNF) e la seconda generazione di
agonisti e antagonisti dei recettori vanilloidi (TRPV1) che non causano aumento
della temperatura corporea come i predecessori (ci sono al momento disponibili
in tutto il mondo patch alla capsaicina e creme per il trattamento del dolore).
In conclusione, gli autori sottolineano che la ricerca sui meccanismi alla
base dell’origine del dolore ha fatto passi da gigante negli ultimi anni e che
sono in fase di sviluppo nuove molecole che si spera avranno un’azione più
efficace delle esistenti e soprattutto con meno effetti collaterali.
Wolkerstorfer A. et al. New approaches to treating pain. Bioorg Med Chem Lett. 2015 Dec 30. pii:
S0960-894X(15)30416-9. doi: 10.1016/j.bmcl.2015.12.103.
PRDM 12
Il gene del dolore
l ricercatori dell'Università di Cambridge (Regno Unito) guidati da GeoffreyWoods e Jan
Senderek hanno individuato il gene del dolore,PRDM12, aprendo così la strada a nuove
terapie.Come riportato da Nature Genetics, la chiave per comprendere meglio come nasca il
dolore,gli studiosi l'hanno trovata proprio in chi è incapace di provarlo, perché affetto da
Insensibilità Congenita al Dolore (CIPA),una rara condizione per cui una persona non riesce a
provare sofferenza fisica.
Così,partendo dallo studio di pazienti con questa patologia, nei membri di famiglie non
imparentate tra loro, che presentavano mutazioni in entrambe le copie del gene PRDM 12, i
ricercatori sono riusciti a identificare 10 diverse mutazioni nel gene PRDM 12.Chi ha queste
mutazioni è, dunque, incapace di sentire il dolore fin dalla nascita e non riesce a distinguere tra
il freddo e un calore sgradevole, mentre le caratteristiche degli altri sensi rimangono normali.
Usando le cellule di topi e uomini senza questa patologia, il team di ricerca ha osservato poi
che il gene PRdMl2 è espresso proprio dai recettori del dolore e cellule collegate e che la
proteina da esso prodotta è un fattore chiave per la genesi dei nervi collegati alle sensazioni e
può essere utilizzata come bersaglio per nuove terapie antidolore.
Fonte: Nature Genetics, 2015
Dolore neuropatico diabetico
Approvato cerotto alla capsaicina
I pazienti con neuropatia diabetica periferica che fanno uso di un cerotto alla capsaicina
vanno incontro ad un maggior sollievo dal dolore ed a una migliore qualità del sonno
rispetto a coloro che vengono trattati con placebo.
Questo dato emerge dallo studio di fase 3 noto come STEP, che accompagna l’ approvazione
di questi cerotti sul territorio europeo anche per l’indicazione addizionale del trattamento di
pazienti adulti diabetici con dolore neuropatico periferico, da soli o in combinazione con
altri antidolorifici.
Il cerotto alla capsaicina era già stato approvato nell’Unione Europea per il dolore
neuropatico, ma la licenza escludeva i pazienti diabetici.
Analogamente, negli USA esso è approvato per il trattamento della nevralgia post herpetica,
ma ciò non include i pazienti diabetici. Secondo Malcolm Stoker della Astellas Pharma
Global Development, che ha presentato lo studio condotto su 369 pazienti, il cerotto,
oltre a portare ai suddetti benefici in termini di livelli di dolore e qualità del sonno, risulta
ben tollerato, con profili di sicurezza coerenti con quanto precedentemente rilevato negli
studi su soggetti con nevralgia posterpetica e neuropatia da Hiv.
Fonte: European Association for the Study of Diabetes 2015 Meeting, ab- stract 64
Agire sul
cervelletto
riduce il dolore
Il cervelletto, oltre alle funzioni di controllo del movimento, ha un ruolo importante
nella modulazione del dolore. É quanto emerge da uno studio coordinato da
Ferdinando Sartucci, direttore della sezione dipartimentale di Neurologia dell'ospedale
Cisanello di Pisa e condotto da Tommaso Bocci, assegnista di ricerca dell'Università di
Pisa.
La ricerca, pubblicata dalla rivista Restorotive Neurology ond Neuroscìence, - frutto della
collaborazione tra gli Atenei di Pisa, Siena, Aalborg (Danimarca) e gli Istituti di ricovero
e cura 'Bambino Gesu" di Roma e Policlinico di Milano - ha dimostrato che l'utilizzo della
"stimolazione transcranica a corrente diretta" (Tdcs) modifica significativamente la
soglia del dolore.
Lo studio ha dimostrato che laTdcs può essere efficace nel trattamento del dolore non
solo attraverso la stimolazione della corteccia frontale ma anche utilizzando il cervelletto.
Fonte: Restorotive Neurology and Neuroscìence, 2015
Programma intensivo riduce dolore e uso degli oppioidi
Un intensivo programma di gestione biopsicosociale del dolore cronico ha portato a significative
riduzioni sia nei livelli di dolore che nell’impiego di oppioidi in un campione di 118 pazienti. Secondo
Bruce Singer, direttore del Chronic Pain and Recovery Center del Silver Hill Hospital di New Canaan ed
autore dell’indagine, il 63% dei pazienti che giungono all’osservazione con dolore cronico e in
terapia con oppioidi viene dimesso senza questi farmaci e con una riduzione del 25% nei livelli di
dolore. Nel programma residenziale proposto, i pazienti con dolore cronico che non hanno risposto
alla terapia con oppioidi vengono seguiti per un minimo di 4 settimane e prendono parte ad un’ampia
gamma di attività terapeutiche per 12 - 14 ore al giorno. Il programma si svolge eminentemente in
gruppo, con attività incentrate sulla costruzione di skill di autogestione per la riduzione del dolore, il
miglioramento della funzionalità ed il trattamento di disordini mentali o di dipendenza concomitanti
con terapie cognitivo-comportamentali o di altro tipo.
Il programma è anche fortemente improntato alla riduzione dell’affidamento sui medicinali ed al
miglioramento della qualità della vita del paziente, essenzialmente tornando a porre il controllo del
dolore di nuovo nelle mani del soggetto. Fra gli altri risultati, il trattamento porta a significative
riduzioni dei livelli di ansia e depressione, nonché del
pensiero catastrofista, caratterizzato da
ruminazione, magnificazione e sentimento di disperazione.
Fonte: American Academy of Pain Management (AAPM) 2015 Annual Meeting
SITUAZIONE LEGISLATIVA EUROPEA
Il controllo e il monitoraggio del consumo dei farmaci oppiacei da parte dei Governi
centrali dovrebbe, di fatto, garantire l’accesso ai pazienti e la possibilita’ per i medici
di prescriverli senza disagi o preclusioni.
La storia recente sull’uso degli oppiacei nel dolore cronico e’ una storia ricca di
progressi, a partire dall’aumento graduale della conoscenza da parte dei medici
sulla loro efficacia e sicurezza e dalle modifiche introdotte dai Governi in relazione a
precedenti restrizioni legislative e al conseguente migliore accesso da parte dei
pazienti alla terapia con oppiacei.
Anche se di recente l’accesso ai farmaci necessari alla cura del dolore, in modo
particolare in Europa, e’ migliorato, permangono tuttavia attitudini negative che
necessitano di strategie di comunicazione e formazione continua.
CANNABIS
TERAPEUTICA
La Cannabis è sicuramente nota a tutti per il suo utilizzo “ludico” e come droga
di abuso per le sue proprietà psicotrope sulla regolazione dell’umore e sulla
sensazione di benessere che ne deriva, tuttavia negli ultimi anni è tornata in
auge per la terapia di alcune forme neurologiche altrimenti non curabili o di
difficile trattamento.
L’ Istituzione che si è proposta allo studio e soprattutto alla regolamentazione è
l’OMC (Office of Medicinal Cannabis) del Ministero della Salute Benessere e
Sport Olandese.
Solo recentemente il Ministero della Salute Italiano ha emanato un
Decreto che inserisce la Cannabis nelle sostanze farmacologicamente
attive e ne dispone le regole per la sua prescrizione, preparazione e
dispensazione.
Indicazioni - Terapia con la cannabis
Le più importanti patologie che si possono trattare con l’infiorescenza della Cannabis
sono:
Disturbi che coinvolgono la spasticità con dolore (sclerosi multipla, lesioni al midollo
spinale)
Nausea e vomito (risultante dalla chemioterapia, radioterapia e terapia combinata
per l’HIV ed Epatite C)
Dolore cronico (in particolare dolore neurogenico)
Sindrome di Gilles de la Tourette
Trattamento palliativo del cancro e dell'AIDS
Glaucoma resistente
Stimolazione dell'appetito in pazienti affetti da cancro o HIV
L'uso di cannabis è indicato solo quando i risultati con i protocolli terapeutici
riconosciuti sono insoddisfacenti o quando sono troppi e gravi gli effetti
collaterali che si verificano.
Tipi di cannabis coltivati e reperibili
Attualmente in commercio ci sono tre tipi di Cannabis distinte a seconda della famiglia del
vegetale da cui sono tratte
1. Cannabis varietà Bedrocan con un titolo del 19% in THC( Tetraidrocannabinolo ) e meno
dell1% in CBD (Cannabidiolo);
2. Cannabis varietà Bedrobinol titolata in 12% in THC e meno dell1% in CBD
3. Cannabis varietà Bediol con il 6% in THC ed il 7,5% in CBD.
Prescrizione e ricetta tipo
La ricetta per la prescrizione della cannabis ha delle particolarità proprie legate
all’attuale legislazione e classificazione. Infatti nella Tabella II, sezione B del
decreto stupefacenti (Dpr 309/90), che inserisce i medicinali vegetali, sia di
origine industriale che allestiti in farmacia, a base di Cannabis, nelle sostanze
stupefacenti, limita la prescrizione a seconda della patologia per la quale è
prescritta.
Le prescrizioni di preparazioni magistrali sono regolamentate dall’articolo 5 del
D.L. 1 febbraio 1998, n. 23, convertito dalla Legge 8 aprile 1998, n. 94 e successive
modifiche ed interpretazioni.
Le preparazioni magistrali di sostanze vegetali a base di cannabis possono essere
allestite dietro presentazione di prescrizione medica non ripetibile.
Gli unici prodotti che possono essere impiegati per l’allestimento di tali
preparazioni sono le sostanze vegetali esportate dall’Office for Medicinal Cannabis
del Ministero della salute, del welfare e dello sport olandese.
Si sottolinea che, non avendo tali preparazioni magistrali a base di sostanze
vegetali indicazioni terapeutiche autorizzate, devono essere applicate le
disposizioni dei commi 3 e 4 del citato articolo 5.
Art. 5 -omissis
3. Il medico deve ottenere il consenso del
paziente al trattamento medico e
specificare nella ricetta le esigenze
particolari che giustificano il ricorso alla
prescrizione estemporanea. Nella ricetta il
medico dovrà trascrivere, senza riportare le
generalità del paziente, un riferimento
numerico o alfanumerico di collegamento a
dati d’archivio in proprio possesso che
consenta, in caso di richiesta da parte
dell’autorità sanitaria, di risalire all'identità
del paziente trattato.
4. Le ricette di cui al comma 3, in originale
o in copia, sono trasmesse mensilmente dal
farmacista all’ASL o all’azienda ospedaliera,
che le inoltrano al Ministero della sanità
per le opportune verifiche.
INTESTAZIONE MEDICO/STUDIO/STRUTTURA SANITARIA
CONSENSO INFORMATO
Io
sottoscritto/a
e
residente
nato/a
a
_______________________
a
in via
il
_____________________________________
______________________
n. ________________
telefono ____________________________
dichiaro di
essere stato correttamente informato dal Dott./Dott.ssa.
particolare riferimento a:
·
·
·
·
in merito alla terapia a cui verrò sottoposto, con
principi attivi prescritti
dosaggio
modalità di somministrazione
durata del trattamento
come da schema terapeutico allegato ed ai potenziali effetti collaterali ed avversi, ed esprimo liberamente il mio consenso al
trattamento.
Data
Firma del paziente
Timbro e firma del medico prescrittore
Recapito a cui fare riferimento in caso di emergenza
_
PIANO TERAPEUTICO
Cognome e nome del paziente ( sigla alfanumerica ): ………………… Codice fiscale:
…………………………………………..
Data di nascita: ………/……./……….. ASL appartenenza: ……..
Provincia: ………………………………….. Regione: …………………………….
Diagnosi: ………………………………………………………………………………………..
……………………………………………………………………………………………………
formulata in data: ………………………………….
Medico specialista: ………………………………………………………..
Centro specialistico: ……………………………………………………………….
Programma terapeutico:
Cannabis flos 19% THC ( Bedrocan)
Una cartina da mg. …………..
Numero cartine totali = …………………… Quantità totale mg. ………………………..
Posologia: ……………………………………..
Assunzione per via:
orale
inalatoria
Durata del trattamento mesi ………………
Data:
timbro struttura
FAC SIMILE RICETTA Bustine filtro/cartine/capsule
Prescrittore:
Cognome e nome
N° iscrizione all’ordine dei medici
Indirizzo telefono
utilizzatore:
Codice numerico/alfanumerico – N.B. non nome e
cognome
data
R/
□ Cannabis flos 19% (HTC 19% - CBD <1%) Bedrocan
□ Cannabis flos 12% (HTC 12% - CBD <1%) Bedrobinol
□ Cannabis flos 6% (HTC 6% - CBD 7,5%) Bediol
eccipienti inerti q.b. e se necessari.
F.S.A.
□ una busta filtro da milligrammi. ……….. e di tali n°……...buste filtro
□ una cartina da milligrammi. ……….. e di tali n°……...cartine
□ una capsula apribile da milligrammi. ……….. e di tali n°……...capsule
Quantità totale cannabis flos milligrammi …………….
S/
□ una busta filtro/capsula apribile ……….. volta/e al giorno da assumersi in decozione per via orale
□ una cartina……….. volta/e al giorno da assumersi per inalazione
RICETTA NON RIPETIBILE
Timbro e firma prescrittore
Motivazione della prescrizione ( non indicare la diagnosi) Esempio: specialità non in commercio
FAC SIMILE RICETTA olio
Prescrittore: utilizzatore:
Cognome e nome
Codice numerico/alfanumerico – N.B. non nome e cognome
N° iscrizione all’ordine dei medici
Indirizzo telefono
data
R/
grammi 5 di:
□ Cannabis flos 19% (HTC 19% - CBD <1%) Bedrocan
□ Cannabis flos 12% (HTC 12% - CBD <1%) Bedrobinol
□ Cannabis flos 6% (HTC 6% - CBD 7,5%) Bediol
in olio extravergine di oliva 50ml
F.S.A.
una soluzione oleosa, secondo metodica indicata nell'articolo scientifico di Luigi L. Romano e Arno
Hazekamp, 2013,
□ protocollo numero 4
□ protocollo numero 5
S/
assumere ……….gocce pure o diulite ….............volte al giorno per per via orale
RICETTA NON RIPETIBILE
Timbro e firma prescrittore
Motivazione della prescrizione ( non indicare la diagnosi) Esempio: specialità non in commercio
Modalità di assunzione
I metodi di somministrazione raccomandati sono due: orale ed inalatorio. Gli effetti farmacologici sono più rapidi ed
intensi, ma meno prolungati, se la somministrazione avviene per inalazione.
Entrambe le metodologie prevedono il riscaldamento della Cannabis, operazione fondamentale per
l’attivazione dei cannabinoidi contenuti nei derivati vegetali.
7.1
Assunzione per via orale
7.1.1
Decozione con buste filtro
Per comprendere correttamente la ragione delle modalità di assunzione è bene sapere che l’infiorescenza di Cannabis, per
poter rilasciare il proprio principio attivo, deve essere riscaldata sopra i 90° C. Per questo viene preparata come un tè anche
se si tratta più precisamente di un decotto.
Bedrocan ( Cannabis flos 19% HTC ) è la varietà più adatta per la preparazione del decotto.
Preparazione:
• Bollire 200 ml circa di acqua in un tegame con il coperchio.
• Aggiungere una busta filtro di cannabis medicinale secondo quanto prescritto dal medico.
• Abbassate il fuoco e lasciate la busta filtro sobbollire dolcemente per 15 minuti con il coperchio ancora sul tegame.
• Prendere il decotto dal fornello e versare direttamente in tazza. La comodità di avere la busta filtro evita di dover colare il
tè.
• Bere il decotto ben caldo. Si può aggiungere zucchero, sciroppo o miele per migliorare il gusto.
Il rapporto tra acqua e droga deve essere di 1000:1 cioè in un litro d’acqua un grammo di droga.
Al posto dell’acqua, per chi lo gradisce, si può usare il latte intero come solvente, con le stesse modalità.
7.1.2
Olio
L'assunzione va indicata dal medico prescrittore ed effettuata concentrata o diluita ed assunta direttamente per via orale.
7.2
Assunzione per via inalatoria
L'inalazione agisce più in fretta e il suo effetto è più forte del decotto. Inoltre, il dosaggio è più facilmente regolabile.
L’apparecchio vaporizzatore specifico sopra illustrato è il Volcano ed ha la funzione di nebulizzare la cannabis per uso
inalatorio
In letteratura la posologia si riferisce generalmente al solo contenuto in mg di THC,
pur sapendo che il fitocomplesso comprende altri principi attivi che possono influire
sull’effetto farmacologico.
La scelta della via di somministrazione influisce notevolmente sulla farmacocinetica e
sulla farmacodinamica del prodotto: la via inalatoria comporta un rapido
assorbimento dei principi attivi ed una rapida comparsa dell’effetto (circa in 15 minuti).
I picchi ematici sono elevati e l’eliminazione rapida. Se assunta oralmente, invece, la
cannabis manifesta i suoi effetti dopo 30-90 minuti raggiungendo il massimo dopo
due o tre ore. L’effetto si prolunga per altre 4-8 ore. L’eliminazione è graduale.
In entrambi i casi, si consiglia di iniziare con dosaggi bassi e attendere due settimane
prima di valutare una variazione della posologia.
Si raccomanda di non “fumare” i prodotti in quanto la combustione
determina una notevole perdita di principi attivi (fino al 40%).
Bedrocan e Bedrobinol sono disponibili in forma di punte di fiori secchi (flos).
Bediol è fornito sotto forma di granuli.
Tutte le tre varietà possono essere usate per fare il decotto o inalate attraverso
il vaporizzatore.
Date le caratteristiche chimico-fisiche dell’HTC, in quanto scarsamente solubile
in acqua, è possibile sostituire l’acqua con il latte o con altro veicolo lipofilo.
In questo caso è possibile assumere il liquido anche freddo in quanto il
principio attivo non si deposita sulle pareti del contenitore.
Quale è il dosaggio della Cannabis Flos?
La posologia dei derivati della Cannabis è estremamente variabile e dipende da numerosi fattori
che concorrono a determinare il dosaggio. Tra i fattori più rilevanti vi sono:
·
·
·
·
·
·
Sesso, età e peso del paziente
Natura della patologia
Tipo e gravità dei sintomi
Risposta individuale
Terapie concomitanti
Via di somministrazione
Perciò il dosaggio deve essere deciso dal medico, valutando caso per caso.
Il produttore raccomanda di iniziare con la dose più bassa possibile, senza però indicare
specificatamente quale possa essere.
In letteratura i dosaggi utilizzati nelle sperimentazioni possono variare notevolmente in base
principalmente alla patologia indagata ed al tipo di materia prima utilizzata (pianta secca, estratti
fluidi, THC puro ecc). Non è perciò possibile stabilire un protocollo di impiego. E’
fondamentale ricordare che i cannabinoidi sono liposolubili e si accumulano nel tessuto adiposo
che li rilascia lentamente.
Questo fa sì che le prime somministrazioni possano sembrare inefficaci, tuttavia il successivo
rilascio di principi attivi da parte del tessuto adiposo innalza la frazione attiva circolante.
È perciò consigliabile iniziare con dosaggi bassi somministrandoli per 7-10 giorni prima di
variare il dosaggio.
La tabella seguente riporta alcune indicazioni su possibili dosaggi in relazione alle varie patologie,
tuttavia è fondamentale ricordare che questi dosaggi sono puramente indicativi e che è
sempre fondamentale la valutazione dell’efficacia del farmaco sul paziente.
INDICAZIONE
TERAPEUTICA
SNC: spasticità da
para/tetraplegia, danno spinale,
SLA, Corea di Huntington, morbo
di Parkinson, ecc.
Sclerosi multipla
Malattia di Alzheimer
Emicrania, emicrania a grappolo
Paura/ansia, stress posttraumatico, depressione
Disturbi del sonno, apnee notturne
Sindrome di Tourette
Dolore cronico: dolore neuropatico,
artrite, dolore fantasma
Fibromialgia
Terapia combinata con oppioidi
BPCO, asma
Malattie infiammatorie intestinali
croniche: morbo di Crohn, colite
ulcerosa, colon irritabile, enteropatia
da glutine
Nausea, vomito da chemioterapia
Anoressia, cachessia
Incontinenza urinaria, disturbi
vescicali
DOSE
THC
Da 10 mg a 20 mg/die.
QUANTITA’ DI BEDROCAN
(19% THC)
Da circa 50 mg/die a circa 100 mg/die
Da 5-10 mg/die fino a 25 mg/die
Da 2,5 mg alla sera fino a 5 mg 2 v. al dì
Singola dose da 5 mg durante l’attacco
Da 2,5 mg a 7,5 mg/die
Da circa 25 mg/die a circa 130 mg/die
Da circa 15 mg/die a circa 25 mg 2 v. al
dì
Circa 25 mg in singola dose
Da circa 15 mg a circa 40 mg/die
Da 2,5 mg a 10 mg/die
Da 10 mg a 20 mg/die
Da 10 mg poi aumentare
settimanalmente di 2,5 mg fino a
70 mg/die
Da 2,5 mg poi aumentare
settimanalmente di 2,5 mg fino a
15 mg/die
Da 10 mg a 20 mg/die
3-4 mg 2 volte al dì, prima dei pasti
Da 7,5 a 15 mg/die
Singola dose da 5-10 o 20 mg 2 ore
prima
del trattamento, ripetuta ogni 3-4
ore fino ad un massimo di 40
mg/die
Da 2,5 mg a 10 mg due volte al giorno
prima dei pasti
Da 5 mg a 25 mg/die
Da circa 15 mg/die a circa 50 mg/die
Da circa 50 mg a circa 100 mg /die
Da circa 50 mg poi aumentare
settimanalmente di circa 15 mg fino
a circa 400 mg/die
Da circa 15 mg poi aumentare
settimanalmente di circa 15 mg fino
a circa 80 mg/die
Da circa 50 mg a circa 100 mg /die
Circa 15-20 mg 2 volte al dì, prima dei
pasti
Da circa 40 mg a circa 80 mg/die
Singola dose da circa 25-50 o 100 mg 2
ore prima del trattamento, ripetuta ogni
3-4 ore fino ad un massimo di circa 210
mg/die
Da circa 15 mg a circa 50 mg due volte
al
giorno prima dei pasti
Da circa 25 mg a circa 130 mg/die
Interazioni
La Cannabis può dare effetti cumulativi se assunta contemporaneamente ad alcool,
benzodiazepine od oppiacei. Se assunta oralmente si ha un effetto di primo
passaggio che può interferire con i farmaci metabolizzati dagli isoenzimi CYP2C9 e
CYP3A4 del sistema del citocromo P450 tra i quali: antibiotici macrolidi, antimicotici,
calcio-antagonisti, inibitori della proteasi HIV, amiodarone ed isoniazide. Questi
farmaci, che hanno una azione inibente sugli enzimi sopracitati, possono aumentare
la biodisponibilità dei cannabinoidi.
Hanno effetto accelerante della metabolizzazione dei cannabinoidi, e di conseguenza
ne diminuiscono la biodisponibilità i farmaci quali: rifampicina, carbamazepina,
fenobarbital, fenitoina, primidone, rifabutina, troglitazione ed iperico.
La cannabis può interferire con i farmaci che si legano alle proteine plasmatiche.
Avvertenze e controindicazioni
Gli utilizzatori inesperti possono essere spaventati dagli effetti psicologici della
Cannabis: si consiglia di effettuare la prima somministrazione del farmaco in
un ambiente controllato, alla presenza di un medico o di altra persona che
possa prestare assistenza.
Gli effetti collaterali più comuni sono: euforia, tachicardia, ipotensione
ortostatica, cefalea, vertigini, bruciore e rossore agli occhi, secchezza delle fauci,
debolezza muscolare. Si sconsiglia di somministrare alte dosi di Cannabis a
pazienti cardiopatici per il rischio di comparsa di tachicardie. Generalmente dopo
alcuni giorni o settimane si sviluppa una tolleranza che permette di aumentare
gradualmente la dose.
Si ricorda che è vietato assumere Cannabis se occorre mettersi alla guida di
automobili, moto od altri macchinari.
L'uso della Cannabis é generalmente controindicato in caso di: gravidanza,
allattamento, malattie psicotiche e nei bambini.
Concludendo
Nell’affrontare il dolore cronico è necessaria una strategia lineare che, riconoscendo gli
obiettivi prioritari, ne assicuri un raggiungimento tempestivo ed efficace. Questo sono:
•
La misurazione del dolore
•
La scelta e la personalizzazione della farmacoterapia
•
La gradualità dell’approccio terapeutico
•
La prevenzione della comparsa del dolore
•
La prevenzione degli effetti collaterali legati alla terapia
Il nuovo modello di assistenza deve essere fondato sul
concetto di Rete.
La Rete garantisce, inoltre, che tutte le componenti dei
processi di cura, attualmente frammentate e disperse
tra più servizi e operatori, siano sempre ricomponibili
e a disposizione del Sistema Sanitario Nazionale (SSN).
Quando tutto sembra chiarito,
l’imprevisto è in agguato …
“ Dottoressa, il dolore è scomparso, ma non potrebbe farmene
ritornare ancora un poco? Altrimenti sento il dolore dei miei
pensieri, che è più forte di quello delle mie ossa rotte”
Quale farmaco ho dimenticato ?
Sir Luke Fildes (1843 – 1918). The doctor, 1881
La dimensione della grandezza dell’ uomo si documenta proprio in quella capacità di
stare, di rimanere, anche là dove si potrebbe documentare solo l’impotenza e questa
cosa non è uguale a nulla.
Grazie per l’attenzione