LE REAZIONI DI ADDIZIONE AL DOPPIO LEGAME NEGLI ALCHENI
Gli alcheni sono idrocarburi caratterizzati dalla presenza di un doppio
legame Carbonio-Carbonio. Questi due atomi hanno tre orbitali ibridi sp2
disposti ad angoli di 120°, il quarto orbitale è di tipo p non ibridato e
perpendicolare al piano degli ibridi sp2. Tra i due atomi di carbonio si crea
un forte legame σ, per sovrapposizione testa-testa dei due orbitali sp2 e
un legame debole π per sovrapposizione laterale dei due orbitali p.
Queste caratteristiche strutturali degli alcheni ne influenzano la reattività
chimica.
Alcune tipiche reazioni che riguardano gli alcheni sono quelle in cui viene
rotto il legame π per formare due nuovi legami σ. Tali reazioni sono dette
REAZIONI DI ADDIZIONE AL DOPPIO LEGAME CARBONIO-CARBONIO.
Possono essere raffigurate cosi:
In generale per reazione di addizione s’intende un processo in cui a
partire da due reagenti, i quali si sommano, si forma un solo prodotto,
senza atomi in avanzo.
Un esempio rilevante di tali reazioni è la reazione degli alcheni con HCl
che porta alla formazione di cloruri alchilici, questo processo è di tipo
polare.
Consideriamo la reazione che vede come reagenti l’Etilene (C₂H₄) e
l’Acido Cloridrico (HCl) e come unico prodotto finale il Cloroetano
(C₂H₅Cl).
Dell’etilene sappiamo che ha tutte le caratteristiche degli alcheni ovvero
un doppio legame C=C derivante dalla sovrapposizione degli orbitali di
due atomi di carbonio ibridati sp2; una componente σ che deriva dalla
sovrapposizione sp2-sp2, mentre una componente π che deriva dalla
sovrapposizione p-p . La densità elettronica in un legame di questo tipo è
forte, infatti ci sono quattro elettroni in un doppio legame. Inoltre sempre
in base alle caratteristiche strutturali possiamo intuire che gli elettroni del
legame π sono facilmente accessibili ai reagenti esterni in quanto non si
trovano in posizione centrale tra i due nuclei, bensì sono situati al di sopra
e al di sotto del piano del doppio legame. Di conseguenza si può stabilire
che i doppi legami carbonio-carbonio si comportano da nucleofili. (sono
definiti nucleofili quei reagenti attratti dalle cariche positive). In quanto
tali, questi atomi reagiranno con sostanze elettrofile (attratte cioè dalle
cariche negative), ecco perché le reazioni di addizione tipiche degli
alcheni sono le ADDIZIONI ELETTROFILE.
Le addizioni elettrofile si svolgono in due fasi distinte: una lenta e una
veloce.
Dell’acido cloridrico sappiamo che è un acido forte quindi un potente
donatore di protoni H+.
Il processo di addizione di questi due reagenti ha inizio con la reazione
dell’etilene con H+. Accade che i due elettroni del legame π creano un
legame σ tra H+ e uno dei carboni dell’etilene, l’altro atomo di carbonio
invece, avendo perso gli elettroni che condivideva è rimasto con un
orbitale p vuoto, ha solo sei elettroni di valenza ed ha una carica positiva,
prende il nome di carbocatione. Esso è un intermedio di reazione. Questo
carbocatione è un elettrofilo e quindi accetta una coppia di elettroni dal
nucleofilo Cl⁻ dando origine al legame C-Cl. Il prodotto di questa
addizione, il cloroetano, sarà quindi neutro.
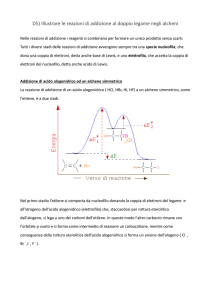
Il momento “lento” della reazione è quello in cui l’alchene si somma alla
componente positiva dell’altro reagente, causando la formazione del
catione carbonio;
il momento “veloce” della reazione è invece quello in cui il carbocatione
elettrofilo viene attaccato da un componente nucleofilo (in questo caso
Cl⁻). Questo stadio è veloce rispetto al primo per il semplice fatto che il
carbocatione, essendo un intermedio di reazione, non è molto stabile.
Alcuni esempi di reazioni elettrofile sono:
Addizioni di acidi alogenidrici (HCl, HBr, HI);
Addizione di acqua;
Alogenazione;
Ozonolisi ecc.
La maggior parte delle reazioni di addizione elettrofile rispetta la regola di
Markovnikov che afferma che in una reazione di addizione elettrofila l’HX
(secondo reagente) che si somma all’alchene (primo reagente) lo fa nel
seguente modo: H si lega al carbonio con minor numero di sostituenti e X
si lega invece al carbonio con maggior numero di sostituenti.
Se i due carboni hanno lo stesso numero di sostituenti allora si otterrà
una miscela di prodotti di addizione. Tenendo conto di questa regola si
può affermare che l’addizione di HX agli alcheni da origine al carbocatione
più sostituito anziché a quello meno sostituito (questo perché si cerca di
dare maggiore stabilità all’intermedio di reazione, infatti più un
carbocatione è sostituito e più è stabile).
Le reazioni che seguono l'orientamento inverso, cioè quelle in cui
l'idrogeno va a legarsi all'atomo di carbonio meno idrogenato, vengono
dette "anti-Markovnikov”.