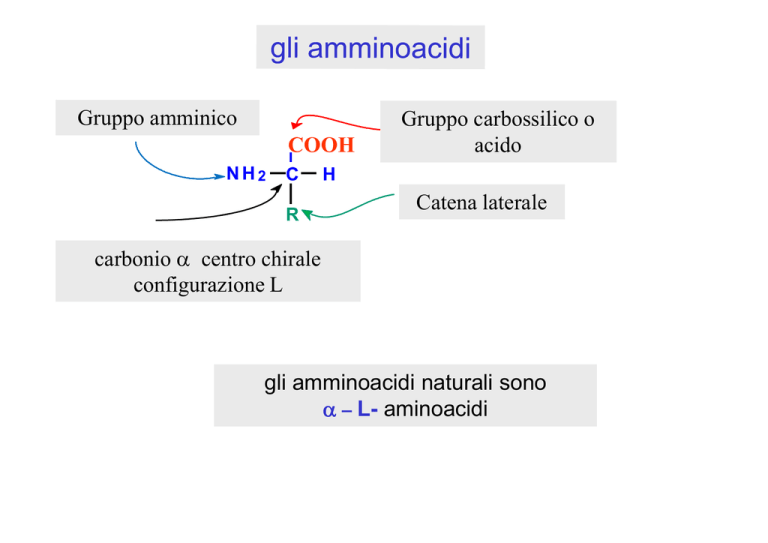
Gruppo amminico
COOH
NH2
C
R
Gruppo carbossilico o
acido
H
Catena laterale
carbonio α centro chirale
configurazione L
gli amminoacidi naturali sono
α – L- aminoacidi
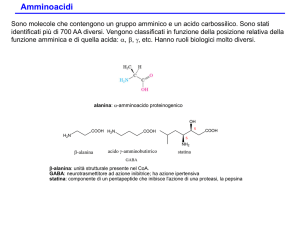
Gli amminoacidi sono anfoteri:
si comportano da basi con gli acidi e da
acidi con le basi.
base
R
CH
acido
COO-
+ H3O+
+ NH3
R
CH
+ NH3
CH
+ NH3
forma anfionica
(zwitterionica)
acido
R
COO-
COOH
+ H2 O
forma cationica
base
+ OH-
R
CH
COO+ H2 O
NH2
forma anionica
Gli amminoacidi delle proteine
differiscono per il gruppo R, che
può essere:
•
non polare
•
polare non carico
•
aromatico
•
dissociabile carico negativamente
•
dissociabile carico positivamente
Alcuni esempi
+
H3N
COO
C
-
H
COO
+
H3N
C
H
CH3
H
+
H3N
-
glicina [G]
(Gly)
alanina [A]
(Ala)
-
COO
COO
C
H
CH2OH
serina [S]
(Ser)
+
H3N
C
R non polare
-
H
CH2
SH
cisteina [C]
(Cys)
R polare non carico
Alcuni esempi
+
H3N
COO
C
-
H
COO
+
H3N
C
-
H
CH2
CH2
CH2
COO
CH2
acido aspartico [D]
(Asp)
R con carica negativa
CH2
+
NH3
lisina [K]
(Lys)
R con carica positiva
Alcuni esempi: R aromatico
+
H3N
COO
C
-
H
CH2
+
H3N
COO
C
-
H
CH2
OH
fenilalanina [F]
(Phe)
tirosina [Y]
(Tyr)
il legame peptidico
R
H 2N
C
H
OH
C
O
H
+ H N
R
C COOH
H
- H 2O
R
H
α
α
H2N C C N C COOH
H O
H
R
il legame peptidico
O
O
H2N
H
H COOH
C OH H N C H
C OH H N
C H
C H
H
CH3
Gly
CH2OH
Ser
Ala
legame peptidico
o carbammidico
amminoacido
N - terminale
La struttura primaria di un polipeptide
è costituita dalla sequenza secondo
la quale i vari amminoacidi si susseguono
nella catena
H2N
O
H COOH
N C H
O
H
C
C
N
C H
C H
CH3
amminoacido
C - terminale
CH2OH
H
Ala - Gly - Ser
(tripeptide)
Piano amidico
cheratina
collagene