“Metodologia clinica e strumentale
per la comprensione fisiopatologica del
paziente con insufficienza aortica.”
E. Congedo
Dipartimento di scienze cardio-toraciche e vascolari
Clinica Cardiologica
Università degli Studi di Padova
Metodo clinico strumentale
Il metodo clinico può essere definito come una successione ordinata di attività
pratiche (raccolta dei dati anamnestici, fisici e di laboratorio) e intellettuali
(ragionamento clinico), che hanno lo scopo di percepire (formulare l’ipotesi) e
definire (formulare la diagnosi) il problema sottostante.
R. Russo, S. Dalla Volta: “riflessioni sulla formazione medica in malattie
del cuore e dei vasi”; S. Dalla Volta, R. Razzolini, L. Daliento;
III edizione Mc Graw Hill pg 795 2005
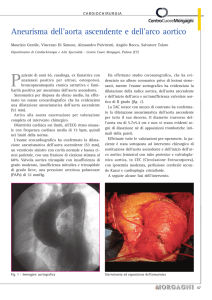
Corrigan: “ The quantity of blood that regurgitates will be largely in proportion
To the degree of inadequacy of the valves and to the lenght of
The pause between contractions of the ventricle during which
Blood can be pouring back”.
Edin Med Surg 1832; 37: 225-45
Fisiopatologia
-Le dimensioni dell’area rigurgitante
-Il gradiente pressorio diastolico aorta – ventricolo sinistro
-La durata della diastole
Influenzano l’entità del volume di rigurgito
E. Congedo, M. Bressan, P. Stritoni
In “malattie del cuore e dei vasi”. S. Dalla Volta
Cardiopatie Valvolari; insufficienza aortica, cap. 27 431-37 III edizione
Mc Graw Hill 2005
La completa comprensione della fisiopatologia richiede considerazioni delle tre
maggiori componenti del processo di malattia:
Il ventricolo sinistro
La valvola aortica
La vascolarizzazione sistemica
Altri fattori: anatomia e flusso coronarico
cambiamenti con l’esercizio fisico
differenze nella presentazione clinica tra rigurgito aortico cronico
ed acuto.
C. Otto: “Aortic regurgitation “, Valvular Heart Desease 302-335 ; II ed
Saunders 2004
Metodo clinico strumentale
Fattori fisiopatologici che influenzano l’accoppiamento ventricolo sx – aorta
nell’insufficienza aortica:
VENTRICOLO
Precarico (volume ventricolare/ritorno venoso)
Postcarico (stress circonferenziale di parete telesistolico)
Gradiente pressorio sistolico transvalvolare aortico
Contrattilità
Frequenza cardiaca
Geometria del ventricolo
Pressione di perfusione coronarica
VALVOLA
Area di rigurgito aortico
Volume di rigurgito
Gradiente di pressione diastolico aortico
Volume sistolico anterogrado
Resistenze vascolari
Compliance vascolare
VASCOLARIZZAZIONE Visco elasticità
SISTEMICA
Inerzia del sangue
Onde di pressione riflesse
C. Otto: “Aortic regurgitation “, Valvular Heart Desease 303 ; II ed
Saunders 2004
Metodologia clinica
I A cronica
compensata
Eziologia
I A cronica in
scompenso
Dissezione aortica
endocardite
Anomalia valvolare
e/o dell’aorta ascendente
Presentazione
clinica
Asintomatica
I A acuta
Graduale inizio dei
Sintomi, tipicamente
da sforzo
Inizio acuto,
Edema polmonare
Ipotensione, shock
Esame obiettivo
Alta frequenza
In decrescendo
olodiastolico
Alta frequenza
In decrescendo
olodiastolico
Pressione arteriosa
Aumento PA
Sist/diastolica
Aumento PA
Sist/diastolica
Itto apicale Vn. Sx.
Ingrandito
Iperdinamico
lateralizzato
Ingrandito
Iperdinamico
lateralizzato
Soffio diastolico
Rullio mesodiastolico
puntale (Austin-Flint)
Segni periferici
presente
presente
presenti
presenti
bassa frequenza
protodiastolico
normale
normale
Breve diastolico
Chiusura precoce mitrale
assenti
Presentazione clinica
Durata malattia ; età ; sesso.
Asintomatica
Sintomatica:
Dispnea da sforzo
Dispnea a riposo
Dispnea parossistica notturna
Edema polmonare
Angina da sforzo o notturna
Severa riduzione della riserva coronarica
Episodi di ischemia miocardica da stress
Progressivo deterioramento della funzione ventricolare sinistra
Metodo strumentale ecocardiografico
-Determinazione dell’eziologia
anomalie dei lembi
valvola aortica bicuspide
malattia valvolare calcifica
malattia valvolare reumatica
valvola aortica mixomatosa
endocardite valvolare
prolasso di cuspide
anomalie della radice aortica
dilatazione della radice aortica ipertensiva
medionecrosi cistica
sindrome di Marfan
dissezione aortica
-Valutazione del rigurgito aortico
-Effetti della lesione rigurgitante sulle dimensioni e funzione del ventricolo sinistro
Metodo ecocardiografico: parametri quantitativi di valutazione del rigurgito
Rapporto altezza jet di rigurgito / diametro tratto efflusso VS
Misura del PHT (tempo dimezzamento gradiente) (ms)
Valutazione del flusso retrogrado in aorta toracica
Misura dell’orifizio rigurgitante ( vena contratta ) ( cm )
Misura del flusso di convergenza al di sopra dell’orifizio (PISA)
Calcolo del volume di rigurgito (ml/battito)
Area orificio rigurgitante (cm2)
Frazione di rigurgito
Metodologia strumentale ecocardiografica : fisiopatologia
I A cronica
compensata
Volume VS
Aumentato
DTS < 55 mm
O < 25 mm/m2
O VTS 85 ml/m2
I A cronica in
scompenso
Aumentato
DTS > 55 mm
O >25 mm/m2
Normale
> 50%
Ridotta
< 50 %
Pressione
Telediastolica VS
Normale
Normale o
aumentata
Diametro
Telediastolico VS
> 70 mm
> 70 mm
FE
Dilatazione aorta
ascendente
> 45-50 mm
> 45-50 mm
I A acuta
normale
Normale o
ridotta
aumentata
Normale o
Poco aumentato
> 50 mm
Insufficienza aortica
Ventricolo sinistro:
dimensione telediastolica < 65 mm
A
frazione di eiezione > 55%
normale performance ventricolare sinistra
Ventricolo sinistro:
dimensione telesistolica > 50 mm
B
frazione di eiezione < 50 %
Disfunzione ventricolare sinistra
Indicazioni alla chirurgia nel paziente con insufficienza aortica
-Severa cronica IA senza aneurisma dell’aorta ascendente
sintomatologia funzionale
diametro telesistolico > 25 mm/m2
e/o diametro telediastolico > 70 mm
FE < 55% a riposo
severo rigurgito aortico cronico
-IA con dilatazione dell’aorta ascendente
diametro dll’aorta ascendente > 50-55 mm indipendentemente dalla severità
del rigurgito
-rischio operatorio
comorbilità
età del paziente
C. Tribouilloy et al. : Impact of echocardiography on indication for
Surgery in chronic mitral and aortic regurgitation.
Clinical cardiology 27; 442-448, 2004
Top, Survival of patients with
chronic severe AR by
symptoms (NYHA class).
Survival in asymptomatic
patients (class I) is no different
than expected (P0.38).
However, patients with class II
symptoms have a significantly
worse survival (P0.02), and
patients with class II to IV
symptoms have a markedly
worse survival (P0.001).
Bottom, Survival for patients
stratified by LV endsystolic
dimension (LVESD). Patients
with LV end-systolic dimension
25 mm/m2 have a markedly
worse survival (P0.001).
Adapted from Dujardin et al.23
Data from Chaliki et al72 show survival in patients after aortic valve replacement
as a function of preoperative LVEF. LoEF indicates markedly reduced LV
function; MedEF, moderately reduced LV function; and Nl EF, normal LV
function. Reprinted with permission.
Conclusioni
-Il metodo clinico strumentale è fondamentale per la comprensione del
processo fisiopatologico nei pazienti con insufficienza aortica.
-Le misure della performance ventricolare sinistra (dimensione e/o volume
telesistolico e frazione d’eiezione) sono eccellenti predittori del trattamento
medico (unloading treatment with vasodilatator) e specialmente
provvidenziali guide per il timing ottimale dell’intervento chirurgico di
sostituzione valvolare.