Facoltà di MEDICINA E CHIRURGIA
Cattedra di Anestesia e Rianimazione
FARMACI COADIUVANTI
PER L’ANALGESIA INTRATECALE
GARAVAGLIA MARCO M.
IL DOLORE
Meccanismo della trasduzione
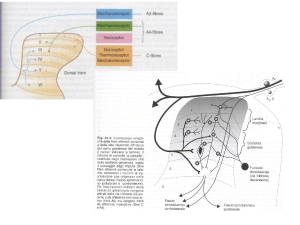
nocicettori periferici
Meccanismo della trasmissione
vie di trasmissione specifiche
+
centri preposti all’elaborazione degli
input algici a partenza periferica
Meccanismo della modulazione
vie discendenti responsabili di
meccanismi endogeni di modulazione e
controllo dell’informazione dolorosa a
vari livelli
Meccanismi neurochimici
(ex. PG, serotonina, sostanza P, …)
TRATTAMENTO DEL DOLORE
DOLORE ACUTO
(ex. postoperatorio)
Anestesia regionale
FANS
DOLORE CRONICO
(ex. neoplastico)
Schema OMS - 1997
Terapia farmacologica
Oppioidi
Stimolazione elettrica transcutanea
VIA INTRATECALE
1) FANS
2) Oppioidi deboli
3) Oppioidi forti
Adiuvanti
Tecniche di neurolesione
Tecniche di neuromodulazione
EPIDURALE
SUBARACNOIDEA
INTRATECALE VS. SISTEMICA
Dosi più basse (fino a 1/300 per la via subaracnoidea)
Minore rischio di effetti collaterali sistemici
Posologia precisa
Facili e rapidi aggiustamenti della dose
Potente analgesia (senza interferire con le funzioni
motorie)
Maggiore pain-relief
Applicazione continua e diretta nella regione del
midollo spinale (soprattutto per dolore cronico)
ANALGESIA BILANCIATA :
oppioidi + adiuvanti (OMS)
OBIETTIVO
QUANDO
Livello analgesico adeguato
mantenibile nel tempo,
minimizzando gli effetti collaterali
legati ai farmaci impiegati
Impossibilità di utilizzare gli oppioidi
effetti collaterali
importanti
rischio di
tolleranza
CARATTERISTICHE FARMACI COADIUVANTI
Proprietà
Intervenire sugli effetti collaterali degli
oppioidi e sui sintomi associati al dolore
Incrementare l’analgesia
ANALGESICI COADIUVANTI
1. Efficacia analgesica in vari modelli di dolore
2. Sicurezza valutazione per neurotossicità
3. Effetti collaterali tollerabili
4. Via loco-regionale migliore vs. sistemica
5. Altre proprietà d’uso vantaggiose per l’analgesia
Requisiti
analgesici
coadiuvanti
i.t.
COADIUVANTI I.T. DI IMPIEGO CORRENTE
NSAIDS
NEOSTIGMINA
CLONIDINA
(2-agonista centrale)
(Parasimpaticomimetico)
STUDI:
1. Animale
2. Uomo
ADENOSINA
(1- agonista)
KETAMINA
(Anestetico)
CALCITONINA
MIDAZOLAM
DROPERIDOLO
CALCITONINA
CHIMICA
Ormone polipeptidico di 32 aminoacidi
Inibizione riassorbimento osseo
su osteoclasti
PROPRIETA’ PRINCIPALI
Ipocalcemizzante
su osso, rene, intestino
USO CLINICO
(patologie con elevato
turn-over osseo)
Pazienti ipercalcemici con carcinoma
Osteoporosi post-menopausale
Iperparatiroidismo primario
Malattia ossea di Paget
QUALE RUOLO NELL’ANALGESIA I.T. ?
CALCITONINA E ANALGESIA I.T.
IPOTESI SUL
MECCANISMO
D’AZIONE
* I recettori oppioidi e il sistema
serotoninergico NON sono coinvolti
NEUROTOSSICITA’
NON sono state
riscontrate lesioni
istologiche di alcun tipo
* Coinvolgimento del sistema
catecolaminergico
* Alterazione del flusso di calcio
attraverso i neuroni
* Interferenza con il sistema PG
* Aumento della reattività di
sostanze - endorfino-simili
* Legame con recettori ad alta
specificità per il CGRP
CALCITONINA E ANALGESIA I.T.
DOLORE CRONICO
DA STUDI
NELL’UOMO
DOLORE ACUTO
CGRP
(calcitonin
gene-peptide
related)
100 UI in infusione epidurale in pazienti
neoplastici con metastasi ossee, quando:
* terapia con oppioidi inefficace
* necessità di ridurre gli oppioidi per
aumento degli effetti collaterali
NON vi sono ancora dati significativi
* E’ ampiamente distribuito
nel SNC e nel midollo spinale
* Interagisce con numerose
sostanze (ex. sostanza P)
* E’ coinvolto in un ampio numero
di processi neuro-metabolici
( neuromodulatore)
Possibile ruolo
nel controllo
del dolore
DROPERIDOLO
CHIMICA
Neurolettico della famiglia dei butirrofenoni
Antagonista della 5-idrossitriptamina
Antagonista recettore dopaminico
Agonista
1
+ debole agonista
PROPRIETA’ PRINCIPALI
2
Psicosi
Sedazione perioperatoria
USO CLINICO
Neuroleptoanestesia
Antiemetico
(nausea e vomito postoperatori)
QUALE RUOLO NELL’ANALGESIA I.T.?
DROPERIDOLO E ANALGESIA I.T.
DA STUDI
SU ANIMALI
DOLORE
CRONICO
DOLORE
ACUTO
DA STUDI
NELL’UOMO
IPOTESI SUL
MECCANISMO
D’AZIONE
* Proprietà -agonista
* Coinvolgimento sistema
dopaminergico cerebrale
NEUROTOSSICITA’
NON si riscontrano
lesioni istologiche
2.5 mg per via subarac. e 1.25-5 mg per via epid.
potenziano gli effetti degli oppioidi e riducono
la tolleranza indotta dagli stessi
Dati contrastanti anche se 2.5 mg per via epid.
sembrano potenziare l’analgesia
ALTRI
EFFETTI
UTILI
* Nel postoperatorio 2.5 mg per
via epid.riducono nausea-vomitoprurito causati da oppioidi
* Riduzione vomito da CMT
MIDAZOLAM
CHIMICA
Benzodiazepina idrosolubile a bassi valori di
pH, che diventa lipofila a pH fisiologico
passa barriera emato-encefalica
Potenzia l’attività del GABA
legandosi a siti specifici adiacenti
al recettore GABAA
PROPRIETA’ PRINCIPALI
Amnesico - sedativo - ipnotico
USO CLINICO
Premedicazione-induzionemantenimento anestesia generale
QUALE RUOLO NELL’ANALGESIA I.T.?
MIDAZOLAM E ANALGESIA I.T.
IPOTESI SUL
MECCANISMO
D’AZIONE
DA STUDI
SU ANIMALI
NEUROTOSSICITA’
DA STUDI
NELL’UOMO
1. Interferenza con neurotrasmissione
delle informazioni dolorifiche afferenti
2. Azione anestetica locale sui nervi
afferenti al midollo spinale
* Riscontro lesioni istologiche della barriera
emato-encefalica e del midollo spinale
* NON dati definitivi per possibili lesioni
catetere-indotte
Aggiunge effetti analgesici centrali, sedativi
e amnesici all’analgesia spinale sia nel dolore
cronico che postoperatorio
DOSI EPIDURALI: * 0.05 mg/Kg a bolo;
* 10-20 mg in infusione continua per 12 ore
CONCLUSIONI
L’ANALGESIA BILANCIATA rappresenta un giusto approccio
al trattamento del dolore
Far precedere una sostanziosa sperimentazione animale
all’impiego di nuovi farmaci coadiuvanti per via i.t. nell’uomo
Necessità di trial clinici randomizzati, controllati
La scelta del trattamento coadiuvante deve avvenire
sulla base della Evidence Based Medicine
Calcitonina, droperidolo e midazolam sono farmaci diversi tra
loro ma accomunati da un possibile impiego come coadiuvanti
Migliorare la QUALITA’ DELLA VITA
nel paziente con dolore