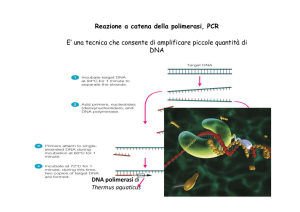
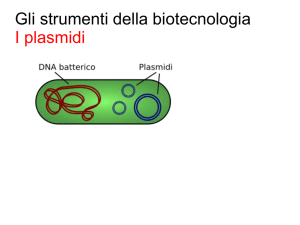
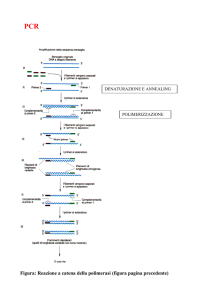
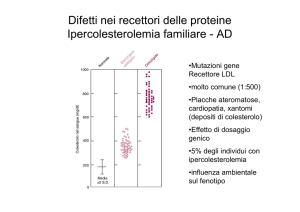
CONTROLLI DI QUALITA’
Controllo negativo 1: amplificazione di (H2O distillata) con i
reagenti della reazione
Controllo negativo 2 amplificazione del DNA di un soggetto sano
Controllo negativo 3 amplificazione del DNA di un gene endogeno
per valutare la qualità del campione
Controllo positivo amplificazione del DNA di un soggetto con
la mutazione
1
2
3
4
5
6
7
8
CN 1 CN2
CP
proteina p210
b3a2
b2a2
1
2 3 4 5 6 7 8 CP
Controllo di qualità 3
1
2
3
4
5
6
7
RT-PCR
Una variante della PCR è la RT-PCR
Consente di valutare l’espressione di determinati mRNA in una
cellula o in un tessuto
1. Estrazione di RNA totale
2. Retro-trascrizione in cDNA (RNA DNA)
3. Amplificazione con oligonucleotidi specifici
4. Analisi dei prodotti di amplificazione mediante elettroforesi
su gel di agarosio
Processo di retrotrascrizione
cDNA
PCR
Reazione di retrotrascrizione (RT)
Perchè effettuiamo la retrotrascrizione: i punti di rottura su alcuni geni
sono posizionati sugli esoni e quindi sono lontani.
L’RNA è abbastanza instabile e quindi convertirlo in CDNA lo rende più
stabile
PCR: vantaggi e svantaggi
1) Velocità e facilità d’uso
In poche ore si possono ottenere milioni di copie della sequenza di
DNA target
2) Sensibilità
Virtualmente è possibile utilizzare il DNA di una singola cellula
come template
3) Robustezza
Amplificazione possibile anche utilizzando DNA di bassa qualità
Necessario conoscere la sequenza del DNA da amplificare per
sintetizzare i primers
4) Non tutte le taq polimerasi hanno attività di proofreading
RT-PCR
Log[DNA]
La RT-PCR non è una tecnica quantitativa
Plateau
Lineare
Prodotto
variabile
Esponenziale
N°
cicli
Limiti della visualizzazione su gel
d’agarosio
Scarsa precisione
Bassa sensibilità
Bassa risoluzione
Discriminazione bande con size marker
Etidio bromuro non è quantitativo
Soluzioni
• Utilizzare i dati ottenuti durante la fase esponenziale
Il prodotto di PCR è proporzionale al template iniziale
• Questo è reso possibile mediante il rilevamento, di una
fluorescenza, che è proporzionale al prodotto di PCR
• La fluorescenza, durante ogni ciclo di amplificazione, può
essere rilevata utilizzando uno strumento quantitativo ma
anche dei marcatori fluorescenti il cui accumulo segue la stessa
c i n e t i c a d e l l a r e a z i o n e d i P C R
PERCHE’ QUANTIFICARE (1)
Molte applicazioni in medicina o in ricerca richiedono la
quantificazione del numero di copie target del
campione di partenza per es:
- determinazione della carica virale nel sangue per la
diagnosi di infezioni di HIV o HCV
- l’analisi dell’espressione genica dai livelli di mRNA
PERCHE’ QUANTIFICARE (2)
DNA:
•alterazioni quantitative, dei geni mutati
•genomi estranei (microorganismi, OGM)
•DNA fetale (nel sangue materno aumenta nei casi di sofferenza del feto)
•DNA tumorale (aumenta nei soggetti affetti da neoplasie)
mRNA:
•trascritti virali
•variazioni temporali
•variazioni individuali
La regolazione dell’espressione genica
varia in funzione del soggetto, patologia,
sesso ecc.
•variazioni patologiche
•trascritti anomali (fusione, splicing)
PCR Real Time
PCR Real Time permette contemporaneamente
- l’amplificazione
- il rilevamento dell’amplificato
La PCR Real Time misura l’amplificazione in tempo reale durante la
fase esponenziale della reazione
Durante ogni ciclo di amplificazione viene rilevata la fluorescenza del
campione proporzionale al prodotto di PCR
La fluorescenza si genera durante la PCR per effetto di reazioni chimiche
come il legame di molecole fluorescenti
Analisi del prodotto di PCR non su gel di agarosio ma mediante valutazione
della fluorescenza tramite software gestito da un computer
PCR Convenzionale vs. PCR Real-Time
Divergenza !!!
rilevazione
tradizionale
Rilevazione
Real-Time PCR
Principio base della Real-Time PCR
Si determina QUANDO viene generato il segnale piuttosto che l‘intensità
del segnale stesso (analisi all‘end –point)
rilevazione
tradizionale
Sample
Ct
threshold
Ct = threshold cycle: Il numero
di cicli al quale il prodotto di
PCR supera la soglia di
rilevabilità
Chimiche fluorescenti
per PCR Real-Time
•La fluorescenza si genera durante la PCR per e f f e t t o
di diverse possibili reazioni chimiche
•Le chimiche principali sono basate sia sul legame di
coloranti fluorescenti che si intercalano nella doppia
elica di DNA, come il SYBR Green, sia sull'ibridazione
d i
s o n d e
s p e c i f i c h e .
SYBR Green
SYBR Green: principio
Utilizza una molecola fluorescente non specifica che si lega al
solco minore del DNA
SYBR Green
All’inizio del processo di amplificazione, la miscela
di reazione contiene DNA denaturato, primers e la
molecola fluorescente
SYBR Green
Dopo l’annealing dei primers, si legano poche
molecole fluorescenti alla doppia elica.
SYBR Green
Durante l’elongazione si verifica un aumento di
fluorescenza che corrisponde all’ aumento del
numero di copie dell’amplicone
SYBR green
• Metodica semplice
• Non costosa
• Non-specifica
– La molecola fluorescente si lega in maniera aspecifica a
t u t t e
l e
d o p p i e
e l i c h e .
– È necessario ottimizzare la metodica per evitare la
formazione di prodotti aspecifici
TaqMan
TaqMan
La Real-Time PCR si può realizzare mediante l’impiego:
coloranti intercalanti ( es. SYBR green), che si legano
in
maniera
aspecifica
a
tutto
il
DNA
sonde ad ibridazione specifiche per il frammento di interesse,
m a r c a t e c o n m o l e c o l e f l u o r e s c e n t i
Esistono diversi tipi di sonde:
Dual-labeled (come le sonde TaqMan)
Molecular beacons
Scorpion
Sonde FRET (Fluorescence Resonance Energy Transfer)
Sonde TaqMan
La sonda di tipo TaqMan è un oligonucleotide che, come i
primers della PCR, viene disegnato per essere complementare
alla sequenza bersaglio da amplificare
R
3’
5’
5’
Primer
3’
5’
Q
3’
5’
Primer
3’
5’
La sonda è disegnata in modo da ibridarsi all’interno
del frammento amplificato nella reazione di PCR
3’
Reporter-Quencher
5’ REPORTER (R): fluorocromo ad alta energia che emette
fluorescenza
3’ QUENCHER (Q): fluorocromo a bassa energia che
spegne la fluorescenza del reporter
R
Q
5’
3’
Se R e Q si trovano vicini, Q spegne l'effetto di R perchè
i fotoni di R vengono assorbiti da Q
Real-Time PCR:
attività 5’>3’ esonucleasica
3’
5’
3’
R
Q
5’
R
3’
Q
5’
5’
R
3’
5’
Q
5’
Curve di amplificazione
Fluorescenza
Plot lineare
Cicli di amplificazione
Per ogni campione si ottiene una curva di amplificazione il cui
CT(=Threshold Cycle) è inversamente proporzionale alla quantità di
template iniziale
Real-Time PCR: applicazioni
•
•
•
•
•
•
•
•
•
Quantificazione virale
Quantificazione dell’espressione genica
Efficacia della terapia farmacologica
Misura dei danni al DNA
Controllo di qualità e validazione dei saggi
Detenzione dei patogeni
Controllo degli OGM
Genotyping
MRD
MRD (Minimal Residual Disease):
Quota residua di cellule neoplastiche non eradicate
dalla terapia farmacologica
Tali elementi neoplastici, presenti ad un
livello inferiore alla capacità di rilevazione delle
metodiche convenzionali, sono in grado di
espandersi e dare origine alla recidiva
TEST GENETICI: DEFINIZIONE
Insieme di analisi che vengono effettuate sul DNA,
RNA,cromosomi, proteine metaboliti che consentono
di evidenziare alterazioni dovute ad una patologia
genetica, ereditabile o meno.
Essi si distinguono in test clinici e di ricerca
TEST GENETICI: CLINICI
Forniscono al paziente ed alla famiglia una risposta
utile per l’inquadramento diagnostico, la prevenzione
o un trattamento terapeutico
I laboratori che effettuano test clinici devono seguire
delle procedure approvate e standardizzate
TEST GENETICI: CLINICI
•Test diagnostici: per confermare o escludere una malattia
genetica nota o sospetta in un individuo sintomatico
•Test predittivi: per individui asintomatici in una famiglia con una
storia di una patologia genetica. Tali test sono indicati nel caso in
cui si possa ridurre la morbidità o mortalità della malattia.
•Test di portatore:per identificare individui con una storia familiare
o anche a gruppi etnici con un elevato numero di portatori di uno
specifico allele patologico
•Test prenatali, effettuati in gravidanza per determinare lo stato di
salute del feto.Tali test si effettuano solo se si conoscono in
anticipo le mutazioni legate alla patologia nella famiglia
TEST GENETICI di ricerca
Tali test hanno invece lo scopo principale è la
migliore comprensione di un disordine genetico o lo
sviluppo di una nuova tecnologia diagnostica
TEST CLINICI
• DIRETTI: quando si conosce la mutazione
causativa della malattia
• INDIRETTI: si conosce solo la localizzazione del
locus (sito cromosomico) sul genoma umano
a. l’indagine diretta non
mutazione causativa
ha
identificato
la
I TEST DIRETTI si eseguono per
diagnosticare
• Malattie ereditarie: alterazioni qualitative o quantitative del
materiale genetico a livello delle cellule germinali
•
•
•
trasmissione alla prole
• Malattie acquisite: alterazioni qualitative o quantitative del
materiale genetico a livello delle cellule somatiche
non viene trasmessa alla prole
I TEST DIRETTI si eseguono per
diagnosticare
• Malattie ereditarie
• Malattie acquisite
FIBROSI CISTICA
TALASSEMIA
DISTROFIA DI DUCHENNE/BECKER
EMOFILIA
ATROFIA MUSCOLO-SPINALE
MALATTIE
EMOLINFOPROLIFERATIVE
MALATTIE INFETTIVE
Tumori
MALATTIE EREDITARIE
Sono autosomiche se trasmesse dai cromosomi
autosomici (dal cromosoma 1 al cromosoma 22)
Sono legate al cromosoma X (x linked) se trasmesse dal
cromosoma X
Mutazioni dominanti: condizioni in un individuo eterozigote, in
cui il l’allele mutato si esprime fenotipicamente.
Mutazioni recessive:condizioni in un individuo eterozigote
in cui l’allele mutato non si manifesta fenotipicamente.
I test INDIRETTI solo per diagnosticare
Malattie ereditarie
si conosce la localizzazione del locus (sito cromosomico) sul genoma umano
Analisi dei polimorfismi del DNA
• Polimorfismo genetico:variazione genetica nella
popolazione caratterizzata da sostituzioni, delezioni
o inserzioni di basi nel DNA
•Può riguardare regioni codificanti
•Quindi i polimorfismi rappresentano dei marcatori
che vengono trasmessi con la lesione genetica
Analisi mediante linkage disequilibrium
•Termine genetico con cui si indica la presenza di associazione statistica tra
alleli specifici che costituiscono un determinato aplotipo (combinazioni di
varianti alleliche)
•il linkage disequilibrium è maggiore in popolazioni omogenee, cioè originate
da un nucleo di individui fondatori come le popolazioni sarda o finlandese
•Individua regioni cromosomiche in cui si collocano i geni responsabili di una
data malattia
•Analisi molecolare delle varianti alleliche in pazienti apparentemente non
imparentati.
• I pazienti che hanno ereditato lo stesso segmento cromosomico, ereditano
anche la stessa mutazione in esso contenuto.
•Risale agli anni '80, il primo gene mappato con questo approccio:
quello della fibrosi cistica in 7q31.2.
Analisi molecolare di polimorfismi
• di sequenza (SNPs-single nucleotide polimorfism,
RFLP-restriction fragment lenght polymorphism)
• di lunghezza (VNTR Variable number
STR-single tandem repeats)
tandem repeats,
VALIDITA’ DEI TEST GENETICI
La maggior parte dei test genetici non è in grado di
identificare tutte le mutazioni patogenetiche
dipende da:
•eterogeneità genetica:quando mutazioni in loci genetici
diversi possono avere lo stesso effetto fenotipico
•eterogeneità allelica :quando mutazioni diverse sono a
carico dello stesso locus
TEST GENETICI
Validità diagnostica
+ al test
Affetti
VP
- al test
FN
Non affetti
FP
VN
Sensibilità del test = veri positivi/totale affetti = VP/(VP + FN)
Specificità del test = veri negativi/totale sani = VN/(VN +FP)
DISORDINI X-LINKED
• Sono circa 500 i
geni mappati sul
cromosoma X, il
70% di questi sono
associati a
malattia.
DISORDINI X-LINKED
• Gene sul cromosoma X
• I maschi, emizigoti per il cromosoma
X, sono più spesso affetti
• Nelle femmine, entrambe le copie
devono essere mutate
DISORDINI X-LINKED
• Distrofia muscolare di
Duchenne/Becker
• Emofilia A e B
DISTROFIA MUSCOLARE DI
DUCHENNE/BECKER (DMD/BMD)
• Miopatia ereditaria degenerativa, dovuta ad
un difetto del gene che sintetizza la
distrofina una proteina che si lega alla
membrana delle fibre muscolari e ne
preserva l’integrità.
• Incidenza: 1/3500 nati maschi
• 1/30000 per la forma Becker
DISTROFIA MUSCOLARE DI
DUCHENNE/BECKER (DMD/BMD)
• La malattia è trasmessa con carattere
recessivo X-linked
• I maschi che veicolano mutazioni nel gene
DMD sono affetti
• Le femmine portatrici sono sane
DUCHENNE o BECKER?
DMD - Duchenne
BMD - Becker
Muscular Dystrophy
Muscular Dystrophy
Forma grave. Assenza
totale o forte riduzione
della sintesi di
distrofina
Fenotipo più lieve.
Distrofina ridotta o
strutturalmente alterata
Caratteristiche cliniche
DMD
• Miopatia degenerativa progressiva
• Insorgenza nella forma grave tra i 2 e 5 anni
• Infiltrazione nel muscolo di tessuto connettivo e
adiposo
• Pseudoipertrofia muscolare
• Progressiva necrosi muscolare
• Complicanze polmonari e/o cardiache portano al
decesso
• Riduzione o assenza della distrofina
CARATTERISTICHE CLINICHE
Distrofia di Becker (BMD)
•
•
•
•
Forma allelica della DMD
Meno grave
Insorgenza tra 12 e 80 anni
Mutazioni del gene della distrofina che
conservano parzialmente la funzionalità della
proteina
DISTROFINA - IL GENE
• Localizzato sul braccio corto del
cromosoma X
• Lungo più di 3000 kb, pari a circa 1,5
% dell’intero cromosoma X
• Costituito da 79 esoni
La proteina
• distrofina
• espressa
soprattutto nel
muscolo
scheletrico e in
piccole quantità
nel cervello
Complesso delle glicoproteine
associate alla distrofina (DAG)
citoscheletro
Muscolo
Fascio di Fibra
muscolare
Proteina
Membrana
cellulare
I-band
Ruolo della distrofina
La distrofina funge da ponte tra l’apparato contrattile
intracellulare e la matrice extra-cellulare, sottoposta a
forte stress meccanico durante la contrazione muscolare.
In assenza di distrofina, anche tutte le proteine
dell’apparato contrattile diminuiscono; pertanto la
mancanza di distrofina produce un difetto al supporto
strutturale della membrana, rendendola più suscettibile a
rotture durante l’attività contrattile.
Nuovi studi sul ruolo della distrofina:oltre al ruolo
meccanico, regola l’attività di altri geni coinvolti nella
fibrosi e nello stress ossidativo
BASI GENETICHE
Circa il 65% delle mutazioni DMD e BMD sono grosse
delezioni del gene che portano alla totale assenza o a
ridottissime quantità di distrofina
delezioni con scivolamento di lettura del codice
DMD
delezioni con lettura corretta
BMD
Tipi di mutazione del gene
della distrofina
• Macrodelezioni
~ 65%
• Macroduplicazioni
~ 5-10%
• Mutazioni puntiformi,
micro-inserzioni e -delezioni
~ 25-30%
Diagnosi di BMD/ DMD
1. biochimica
creatina fosfochinasi sierica elevata (CPK)
2. istopatologica
biopsia muscolare -colorazione per la distrofina
3. Analisi del DNA
screening di delezioni comuni o mutazioni note in
famiglia
Indagine Biochimica
• Determinazione dei livelli sierici della componente muscolare
MM della CPK
valori di rifierimento (v.n. uomo 350 UI/l - donna 250 UI/l)
Maschi
% individui affetti
ConcentrazioneCPK
CK
Concentrazione
sierica
DMD
100%
100%
> 10volte
voltelalanorma
norma
>10
BMD
100%
100%
> 5volte
voltela
lanorma
norma
>5
Indagine Biochimica
• Determinazione dei livelli sierici della componente muscolare
MM della CPK
valori di rifierimento (v.n. uomo 350 UI/l - donna 250 UI/l)
Maschi
Femmine portatrici
% individui affetti
% individui affetti
DMD
DMD
100%
circa 50%
Concentrazione CK
Concentrazione
sierica CPK
sierica
> 10 volte la norma
2-10 volte la norma
BMD
BMD
100%
circa 30%
> 5 volte la norma
2-10 volte la norma
•Nelle fasi di attiva necrosi muscolare possono aumentare i livelli di LDH,
transaminasi e aldolasi
DIAGNOSI ISTOLOGICA
colorazione della
distrofina sul contorno
delle fibre muscolari di
soggetto sano
Distrofia di Becker:
ridotta colorazione
delle fibre
X
Tronca o normale (BMD)
Distrofia di Duchenne:
assenza di distrofina
X
Delezioni genomiche
(assenza di distrofina)
Tecniche Molecolari per la diagnosi della DMD
Western blot per l’espressione della distrofina da biopsia muscolare di pazienti
con BMD o DMD effettuato su biopsie muscolari di pazienti affetti
Analisi di espressione della proteina distrofina
File 1-2: distrofia di Becker
Fila 3: normale espressione di distrofina
File 4-5: distrofia di Duchenne
Western blot per distrofina da biopsia muscolare di pazienti con BMD o DMD
Cos’e’ un Western Blot?
• Una tecnica in cui le proteine sono separate
mediante elettroforesi su gel e successivamente
trasferite su un supporto (membrana o filtro).
•
Successivamente la specifica proteina di cui
stiamo andando a valutare l’espressione viene
identificata mediante la sua reazione con un
anticorpo specifico.
Fasi di un Western Blot
• Prima fase: elettroforesi su gel.
(Le proteine del campione vengono separate su
un gel in base alle loro dimensioni)
• Seconda fase: trasferimento su membrana.
(Le proteine nel gel sono poi trasferite su una
membrana di nitrocellulosa mediante un campo
elettrico)
• Terza fase: saturazione o “blocking”.
(La saturazione e’ usata per prevenire le
interazioni non specifiche tra l’anticorpo e la
membrana)
Fasi di un Western Blot
• Quarta fase: legame dell’anticorpo primario.
(L’anticorpo riconosce la proteina specifica
immobilizzata sulla membrana)
• Quinta fase: legame dell’anticorpo secondario.
(L’anticorpo secondario, coniugato a un enzima (AP o
HRP), riconosce specificamente l’anticorpo primario,
gia’ legato alla proteina sulla membrana)
• Sesta fase: rivelazione o “detection”.
(L’enzima coniugato all’anticorpo secondario scinde
un substrato che, in corrispondenza della proteina
specifica, sviluppa precipitato colorato o
chemioluminescente)
PRIMA FASE: denaturazione e CORSA ELETTROFORETICA
Western blot: seconda fase
Immobilizzazione e trasferimento
• Elettroblotting
– Apparato di trasferimento
– Il gel e’ messo tra strati di carta da filtro con la
membrana a diretto contatto col gel sul lato
verso l’elettrodo positivo
– Viene applicato un campo elettrico e le
proteine migrano fuori dal gel verso l’elettrodo
positivo e si legano alla membrana
– Fatto a 4°C per evitare surriscaldamento,
decomposizione del tampone e degradazione
delle proteine
Seconda fase
Immobilizzazione e trasferimento
membrana
Western blot: seconda fase
Immobilizzazione e trasferimento
Trasferimento dal
catodo (-) all’ anodo
(+)
1)
2)
3)
4)
5)
6)
Spugnette
3 fogli di carta da filtro
imbevuti di tampone di
trasferimento
Gel
Membrana
3 fogli di carta da filtro
imbevuti di tampone di
trasferimento
Spugnette
Apparato per il trasferimento “Semi-dry”
Western blot: terza fase
saturazione o “blocking”
• Per saturare i siti
idrofobici liberi sulla
membrana
• Per prevenire il legame
dell’anticorpo primario
alla membrana stessa
• Latte scremato o
Albumina di Siero Bovino
(BSA)
Western blot: quarta fase
incubazione con anticorpo primario
• L’anticorpo primario riconosce la proteina
di interesse e non lega le altre proteine
immobilizzate sulla membrana
Western blot: quarta fase
incubazione con anticorpo primario
Western blot: quinta fase
Incubazione con anticorpo secondario
Western blot: sesta fase
rivelazione o “detection”
• Fosfatasi alcalina (AP) o perossidasi del
rafano (HRP)
– Conversione di un substrato colorimetrico in
un precipitato colorato
• Substrati Chemioluminescenti
– Emettono luce se convertiti dall’enzima
– Possono essere visualizzati su lastre
radiografiche
• Marcatura radioattiva
Western blot
substrato
HRP
Anticorpo primario
Anticorpo secondario
HRP
luce
Rivelazione
Il substrato metabolizzato dalla perossidasi (HRP) emette luce
pg proteina
Analisi diretta:
Macro-delezioni del gene della distrofina
• Sono localizzate preferenzialmente in due zone del
gene: la deletion rich region prossimale (esoni 1-20) e
la deletion rich region distale (esoni 45-53);
• le mutazioni out of frame sono responsabili più
frequentemente del fenotipo Duchenne
• le mutazioni in frame sono responsabili più
frequentemente del fenotipo Becker
Esoni del gene DMD
1 2 3 4 5 6 8
12 13
17
19
Deletion rich prossimale
41…………………… … 53
Deletion rich distale
Genetica Molecolare
•Analisi del DNA su leucociti del sangue
•Linee guida del gruppo collaborativo europeo per la diagnosi
Molecolare della Distrofia DMB/DMD
•MPLA (multiple ligation probe amplification), analizza tutti
gli esoni del gene della distrofina in contemporanea
(delezioni e duplicazioni)
•Questo approccio consente di evidenziare circa il 98% delle
delezioni del gene della distrofina
MPLA
Poiche solo le sonde legate vengono amplificate in maniera esponenziale durante la reazione di PCR,
il numero di prodotti di PCR legati rappresenta una misura diretta delle sequenze target nel campione
esaminato
ELETTROFORESI CAPILLARE
•Migrazione dei campioni all’interno di un capillare di silice collegato a
due elettrodi
•Strumenti automatizzati per l’analisi di frammenti e l’analisi di
sequenze
•Utilizzo per l’amplificazione di un primer fluorescente
Vantaggi
Velocità di corsa
Analisi di ridotte
quantità di campione
Alto potere risolutivo
Principio
Diagnosi DMD mediante Elettroforesi
capillare
Tipi di mutazione del gene
della distrofina
• Macrodelezioni
~ 65%
• Macroduplicazioni
~ 5-10%
• Mutazioni puntiformi,
micro-inserzioni e -delezioni
~ 25-30%
DHPLC
Denaturing
High
Performance
Liquid
Chromatography
E’ una tecnica relativamente recente che sfrutta i principi
della cromatografia liquida ad alta risoluzione (HPLC)
per la separazione e l’analisi degli acidi nucleici.
Principio del metodo:
Fase stazionaria: copolimero non polare idrofobico (polistirenedivinilbenzene)
Fase mobile:
1) Tri-Etil Ammonio Acetato (TEAA), molecola anfipatica, che fungendo
da ponte (accoppiante ionico), permette alle molecole di DNA
(cariche negativamente) di interagire con la matrice
2) Acetonitrile (ACN), solvente organico
3) Acqua
Opportune condizioni di gradiente di
fase mobile, a concentrazione crescente
di
solvente organico (ACN), permettono
prima l’adsorbimento e poi l’eluizione
dei frammenti di acido nucleico
in funzione della lunghezza
(condizioni non denaturanti) e/o
in funzione della sequenza (condizioni
parzialmente denaturanti).
Caratteristiche
• La separazione dei frammenti di DNA in base alla diversa
dimensione e alla diversa conformazione è permessa dal
diverso adsorbimento e ripartizione tra la fase
stazionaria (matrice) e la fase mobile (buffer).
• Procedura
rapida
completamente
automatizzata,
strumentazione costosa ma con bassi costi di analisi,
• Non è possibile localizzare e identificare precisamente la
mutazione, utile per screening su grandi popolazioni.
Applicazioni del DHPLC
Permette di separare ssDNA e dsDNA operando in tre diverse condizioni a
seconda delle finalità desiderate:
- non denaturanti, ~ 50°C (sizing dsDNA, STR)
- parzialmente denaturanti, > 50°C (mutation detection, SNP)
- totalmente denaturanti, > 75°C (sintesi e purificazione di oligo)
• Condizioni non denaturanti
• Analisi di frammenti dsDNA
• Il tempo di ritenzione è direttamente proporzionale alla lunghezza dei frammenti
12.82
13.02
13.53
5
16.10
15.06
15.30
pUC18HAEIII
4
10.67
3
7.22
2
5.52
Absorbance (mV)
SIZING
1
0
2
4
6
8
10
12
Time (Minutes)
14
16
18
20
B
A
bp
587
458
434
298
257+267
174
102
80
Analisi di mutazione
e’ un metodo temperatura dipendente
basato sulla separazione cromatografica di molecole di DNA ds contenenti basi
non appaiate (eteroduplex)
Applicazione del DHPLC nella DMD
Esempio di femmina con
mutazione
puntiforme ex 59
Esempio di femmina
eterozigote
con delezione ex 67
Limiti del DHPLC
La metodica del DHPLC non consente l’identificazione
della posizione della mutazione e tantomeno la sua
tipologia, quindi per i campioni che mostrano profili di
eluizione alterati rispetto ai wild-type è previsto
sempre il successivo sequenziamento diretto.
Trattamento e terapie
• Attualmente non esistono terapie.
• Tutti i trattamenti mirano al controllo dei sintomi
e a migliorare la qualità della vita
TERAPIA GENICA PER DMD: cosa si è fatto
e cosa si sta facendo
•
•
•
•
Terapia genica mediante l’utilizzo di un vettore che trasporta una minidistrofina (solo una parte della sequenza codificante).
Il ruolo del vettore virale è quello di veicolare porzioni geniche per
ripristinare il corretto schema di lettura nel DNA delle cellule muscolari
del paziente e stimolare la produzione di nuova distrofina.
Difficoltà delle’approccio: il gene responsabile, quello della distrofina,
è molto grosso e quindi difficile da “impacchettare” nei vettori virali
attualmente disponibili per il trasferimento nelle cellule dei malati
Altra strategia coreggere il difetto genico a livello dell’RNA
rispristinando la produzione di una distrofina più corta ma funzionale.
Identificazione, come conseguenza del danno muscolare di microRNA,
che rilasciati in circolo inibiscono l’espressione genica.
L’analisi di questi piccoli RNA potrebbe essere adoperata come un
marker biologico per diagnosticare la malattia e misurare l’efficacia dei
trattamenti terapeutici.