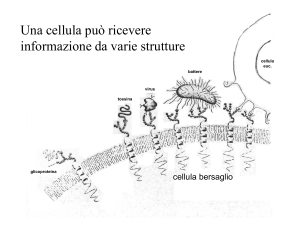
Recettori delle neurotrofine e
Traffico Vescicolare nei
Neuroni
Neurotrofine
Le neurotrofine costituiscono una famiglia di proteine essenziali per
lo sviluppo, la sopravvivenza e la funzionalità dei neuroni.
Esse comprendono:
- Nerve Growth Factor (NGF)
- Brain-Derived Growth Factor (BDNF)
- Neurotrofina-3 (NT-3)
- Neurotrofina-4/5 (NT-4/5)
Le neurotrofine sono prodotte sia da neuroni che da altri tipi cellulari
(ad esempio le cellule gliali).
Sono sintetizzate nel reticolo endoplasmatico come pro-neurotrofine
(240-260 aa), processate da proteasi a polipeptidi di 118-129 aa e
quindi secrete nel mezzo extracellulare come omodimeri.
In alcuni casi tuttavia le pro-neurofine possono essere secrete come
tali e processate a neurotrofine nel mezzo extracellulare
Le neurotrofine riconoscono ed attivano due classi di recettori
transmembrana:
i) i recettori TRK (Tropomyosin Receptor Kinase)
ii) il recettore p75 (p75NTR) (Neurotrphin Receptor)
L’acronimo TRK sta per Tropomyosin Receptor Kinase.
Ciò perché, nel 1986, fu isolato per la prima volta un oncogene
umano formato dalla fusione di una sequenza tronca tropomiosinica
associata ad una sequenza tirosin chinasica riscontrata in seguito nei
recettori per i fattori di crescita.
I recettori delle neurotrofine: TRK e p75
Le diverse neurotrofine si legano specificamente ai propri recettori TRK,
mentre tutte si legano a al recettore p75.
I recettori TRK contengono un dominio extracellulare IgG (immunoglobulin Glike), che interagisce con il ligando, ed un sito catalitico intracellulare tirosinchinasico. I recettori attivano varie vie dei trasduzione del segnale.
Il recettore p75 non ha attività tirosin chinasica ed appartiene alla famiglia di
recettori per il Tumor Necrosis Factor (TNF). La porzione extracellulare di p75
contiene quattro domini ricchi in cisteina (cysteine-rich repeats), mentre
quella intracellulare contiene un ‘death domain’.
Il legame delle neurotrofine a p75 può innescare varie risposte nello specifico
contesto di attivazione (in particolare sopravvivenza o morte cellulare).
Inoltre, l’interazione di p75 con TRK aumenta l’affinità dei ligandi per TRK.
Vie di trasduzione del segnale attivate dai recettori
TRK
L’attivazione di Ras e delle MAPKs è necessaria per il differenziamento
neuronale. Una volta attivate le MAPK traslocano nel nucleo, dove
fosforilano CREB (cAMP Responsive Element Binding- protein) , un fattore
di trascrizione necessario per l’espressione di proteine coinvolte nel
differenziamento stesso.
La PI3K è necessaria per l’attivazione di Akt. L’attivazione di Akt è
necessaria sia per il differenziamento che per la sopravvivenza dei neuroni.
L’attivazione della PLC-g induce l’idrolisi del PIP2, con produzione di DAG
(che attiva la PKC) ed IP3 (che mobilizza il Ca2+ ed attiva la CaMKII). Questa
via sembra essere importante per per impedire la degenerazione e favorire
la rigenerazione assonale.
Pro-neutrofine, sortilina e morte cellulare
Mentre i complessi recettoriali TRK/p75 assicurano la
sopravvivenza dei neuroni, l’associazione di p75 con la proteina
sortilina induce morte cellulare in seguito al legame di proneurotrofine.
La sortilina è sintetizzata come precursore che include un propeptide di 44 aa. Quest’ultimo agisce come chaperone intrinseco
per il corretto folding e trasporto della proteina e previene la sua
interazione prematura con i ligandi.
La rimozione del pro-peptide, per azione di una pro-proteina
convertasi, avviene lungo la via secretoria nel ’trans-Golgi
network’ ed è essenziale per la maturazione funzionale della
proteina.
Un frammento del propetide liberato, denominato spadina, viene
secreto e agisce come fattore di controllo dei canali del K+.
Meccanismi apoptotici dei
complessi p75/ sortilina/ proNT
Le pro-neurotrofine (proNTs) possono segnalare per la morte
cellulare attraverso il complesso sortilina/p75NTR mediante il
reclutamento della proteina adattatrice NRAGE (Neurotrophin
Receptor-interacting MAGE homolog) a livello di p75.
Il reclutamento di NRAGE induce l’attivazione di JNK (c-Jun NH2terminal kinase) che regola positivamente l’attività delle caspasi
(Casp) 3, 6 and 9, o il rilascio del tumor necrosis factor (TNFa).
Inoltre, NRAGE attivata la protein fosfatasi PTEN, che defosforila il
PIP3 a PIP2. In questo modo, è soppressa l’attivazione di Akt, che è
un importante fattore di spravvivenza.
Traffico dei TrkA e teoria dell’endosome signalling
NGF
Recycling endosomes
NGF-TrkA signalling endosomes
I complessi recettore-neurotrofina possono essere internalizzati
per endocitosi e trasportati per via vescicolare in comparti
endosomali.
L’internalizzazione è stata per lungo tempo considerata un
meccanismo di termine della segnalazione, supponendo che
questa avvenisse soltanto a livello della membrana plasmatica e
che il pathway endocitico fosse necessario solo per indirizzare i
complessi nei late endosomes e nei lisosomi per la degradazione.
Tuttavia è oggi chiaro che, una volta internalizzati, i complessi
lingando- recettore possono anche operare attivamente la
trasduzione del segnale (teoria dell’endosome signalling).
In altre parole i recettori vengono internalizzati non solo con il
ligando ma anche con proteine coninvolte nella segnalazione (e.g.
PLC-g, MAP chinasi e PI3K).
Internalizzazione dei complessi neurotrofina TRK
I complessi neurotrofina recettore TRK sono
generalmente internalizzati
attraverso un processo
clatrina/dinaminadipendente.
Tuttavia, in alcuni casi,
l’internalizzazione può
avvenire per via caveolare
(clatrina-indipendente).
Proteine
motrici
Formazione delle ‘coated vesicles’
Cytosol
Il processo di vescicolazione richiede l’intervento di varie proteine:
le adaptine (recettori per le proteine-cargo), le coat proteins (COPI,
COPII e clatrina, nei diversi comparti della cellula) e la dinamina.
Le coat proteins inducono una curvatura della membrana, come
risultato della loro reciproca interazione geometrica, che si
accentua progressivamente ed è essenziale per il budding
vescicolare.
Le adaptine interagiscono non solo con le molecole-cargo, ma
anche con le coat proteins.
Nella fase finale della vescicolazione la dinamina constringe il
collo della vescicola, che gemma e viene rilasciata mediante un
processo che richiede l’apporto di ATP.
Dopo la vescicolazione il rivestimento adaptina / coat protein viene
disassemblato ( uncoating vescicolare).
Le small GTPasi Arf e Rab controllano rispettivamente
il budding delle coated-vesicles e la loro fusione con il
comparto accettore
L’assemblaggio ed il budding delle coated vesicles è sotto
il controllo delle small G proteins Sar e Arf (Sar è un
membro della superfamiglia Arf)
Le vescicole rivestite da COP I e clatrina interagiscono con
Arf, mentre le vescicole COP II interagiscono con Sar.
Dopo il rilascio dei coatomeri, il traffico vescicolare ed il
docking alle membrane bersaglio è operato dalle small G
proteins della famiglia Rab.
Complessi di migrazione vescicolare
Sulla superficie vescicolare sono presenti complessi di proteine
adattatrici che possono reclutare proteine motrici (kinesine, dineine
e miosine), attivandole e promuovendo il traffico intracellulare
mediante l’energia prodotta dall’idrolisi di ATP.
Le kinesine e le dineine si muovono lungo i microtubuli.
I microtubuli originano dal ‘microtubule organizing center‘ (MTOC),
in prossimità del nucleo [minus (-) end], e si diramano distalmente
verso la periferia [plus (+) end].
Le kinesine e le dineine si muovono in direzioni opposte: dal (-) al
(+) end e viceversa, rispettivamente.
Le miosine si muovono invece multi-direzionalmente lungo i
filamenti di actina.
Proteine motrici
Le tre classi di protein motrici (Kinesine, Dineine e
Miosine) condividono varie caratterische.
Il dominio motore usa l’energia derivante dall’idrolisi
dell’ATP per innescare cambiamenti di conformazione
che generano I passi (steps) lungo il track.
Kinesine e dineine si muovono lungo I microtubuli,
mentre le miosine lungo i filamenti di actina.
L’ampiezza del passo è di circa 8 nm per le kinesine e le
dineine e variabile per le diverse isoforme di miosina (da
pochi a 36 nm).
Il trasporto assonale consente al terminale assonale di inviare
segnali al comparto somato-dendritico e viceversa.
Le proteine sintetizzate nel soma richiedono un efficiente sistema
di trasporto verso l’assone ed i dendriti. Inoltre, alcuni mRNA
debbono essere trasportati all’assone o ai dendriti per essere
tradotti localmente. (Trasporto anterogrado)
Viceversa, proteine provenienti dall’estremità dell’assone
debbono raggiungere il nucleo od il citoplasma perinucleare per
innescare delle risposte cellulari (Trasporto retrogrado).
I due tipi di trasporto avvengono generalmente per traffico
vescicolare.
Meccanismo di fusione vescicolare nel
comparto endosomale : Vesicle docking
(synaptobrevin)
Le proteine SNARE (un acronimo per "SNAP (Soluble
NSF Attachment Protein) REceptor") costituiscono una
superfamiglia con più di 60 membri.
Le funzioni primarie dell proteine SNARE sono quelle di mediare la
fusione vescicolare.
Il riconoscimento e l’interazione delle vescicole con la membrana
accettrice (docking) è regolato dalle protein Rab, che riconoscono
specifiche protein effettrici sulla membrane bersaglio.
Lo stretto avvicinamento delle due membrane non solo le porta in
posizione di fusione ma favorisce anche l’ interazione di proteine
necessarie per la fusione: VAMP sulla vescicola e SNAP-25 e
sintaxina sulla membrane accettrice.
Meccanismo di fusione vescicolare nel
comparto endosomale
VAMP
(synaptobrevin)
L’interazione tra VAMP (sulla vescicola) con la syntaxina e SNAP25 (sulla membrana accettrice), promuove il super-avvolgimento
reciproco delle suddette proteine (SNARE complex), che portano
ad un ulteriore avvicinamento delle membrane e quindi alla loro
fusione, attraverso un processo guidato probabilmente da RabGTP.
Dopo la fusione il GTP viene idrolizzato e Rab torna nella forma
inattiva (Rab-GDP).
Riorganizzazione della componente lipidica nel
processo di fusione delle membrane
Diaframma di
emifusione
A) Stretta interazione dei piani delle due membrane.
B) I foglietti esterni (sfere rosse) dei due doppi strati lipidici si
fondono, generando una condizione iniziale di emifusione.
C) Il processo si espande, generando un diaframma di emifusione
dovuto alla giustapposizione dei foglietti interni (sfere arancioni).
(D) Il diaframma di emifusione si rompe ed i foglietti interni (sfere
arancioni) consentono ora la continuità dell’ambiente accquoso
nella struttura.
(E) La fusione procede generando due doppi strato lipidici continui,
appartenenti alla stessa struttura.
Innesco Ca2+/mediato dell’apertura del poro di fusione
La vescicola in arrivo al terminale sinaptico è associata con la sinaptobrevina/
VAMP e la sinaptotagmina, che presenta siti di legame per il Ca2+.
Sul versante citosolico della membrana plasmatica sono presenti le proteine
SNAP-25 e sintaxina.
Prima dell’assemblaggio del complesso di fusione la sintaxina è presente
sulla membrana plasmatica in una conformazione inattiva, che previene
l’interazione con altre proteine. Ad essa è associata la proteina Munc18 che
stabilizza questo stato.
Nella fase di prefusione Munc 18 subisce uno spostamento che consente
l’avvolgimento reciproco della sinaptobrevina/VAMP, SNAP-25 e sintaxina
(Fase priming I). A questa struttura si lega la complessina (Fase priming II).
Il Ca2+ innesca l’apertura del poro di fusione legandosi alla sinaptotagmina ed
inducendo il suo super-avvolgimento con le altre proteine SNAREs.
L’ampiezza del poro di apertura è poi accentuata dall’interazione con le
proteine NSF e SNAP.