Esposito Ferraio Chiara 41
PREMESSA
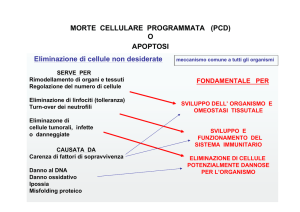
Proliferazione e morte cellulare sono due fenomeni fortemente correlati,dal cui equilibrio dipende un principio base per la sopravvivenza degli organismi
multicellulari:l’omeostasi cellulare.
L’importanza di questo equilibrio è chiaramente riscontrabile analizzando soggetti in cui è presente una predominanza,anche se piccola,dei due fenomeni.
Un’accentuata apoptosi,infatti,comporta distruzione non fisiologica di cellule,causando gravi patologie,come quelle neurodegenerative,mentre un’inibizione eccessiva
rende le cellule“immortali”,cancerose,capaci di proliferazioni incontrollate.
Ai fini dell’omeostasi quindi non conta solo la frequenza di divisioni cellulari ma anche la frequenza di morte.
Ma qual è il vero significato dell’apoptosi e quali i meccanismi di base che lo regolano?
DISCUSSIONE
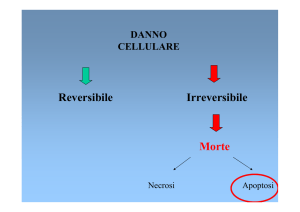
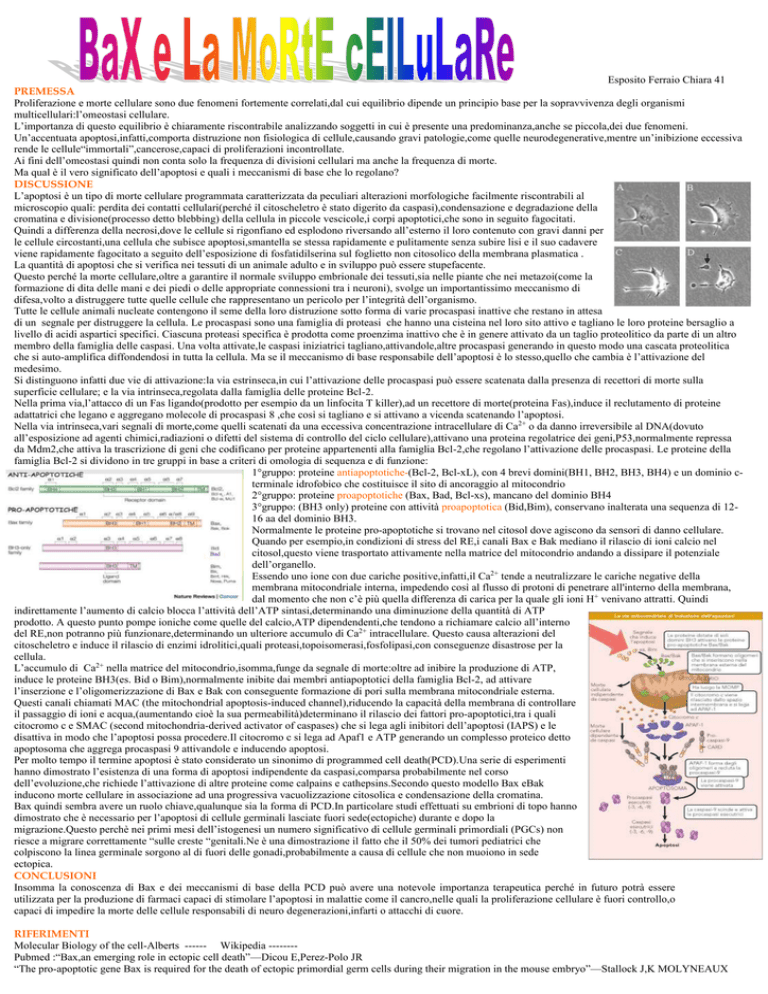
L’apoptosi è un tipo di morte cellulare programmata caratterizzata da peculiari alterazioni morfologiche facilmente riscontrabili al
microscopio quali: perdita dei contatti cellulari(perché il citoscheletro è stato digerito da caspasi),condensazione e degradazione della
cromatina e divisione(processo detto blebbing) della cellula in piccole vescicole,i corpi apoptotici,che sono in seguito fagocitati.
Quindi a differenza della necrosi,dove le cellule si rigonfiano ed esplodono riversando all’esterno il loro contenuto con gravi danni per
le cellule circostanti,una cellula che subisce apoptosi,smantella se stessa rapidamente e pulitamente senza subire lisi e il suo cadavere
viene rapidamente fagocitato a seguito dell’esposizione di fosfatidilserina sul foglietto non citosolico della membrana plasmatica .
La quantità di apoptosi che si verifica nei tessuti di un animale adulto e in sviluppo può essere stupefacente.
Questo perché la morte cellulare,oltre a garantire il normale sviluppo embrionale dei tessuti,sia nelle piante che nei metazoi(come la
formazione di dita delle mani e dei piedi o delle appropriate connessioni tra i neuroni), svolge un importantissimo meccanismo di
difesa,volto a distruggere tutte quelle cellule che rappresentano un pericolo per l’integrità dell’organismo.
Tutte le cellule animali nucleate contengono il seme della loro distruzione sotto forma di varie procaspasi inattive che restano in attesa
di un segnale per distruggere la cellula. Le procaspasi sono una famiglia di proteasi che hanno una cisteina nel loro sito attivo e tagliano le loro proteine bersaglio a
livello di acidi aspartici specifici. Ciascuna proteasi specifica è prodotta come proenzima inattivo che è in genere attivato da un taglio proteolitico da parte di un altro
membro della famiglia delle caspasi. Una volta attivate,le caspasi iniziatrici tagliano,attivandole,altre procaspasi generando in questo modo una cascata proteolitica
che si auto-amplifica diffondendosi in tutta la cellula. Ma se il meccanismo di base responsabile dell’apoptosi è lo stesso,quello che cambia è l’attivazione del
medesimo.
Si distinguono infatti due vie di attivazione:la via estrinseca,in cui l’attivazione delle procaspasi può essere scatenata dalla presenza di recettori di morte sulla
superficie cellulare; e la via intrinseca,regolata dalla famiglia delle proteine Bcl-2.
Nella prima via,l’attacco di un Fas ligando(prodotto per esempio da un linfocita T killer),ad un recettore di morte(proteina Fas),induce il reclutamento di proteine
adattatrici che legano e aggregano molecole di procaspasi 8 ,che così si tagliano e si attivano a vicenda scatenando l’apoptosi.
Nella via intrinseca,vari segnali di morte,come quelli scatenati da una eccessiva concentrazione intracellulare di Ca2+ o da danno irreversibile al DNA(dovuto
all’esposizione ad agenti chimici,radiazioni o difetti del sistema di controllo del ciclo cellulare),attivano una proteina regolatrice dei geni,P53,normalmente repressa
da Mdm2,che attiva la trascrizione di geni che codificano per proteine appartenenti alla famiglia Bcl-2,che regolano l’attivazione delle procaspasi. Le proteine della
famiglia Bcl-2 si dividono in tre gruppi in base a criteri di omologia di sequenza e di funzione:
1°gruppo: proteine antiapoptotiche-(Bcl-2, Bcl-xL), con 4 brevi domini(BH1, BH2, BH3, BH4) e un dominio cterminale idrofobico che costituisce il sito di ancoraggio al mitocondrio
2°gruppo: proteine proapoptotiche (Bax, Bad, Bcl-xs), mancano del dominio BH4
3°gruppo: (BH3 only) proteine con attività proapoptotica (Bid,Bim), conservano inalterata una sequenza di 1216 aa del dominio BH3.
Normalmente le proteine pro-apoptotiche si trovano nel citosol dove agiscono da sensori di danno cellulare.
Quando per esempio,in condizioni di stress del RE,i canali Bax e Bak mediano il rilascio di ioni calcio nel
citosol,questo viene trasportato attivamente nella matrice del mitocondrio andando a dissipare il potenziale
dell’organello.
Essendo uno ione con due cariche positive,infatti,il Ca2+ tende a neutralizzare le cariche negative della
membrana mitocondriale interna, impedendo così al flusso di protoni di penetrare all'interno della membrana,
dal momento che non c’è più quella differenza di carica per la quale gli ioni H+ venivano attratti. Quindi
indirettamente l’aumento di calcio blocca l’attività dell’ATP sintasi,determinando una diminuzione della quantità di ATP
prodotto. A questo punto pompe ioniche come quelle del calcio,ATP dipendendenti,che tendono a richiamare calcio all’interno
del RE,non potranno più funzionare,determinando un ulteriore accumulo di Ca2+ intracellulare. Questo causa alterazioni del
citoscheletro e induce il rilascio di enzimi idrolitici,quali proteasi,topoisomerasi,fosfolipasi,con conseguenze disastrose per la
cellula.
L’accumulo di Ca2+ nella matrice del mitocondrio,isomma,funge da segnale di morte:oltre ad inibire la produzione di ATP,
induce le proteine BH3(es. Bid o Bim),normalmente inibite dai membri antiapoptotici della famiglia Bcl-2, ad attivare
l’inserzione e l’oligomerizzazione di Bax e Bak con conseguente formazione di pori sulla membrana mitocondriale esterna.
Questi canali chiamati MAC (the mitochondrial apoptosis-induced channel),riducendo la capacità della membrana di controllare
il passaggio di ioni e acqua,(aumentando cioè la sua permeabilità)determinano il rilascio dei fattori pro-apoptotici,tra i quali
citocromo c e SMAC (second mitochondria-derived activator of caspases) che si lega agli inibitori dell’apoptosi (IAPS) e le
disattiva in modo che l’apoptosi possa procedere.Il citocromo c si lega ad Apaf1 e ATP generando un complesso proteico detto
apoptosoma che aggrega procaspasi 9 attivandole e inducendo apoptosi.
Per molto tempo il termine apoptosi è stato considerato un sinonimo di programmed cell death(PCD).Una serie di esperimenti
hanno dimostrato l’esistenza di una forma di apoptosi indipendente da caspasi,comparsa probabilmente nel corso
dell’evoluzione,che richiede l’attivazione di altre proteine come calpains e cathepsins.Secondo questo modello Bax eBak
inducono morte cellulare in associazione ad una progressiva vacuolizzazione citosolica e condensazione della cromatina.
Bax quindi sembra avere un ruolo chiave,qualunque sia la forma di PCD.In particolare studi effettuati su embrioni di topo hanno
dimostrato che è necessario per l’apoptosi di cellule germinali lasciate fuori sede(ectopiche) durante e dopo la
migrazione.Questo perchè nei primi mesi dell’istogenesi un numero significativo di cellule germinali primordiali (PGCs) non
riesce a migrare correttamente “sulle creste “genitali.Ne è una dimostrazione il fatto che il 50% dei tumori pediatrici che
colpiscono la linea germinale sorgono al di fuori delle gonadi,probabilmente a causa di cellule che non muoiono in sede
ectopica.
CONCLUSIONI
Insomma la conoscenza di Bax e dei meccanismi di base della PCD può avere una notevole importanza terapeutica perché in futuro potrà essere
utilizzata per la produzione di farmaci capaci di stimolare l’apoptosi in malattie come il cancro,nelle quali la proliferazione cellulare è fuori controllo,o
capaci di impedire la morte delle cellule responsabili di neuro degenerazioni,infarti o attacchi di cuore.
RIFERIMENTI
Molecular Biology of the cell-Alberts ------ Wikipedia -------Pubmed :“Bax,an emerging role in ectopic cell death”—Dicou E,Perez-Polo JR
“The pro-apoptotic gene Bax is required for the death of ectopic primordial germ cells during their migration in the mouse embryo”—Stallock J,K MOLYNEAUX