scaricato da www.sunhope.it
scaricato da www.sunhope.it
ACIL CoA DEIDROGENASI
scaricato da www.sunhope.it
La membrana mitocondriale non
è permeabile al NADH citosolico.
Speciali sistemi navetta (shuttle)
trasportano gli equivalenti
riducenti dal NADH citosolico
all’interno dei mitocondri
scaricato da www.sunhope.it
I principali sistemi navetta sono:
Shuttle glicerolo fosfato
(muscoli, tessuto nervoso)
Shuttle malato-aspartato
(fegato, reni cuore)
scaricato da www.sunhope.it
scaricato da www.sunhope.it
scaricato da www.sunhope.it
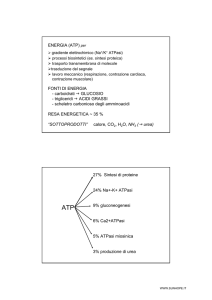
RESA IN ATP PER MOLECOLA DI Glc OSSIDATA
Glicolisi
Glc
Glc-6P
Frut-6P
Frut1,6P
2 NADH (shuttle)
Fosforilazione
a livello del substrato
Dec ossidativa piruvato
2 NADH
Ciclo di Krebs
6NADH
2FAH2
2GTP
-1 ATP
-1 ATP
+ 3-5 ATP
+ 2 ATP
+ 5 ATP
+ 15 ATP
+ 3 ATP
+ 2 ATP
30 o 32 ATP
scaricato da www.sunhope.it
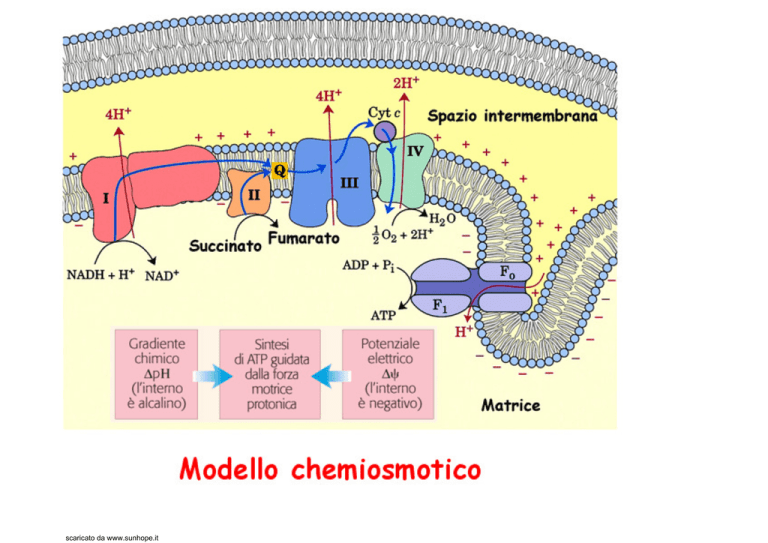
Il flusso degli e- è accompagnato da una
traslocazione di H+ che produce un gradiente
∆pH) e un gradiente elettrico (∆ψ
∆ψ).
chimico (∆
∆ψ
Si crea così un gradiente elettrochimico che genera
la forza motrice protonica che fornisce l'energia
per la sintesi di ATP quando gli H+ ritornano nella
o
matrice attraverso una canale protonico, F ,
1
associato con il complesso F dell’ATP sintasi
scaricato da www.sunhope.it
Mitocondrio di Neurospora in un
campione congelato in assenza di
fissativi o coloranti che possano
alterare le caratteristiche delle
strutture interne.
Wadsworth Center.
Creste tubulari si connettono
alla membrana interna
attraverso passaggi stretti che
possono limitare la velocità di
equilibrio di H+
fra il lume delle creste e lo spazio intermembrana. Ci sono
evidenze che i protoni estratti dalla matrice si disperdono lungo
la superficie anionica delle membrane e solo lentamente si
equilibrano con il grosso della fase circostante, massimizzando il
reale gradiente di H+.
scaricato da www.sunhope.it
scaricato da www.sunhope.it
scaricato da www.sunhope.it
Il dinitrofenolo (DNF) è un disaccoppiante della FO
Il DNF possiede un protone dissociabile ed è molto idrofobico:
agisce trasportando H+ attraverso la membr. mitoc. int. e
dissipando il gradiente protonico
scaricato da www.sunhope.it
I mitocondri manipolati
in modo da generare
una differenza di pH e
di carica tra le due
superfici della
membrana interna
sintetizzano ATP in
assenza di un substrato
ossidabile: la forza
motrice protonica è
sufficiente a favorire la
sintesi di ATP
scaricato da www.sunhope.it
L‘ ATP sintasi, detta anche complesso V, è
formata da due componenti distinte:
1
F , una proteina periferica della membrana
(il primo fattore identificato)
o
F , una proteina integrale della membrana
(o sta ad indicare che questa è la
porzione che conferisce al complesso
la sensibilità all’oligomicina)
scaricato da www.sunhope.it
In laboratorio, piccole vescicole della membr. mitoc.
1
int. mancanti di F sono in grado di catalizzare il
trasferimento degli e- ma non possono produrre ATP
Quando F1 purificato viene aggiunto alle vescicole esso
si riassocia ad Fo e può catalizzare la sintesi di ATP
1
La porzione F isolata catalizza l’idrolisi (non la sintesi)
1
di ATP e all’inizio venne chiamata F ATPasi
scaricato da www.sunhope.it
L‘ ATP sintasi, detta anche complesso V,
è formata da due componenti distinte:
1
F , una proteina periferica della membrana
o
F , una proteina integrale della membrana
scaricato da www.sunhope.it
1
F ha una forma a pomello ed è costituita da
un’alternanza di subunità α e β disposte come
gli spicchi di un’arancia.
La subunità γ attraversa il centro della
struttura sferoidale costituendo l’asta del pomello.
scaricato da www.sunhope.it
Più precisamente, γ contiene un dominio che
attraversa F1 ed un altro dominio che è associato
ad una delle tre subunità β
È proprio l’associazione di γ con le subunità β che
costringe ciascuna di esse ad assumere
conformazioni differenti e
con diverse affinità per i nucleotidi
scaricato da www.sunhope.it
1
F consiste in 9 subunità
di 5 tipi diversi, con la
3 3
composizione α β γ δε
γ ed ε costituiscono una
sorta di “gamba e piede”
scaricato da www.sunhope.it
o
Il canale protonico F è
composto da 3 tipi di
2 10
subunità: ab c
2
Le b , insieme con δ,
scaricato da www.sunhope.it
o
F
Vista laterale
Vista frontale
Ciascuna delle dieci subunità c (organizzate in 2 cerchi
concentrici) sono formate da due eliche transmembrana
Le eliche N-terminali sono situate all’interno;
quelle C-terminali all’esterno
scaricato da www.sunhope.it
ATP sintasi
Subunità γ
Il rotore è l’anello is c & γε
Il rimanente è stazionario (statore)
Subunità dell’anello c
La subunità ‘a’ si
lega all’anello
esterno
La colonna
esteriore
ha 1 subunità a
2 subunità b, e
la subunità δ
Subunità α
scaricato da www.sunhope.it
0
F contiene l’anello del
canale protonico
1
di 10-14 subunità c
La subunità F ha 5 tipi di
catena polipetidica
3
(α3, β , γ,βδ,subunit
ε), e presenta
Subunità
attività ATPasica
α& β sono membri della
famiglia P-loop
Meccanismo di sintesi dell’ATP
i
Un atomo di ossigeno dell’ADP attacca il fosforo del P per
formare un intermedio pentavalente che poi forma ATP
2
e rilascio una molecola di H O
scaricato da www.sunhope.it
Osservazione della rotazione dell’ATP sintasi
marcato con fluoresceina
e legato alla subunità γ
La rotazione osservata
mediante un microscopio a
fluorescenza
dopo idrolisi di ATP
3
L’esamero α3β fissato su una superficie
scaricato da www.sunhope.it
Componenti dell’unita’ di conduzione dei protoni
2 α helices span the membrane
Structure not yet directly observed
scaricato da www.sunhope.it
Subunit c
Asp 61 in the middle of
the second helix
scaricato da www.sunhope.it
Subunit a
Proton enters
Proton exits
scaricato da www.sunhope.it
Proton motion across the membrane drives rotation
Proton enters cytosolic half-channel, neutralizes Asp
Proton enters matrix, resetting system
scaricato da www.sunhope.it
Asp enters matrix half-channel
Proton path through the membrane
Cytosolic
half-channel
Matrix
half-channel
scaricato da www.sunhope.it
o
1
0
La reazione sulla superficie di F F ha un ∆G’
vicino allo 0, con una K’eq di circa 1: si
1
tratta, cioè, di una reazione reversibile
F isolata catalizza invece l’idrolisi, non la sintesi,
1
di ATP (tanto da venir chiamata F ATPasi) con un
0
scaricato da www.sunhope.it
L‘ATP sintasi rende l'ATP stabile quanto i
suoi prodotti di idrolisi ADP e Pi, legando
molto saldamente l'ATP e fornendo in questo
modo l'energia necessaria per controbilanciare
quella richiesta per la sintesi dell’ATP stesso
scaricato da www.sunhope.it
FoF1 lega l'ATP con un‘affinità
7
10 più elevata di quella con cui lega l’ADP
Questa differenza di energia di legame è
sufficiente a spostare l'equilibrio verso la
formazione del prodotto ATP
scaricato da www.sunhope.it
Nella reazione catalizzata dall'ATP sintasi la
principale barriera energetica non è la sintesi
di ATP ma il suo rilascio dall'enzima
L'energia libera richiesta per il rilascio dell‘
ATP è fornita dalla forza motrice protonica
scaricato da www.sunhope.it
Per la continua sintesi di ATP, l'enzima deve
effettuare un ciclo tra una forma che lega
saldamente ATP e una forma che lo rilascia
Studi chimici e cristallografici sull’ATP sintasi
hanno rivelato le basi strutturali di questa
alternanza di funzionalità
scaricato da www.sunhope.it
F1 possiede tre siti di legame per nucleotidi
adenilici, uno per ogni coppia αβ,
αβ con
conformazioni non equivalenti
I tre siti attivi di F1 catalizzano a turno la
sintesi di ATP
(catalisi rotazionale)
scaricato da www.sunhope.it
Le tre conformazioni sono:
- β-ATP che lega
saldamente l’ATP
- β-ADP che lega
debolmente l’ATP
- β -vuota
che lega l’ATP ancora
più debolmente
La forza motrice protonica
provoca la rotazione del
cilindro c e di γ
(freccia verde)
ed il contatto di questa
con ciascuna coppia αβ
scaricato da www.sunhope.it
Ciò produce una modificazione
conformazionale cooperativa:
- il sito β-ATP è convertito nella
conformazione β-vuota e rilascia
l'ATP
− β -ADP è convertito in β -ATP,
che provoca la condensazione di
ADP e Pi per formare ATP
- β -vuoto diventa β -ADP che lega
debolmente ADP e Pi provenienti
dal solvente
L'ATP non può essere rilasciato
da un sito finché ADP e Pi
non sono legati all'altro
scaricato da www.sunhope.it
Il passaggio di H+ attraverso la porzione Fo
provoca la rotazione del cilindro costituito dalle
subunità c e dalla subunità y ad esso attaccata.
Ogni rotazione di 120° pone in contatto y con
una diversa subunità β e la costringe ad assumere
la conformazione β-vuota.
scaricato da www.sunhope.it
Le tre subunità β interagiscono tra di loro in
modo tale che quando una assume la
conformazione β-vuota, la subunità presente
su di un lato deve assumere la forma β-ADP
mentre quella sull'altro lato acquista la
conformazione β-ATP
scaricato da www.sunhope.it
Per ogni rotazione completa di γ, ogni subunità β
compie un ciclo attraverso le tre possibili
conformazioni e vengono sintetizzate e rilasciate
dalla superficie dell’enzima tre molecole di ATP
scaricato da www.sunhope.it
Per molti anni i libri di testo hanno riportato
un rapporto P/O = 3
quando il donatore di e- era il NADH
un rapporto P/O = 2
quando il donatore di e- era il succinato
L'introduzione della teoria chemiosmotica consentì
di ipotizzare che il rapporto P/O non fosse
necessariamente un numero intero.
scaricato da www.sunhope.it
+
Si è stabilito che il numero di H
-
pompati fuori per coppia di e trasportati è di
10 per il NADH e di 6 per il succinato.
+
Si è concordato che il numero di H richiesti per la
sintesi di una molecola di ATP è di 4, di cui uno è
usato per trasportare Pi, ATP e ADP
attraverso la membr. mitoc.
scaricato da www.sunhope.it
Il rapporto P/O è 2.5 (10:4)
quando il donatore di e- è il NADH
Il rapporto P/O è 1.5 (6:4)
quando il donatore di e- è il succinato
scaricato da www.sunhope.it
La funzione dell'ATP sintasi è strettamente
integrata con quella di due traslocasi:
- t. dei nucleotidi adenilici (antiporto)
- t. del fosfato (simporto)
Nel loro insieme le tre proteine costituiscono
un complesso, l‘ATP sintasoma
scaricato da www.sunhope.it
scaricato da www.sunhope.it
La traslocasi dei nucleotidi adenilici lega una molecola
3-
di ADP
nello spazio intermembrana
e la trasporta nella matrice, in antiporto con
4-
una molecola di ATP
Questo trasporto di 4 cariche negative all'esterno e
3 all'interno è favorito dal fatto che la matrice è
scaricato da www.sunhope.it
La fosfato traslocasi catalizza il simporto nella
matrice di uno ione H2PO4- e di uno ione H+.
Anche questo processo è favorito dal gradiente
+
protonico: un H passa dal lato p al lato n
della membrana interna, consumando parte
dell'energia prodotta dal trasferimento degli eK.
scaricato da www.sunhope.it
-
2
Per ogni coppia di e che arriva all‘O
vengono prodotte
1.5 molecole di ATP
nello shuttle del glicerolo 3P
2.5 molecole di ATP
nello shuttle Mal-Asp
scaricato da www.sunhope.it
scaricato da www.sunhope.it
L'ossidazione completa di una molecola di Glc
produce 30/32 molecole di ATP, mentre la
glicolisi anaerobia ne produce solo 2
La via ossidativa aerobia accoppiata alla FO
è dunque la fonte primaria dell’ATP prodotto
dal catabolismo
scaricato da www.sunhope.it
La velocità di ossidazione delle sostanze
nutrienti è finemente regolata in modo tale
da produrre una quantità di ATP adeguata
alle necessità energetiche della cellula
scaricato da www.sunhope.it
La velocità della respirazione (consumo di O2) nei
mitocondri è altamente controllata e strettamente
dipendente dalla concentrazione dell’ADP
(controllo dell'accettore della respirazione)
Avendo a disposizione più ADP per la FO ossidativa,
la velocità della respirazione aumenta, determinando
la rigenerazione dell'ATP
scaricato da www.sunhope.it
scaricato da www.sunhope.it
Nei neonati e negli animali in letargo vi è un
particolare tipo di tessuto adiposo, chiamato
grasso bruno (per la per la presenza di
numerosi mitocondri)
Questi mitocondri possiedono nella loro
membrana interna una proteina speciale,
la termogenina, chiamata anche
proteina disaccoppiante
scaricato da www.sunhope.it
Questa proteina costituisce una via di ritorno
o
1
per gli H+ che non attraversano F F
per effetto di questo cortocircuito, l'energia
delle ossidazioni non viene utilizzata per
produrre ATP
ma viene “dissipata” come
calore necessario a mantenere il corpo a
temperatura costante
scaricato da www.sunhope.it
scaricato da www.sunhope.it
Quando una cellula è ischemica (privata di O2),
come avviene durante un attacco di cuore, il
-
+
trasferimento di e all‘O2 e il pompaggio di H si
interrompono, e la forza motrice protonica collassa
immediatamente
In queste condizioni, l‘ATP sintasi potrebbe agire
in modo opposto, idrolizzando l'ATP per pompare
gli H+ nella direzione inversa e causando una
disastrosa riduzione dei livelli di ATP
scaricato da www.sunhope.it
Ciò viene impedito da una piccola (84 aa) proteina
inibitrice, IF1, che lega simultaneamente due molecole
di ATP sintasi, inibendo la loro attività ATPasica
L'inibitore è attivo solo nella sua forma dimerica,
che si produce a valori di pH inferiori a 6,5.
In una cellula privata di O2, la glicolisi anaerobia
fa abbassare il pH, favorendo la dimerizzazione di IF1
Quando viene ripristinato il metabolismo aerobio, il pH
sale, il dimero IF1 si destabilizza e l'inibizione dell'ATP
sintasi viene rimossa.
scaricato da www.sunhope.it
“SVANTAGGI DELLA F.O.”
• Specie reattive dell’ossigeno
(ROS)
.
2
2
O + e- → O
• Superossidodismutasi
.
scaricato da www.sunhope.it