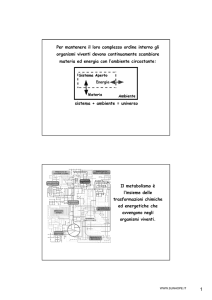
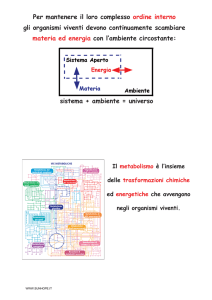
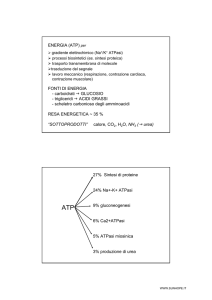
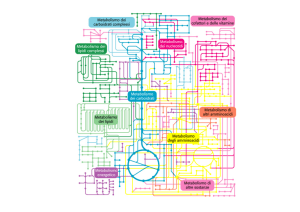
∆G’0 = variazione di energia libera standard
• è una costante fisica caratteristica di ogni reazione
• è correlata alla costante di equilibrio
• si riferisce a condizioni standard: [S]=[P]=1 M
∆G’ = variazione di energia libera reale
• è una variabile e dipende da ∆G’0 e dalle reali [S] e [P]
A
B
WWW.SUNHOPE.IT
1
A
B
A
B
WWW.SUNHOPE.IT
2
Le variazioni di energia libera sono additive.
Le costanti di equilibrio sono moltiplicative.
L’ATP è il principale trasportatore di energia
ed il punto di unione tra i processi che
producono e quelli che richiedono energia.
L’idrolisi dell’ATP fornisce l’energia
per vari tipi di lavoro
(biosintetico, osmotico, meccanico).
WWW.SUNHOPE.IT
3
La contrazione muscolare
rappresenta uno dei pochi casi
in cui l’idrolisi dell’ATP è di per sé
la fonte dell’energia chimica.
L’attività ATPasica della miosina
libera energia che viene convertita
in movimento:
la molecola si curva di scatto
dando un “colpo di remo”.
In tutti gli altri casi l’ATP interagisce covalentemente
con un substrato o con un enzima attraverso
il trasferimento di un gruppo (Pi, PPi, AMP).
La fosforilazione è la prima reazione
del metabolismo del Glc.
Un gran numero di enzimi sono modulati
mediante fosforilazione-defosforilazione.
WWW.SUNHOPE.IT
4
L’ATP ha un turnover rapidissimo:
una molecola viene idrolizzata
circa 1 min dopo la sua formazione.
Nel rene e nel cervello più dei 2/3 dell’ATP
prodotto sono utilizzati dalla
pompa Na+/K+ ATPasi.
WWW.SUNHOPE.IT
5
Basi strutturali dell’elevato ∆G’0 dell’ATP
-
Repulsione elettrostatica
-
Stabilizzazione per risonanza
-
“
“ ionizzazione
-
“
“ idratazione
La tensione dovuta alla repulsione elettrostatica
diminuisce quando l’ATP è idrolizzato
WWW.SUNHOPE.IT
6
I prodotti dell’idrolisi hanno una maggiore stabilità
rispetto alla molecola intatta dell’ATP.
∆G’0 fortemente negativo dell’ATP
elevato potenziale di trasferimento del gruppo Pi
Benché il ∆G’0 sia fortemente negativo, l’ATP è
stabile e idrolizzabile solo dallo specifico enzima.
WWW.SUNHOPE.IT
7
L’ATP e l’ADP sono sempre presenti
come complessi con il Mg2+, che maschera
in parte le loro cariche negative
Il ∆G’ dell’idrolisi dell’ATP dipende, oltre che
dalle reali concentrazioni dei reagenti, anche
dal pH e dalla concentrazione di Mg2+
∆G’0 = - 7.3 kcal/mole
∆G’ = - 12 kcal/mole
WWW.SUNHOPE.IT
8
WWW.SUNHOPE.IT
9
Composti fosforilati quali
- fosfoenolpiruvato (PEP)
- 1,3-bisfosfoglicerato (1,3-BPG)
- creatina fosfato (CP)
hanno un ∆G’ di idrolisi superiore a quello dell’ATP.
0
Anche i prodotti in cui essi si convertono
si stabilizzano con meccanismi analoghi ai prodotti
dell’idrolisi dell’ATP.
È questa posizione intermedia che consente
all’ATP di funzionare in modo efficace come
trasportatore di gruppi fosforici.
WWW.SUNHOPE.IT
10
Catabolismo e anabolismo sono finemente e
reciprocamente regolati per ottenere
il massimo equilibrio e la massima economia.
ANABOLISMO e CATABOLISMO
di una certa molecola
- seguono vie in tutto o in parte diverse
- la regolazione di entrambe le vie è reciprocamente
coordinata
- possono avvenire in compartimenti cellulari diversi
- almeno una reazione è termodinamicamente
“favorita” in un senso e “sfavorita” in quello
opposto
WWW.SUNHOPE.IT
11
- 7 tappe sono catalizzate dagli stessi enzimi
3 da enzimi diversi
- le due vie sono regolate reciprocamente per
evitarne il funzionamento simultaneo
WWW.SUNHOPE.IT
12