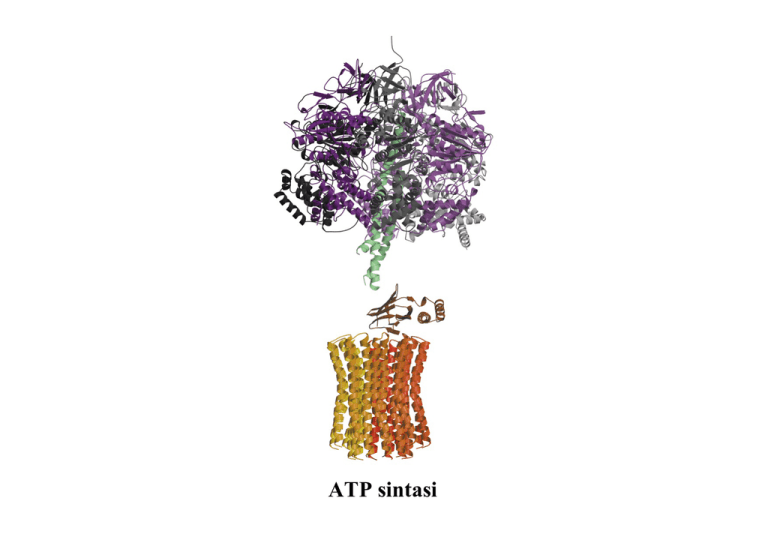
ATP sintasi
Gli organismi possono essere suddivisi in due grandi gruppi in
base alla forma chimica da cui ricavano atomi di carbonio.
Autotrofi:
Possono usare la CO2 dell’atmosfera come unica
fonte di atomi di carbonio.
Molti organismi autotrofi sono fotosintetici e ricavano l’energia
dalla luce solare.
Eterotrofi:
Non possono usare la CO2 e ottengono gli atomi di
carbonio sotto forma di molecole organiche come il
glucosio.
Le cellule eterotrofe ricavano l’energia dalla degradazione delle
molecole organiche prodotte dagli autotrofi.
Il continuo riciclo di CO2 e
O2 tra i domini autotrofici
(fotosintetici) e eterotrofici
della biosfera.
Circa 4 x 1011 tonnellate di
carbonio vengono riciclate
annualmente nella biosfera
Tutti gli organismi viventi hanno bisogno di una fonte di azoto.
Piante:
In genere sono capaci di usare come fonte di azoto
ammoniaca o nitrati solubili.
Animali:
Devono ottenere l’azoto sotto
amminoacidi o altri composti azotati.
forma
di
Batteri che fissano
l’azoto:
Convertono (“fissano”) l’azoto atmosferico (N2) in
NH3.
Alcuni di questi batteri vivono in simbiosi sulle
radici di alcune piante leguminose.
Batteri
nitrificanti: Ossidano l’ammoniaca a nitriti e nitrati.
a) Vie cataboliche convergenti
b) Vie anaboliche divergenti
c) Via ciclica in cui uno dei composti di partenza viene rigenerato e rientra nella via
A+B'C+D
[C][D]
ΔG = ΔG + RT log
[A ][B]
o'
ΔGo’= variazione di energia libera standard a ph 7
La variazione di energia libera complessiva di una serie di
reazioni accoppiate è uguale alla somma delle variazioni di
energia libera delle sigole reazioni:
A'B+C
ΔGo’= + 5 kcal/mole
B'D
ΔGo’= - 8 kcal/mole
A'C+D
ΔGo’= - 3 kcal/mole
Una reazione termodinamicamente non favorevole può essere
trascinata da una reazione termodinamicamente favorevole ad
essa accoppiata
Gli esseri viventi richiedono un continuo rifornimento di energia
libera:
•Lavoro meccanico (es. contrazione muscolare)
•Trasporto attivo di molecole
•Sintesi di macromolecole
Chemotrofi: ottengono questa
sostanze nutrienti.
Fototrofi:
Chemotrofi
Fototrofi
energia
dall’ossidazione
utilizzano l’energia della luce solare.
Adenosina trifosfato
(ATP)
ATP
delle
In tutti i sistemi biologici l’ATP è il trasportatore universale di
energia libera
Mg2+
L’ATP è una molecola ricca di energia in quanto la sua unità trifosfato
contiene 2 legami fosfoanidrinici:
ATP + H2O ' ADP + Pi + H+
ΔGo’ = - 7,3 kcal/mole
ATP + H2O ' AMP + PPi + H+
ΔGo’ = - 7,3 kcal/mole
PPi + H2O ' 2 Pi Pi
ΔGo’ = - 8 kcal/mole
ΔG = ΔG
o'
[C][D]
+ RT log
[A ][B]
ΔGo’= - 30,5 kj/mole
Alle concentrazioni delle varie specie presenti negli eritrociti:
ΔG ≅ - 51,8 kj/mole
Nei sistemi biologici l’ATP ha la funzione di donatore immediato di
energia libera per favorire reazioni che richiedono un apporto di energia.
Movimento
Trasporto attivo
Biosintesi
ATP
ADP
Fotosintesi
o
Ossidazione di molecole derivate da sostanze nutrienti
•Il turnover dell’ATP è molto rapido
•L’ATP viene continuamente rigenerato dall’ADP.
Idrolisi, con rimozione
della repulsione tra le cariche
Stabilizzazione
per risonanza
ionizzazione
L’ATP fornisce energia mediante trasferimento di gruppo,
non per semplice idrolisi
Il gruppo fosforico o l’adenilato
vengono prima trasferiti a una
molecola di substrato o a un residuo
amminoacidico dell’enzima.
L’ATP partecipa alla reazione a cui
deve fornire energia libera
Idrolisi del fosfoenolpiruvato
Piruvato
(forma enolica)
Piruvato
(forma chetonica)
Il prodotto dell’idrolisi può esistere in due forme tautomeriche,
mentre il reagente ha una sola forma, la forma enolica.
Il prodotto è più stabile del reagente.
Idrolisi dell’ 1,3-bisfosfoglicerato
Il prodotto dell’idrolisi è il 3-fosfoglicerato
il cui gruppo carbossilico, dopo la
formazione, può andare incontro a
dissociazione.
La ionizzazione e le strutture di risonanza
rendono possibile la stabilizzazione dei
prodotti della reazione idrolitica.
Un ulteriore contributo alla variazione di
energia libera è dovuto alla stabilizzazione
per risonanza del Pi.
Idrolisi della fosfocreatina
Il prodotto dell’idrolisi è stabilizzato per risonanza, mentre il
reagente no.
Il prodotto è più stabile del reagente.
Nei muscoli dei vertebrati la fosfocreatina costituisce una
riserva di gruppi fosfato che possono esere trasferiti all’ATP.
fosfocreatina + ADP + H+ ' ATP + creatina
Enzima che catalizza la reazione = creatina chinasi
Fonti di ATP durante l’esercizio fisico
Nei secondi iniziali l’energia necessaria per l’esercizio fisico è fornita dai
composti ad alto potenziale di trasferimento del gruppo fosforico (ATP e
creatina fosfato). Successivamente l’ATP deve essere rigenerato dalle vie
metaboliche
L’energia libera necessaria viene ottenuta dagli organismi chemotrofi
dall’ossidazione delle molecole delle sostanze nutrienti.
Negli organismi aerobici l’accettore finale degli elettroni è l’O2.
Gli elettroni non vengono trasferiti direttamente dalle sostanze nutrienti
all’O2.
Il NADH e il FADH2 sono i principali trasportatori di elettroni nelle
ossidazioni delle sostanze nutrienti.
Da questi nucleotidi gli elettroni vengono trasferiti all’O2 attraverso la catena
di trasporto degli elettroni, localizzata nella membrana interna dei
mitocondri (fosforilazione ossidativa).
Il nicotinamide adenin dinucleotide
Il nicotinamide adenin dinucleotide
Il NAD+ è il principale accettore di elettroni
nelle ossidazioni di molecole nutrienti.
La parte reattiva del NAD+ è l’anello
nicotinamidico.
Nell’ossidazione del substrato l’anello nicotinamidico accetta 1 protone (H+) e 2 elettroni
(e-), cioè 1 ione idruro (H-).
La forma ridotta è detta NADH
Il nicotinamide adenin dinucleotide
Il NAD+ è l’accettore di elettroni in reazioni del tipo:
H
NAD+ + R - C - R’ ' NADH + R - C - R’ + H+
OH
Entrambi gli elettroni sono trasferiti al NAD+.
O
Nella maggior parte delle biosintesi i precursori sono più ossidati dei
prodotti.
Le biosintesi richiedono potere riducente oltre all’ATP.
Il donatore di elettroni in molte delle biosintesi riduttive è il NADPH.
Il NAPDH viene usato quasi esclusivamente per le biosintesi riduttive,
mentre il NADH viene usato principalmente per produrre ATP.
Il gruppo fosforico in più nella molecola di NADPH indirizza questo
trasportatore verso specifici enzimi biosintetici.
I nucleotidi flavinici.
Anello isoallossazinico
Alcuni enzimi (le flavoproteine)
catalizzano reazioni di ossidoriduzione usando come cofattori
nucleotidi flavinici.
Nella maggior parte delle flavoproteine i nucleotidi flavinici sono legati
saldamente ed in alcuni casi covalentemente.
Questi cofattori legati saldamente sono detti più
propriamente gruppi prostetici.
I nucleotidi flavinici.
Il FAD è l’accettore di elettroni in reazioni del tipo:
H H
FAD + R - C - C - R’' FADH2 + R - C = C - R’
H H
H H
L’ossidazione delle sostanze organiche è una fonte importante di
energia cellulare
Nell’ossidazione aerobica l’accettore ultimo di elettroni nell’ossidazione del
carbonio è O2, e il prodotto di ossidazione è CO2.
Quanto più ridotto è all’inizio un atomo di carbonio, tanto più esoergonica è la
sua ossidazione.
Quando una molecola organica complessa viene ossidata la reazione di
ossidazione coinvolge un atomo di carbonio alla volta.
Stato di ossidazione del C
Alcano < alcol < aldeide < acido carbossilico < anidride carbonica
Stato di ossidazione del C
Alcano < alcol < aldeide < acido carbossilico < anidride carbonica
I combustibili principali
I grassi sono una fonte di energia superiore ai carboidrati perché i loro atomi
di carbonio sono più ridotti.
Per molte reazioni di acetilazione è necessario un cofattore chiamato
coenzima A (CoA, la A sta per acetilazione)
unità di
β-mercaptoetilamina
unità di
pantotenato
Il sito attivo è il gruppo sulfidrilico terminale
I gruppi acile si legano al CoA con un legame tioestere formando un acilCoA.
O
R - C - S - CoA
AcilCoA
O
H3C - C - S - CoA
AcetilCoA
L’acetilCoA ha un elevato potenziale di trasferimento del gruppo acetile
- 7,5 kcal/mole
Una unità di adenosina fosfato è presente in:
•ATP
•NADH
•FADH2
•Coenzima A
Il ruolo fondamentale dei ribonucleotidi nel
metabolismo riflette la loro origine antica.
Le migliaia di reazioni metaboliche possono essere suddivise
in sei tipi
1) Reazioni di ossidoriduzione
2) Reazioni di sintesi
…formano legami utilizzando l’energia libera derivante dalla scissione
dell’ATP
3) Reazioni di isomerizzazione
..modificano la disposizione di particolari atomi in una molecola. Hanno
spesso il ruolo di preparare una molecola per reazioni successive come le
reazioni di ossidoriduzione.
4) Reazioni di trasferimento di gruppo
..svolgono molte funzioni. Vengono anche utilizzate per sintetizzare ATP
5) Reazioni idrolitiche
..scindono legami mediante l’aggiunta di una molecola d’acqua. Es.:
degradazione grandi molecole.
6) Reazioni di aggiunta di gruppi funzionali a doppi legami o la
rimozione di gruppi per formare doppi legami
Deidratazioni che formano doppi legami
Gli enzimi che catalizzano queste reazioni sono denominati liasi.
Motivi metabolici
Alcune vie metaboliche hanno in comune sequenze di reazioni simili.
Es.: ossidazione (FAD dipendente), addizione di un gruppo funzionale (proveniente
da una molecola di acqua) a un doppio legame, II ossidazione (NAD+ dipendente)