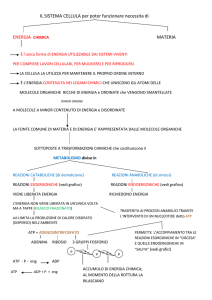
METABOLISMO
È l’insieme delle reazioni chimiche
che avvengono nel corpo degli esseri
viventi e che intercorrono tra
l’introduzione di sostanze di origine
chimica e l’eliminazione degli scarti.
ENERGIA
ENERGIA =
ATTIVITÀ, FORZA
CAPACITÀ DI COMPIERE UN LAVORO
SPOSTARE LA MATERIA
ENERGIA CHIMICA
• Fondamentale per i viventi.
• È depositata nelle molecole sotto forma di legami
chimici.
• È resa utilizzabile in decorrenza alla demolizione
delle molecole.
• È resa disponibile per compiere lavoro.
USO DELL’ENERGIA
• L’uso dell’energia dipende:
– dalla capacità di trasformarsi in forme diverse
– dalla capacità di trasferirsi da un corpo all’altro
• Energia utile in uscita è MINORE a quella in
entrata
perdita sotto forma di
CALORE – forma di energia non utilizzabile per
compiere un lavoro
SISTEMI TERMODINAMICI
SISTEMA
ISOLATO
non scambia
né energia
né materia
SISTEMA
CHIUSO
scambia
energia ma
non materia
SISTEMA
APERTO
scambia
energia e
materia
LEGGI FONDAMENTALI DELL’ENERGIA
PRIMA LEGGE DELLA TERMODINAMICA
Nulla si crea, nulla si distrugge tutto si trasforma
SECONDA LEGGE DELLA TERMODINAMICA
L’energia dell’universo si degrada in modo
irreversibile
tende a disperdersi sotto
forma di calore e a degradarsi in maniera
disorganizzata
ENTROPIA
ENERGIA E I VIVENTI
• I viventi sono sistemi aperti molto organizzati
a bassa entropia.
• Per il mantenimento della vita c’è la necessità
di un continuo scambio e flusso di MATERIA
ed ENERGIA.
ENERGIA E I VIVENTI
I viventi utilizzano solo due forme di
manifestazione dell’energia:
Energia
luminosa
Energia
chimica
Organismi
autotrofi
Organismi
eterotrofi
fotosintesi
Ingestione di
molecole
organiche
ENERGIA E I VIVENTI
2 TIPI DI REAZIONI
ESOERGONICA
• Energia dei prodotti minore
di quella dei reagenti
• Libera enegia
spontaneamente
• Può produrre lavoro
• Es: respirazione cellulare
• Energia dei prodotti maggiore
di quella dei reagenti
• Richiedono spesa di energia
ENDOERGONICA
• Esigono lavoro per poter
avvenire
• Es. fotosintesi
reagenti
reagenti
prodotti
prodotti
ATP
• L’energia liberata dalle reazioni esoergoniche
deve essere “intrappolata” dai viventi,
affinché non si disperda in forma di calore.
• Viene perciò spesso trasferita ad uno speciale
trasportatore di energia: l’ATP
ATP = ADENOSINA TRIFOSFATO
ATP
È il collegamento universale tra le reazioni eso e
endoergoniche e funziona:
fornendo energia
ADP + P ATP
richiedendo energia
ATP ADP + P
o
ATP AMP + 2P
ATP e RISERVA ENERGETICA
• Il fabbisogno energetico di uma cellula si
esprime in 2 modi:
– Bisogno immediato – energia da spendere
istantaneamente (uso di ATP).
– Deposito energetico – riserva energetica a lungo
termine (uso di polimeri grandi come amido nelle
piante e glicogeno negli animali).
ENERGIA DI ATTIVAZIONE
• È l’energia necessaria per innescare uma
reazione
• È questa che determina l’effettivo svolgimento
di una reazione e ne controlla la velocità
• In caso di assenza – cellula raggiunge entropia
massima e muore
• In caso di presenza – cellula può fare avvenire
le reazioni e può controllarla abbassandola
(azione enzimatica).
Reazione esoergonica
Energia di attivazione
Energia reagenti
Energia prodotti
Reazione endoergonica
Energia di attivazione
Energia prodotti
Energia reagenti
REAZIONI DI INTERESSE BIOLOGICO
OSSIDORIDUZIONI – REAZIONI REDOX
• Consistono nel trasferimento di elettroni
isolati o di elettroni e ioni idrogeno (protoni)
da un composto (DONATORE) ad un altro
(ACCETTORE).
OSSIDAZIONE – perdita di elettroni
RIDUZIONE – guadagno di elettroni
REDOX
• Le ossidazioni e le riduzioni sono sempre
abbinate perché gli elettroni non possono
essere mai eliminati, ma solo trasferiti.
• Al passaggio degli elettroni coincide un
passaggio di energia che non viene passata
tutta in una volta, ma gradualmente
attraverso reazioni intermedie che liberano
ciascuna una piccola porzione di energia.
REDOX
• In tal senso si evita che l’energia liberata tutta
insieme sotto forma di calore, innalzi la
temperatura della cellula fino alla sua morte.
• Ciò è possibile grazie ai trasportatori di
elettroni, che sono catene speciali di
molecole, disposte in ordine che liberano
energia gradativamente.
In laboratorio
Nella cellula
ENERGIE DI
ATTIVAZIONE
PICCOLE PER OPERA
DEGLI ENZIMI
ENERGIA DI
ATTIVAZIONE
GRANDE
Non viene
immagazzinata
nessuna energia
GLUCOSIO + O2
GLUCOSIO + O2
E
E
E
ATP
E
E
E
CO2 + H20
E
CO2 + H20
TRASPORTATORI DI ELETTRONI
Esempi:
• NAD – nicotinnamide adenin nucleotide
• NADP – nicotinnamide adenin dinucleotide
fosfato
• FAD – flavina adenin dinucleotide
• CITOCROMI – presenti nei mitocondri
CATALISI
• Le reazioni biochimiche nelle cellule sono quasi tutte
ad alta energia di attivazione.
• Le cellule quindi ricorrono ai CATALIZZATORI,
sostanze la cui funzione è quella di ABBASSARE
L’ENERGIA DI ATTIVAZIONE, AUMENTANDONE LA
VELOCITÀ.
• Le cellule usano catalizzatori organici che sono gli
ENZIMI.
• Questo processo è denominato CATALISI.
FATTORI CHE INFLUENZANO
L’ATTIVITÀ ENZIMATICA
• TEMPERATURA – aumento della temperatura
porta all’aumento della velocità delle reazioni,
ma oltre um certo grado può avvenire la
denaturazione irreversibile delle proteine.
• pH – piccole variazioni sono sufficienti per
ridurre l’attività enzimatica; variazioni grandi
denaturano gli enzimi.