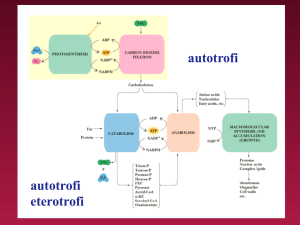
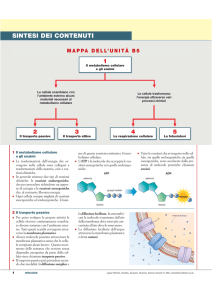
IL SISTEMA CELLULA per poter funzionare necessita di
ENERGIA CHIMICA
MATERIA
È l’unica forma di ENERGIA UTILIZZABILE DAI SISTEMI VIVENTI
PER COMPIERE LAVORI CELLULARI, PER MUOVERSI E PER RIPRODURSI
LA CELLULA LA UTILIZZA PER MANTENERE IL PROPRIO ORDINE INTERNO
È L’ENERGIA CONTENUTA NEI LEGAMI CHIMICI CHE UNISCONO GLI ATOMI DELLE
MOLECOLE ORGANICHE RICCHE DI ENERGIA e ORDINATE che VENGONO SMANTELLATE
DANDO ORIGINE
A MOLECOLE A MINOR CONTENUTO DI ENERGIA e DISORDINATE
LA FONTE COMUNE DI MATERIA E DI ENERGIA E’ RAPPRESENTATA DALLE MOLECOLE ORGANICHE
SOTTOPOSTE A TRASFORMAZIONI CHIMICHE che costituiscono il
METABOLISMO diviso in
REAZIONI CATABOLICHE (di demolizione)
REAZIONI ANABOLICHE (di sintesi)
REAZIONI ESOERGONICHE (vedi grafico)
REAZIONI ENDOERGONICHE (vedi grafico)
VIENE LIBERATA ENERGIA
RICHIEDONO ENERGIA
L’ENERGIA NON VIENE LIBERATA IN UN'UNICA VOLTA
MA A TAPPE (RILASCIO FRAZIONATO)
TRASFERITA AI PROCESSI ANABOLICI TRAMITE
L’INTERVENTO DI UN NUCLEOTIDE detto ATP
ciò LIMITA LA PRODUZIONE DI CALORE DISSIPATO
(DISPERSO) NELL’AMBIENTE
ATP = ADENOSINTRIFOSFATO
ADENINA
RIBOSIO
3 GRUPPI FOSFORICI
P
ATP - P - eng
ATP
PERMETTE L’ACCOPPIAMENTO TRA LE
REAZIONI ESORGONICHE IN “DISCESA”
E QUELLE ENDOERGONICHE IN
“SALITA” (vedi grafici)
P
P
ADP
ADP + P + eng
ACCUMULO DI ENERGIA CHIMICA;
AL MOMENTO DELLA ROTTURA LA
RILASCIANO
Grafici della variazione di energia.
R= reagenti
P= prodotti
Ea (energia di attivazione)= dislivello massimo, l’energia necessaria per far partire la reazione
∆e= energia dei prodotti meno (-) l’energia dei reagenti ∆e= Ep-Er
Reazione endoergonica.
∆e>0 ∆e+ (positivo)
Energia
Ea
R
P
∆e
tempo
Reazione esoergonica.
∆e<0 ∆e- (negativo)
Energia
Ea
R
∆e
P
tempo