Liceo Scientifico Statale “ C. Cattaneo” di Torino.
Anno Scolastico 2011 -2012
Programma svolto di Chimica
Classe 4 A
Insegnante Cortassa Rita Cristina
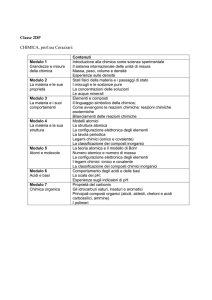
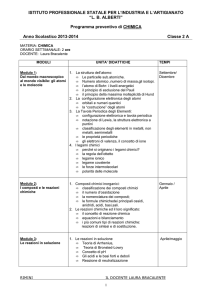
LA STRUTTURA DELLA MATERIA
La materia e le sue proprietà . Individui chimici : elementi e composti . Gli stati di
aggregazione della materia . Sistemi omogenei ed eterogenei .
I COMPOSTI E LA LORO COMPOSIZIONE
Concetto e significato di : peso atomico ,
peso molecolare , grammoatomo e
grammomolecola . Numero di Avogadro . Formule chimiche . Nomenclatura dei composti
inorganici.
EQUAZIONI CHIMICHE
Tipi di reazioni chimiche. Bilanciamento dell’equazione chimica . Calcoli stechiometrici.
I COMPONENTI E LA STRUTTURA DELL 'ATOMO
Le particelle subatomiche : elettrone , protone , neutrone. La scoperta del nucleo :
numero atomico , massa atomica , numero di massa . La luce e lo spettro
elettromagnetico . Il fotone. L' elettrone : natura corpuscolare ed ondulatoria . I numeri
quantici . Gli orbitali ; la distribuzione degli elettroni negli orbitali ; configurazione
elettronica e sistema periodico degli elementi .
I LEGAMI CHIMICI
Le molecole ed il legame chimico; gli elettroni nella molecola. Elettronegatività degli atomi;
il legame covalente puro e polare ; il legame ionico ; il legame dativo ; il legame
metallico. Forze di Van der Waals . Legami chimici secondari . Energia di legame . Orbitali
ibridi . Orbitali molecolari .
GLI STATI FISICI DELLA MATERIA
Gas. Pressione , volume , temperatura di un gas e loro relazioni (leggi dei gas) . Teoria
cinetica .
LE SOLUZIONI
Aspetti generali . Metodi per esprimere la concentrazione delle soluzioni . Il processo di
solubilizzazione . Proprietà delle soluzioni . Pressione osmotica ed osmosi . Gli elettroliti .
LE REAZIONI DI OSSIDORIDUZIONE
Il numero di ossidazione . Le ossido-riduzioni e il loro bilanciamento .
LA CINETICA DELLE REAZIONI CHIMICHE
La velocità di reazione ed i fattori che la influenzano . La meccanica di una reazione ;
energia di attivazione .Catalizzatori .
EQUILIBRIO CHIMICO
Lo stato di equilibrio . La legge di azione di massa . La costante di equilibrio . Equilibri
eterogenei .Principio di Le Châtelier.
EQUILIBRI IN SOLUZIONE ACQUOSA
L' equilibrio negli elettroliti . La dissociazione ionica dell' acqua . Prodotto ionico dell'acqua
e scala del pH . Ampliamento del concetto di acido e di base . La neutralizzazione . I
composti anfoteri . Idrolisi .
INTRODUZIONE ALLO STUDIO DELL’ ELETTROCHIMICA
Soluzioni di elettroliti . Conducibilità elettrica . Elettrolisi . Celle galvaniche o voltaiche .
Potenziali di ossido-riduzione . Celle elettrolitiche .
INTRODUZIONE ALLA CHIMICA NUCLEARE
La stabilità del nucleo . Radioattività ; reazioni nucleari ed energia .Fissione e fusione
nucleare .
Torino, 4 giugno 2012
L’Insegnante
Firmato in originale
Gli studenti
Firmato in originale