112
Casistica
Recenti Prog Med 2013; 104: 112-115
Severa iponatriemia secondaria
a sindrome da inappropriata secrezione di ormone antidiuretico
Luca Foppiani1, Francesca Raggi1, Milena Tagliabue2, Andrea Benso3, Irene Brandolin1, Giuliano Lo Pinto1
Riassunto. La sindrome da inappropriata secrezione di ormone antidiuretico (SIADH) rappresenta una causa frequente, multifattoriale e spesso non diagnosticata di iponatriemia. Meccanismo fisiopatologico comune è l’aumentata produzione e/o azione a livello renale di ormone antidiuretico con conseguente iponatriemia ipotonica. Una correzione inappropriata dell’iponatriemia può avere conseguenze neurologiche fatali, determinando mielinolisi pontina.
Viene presentato il caso di un paziente con anamnesi recente di trauma cranico giunto alla nostra osservazione per
uno stato confusionale acuto secondario a grave iponatriemia da SIADH ad eziologia multipla.
Severe hyponatremia secondary to the syndrome of inappropriate secretion of antidiuretic hormone.
Parole chiave. Iponatriemia, sindrome da inappropriata secrezione di ormone antidiuretico, terapia, vaptani.
Key words. Hyponatremia, syndrome of inappropriate secretion of antidiuretic hormone, therapy, vaptans.
Introduzione
sivo peggioramento. In anamnesi è presente un incidente motociclistico circa 3 settimane prima con trauma cranico commotivo [tomografia computerizzata
(TC) cerebrale negativa] e fratture costali con conseguente assunzione di farmaci antinfiammatori non
steroidei (FANS). All’ingresso in PS il paziente è eupnoico, confuso e disorientato, con elevati valori pressori (200/100 mmHg), per cui viene somministrato
captopril con normalizzazione della pressione arteriosa. Nella norma sono ECG, emogasanalisi arteriosa e
TC cerebrale. Gli esami ematochimici evidenziano una
severa iponatriemia (Na+: 115 mEq/l, v.n. 136-145), negativa risulta la ricerca di oppiacei o sostanze stimolanti il sistema nervoso centrale; una valutazione neurologica riconduce lo stato mentale alla grave iponatriemia. Nella serata, il paziente viene ricoverato
presso il nostro reparto di Medicina Interna dove, persistendo stato di agitazione e disorientamento, viene
consultato lo psichiatra che consiglia somministrazione parenterale di benzodiazepine e fenotiazine. Il medico di guardia avvia infusione di salina. La mattina
successiva, perdurando il quadro clinico, viene ricontrollata la sodiemia, che risulta invariata (115 mEq/l),
eseguita l’osmolarità plasmatica, che risulta ridotta
(232 mOsm/kg, v.n. 275-301), e la sodiuria spot, che risulta attivata (25 mEq/l). Essendo il paziente residente a Torino, i familiari decidono la dimissione volontaria.
La sindrome da inappropriata secrezione di ormone antidiuretico (SIADH) rappresenta una causa frequente di iponatriemia la cui eziologia comprende patologie neoplastiche, infiammatorie,
traumatiche cerebrali e farmacologiche, queste ultime prevalenti nel paziente anziano1-4. Una corretta diagnosi eziologica della SIADH è fondamentale ai fini di una terapia appropriata e diversificata in base alle manifestazioni cliniche che dipendono dalla gravità dell’iponatriemia e dalla velocità con cui questa si instaura. Una correzione
troppo rapida dell’iponatriemia può portare a complicanze neurologiche fatali1-4. Descriviamo il caso
di un paziente ricoverato per uno stato confusionale acuto secondario ad una grave iponatriemia
la cui eziologia è stata successivamente ricondotta
ad una SIADH ad eziologia multipla.
Descrizione del caso
Maschio di 55 anni, al Pronto Soccorso dell’Ente
Ospedaliero Ospedali Galliera, Genova per insorgenza
da alcuni giorni di uno stato confusionale in progres-
Summary. The syndrome of inappropriate secretion of antidiuretic hormone (SIADH) is a common and multifactorial cause of hyponatremia that is often overlooked. The common pathophysiological mechanism is the increased production and/or action of antidiuretic hormone within the
kidney, resulting in hypotonic hyponatremia. Inadequate
correction of hyponatremia may have fatal neurological
consequences leading to central pontine myelinolysis. We
report the case of a patient with a history of recent head
trauma, who came to our observation for acute-onset mental confusion secondary to severe hyponatremia due to
SIADH of combined etiology.
1
Struttura Complessa Medicina Interna, Ente Ospedaliero Ospedali Galliera, Genova; 2Struttura Complessa Dipartimentale Universitaria di Endocrinologia, Diabetologia e Metabolismo, Dipartimento di Medicina, Azienda Ospedaliera Città della Salute e della Scienza, Torino; 3Struttura Complessa Dipartimentale Universitaria di Endocrinologia, Diabetologia e Metabolismo, Dipartimento di Scienze Mediche, Università di Torino.
Pervenuto il 3 dicembre 2012.
L. Foppiani et al.: Severa iponatriemia secondaria a sindrome da inappropriata secrezione di ormone antidiuretico
Na + (mEq/L)
Il paziente, tutt’ora confuso, viene trasferito presso il PS
dell’Ospedale Molinette di To150
dimissione
rino dove è confermata una setrauma
cranico
145
vera iponatriemia (118 mEq/l)
ipoosmolare (250 mOsm/kg)
140
con sodiuria attivata (38
mEq/l) ed osmolarità urinaria
135
conservata (300 mOsm/kg), e
viene riscontrata rabdomiolisi
130
(1135 U/l, v.n. 25-190). Segue il
ricovero in Medicina d’Urgen125
za dove, dopo calcolo del deficit
di Na+ (294 mEq/l), è stata av120
tolvaptan
restrizione tolvaptan
viata infusione di salina iper7,5 mg gg alterni
idrica 7,5 mg/die
tonica (1,8%), cui segue parzia115
sol
le miglioramento clinico, della
ipert
sodiemia (figura 1) e normaliz110
zazione della creatinfosfochi-20 -15 -10 -5 0 5 10 15 20 25 30 35 40 45 50 55 60 65 70 75 80 85 90 95 100
nasi. La Risonanza Magnetica
Genova (PS/Med)
giorni
cerebrale con mezzo di contraTorino (PS/Med Urg)
sto e la TC toraco-addominale
risultano nella norma. Dopo 4
giorni, il paziente, parzialmenFigura 1. Variazioni della sodiemia.
te confuso, viene trasferito
presso il reparto di Endocrinologia dello stesso nosocomio; i
tico caso-controllo più recente su 104 pazienti (età
livelli di sodio permangono significativamente ridotti
(121 mEq/l) [figura 1]. L’avvio della restrizione idrica
media 69 anni) ospedalizzati con severa ipona(700 ml/die) causa un progressivo aumento della sodietriemia (<125 mEq/l) conferma un aumento della
mia (zenith Na+: 132 mEq/l); tuttavia si sono manifestamortalità in questi soggetti rispetto a quelli norti altri episodi di agitazione psicomotoria che hanno rimonatriemici8. Infine, una recente revisione delchiesto terapia parenterale con fenotiazine e benzodiala letteratura9 evidenzia come fino al 12% dei pazepine. Il controllo della funzionalità tiroidea (FT4: 17,0
zienti
ospedalizzati presenti una SIADH, in parng/ml; FT3: 2,8 pg/ml; TSH: 0,9 µU/ml) e dell’asse ipoticolare
quando sono in terapia simultanea con
talamo-ipofisi-surrene (ACTH: 32 pg/ml; cortisolo: 19,7
neurolettici/antidepressivi, diuretici e fluidi e.v. È
µg/dl) è nella norma. I livelli plasmatici di ormone antidiuretico (ADH) risultano normali (5 pg/ml, v.n. <6,7) ma
pertanto fondamentale diagnosticare l’eziologia
inappropriati per l’ipo-osmolarità plasmatica. Vista la
della SIADH al fine di intraprendere la terapia
scarsa compliance del paziente alla restrizione idrica,
più adeguata. Oltre a patologie neoplastiche, inviene avviata terapia con tolvaptan (antagonista seletfiammatorie, traumatiche cerebrali, i farmaci (tativo dei recettori V2 della vasopressina) a bassa posolobella 1 alla pagina seguente) rappresentano una
gia (7,5 mg/die) con normalizzazione della sodiemia (142
causa frequente di SIADH10; pertanto un’accuramEq/l) e completa risoluzione del quadro clinico. Le vata anamnesi farmacologica è fondamentale nelriazioni della sodiemia sono mostrate nella figura 1. All’approccio clinico a questi pazienti. Indipendenla dimissione la somministrazione del vaptano viene ritemente dall’eziologia, il meccanismo fisiopatolodotta a giorni alterni e proseguita con controllo ambulatoriale per circa 2 mesi; ad 1 mese dalla sospensione, la
gico comune della SIADH è l’aumentata produsodiemia è nella norma (141 mEq/l).
zione/azione di ADH con conseguente riassorbi-
Discussione
La SIADH, descritta per la prima volta da
Schwartz5,6 nel 1957, rappresenta la causa del 3040% delle iponatremie e costituisce, insieme alla
terapia con diuretici, la causa più frequente di
questa alterazione elettrolitica1-4. Dati di letteratura non recenti ma su un’ampia (~700) popolazione di anziani (>75 anni) ricoverati durante l’arco di 10 mesi in un contesto geriatrico evidenziavano una prevalenza dell’iponatriemia (<130
mEq/l) nell’11% dei pazienti, che risultava grave
(<125 mEq/l) nel 4,5%7. Nel 70% dei casi, le cause dell’iponatriemia erano la terapia diuretica o
l’infusione di soluzioni ipotoniche, e la mortalità
dei pazienti con iponatriemia era doppia rispetto
a quella degli altri pazienti7. Uno studio prospet-
mento dell’acqua, mediata dall’aquaporina 2, a livello dei tubuli collettori.
I criteri eziologici della SIADH sono: a) iponatriemia (<135 mEq/l); b) ipotonicità plasmatica
(<275 mOsm/kg); c) iperosmolarità urinaria (>100
mOsm/kg); d) sodiuria attivata (>30 mEq/l); e) euvolemia; f) normale funzione renale, surrenalica e
tiroidea1-6. Le manifestazioni cliniche della
SIADH, indipendentemente dalla sua eziologia, dipendono oltre che dalla gravità dell’iponatriemia,
dalla rapidità con cui questa si manifesta. I sintomi neurologici, riconducibili all’edema cerebrale
secondario all’ipotonicità plasmatica, generalmente compaiono per una sodiemia ≤120-125 mEq/l ad
esordio acuto (entro le 48 h) e possono diventare
gravi fino al coma ed all’exitus1-4. L’esordio clinico
del nostro paziente è stato quello di uno stato confusionale acuto riconducibile ad una severa iponatriemia ipotonica euvolemica.
113
114
Recenti Progressi in Medicina, 104 (3), marzo 2013
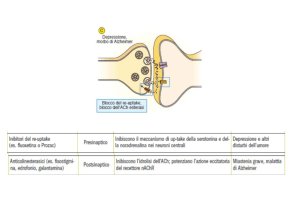
Tabella 1. Farmaci e sindrome da inappropriata secrezione di
ormone antidiuretico.
Aumentata produzione di ADH
Antidepressivi
– Triciclici (amitriptilina, desipramina)
– SSRI
Antipsicotici
– Fenotiazine (tioridazina)
– Butirrofenoni (aloperidolo)
Antiepilettici
Carbamazepina, oxcarbazepina, leviracetam,
sodio valproato
Antineoplastici
– Alcaloidi della vinca (vincristina, vinblastina)
– Composti del platino (cisplatino, carboplastino)
– Agenti alchilanti (ciclofosfamide, melfalan)
– Miscellanea: metotrexate, interferone α e β, anticorpi monoclonali
Oppioidi
Potenziamento dell’azione dell’ADH
Antiepilettici
– Carbamazepina, lamotrigina
Antidiabetici (non più usati)
– Clorpropamide, tolbutamide
FANS
Antineoplastici (ciclofosfamide)
Azione ADH-simile
– DDAVP, ossitocina
Resetting dell’osmocettore per l’ADH
Antidepressivi (venlafaxina)
Miscellanea: ACE-inibitori, ectasy, chinolonici, amiodarone,
inibitori di pompa protonica
Legenda: ACE= enzima di conversione dell’angiotensina; ADH= ormone antidiuretico; DDAVP= desamino-D-arginina-vasopressina; FANS=
farmaci antinfiammatori non steroidei; SSRI= inibitori selettivi del reuptake della serotonina. Modificata da Liamis et al.10.
Durante l’iter degenziale in due diverse strutture ospedaliere, è stata ripetutamente necessaria
una valutazione psichiatrica e l’avvio di terapia parenterale con fenotiazine e benzodiazepine per il
controllo del quadro clinico. La grave iponatriemia
ha inoltre causato il peggioramento della rabdomiolisi post-traumatica, risoltasi con la normalizzazione dei livelli di sodio.
L’indagine anamnestica rimane un punto cardine nella diagnosi eziologica della SIADH. Nell’anamnesi del nostro paziente era presente: a) un
politrauma (anche cerebrale commotivo) recente
(circa 3 settimane prima del ricovero); b) conseguente utilizzo di FANS. È noto che il trauma cranico può causare stimolazione dei neuroni localizzati nel nucleo sopraottico e paraventricolare con
conseguente rilascio di ADH e comparsa di ipona-
triemia ipotonica euvolemica. Nel corso degli ultimi anni, sempre maggiore attenzione è stata rivolta alla possibile insorgenza di ipopituitarismo
(totale o parziale) nei giorni/mesi successivi ad un
trauma cranico, la cui prevalenza può raggiungere il 27%11. Comunque, nel nostro paziente la valutazione ormonale dell’asse ipotalamo-ipofisi-tiroide ed ipotalamo-ipofisi-surrene ad 1 mese dal
politrauma è risultata nella norma così come lo
studio morfologico della regione ipotalamo-ipofisaria; pertanto l’iponatriemia riscontrata non era
riconducibile ad un ipotiroidismo e/o ad un iposurrenalismo secondari. Il dosaggio plasmatico
dell’ADH ha evidenziato un valore inappropriatamente normale in relazione all’ipotonicità plasmatica. Questa determinazione non è di routine
nella pratica clinica per difficoltà metodologiche,
estrema fluttuazione dei livelli plasmatici di ADH
e sulla base fisiopatologica che essa non costituisce un test probante per la diagnosi di SIADH. Infatti, la concentrazione di ADH risulta nella norma/modestamente aumentata (nell’ordine di pochi
pg/ml), ma inappropriata in rapporto all’ipo-osmolarità plasmatica1,3; in condizioni fisiologiche il rilascio di ADH è soppresso quando l’osmolarità plasmatica è <275 mOsm/kg. Inoltre, concentrazioni
di ADH aumentate si possono osservare in quadri
clinici diversi dalla SIADH, in cui si ha deplezione di liquidi. Molte classi di farmaci (tabella 1)
possono causare una SIADH, tramite il potenziamento dell’effetto dell’ADH sul rene o con azione
“ADH-like”. Nel nostro paziente, l’impiego di
FANS può aver aumentata l’azione dell’ADH a livello renale tramite la riduzione della sintesi locale delle prostaglandine, fisiologici inibitori dell’ADH.
La gestione della SIADH è multifattoriale. Oltre alla cura della patologia infettiva e, quando
possibile, di quella neoplastica e/o la sospensione
dei farmaci responsabili della SIADH, essa richiede, quando l’iponatriemia è sintomatica (generalmente con sodiemia ≤125 mEq/l), misure atte a normalizzare lentamente i livelli plasmatici
del sodio. La terapia comprende diversi approcci
in base alla gravità dell’iponatriemia ed alla velocità del suo instaurarsi. In pazienti asintomatici con lieve iposodiemia spesso non è necessaria
alcuna terapia, ma solo la sospensione dei farmaci potenzialmente responsabili. A tale riguardo il
concetto di “iponatriemia asintomatica” è stato
posto in discussione ed attualmente non accettato, da quando è stato evidenziato come questa alterazione elettrolitica predisponga alle cadute (e
quindi a possibili fratture) ed a deficit di attenzione negli anziani12. Se i sintomi sono lievi, in assenza di farmaci interferenti, si ricorre alla restrizione idrica (500-800 ml H2O/die, o più precisamente calcolando la quantità di liquidi consentiti come: diuresi delle 24 h precedenti: –500 ml).
In presenza di sintomi rilevanti, specie a carico
del sistema nervoso centrale, si ricorre all’infusione di salina ipertonica 3%.
L. Foppiani et al.: Severa iponatriemia secondaria a sindrome da inappropriata secrezione di ormone antidiuretico
Si deve prestare particolare attenzione a non
provocare aumenti della sodiemia >10-12 mEq/24
h (>8 mEq/24 h in presenza di ipopotassiemia, alcolismo, malnutrizione, gravi epatopatie) per il
conseguente rischio di disidratazione osmotica cellulare cerebrale con mielinolisi pontina2-4. Questa
terapia necessita di un monitoraggio accurato della sodiemia e va sospesa al raggiungimento di una
sodiemia di 120-125 mEq/l. A tale riguardo, esistono varie formule utili nel calcolare a) la quantità di
sodio da infondere; b) le variazioni della sodiemia
dopo infusione di salina ipertonica; c) la velocità di
infusione della soluzione ipertonica (tabella 2).
Recentemente, una nuova classe farmacologica
è a disposizione per il trattamento della SIADH:
gli antagonisti selettivi non peptidici del recettore
V2 dell’ADH o acquaretici, denominati vaptani, di
cui nel nostro paese è a disposizione il tolvaptan,
con l’indicazione terapeutica per le iponatriemie
euvolemiche13-15. L’avvio della terapia, a posologie
variabili tra 7,5-30 mg/die per os, deve avvenire in
regime ospedaliero, data la necessità di uno stretto monitoraggio della volemia e della sodiemia.
Tabella 2. Formule comunemente utilizzate per un’appropriata
terapia con soluzione ipertonica nell’iponatriemia.
Deficit di Na+= ACT x (125- Na+ attuale)
Variazione di Na+ dopo infusione di soluzione ipertonica =
Na+ infuso – Na+ sierico/ACT + 1
V. infusione salina ipertonica (ml/h):
peso corporeo x incremento Na/h desiderato
Legenda: ACT= acqua corporea totale: peso corporeo x 0,6 (maschio), peso corporeo x 0,5 (femmina), peso corporeo x 0,45 (anziano); V = velocità.
Nel caso da noi descritto, in base alle variazioni nel tempo del quadro clinico, sono state utilizzate le tre modalità terapeutiche disponibili per il
trattamento della SIADH.
Inizialmente, comunque, durante la gestione
notturna all’ingresso da parte del medico di guardia, è stata infusa soluzione fisiologica. Questa
strategia è spesso utilizzata in pazienti in cui non
è semplice la distinzione tra ipovolemia (magari
modesta) ed euvolemia in quanto costituisce un
trattamento di prima linea più affidabile della restrizione idrica, in grado di esacerbare un’iponatriemia ipovolemica non diagnosticata inizialmente. Successivamente, visto il severo quadro neurologico, è stata infusa salina ipertonica; con il miglioramento clinico è stata, poi, messa in atto la restrizione idrica ed infine, per la scarsa compliance
a questo regime, il tolvaptan a basse dosi. Il vaptanico ha consentito la normalizzazione della soIndirizzo per la corrispondenza:
Dott. Luca Foppiani
Ente Ospedaliero Ospedali Galliera
Struttura Complessa Medicina Interna
Mura delle Cappuccine, 14
16128 Genova
E-mail: [email protected]
diemia e del quadro clinico; alla sospensione, la sodiemia è rimasta nella norma.
In conclusione, la SIADH, una patologia di frequente riscontro nei pazienti ospedalizzati, deve
essere sempre ricercata nella diagnostica differenziale delle iponatriemie. I vaptani offrono una nuova ed efficace possibilità nel trattamento di questa
sindrome multifattoriale.
Bibliografia
1. Hannon MJ, Thompson CJ. The syndrome of inappropriate antidiuretic hormone: prevalence, causes
and consequences. Eur J Endocrinol 2010; 162 (suppl 1): S5-S12.
2. Sherlock M, Thompson CJ. The syndrome of inappropriate antidiuretic hormone: current and future
management options. Eur J Endocrinol 2010; 162
(suppl 1): S13-S18.
3. Peri A, Pirozzi N, Parenti G, Festuccia F, Menè P.
Hyponatremia and the syndrome of inappropriate
secretion of antidiuretic hormone (SIADH). J Endocrinol Invest 2010; 33: 671-82.
4. Adrogué HJ, Madias NE. Hyponatremia. N Engl J
Med 2000; 342: 1581-9.
5. Schwartz WB, Bennett W, Curelop S, Bartter FC. A
syndrome of renal sodium loss and hyponatremia
probably resulting from inappropriate secretion of
antidiuretic hormone. Am J Med 1957; 23: 529-42.
6. Bartter FC, Schwartz WB. The syndrome of inappropriate secretion of antidiuretic hormone. Am J
Med 1967; 42: 790-806.
7. Sunderam SG, Manikar GD. Hyponatraemia in the
elderly. Age Ageing 1983; 12: 77-80.
8. Gill G, Huda B, Boyd A, et al. Characteristics and
mortality of severe hyponatraemia: a hospital-based
study. Clin Endocrinol 2006; 65: 246-9.
9. Reddy P, Mooradian AD. Diagnosis and management
of hyponatraemia in hospitalised patients. Int J Clin
Pract 2009; 63: 1494-508.
10. Liamis G, Milionis H, Elisaf M. A review of drug-induced hyponatremia. Am J Kidney Dis 2008; 52:
144-53.
11. Gasco V, Prodam F, Pagano L, et al. Hypopituitarism
following brain injury: when does it occur and how
best to test? Pituitary 2012; 15: 20-4.
12. Renneboog B, Musch W, Vandemergel X, Manto MU,
Decaux G. Mild chronic hyponatremia is associated
with falls, unsteadiness, and attention deficits. Am J
Med 2006; 119: 71.e1-e8.
13. Thibonnier M. Vasopressin receptor antagonists in
heart failure. Curr Opin Pharmacol 2003; 3: 683-7.
14. Schrier RW, Gross P, Gheorghiade M, et al; SALT Investigators. Tolvaptan, a selective oral vasopressin
V2-receptor antagonist, for hyponatremia. N Engl J
Med 2006; 355: 2099-112.
15. Esposito P, Piotti G, Bianzina S, Malul Y, Dal Canton
A. The syndrome of inappropriate antidiuresis: pathophysiology, clinical management and new therapeutic
options. Nephron Clin Pract 2011; 119: c62-c73.
115