UNIVERSITA’ LA SAPIENZA DI ROMA
POLICLINICO UMBERTO PRIMO
MASTER UNIVERSITARIO DI SECONDO
LIVELLO IN TERAPIA INTENSIVA
NEONATALE E PEDIATRICA
TACHICARDIA PAROSSISTICA
SOPRAVENTRICOLARE,
DESCRIZIONE DI UN CASO
CLINICO
Dr.ssa Magi Letizia
T.I.N. Ospedale S. Donato di Arezzo
Anno Accademico 2009-2010
ARITMIE SOPRAVENTRICOLARI
Con il termine di aritmie sopraventricolari s’intendono quelle anomalie del
ritmo che originano a livello degli atri e/o della giunzione atrioventricolare.
Sono i disturbi del ritmo in assoluto più frequenti in età pediatrica.
A tale categoria appartengono l’extrasistolia atriale e giunzionale, le
tachicardie sopraventricolari, il flutter e la fibrillazione atriale.
TACHICARDIE SOPRAVENTRICOLARI
Le
tachicardie
sopraventricolari
rappresentano
sicuramente
l’aritmia
complessa di più frequente riscontro in età pediatrica.
Il concetto che la tachicardia sopraventricolare potesse essere causata da un
meccanismo di rientro a livello del nodo AV è stato proposto per la prima
volta da Barker et al nel 1943. Gli autori non erano in grado di confermare
tale concetto per le scarse risorse tecniche investigative. Ci sono voluti circa
30 anni rima che gli studi di elettrofisiologia cardiaca diventassero una
routine clinica, per poter definire i meccanismi elettrofisiologici alla base
delle tachiaritmie.
INCIDENZA
La tachicardia sopraventricolare (SVT) è osservata nei pazienti pediatrici con
un’incidenza di 0,1-0,4%. Sebbene la tachicardia parossistica atrioventricolare
sia il meccanismo più frequente, la tachicardia atriale ectopica rappresenta il
5-20% delle SVT in età pediatrica.
2
Generalmente le TSV si manifestano in soggetti senza altre patologie
cardiache, nel caso di soggetti cardiopatici le anomalie di più frequente
riscontro sono: la malattia di Ebstein che nel 30% dei casi si accompagna a
vie accessorie spesso multiple, il prolasso della mitrale e infine alcune
cardiopatie congenite operate e tra queste prevalente la trasposizione dei
grossi vasi arteriosi corretta con la tecnica di Mustrd o Senning e il cuore
univentricolare o altre anomalie complesse operate con intervento di Fontan.
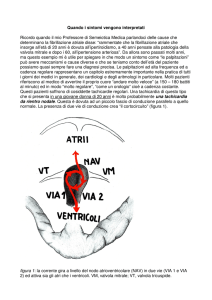
MECCANISMO FISIOPATOLOGICO
In base al meccanismo elettrofisiologico che è alla loro base, le tachicardie
sopraventricolari
vengono suddivise in forme da rientro, da anormale
automatismo e da automatismo triggerato.
Si parla di rientro quando lo stimolo elettrico viene condotto per più di una
volta in un circuito chiuso. Questo per potersi realizzare richiede la presenza
di un substrato anatomofunzionale capace di essere attivato da appropriati
stimoli, ad esempio battiti ectopici. Tale substrato deve essere costituito da
due vie con le seguenti caratteristiche: differente durata dei periodi refrattari,
comparsa di blocco unidirezionale su di una via, contemporaneo
rallentamento della velocità di conduzione sull’altra via.
3
I circuiti di rientro possono avere varia estensione e utilizzare più strutture
cardiache. Infatti, possono essere limitate a poche fibre miocardiche nel
contesto degli atri o della giunzione atrio ventricolare (micro rientri), oppure
essere più estesi e interessare da una parte il normale asse di conduzione
nodohissiano e dall’altra vie accessorie atrioventricolari (macrorientri). Le vie
accessorie atrioventricolari sono la causa più frequente di tachicardia
sopraventricolare a esordio in età pediatrica, mentre è decisamente ridotta
rispetto alla popolazione adulta l’incidenza di tachicardia sopraventricolare da
doppia via nodale.
Le vie accessorie sono alla base sia della sindrome di Wolf-ParkinsonWithe sia molto più raramente di una forma molto particolare nota come
Tachicardia Permanete Giunzionale Reciprocante che è caratteristica dell’età
pediatrica. Questa dipende da una sottile via accessoria a sede settale in cui lo
stimolo è condotto molto lentamente e solo in senso retrogado, tale
caratteristica elettrofisiologica rende l’aritmia usualmente incessante.
Le vie accessorie sono costituite da fasci di miocardio comune, variamente
disposti a cavallo dell’anello fibroso mitralico e/o tricuspidale, che
permettono di bypassare l’asse nodohissiano sia in senso a anterogrado , e in
questo caso facilmente identificabili sull’ECG di superficie in ritmo sinusale
per la presenza di PR breve e onda delta, sia in senso retrogrado. Le vie
accessorie possono avere una conduzione anterograda e retrograda oppure
solo retrograda, le cosiddette vie occulte. Entrambi i tipi di vie predispongono
all’innesco e al mantenimento delle tachicardie sopraventricolari.
L’automatismo anormale è una proprietà che in condizioni fisiologiche è
posseduta solo dal nodo del seno e dal tessuto di conduzione. L’automatismo
consiste nella depolarizzazione diastolica lenta e spontanea sino a raggiungere
il potenziale soglia che condiziona quindi la comparsa del potenziale
d’azione. La frequenza di attivazione decresce dal nodo del seno, che
4
rappresenta il segnapassi del cuore, alle fibre di Purkinje ventricolari. In
determinate situazioni, come in seguito a un danno miocardico, oppure come
conseguenza di modificazioni dei liquidi extracellulari, o più frequentemente
senza una ragione conosciuta, alcune cellule cardiache possono acquisire la
proprietà dell’automatismo e, se dotate di una frequenza maggiore di quella
sinusale, divenire il principale pacemaker del cuore.
Le tachicardie sopraventricolari possono essere atriali o giunzionali. Delle
giunzionali se ne conoscono due forme: una idiopatica molto rara e l’altra
relativamente più frequente che complica l’immediato postoperatorio
cardochirurgico.
Le forme automatiche sono caratteristiche dell’età pediatriche hanno, per le
loro caratteristiche elettrofisiologiche, un andamento incessante.
L’automatismo triggerato si ha quando le fibre miocardiche presentano una
depolarizzazione diastolica (automatismo)indotta da uno stimolo (trigger). La
depolarizzazione diastolica è nota come potenziale tardivo
e, se
sufficientemente ampio e tale da raggiungere la soglia, potrà provocare la
comparsa di potenziali d’azione ripetitivi e auto mantenersi. Questo
meccanismo è raramente alla base della tachicardia sopraventricolare a
esordio nell’età pediatrica, mentre è più frequentemente responsabile di una
forma di tachicardia ventricolare nota come tachicardia fascicolare.
Il meccanismo elettrofisiologico che è alla base delle singole tachicardie
sopraventricolari condiziona anche la loro risposta ai tentativi d’induzione e
d’interruzione delle tachicardie durante studio elettrofisiologico. Così le
forme da rientro e triggerate sono inducibili e interrompibili, mentre quelle da
aumentato automatismo non sono né inducibili né interrompibili, ma possono
essere catturate solo se si stimola l’atrio ad una frequenza maggiore di quella
della tachicardia.
5
6
QUADRO CLINICO
L'espressione clinica delle aritmie dipende fondamentalmente dagli effetti che
l'aritmia stessa produce sulla gittata cardiaca, dalla presenza di una sottostante
patologia cardiaca e dall'età del bambino.
Come spesso accade nel corteo sintomatologico possiamo distinguere segni e
sintomi aspecifici (e quindi, spesso, subdoli) quali l'astenia, la riduzione
dell'appetito, la suzione inefficace, il dolore toracico ed altre manifestazioni,
invece, più specifiche quali il cardiopalmo, la sincope, l'arresto e
l'insufficienza cardiaca.
Spesso, però, anche di fronte a quelli che possono essere considerati segni e
sintomi di specifico indirizzo cardiologico ci troviamo a fare i conti con una
aspecificità eziologica “imbarazzante”. Basti pensare, ad esempio, che sia le
tachiaritmie che le bradiaritmie severe possono manifestarsi con un quadro
clinico molto simile; ne deriva che la diagnosi eziologica specifica non può
prescindere, nella maggior parte dei casi, da una documentazione ECG in
corso di evento acuto.
Nel feto un quadro di tachiaritmia parossistica sostenuta si associa spesso
all'evidenza di idrope fetale o insufficienza cardiaca congestizia acuta.
Nei lattanti e nei neonati le tachiaritmie decorrono in modo sostanzialmente
asintomatico fino all'evidenza di una compromissione emodinamica.
Nel bambino più grandicello sintomi di sospetto sono: il cardiopalmo, il
dolore toracico, il pallore, la dispnea e la nausea.
Tali manifestazioni cliniche spesso si evidenziano in presenza di condizioni
slatentizzanti quali la febbre, l'esercizio fisico e le condizioni di stress in
genere.
La tachicardia sopraventricolare è caratterizzata da esordio e cessazione
improvvisi; l’attacco può essere precipitato anche da una infezione acuta,
solitamente a riposo. Gli attacchi possono continuare solo per alcuni secondi o
7
persistere per ore. La frequenza cardiaca è solitamente superiore a 180
batt/min e occasionalmente può essere superiore a 300/min.
Tipicamente le tachicardie sopraventricolari hanno due picchi di insorgenza:
uno nel primo anno di vita e dopo i 7-9 ani di età. L’incidenza delle forme è
anch’essa dipendente dall’età, essendo alcuni tipi più comuni nei primi anni di
vita, come le tachicardie sopravenrticolari da via accessoria, e altre più
frequenti nell’adolescenza come le forme a doppia via nodale. L’età è inoltre
importante ai fini della modalità di presentazione: dopo i 2-3 annidi vita il
cardiopalmo e più raramente le sincopi e le presincopi rappresentano la
modalità di presentazione più comune, al di sotto dell’anno di vita invece la
sintomatologia è molto subdola e spesso di difficile inquadramento, per cui la
tachicardia a volte può venire riconosciuta solo in seguito alla comparsa di
scompenso cardiaco.
Nel lattante i sintomi premonitori di una tolleranza non ottimale dell’aritmia
sono le modificazioni dell’umore, la comparsa di pallore e le difficoltà ad
alimentarsi. Sebbene tale sintomatologia sia aspecifica e comune anche ad
altre patologie, se si manifesta in un lattante noto portatore di tachicardia
sopraventricolare deve far subito porre in diagnosi differenziale la presenta di
una tachiaritmia.
Tipi e caratteristiche ECG delle più comuni forme di tachicardia parossistica del bambino
RNAV
R WPW
Via occulta
TGRP
TAE
TG
Asse P
Non visibile
90-270
90-70
270-360
Qualsiasi
0-90
PR>RP
Si
Si
Si
No
No
BAV
FC
220
260
230
170
160
180
BAV
No
No
No
No
Si
Si
tipo
P
P
P
I
I
I
P: parossistico; I:incessante
8
Molto più raramente le tachicardie sopraventricolari possono essere
riconosciute occasionalmente. Questo avviene essenzialmente per le forme
automatiche del lattante dove la tachicardia ha valori di frequenza cardiaca
usualmente compresi tra 180 e 200 batt/min e quindi risulta essere ben
tollerata molto più a lungo delle forme reciprocanti che hanno frequenze
cardiache molto più elevate.
Le tachicardie sopraventricolari quindi possono essere sospettate in base sia
alla sintomatologia sia in seguito al riconoscimento di valori elevati di
frequenza cardiaca all’esame obiettivo. La conferma della presenza di una
tachiaritmia può essere ottenuta però solo con l’elettrocardiogramma.
Usualmente la tachicardia sopraventricolare si presenta come una tachicardia
a QRS stretto con valori di FC compresi tra 180 e 320 batt/min. Sebbene
l’aberranza di conduzione sia frequente nei primi battiti della tachicardia, il
riscontro di un QRS largo deve sempre far sospettare una tachicardia
ventricolare.
A) tachicardia sinusale con normale morfologia delle onde P, (B) con SVT anomalo asse dell'onda P.
9
Entrambi ECGsare da neonati.
Nell’analisi del tracciato elettrocardiografico particolare attenzione andrà
posta nella ricerca dell’onda P per definire sia la morfologia sia i rapporti con
il QRS. Infatti questi due elementi associati ai valori di FC usualmente sono
sufficienti a permettere la diagnosi differenziale tra le varie forme di
tachicardia sopraventricolare. E’ molto importante anche l’analisi del
tracciato una volta ristabilito il ritmo sinusale , in quanto potrebbe rendersi
manifesta una sindrome di Wolf-Parkinson-Withe.
Figura pag 294
La valutazione del paziente con tachicardia sopraventricolare deve sempre
comprendere lo studio ecocardiografico per valutare la presenza di e il grado
d’impegno di un’eventuale cardiopatia, nonché le ripercussioni emodinamiche
della tachicardia, soprattutto se ad andamento incessante.
L’Holter e la prova da sforzo andranno riservate ai pazienti con forme
croniche nei quali è importante avere dati basali per valutare l’efficacia della
terapia. La stimolazione atriale trans esofagea (SATE) andrà eseguita nei
pazienti con tachicardia sopraventricolare da rientro nei quali non è stato
possibile definire il circuito che ne è alla base, nei pazienti con sintomatologia
suggestiva di tachicardia sopraventricolare che però non è mai stata
documentata in quanto a rapida risoluzione ed infine nei pazienti con
sindrome di WPW per una precisazione del rischio aritmico.
10
TRATTAMENTO:
La terapia delle tachicardie sopraventricolari può essere acuta con lo scopo di
interrompere l’aritmia, oppure cronica per prevenire le recidive.
TERAPIA ACUTA: manovre vagali, farmaci antiaritmici
oppure terapia
elettrica.
Manovre vagali: le più comuni sono rappresentate dalla compressione del
seno carotideo, dalla manovra di Valsalva sono solitamente inefficaci sotto i
2-3 anni di vita. La compressione dei bulbi oculari, frequentemente utilizzata
nell’adulto, non dovrebbe invece venire impiegata nel bambino e in
particolare nel lattante in quanto potenzialmente lesiva per la retina. Nel
primo anno di vita il diving reflex rappresenta la manovra vagale di più
frequente impiego. Tale manovra viene eseguita comprimendo sul naso e
sulla bocca del bambino un contenitore di gomma riempito di ghiaccio, per
circa 15-20 secondi. Il diving reflex è ripetibile e deve essere eseguito sotto
monitoraggio del ritmo cardiaco; la sua efficacia è massima nel trattamento
delle forme reciprocanti/parossistiche di recente insorgenza. Il divin reflex è
un riflesso primordiale che comporta un’attivazione vagale massima in
seguito alla stimolazione con freddo dei recettori periorali e perinatali, la sua
efficacia si riduce drasticamente dopo l’anno di età.
Terapia farmacologica: attualmente sono molti i farmaci antiaritmici che
possono essere utilizzati nel trattamento della tachicardia sopraventricolare.
La scelta è strettamente dipendente dal tipo di meccanismo elettrofisiologico
che è alla base della tachicardia. Le forme da rientro in genere rispondono
molto bene sia a farmaci come ATP, Adenosina e Verapamil che
11
essenzialmente bloccano il seno atrio-ventricolare sia al Propafenone e alla
Flecainide che agiscono sul nodo AV e sulle vie accessorie.
Tra questi farmaci la preferenza dovrebbe essere data all’ATP e all’Adenosina
poiché hanno una brevissima emivita inferiore a cinque minuti, da un lato
sono così facilmente ripetibile e dall’altro non preclude l’impiego di atri. Non
hanno inoltre effetto inotropo negativo per cui sono particolarmente utili in
corso di scompenso.
Trattamento con Adenosina :Si tratta di un farmaco a breve emivita in grado
di indurre un blocco farmacologico a livello dei nodi SA e AV. Va
somministrata in bolo e.v. rapido (con successivo lavaggio con 2.5-5 cc SF)
alla dose iniziale di 0.1 mg/kg che può essere poi aumentata a 0.2 mg/kg.
L'efficacia del farmaco si dimostra con un brusco rallentamento della FC,
talora con l'evidenza di una breve fase di asistolia, seguita da una rapida
ripresa della normale attività cardiaca.
Sotto l’anno di vita è sconsigliato l’uso del Verapamil in quanto è stato
descritto provocare dissociazione elettromeccanica comunque reversibile con
la somministrazione endovenosa di calcio gluconato.
Nelle tachicardie sopraventricolari automatiche invece è raro dover ricorrere
alla terapia acuta a meno che il paziente non sia in scompenso cardiaco o in
casi di insorgenza nell’immediato periodo post-operatorio cardioghirurgico.
In questi casi è preferibile l’utilizzo di Amiodarone, Beta-bloccanti e Digitale
anche in associazione. Nella tachicardia giunzionale post-operatoria la terapia
più efficace è risultata la riduzione della temperatura corporea a valori di 3135°C.
Lo scopo della terapia acuta è quello di ridurre la frequenza cardiaca a valori
compresi tra 130-140 batt/min, in tali alterazioni del ritmo è molto difficile
ottenere in modo acuto il ripristino stabile del ritmo sinusale.
12
Nei casi in cui non si ottiene ripristino del ritmo sinusale con la terapia
farmacologica si ricorre nelle forme di tachicardia sopraventricolare da rientro
alla SATE oppure alla cardioversione elettrica sincronizzata (0.5 – 1 J/Kg).
. ******aggiungere protocollo
TERAPIA CRONICA:
Il tipo di trattamento dipende dal tipo di tachicardia. Nelle forme da rientro,
dopo che la tachicardia è stata interrotta la decisione se iniziare un trattamento
cronico dipende da numerosi fattori: età d’esordio durata e sintomatologia
della tachicardia, caratteristiche elettrofisiologiche del substrato aritmico.
In caso di indicazione alla terapia cronica, il farmaco di scelta dipende dal
tipo di rientro (forme dipendenti da via accessoria, forme a doppia via nodale.
SINDROME DI WOLF-PARKINSON-WITHE
Tale sindrome è dovuta alla presenza di fibre muscolari accessorie poste a
cavallo dell’anello mitralico e/o tricuspidale.
L’incidenza nella popolazione normale è pari allo 0,5-2‰. Nel 20-30 % dei
casi è associata a cardiopatia congenita, prevalentemente malattia di Ebstein
dove le vie accessorie sono generalmente multiple o a trasposizione delle
grosse vie arteriose congenitamente corretta. Il 50-60% dei soggetti pur
avendo una situazione di base predisponente all’innesco di tachicardia
sopraventricolare rimane asintomatico per tutta a vita. Il 40-50% dei soggetti
invece diverrà sintomatico per episodi di tachicardia sopraventricolare che
nell’età pediatrica ha due picchi d’incidenza: uno nei primi 3-6 mesi d’età
13
l’altro dopo i 7-8 anni. L’età d’insorgenza è importante ai fini dell’evoluzione
infatti nei soggetti con esordio precoce queste scompaiono stabilmente dopo il
primo anno di vita nel 60-70% dei casi. La possibilità di regressione
spontanea si riduce se l’esordio è stato tardivo.
La sindrome di Wolf-Parkinson-Withe può rendersi responsabile di morte
improvvisa per invasione elettrica dei ventricoli attraverso la via accessoria in
corso di flutter o fibrillazione atriale. L’incidenza di tale evenienza è molto
bassa pari a 2‰/anno nei pazienti sintomatici e 0,75‰/anno in quelli
asintomatici.
Tali pazienti possono essere determinati attraverso la
stimolazione transesogfagea che attualmente rappresenta il metodo valutativo
di prima scelta del paziente con sindrome di WPW.
Sindrome WPW. Si noti il breve intervallo PR e storpiato salita QRS (onda delta)
14
CASO CLINICO
Caterina B. è nata il 18.05.2008 a 41 settimane di età gestazionale
da II gravidanza
(1 precedente aborto spontaneo) decorsa con
ricovero alla 35° settimana per sospetto ritardo di crescita
intrauterina, eseguita amniocentesi risultata nella norma. Parto
distocico per applicazione di vacuum, ha avuto un buon
adattamento alla vita extrauterina; I.A. 9-10; peso Kg. 2,910.
Alla
prima
visita
è
evidenziata
all’esame
obiettivo
una
microretrognazia, ugula bifida e un lieve ipertelorismo.
A 24 ore di vita durante la visita pediatrica veniva segnalato un
ipertono degli arti inferiori e del tronco, era presente acrocianosi,
nella norma la restante obiettività clinica. Venivano prescritti esami
ematici di routine, cariotipo ( negativo), emogasanalisi ed era
prescritto il monitoraggio dei parametri vitali. Durante il
monitoraggio al nido si evidenziavano episodi di desaturazione e
cianosi periorale e quindi la neonata veniva ricoverata presso il
reparto di Patologia Neonatale.
All’ingresso in reparto erano richiesti l’Rx torace e l’ECG risultati
nella norma e un’ ecografia cardiaca che metteva in evidenza
apertura del dotto arterioso con shunt sinistro-destro, nella norma i
restanti reperti. E’ stata eseguita anche l’ecografia cerebrale che
diagnosticava un’agenesia parziale del corpo calloso.
A 48 ore di vita la neonata presentava difficoltà all’alimentazione,
scarsa suzione e aveva numerosi rigurgiti, per tale motivo erano
prescritti esami ematici risultati nella norma ( compresa la PCR),
15
un’urinocoltura, l’esame urine risultato positivo per nitriti e per
tanto veniva iniziata terapia antibiotica. (Urinocoltura era positiva
per Enterococco con carica > 1.000.000 ufc/Ml).
Nonostante la terapia antibiotica a largo spettro la neonata
presentava ancora difficoltà ad alimentarsi tanto che in gran parte
era alimentata a gavage e in nutrizione parenterale parziale
attraverso catetere venoso. Sono state eseguite anche un’ ecografia
dell’addome e dei reni che metteva in evidenza la normalità del
piloro per lunghezza e spessore e numerosi episodi di reflusso.
I reni, normali per morfologia e in sede, presentavano una normale
differenziazione corticomidollare ed iperecogenicità degli apici
midollari, vi era una pielectasia sinistra intraparenchimale con
diametro di 7 mm.
A 12 giorni vita nonostante l’ampio spettro della terapia antibiotica
e antireflusso la piccola aveva ancora numerosi rigurgiti e vomiti
con
variazione
dell’obiettività
addominale:
l’addome
era
intensamente meteorico anche se non dolente e nel profilo
ematochimico la PCR era in salita. Sospesa l’alimentazione
enterale, sono state eseguite colture di controllo( feci ed urine
risultate negative) e l’Rx addome era refertato con regolare
distribuzione del meteorismo intestinale. Su questi dati era stata
variata la terapia antibiotica fatta finora in base all’antibiogramma
della prima urinocoltura positiva per Enterococco.
A 13 giorni di vita la neonata si presentava molto irrequieta,
colorito pallido,
con rilievo di frequenza cardiaca > di 200
battiti/min., era febbrile e agli esami ematici era presente una
16
leucocitosi neutrofila e un ulteriore aumento della PCR ( valore
max. di 9,26 mg/dl).
Eseguito l’ECG era presente una tachicardia sopraventricolare con
Freq.cardiaca intorno a 250batt./min. ( ALLEGATO 1 E 2).
Il trattamento tempestivo era eseguito in bolo con adenosina e.v.
rapida ( 0,1 mg/kg) con cardioversione e rientro del ritmo sinusale.
La cardiologa eseguendo in seguito a questo episodio di tachicardia
sopraventricolare l’ecografia cardiaca dimostrava una variazione
del quadro cardiologico precedente. Il ventricolo sinistro era di
aspetto globoso, disfunzionante, con la presenza di numerose
trabecole e recessi a livello soprattutto della porzione media ed
apicale, con presenza di sangue negli spazi intertrabecolari.
L’aspetto del ventricolo destro era simile, la frazione di eiezione era
del 46%. Il dotto arterioso era chiuso, normali le strutture valvolari
e i ritorni venosi. Il quadro era compatibile con la diagnosi di
ventricolo sinistro Non-Compattato. (iniziata terapia con lanoxin)
Migliorate le condizioni generali con apiressia, con il netto
miglioramento dell’obiettività addominale la piccola Caterina
presentava al 20° giorno di vita variazione dell’esame neurologico.
A 20 giorni di vita aveva presentato 2 equivalenti convulsivi con
desaturazione importante e un 3° episodio di desaturazione con
ipertono generalizzato, cianosi diffusa, apnea, sguardo fisso risolto
con ventilazione in maschera. Era iniziato bolo di attacco con
fenobarbital con risoluzione della crisi convulsiva.
Eseguiva il giorno successivo EEG che mostrava anomalie
elettrografiche caratterizzate da un’attività parossistica di punte ed
onde
puntute
di
grande
ampiezza
17
localizzate
nei
settori
frontocentrali dei due emisferi con andamento indipendente dal
ritmo di fondo.
La neonata eseguiva anche la RM encefalo che confermava
l’agenesia parziale del corpo calloso con assenza dello splenio e del
rostro, nella norma le restanti strutture.
A questo punto era sospettata una malattia metabolica dato il
quadro neurologico e cardiaco degenerativo, erano stati fatti esami
di scrrening metabolici di I° e II° livello risultati nella norma.
Per tale motivo la piccola veniva trasferita presso l’Ospedale Meyer
per eseguire accertamenti metabolici di III° livello.
La piccola ha eseguito esami che hanno escluso una malattia
metabolica ma la consulenza genetica e l’esecuzione del cariotipo
con metodica F.I.S.H hanno fatto diagnosi di difetto genetico con
delezione del cromosoma 1………
La piccola Caterina attualmente a 2 anni e ½ presenta un importante
ritardo psicomotorio, è in terapia con depakin sosp., presenta
frequenti episodi di convulsioni febbrili.
Il quadro cardiologico è regredito tornando ad una struttura
ventricolare normale.
18
19
20
FONTI BIBLIOGRAFICHE
• Behrman, Kliegman, Jenson. “Nelson- Textbook of Pediatrics” XVII
ed. Saunders
• D. Dubin “Rapida interpretazione dell'E.C.G” quarta ed. italiana, Ed.
Marrapese Roma
• Kasper, Braunwald, Fauci, Hauser, Longo, Jameson. “Harrison's
Principles of Internal Medicine” 16th Edition, Mc Graw Hill
• Società Italiana di
Emergenza
e
Urgenza
Pediatrica,
Italian
Resuscitation Council – “EPLS- Pediatic Advanced Life Support” –
2006
• N. Carano, U. Squarcia. “Cardiologia Pediatrica” Ed. McGraw-Hill.
Maggio 1998.
• Calabrò MP, Cerrito M, Luzza F, Oreto G. “Supraventricular
tachicardia in infants: epidemiology and clinical management” Curr
Pharm Des 2008; 14(8):723-8.
• Mark A, McGuire PhD. “Paroxysmal Supraventricular Tachycardia: a
centry of progress”
• Hamash CR, Crosson JE. “Emergenzy diagnosis and management of
paediatric arhythmias”. J Emerg Trauma Shock. 2010 Jul; 3(3):25-60
• Vignati
G,
Annoni
G.
“Characterization
of
supraventricular
tachycardia in infants: clinical and instrumental diagnosis”. Curr
Pharm Des. 2008;14(8):729-35.
• Goldman LE, Boramanand NK, Acevedo V, Gallagher p, Nehgme R.
“Preterm infants with paroxysmal supraventricular tachycardia:
presenatation, response therapy and outome” J Interv Card
Electrophysiol. 2001 Sep;5(3):293-7.
• Blomström-Lundqvist C, Scheinman MM, Aliot EM, Alpert JS, Calkins H,
Camm AJ, Campbell WB, Haines DE, Kuck KH, Lerman BB, Miller DD,
21
Shaeffer CW, Stevenson WG, Tomaselli GF, Antman EM, Smith SC Jr,
Alpert JS, Faxon DP, Fuster V, Gibbons RJ, Gregoratos G, Hiratzka LF,
Hunt SA, Jacobs AK, Russell RO Jr, Priori SG, Blanc JJ, Budaj A, Burgos
EF, Cowie M, Deckers JW, Garcia MA, Klein WW, Lekakis J, Lindahl B,
Mazzotta G, Morais JC, Oto A, Smiseth O, Trappe HJ; European Society of
Cardiology Committee, NASPE-Heart Rhythm Society. “ACC/AHA/ESC
guidelines for the management of patients with supraventricular arrhythmias-executive summary. a report of the American college of cardiology/American
heart association task force on practice guidelines and the European society
of cardiology committee for practice guidelines (writing committee to develop
guidelines for the management of patients with supraventricular arrhythmias)
developed in collaboration with NASPE-Heart Rhythm Society”.J Am Coll
Cardiol. 2003 Oct 15;42(8):1493-531.
• Bourgugnont A, Coremans C, Waucquez JL, Massin M. “Paroxysmal
tachyarrhithmiasin pediatrics”. Rev Med Liege 2004 May;59(5):3159.
22