NANOYOU Kit di Formazione sulle nanotecnologie per gli Insegnanti di studenti di età 14-18 anni
(Modulo esperimenti)
INTRODUZIONE PER GLI STUDENTI PER L’ESPERIMENTO A:
NANOMATERIALI NATURALI
Attorno a noi ci sono molti nanomateriali naturali e in questo esperimento imparerai che due di essi
sono materiali molto comuni: il latte e la gelatina. Le proprietà di questi materiali sono direttamente
collegate alla loro organizzazione supra-molecolare, che comprende le nanostrutture.
In questo esperimento:
1. Preparerai la gelatina e la testerai con una penna laser per confermarne la natura colloidale.
2. Avrai la conferma che il latte è un colloide e lo tratterai con un acido per indurne l’aggregazione.
Questo esperimento ti darà la prova pratica del legame tra struttura e funzione, e di come la
manipolazione dell’organizzazione molecolare di un materiale, come il latte, porta a materiali con
colore, odore e gusto diversi!
INTRODUZIONE
Nanomateriali naturali
Molti materiali che appartengono al mondo naturale (animale e minerale) hanno proprietà risultanti
dalle loro insite nella loro nanostruttura.
L’interazione di luce, acqua e altri materiali con queste nanostrutture conferisce a questi materiali
naturali le notevoli proprietà che possiamo vedere con i nostri occhi. Queste nanostrutture traggono
origine dall’organizzazione supra-molecolare del materiale: da dieci a cento molecole organizzate in
forme e strutture nella gamma della nanoscala. Ogni giorno abbiamo centinaia di esempi di
nanoscienza davanti agli occhi, dai gechi che camminano a testa in giù su un soffitto, apparentemente
sfidando la forza di gravità, alle farfalle dai colori iridescenti, alle lucciole che brillano la notte.
Figura 1. Esempi di nanomateriali naturali. Dall’alto
a sinistra, in senso orario: una farfalla, la zampa di un
geco, foglie di nasturzio, latte (crediti iconografici: in
alto a sx. Wiki Commons, Creative Commons
Attribute ShareAlike 3; in alto a dx: A. Dhinojwala,
University of Akron, NISE network, ristampato sotto i
termini e le condizioni del network NISE; in basso a
sx: Wiki Commons, Creative Commons Attribute
ShareAlike 3; in basso a dx: iNANO, University of
Aarhus, Creative Commons Attribution ShareAlike
3.0)
Le ricerche che hanno portato a questi risultati sono state finanziate dal Settimo Programma Framework della Comunità
Europea (FP7/2007-2013), contratto di concessione n° 233433
Pagina 1 di 7
NANOYOU Kit di Formazione sulle nanotecnologie per gli Insegnanti di studenti di età 14-18 anni
(Modulo esperimenti)
In natura troviamo alcune straordinarie soluzioni a problemi complessi sotto forma di raffinate
nanostrutture cui sono associate precise funzioni.
In questo esperimento, i nanomateriali che analizzerai sono gelatina e latte. Entrambi sono colloidi. Un
colloide è un tipo di miscela chimica nella quale una sostanza viene dispersa uniformemente attraverso
un’altra, ma le particelle della sostanza dispersa sono solamente sospese nella miscela, non sono del
tutto dissolte in essa (a differenza di quanto avviene in un soluzione). Ciò avviene perché, in un colloide,
le particelle hanno dimensioni maggiori di quelle di una soluzione. In termini generali, un colloide è
composto di particelle che variano dai 10 ai 300nm. Queste particelle sono abbastanza piccole da poter
essere disperse uniformemente e mantenere un aspetto omogeneo, ma abbastanza grandi da
diffondere la luce. Le particelle in un colloide possono disperdersi così bene da assumere l’aspetto di
una soluzione (es. trasparente).
Un modo semplice per verificare se una miscela è una soluzione o un colloide è quello di illuminarla con
un raggio laser: la luce si diffonderà solo in presenza del colloide. AVVERTENZA: non puntare mai un
raggio laser vicino agli occhi, e non guardare mai direttamente nel raggio!
In questo esperimento ti renderai conto del fatto che senza queste nanostrutture, materiali comuni
come il latte perdono il loro aspetto e la loro funzione.
Gelatina
La gelatina è una sostanza solida insapore, derivata dal collagene presente nella pelle e nelle ossa degli
animali; è utilizzata come agente gelificante nei prodotti alimentari (torte, dolciumi, ecc.), nei prodotti
farmaceutici (es. capsule di gelatina), in quelli cosmetici e nella fotografia.
La gelatina è una proteina prodotta dalla parziale idrolisi del collagene presente nelle ossa, nei tessuti
connettivi, negli organi e in tratti dell’intestino dei mammiferi, come i maiali. Tuttavia, sta prendendo
piede anche la gelatina di pesce.
La gelatina si trova spesso in polvere. Quando mescolata con acqua, forma una soluzione ad alta
viscosità che quando si raffredda diventa un gel e forma un gel colloidale. Quando riscaldato, il gel di
gelatina si scioglie e diventa liquido, mentre si solidifica al raffreddamento. Pertanto, la sua esistenza in
forma di gel è limitata a una specifica finestra di temperatura.
IN COSA E’ “NANO”? Recenti studi con il microscopio a forza atomica (AFM) hanno rilevato che la
gelatina è in realtà formata da numerose nanostrutture che presentano varie forme a seconda del tipo
Le ricerche che hanno portato a questi risultati sono state finanziate dal Settimo Programma Framework della Comunità
Europea (FP7/2007-2013), contratto di concessione n° 233433
Pagina 2 di 7
NANOYOU Kit di Formazione sulle nanotecnologie per gli Insegnanti di studenti di età 14-18 anni
(Modulo esperimenti)
di gelatina analizzata. Per esempio, l’analisi AFM della gelatina estratta dalla pelle di pesce gatto
(Ictalurus punctatus) ha rivelato la presenza di pori anulari con diametri medi di 118 nm e nanoaggregati sferici con diametro attorno ai 260 nm. La presenza di queste nanostrutture dimostra che la
gelatina è un colloide e spiega il suo comportamento di diffusione della luce.
Figura 2. Queste immagini AFM di
gelatina di pesce gatto rivelano la
presenza di nanostrutture sferiche.
(Crediti iconografici: ristampata su
concessione di Wiley-Blackwell Publishing
Ltd from Yang et al., Journal of Food
Science (2006), 72(8), pp c430-c440,
copyright
(2006)
Wiley-Blackwell
Publishing Ltd.).
Latte
Il latte bovino contiene una serie di biomolecole, come i lipidi e le proteine, che si disperdono
nell’acqua. A seconda dell’alimentazione dell’animale, la quantità di proteine varia dal 2,5 al 3,5%, l’80%
delle quali sono caseine (le restanti sono proteine di siero di latte o di siero). Quattro proteine
compongono il gruppo delle caseine: α s1 -caseina, α s2 -caseina, β-caseina and k-caseina. Le caseine sono
caratterizzate dal fatto che sono fosfoproteine che precipitano a pH 4.6 (punto isoelettrico), al cui pH le
proteine di siero restano solubili. Un’altra proprietà delle caseine è la loro esistenza in quanto micelle di
caseina che variano dai 50 ai 300 nm. Le micelle contengono la caseina combinata con calcio, fosfato e
piccole quantità di citrato. Come tale, il latte è un colloide (una miscela di nanoparticelle disperse in
maniera uniforme ma solo sospese in un elemento liquido). La presenza di queste micelle determina il
colore bianco del latte, che si deve alla loro diffusione della luce.
DALLA STRUTTURA ALLA FUNZIONE
La finissima auto-organizzazione molecolare delle proteine e dei minerali nel latte è fondamentale per
eseguire la sua naturale funzione di trasporto del calcio dalla madre al figlio. Numerosi studi hanno
evidenziato che questa organizzazione dà origine a nanostrutture che hanno funzioni precise (micelle di
caseina). Nella prossima sezione descriveremo in che modo questa organizzazione è determinata dalle
interazioni elettrostatiche, ma anche dalle interazioni idrofobe fra le proteine che compongono il latte e
alcuni minerali ad esse associati. Senza questa raffinata organizzazione, il calcio non verrebbe
“intrappolato” nelle micelle del latte e non si avrebbe la funzione biologica del latte stesso.
Le ricerche che hanno portato a questi risultati sono state finanziate dal Settimo Programma Framework della Comunità
Europea (FP7/2007-2013), contratto di concessione n° 233433
Pagina 3 di 7
NANOYOU Kit di Formazione sulle nanotecnologie per gli Insegnanti di studenti di età 14-18 anni
(Modulo esperimenti)
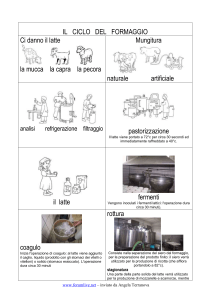
LAVORAZIONE DEL LATTE
La lavorazione del latte con diversi trattamenti è ampiamente usata nell’industria casearia. Per
esempio, lo yogurt è prodotto dal latte fermentato ottenuto con la crescita controllata di specifici
microrganismi, per lo più batteri che convertono il lattosio (zucchero del latte) in acido lattico.
Abbassando il pH del latte, cambiano gusto e consistenza. Nella produzione del formaggio, gli enzimi
vengono utilizzati per indurre l’aggregazione e la precipitazione delle caseine. Come vedremo nella
prossima sezione, in tutti i metodi di lavorazione del latte, l’organizzazione molecolare delle caseine
viene alterata, il che porta a inspessimento, precipitazione e altri effetti. L’aspetto, il gusto e altre
“macro” proprietà del latte sono profondamente connesse alla sua (nano) struttura supra-molecolare.
In questo esperimento userai l’aceto (una fonte di acido) e il calore per alterare le proprietà del latte.
CASEINE
La caseina del latte (che ha un pH vicino alla neutralità, circa 6,7) viene caricata negativamente (l’I.P. è
4,6). Tutte le caseine, fatta eccezione per la k-caseina, hanno la capacità di legarsi al Ca2+, il che avviene
soprattutto attraverso i fosfati residui. Il legame del Ca2+ è fondamentale affinché il latte adempia alla
sua funzione, cioè quella di trasportare il calcio (e altri nutrienti) dalla madre al figlio. Ciascuna caseina è
composta da una diversa sequenza peptidica e pertanto ha una diversa struttura secondaria e terziaria.
MICELLE DI CASEINA: STRUTTURA E FUNZIONE
Si ritiene che, nel latte, le caseine esistano in forma di micelle di caseina, che variano tra i 50 e i 300 nm.
Le micelle contengono le caseine combinate con calcio, fosfato e piccole quantità di citrato. La
struttura delle micelle di caseina (come quella della caseina stessa) è ancora oggetto di dibattito e
intensa ricerca. Dal momento che tutte le caseine sono dotate di una regione idrofobica e di una polare,
si ritiene che le interazioni idrofobiche e quelle elettrostatiche svolgano un ruolo nell’auto-associazione
delle caseine per formare le micelle di caseina. Le micelle di caseina si differenziano dai polimeri delle
caseine individuali per un motivo fondamentale: contengono fosfato di calcio inorganico, che esiste in
forma di piccole inclusioni microcristalline chiamate nanocluster di calcio. Che la stabilità delle micelle di
caseina non sia dovuta soltanto all’interazione elettrostatica è stato dimostrato dal fatto che le micelle
di caseina possono essere dissociate usando l’urea, un agente non interrompe le associazioni del
fosfato di calcio.
Sono stati postulate due tipi di associazioni fra le micelle di caseina:
- La prima è idrofobica, e si ha quando due o più regioni idrofobiche di diverse molecole (α-caseine e β
caseine) formano un cluster legati. Queste sono indicate come una barra rettangolare in Figura 4.
Le ricerche che hanno portato a questi risultati sono state finanziate dal Settimo Programma Framework della Comunità
Europea (FP7/2007-2013), contratto di concessione n° 233433
Pagina 4 di 7
NANOYOU Kit di Formazione sulle nanotecnologie per gli Insegnanti di studenti di età 14-18 anni
(Modulo esperimenti)
- Le seconda associazione è di regioni idrofile caricate che
contengono cluster di fosfoserina che si legano ai nanocluster di
fosfato di calcio colloidale (indicati con CCP in Figura 4).
Le k-caseine non hanno il gruppo della fosfoserina per legarsi
con i nanocluster di calcio; pertanto, la loro associazione è
possibile solo attraverso interazioni idrofobiche. Inoltre, le
micelle non possono espandersi oltre le k-caseine, che pertanto
agisce come rivestimento esterno della micella. Il ruolo delle kcaseine è quello di stabilizzare le micelle di caseina, evitando
una crescita eccessiva e l’aggregazione micellare, che altrimenti
porterebbe all’aggregazione.
Figura 3. Modello di doppio legame nelle
micelle di caseina, con le a, b e k-caseine
raffigurate come indicato. Ristampato da:
Horne D.S., Inter. Dairy Journal (1998), 8
(3), 171-177, su autorizzazione di Elsevier.
DISSOCIAZIONE E AGGREGAZIONE DELLE MICELLE DI CASEINA
Come descritto più sopra, si ritiene che le micelle di caseina abbiano un’intricata struttura che è
un’azione reciproca di reazioni idrofobiche ed elettrostatiche. Il mantenimento dell’integrità micellare è
un atto di equilibratura, ed esistono diversi metodi per rompere questo equilibrio. Questi metodi sono
ampiamente utilizzati nell’industria casearia per produrre il formaggio e i prodotti fermentati come lo
yogurt.
- aumentare il pH (a circa 8) porta la dissociazione delle micelle di caseina, e l’effetto che si ottiene è
che il latte scaldato diventa traslucido. La ragione di questo fenomeno è che aumentare il pH dalla
neutralità che si presenta in natura converte i gruppi di fosfoserile da unità singolarmente caricate a
unità a carica doppia, che non sono più in grado di legare i nanocluster di fosfato di calcio. L’aumentata
carica negativa delle micelle induce la repulsione elettrostatica, e le micelle si dissociano.
- diminuire il pH al punto isoelettrico (4,6) induce la dissociazione delle micelle di caseina. Ciò è dovuto
al fatto che le micelle di calcio esistono solo in ragione della presenza del fosfato di calcio; pertanto, la
sua dissoluzione causa necessariamente dei cambiamenti nella stabilità delle micelle. Se un acido (un
donatore di protoni) viene aggiunto al latte, i gruppi fosfoserile e carbossile nelle proteine diventano
protonati, quindi non sono più in grado di interagire elettrostaticamente con i nanocluster di fosfato di
calcio, e questi vengono rilasciati dalle micelle. Occorre notare che ciò non fa necessariamente in modo
che le caseine si dissocino dalle micelle. A temperature inferiori a 25°C, si ha un aumento della
Le ricerche che hanno portato a questi risultati sono state finanziate dal Settimo Programma Framework della Comunità
Europea (FP7/2007-2013), contratto di concessione n° 233433
Pagina 5 di 7
NANOYOU Kit di Formazione sulle nanotecnologie per gli Insegnanti di studenti di età 14-18 anni
(Modulo esperimenti)
dissociazione, altrimenti le caseine rimangono all’interno delle micelle. Questo effetto sarà testato
nell’esperimento con l’aggiunta di aceto (una fonte di acido) al latte freddo. La ragione di questo
fenomeno sta nel fatto che la stabilità delle micelle di caseina non è connessa esclusivamente
all’interazione elettrostatica, ma anche alle interazioni idrofobiche. Queste ultime sono estremamente
sensibili alla temperatura: le interazioni idrofobiche sono più forti a temperature più elevate. Pertanto,
le interazioni idrofobiche mantengono la stabilità delle micelle di caseina nel latte freddo anche
quando il suo pH è stato abbassato al punto isoelettrico. Dall’altra parte, se l’acidificazione avviene
dopo che il latte è stato scaldato (a circa 60°C), le micelle vengono dissociate (il fosfato di calcio viene
rilasciato dalla micella) e si aggregherà a causa delle accresciute forze elettrostatiche e dell’aumentata
interazione idrofobica. Questo verrà testato nell’esercizio con l’aggiunta di aceto al latte caldo o freddo.
- L’attacco della chimosina porta alla precipitazione delle micelle e alla formazione della cagliata.
Questo processo viene utilizzato nella produzione del formaggio. La chimosina è un enzima che
costituisce il principio attivo del presame, un estratto dello stomaco del vitello utilizzato nella
produzione del formaggio. La chimosina attacca specificamente un legame singolo nella k-caseina. Come
già detto, la presenza delle k-caseine è fondamentale per la stabilità generale della micella di caseina;
pertanto, la sua disgregazione fa sì che le micelle perdano stabilità, si aggreghino e infine formino la
cagliata.
- L’aggiunta controllata di batteri dell’acido lattico (batteri che producono acido lattico, come il
Lactobacillus, Lactococcus, e Leuconostoc) in specifiche condizioni di lavorazione permette di produrre
prodotti a base di latte fermentato come lo yogurt. Questo processo si differenzia dalla semplice
acidificazione dal momento che il latte è trattato a caldo e vengono incorporate anche le proteine del
siero. La coagulazione è indotta dall’acidificazione, ma questo non porta alla formazione della cagliata,
ma a un prodotto più viscoso del semplice latte.
COSA PUÒ INSEGNARE QUESTO ESPERIMENTO SULLE NANOTECNOLOGIE? Grazie a questo esercizio
imparerai due concetti fondamentali:
- Struttura significa proprietà fisiche (colore, odore, ecc.): i materiali nel mondo naturale “reale”, come
il latte, hanno l’aspetto che conosciamo in virtù delle loro raffinate nanostrutture. Il latte è bianco
perché contiene nanoparticelle colloidali (micelle). Se alteriamo la struttura di queste micelle, alteriamo
alcune “macro” proprietà del latte, come il colore e l’odore.
- Struttura significa funzione: i materiali naturali hanno funzioni specifiche, che sono dettate dalla
supra-organizzazione delle loro molecole (nanostrutture). Se alteriamo queste ultime, possiamo
Le ricerche che hanno portato a questi risultati sono state finanziate dal Settimo Programma Framework della Comunità
Europea (FP7/2007-2013), contratto di concessione n° 233433
Pagina 6 di 7
NANOYOU Kit di Formazione sulle nanotecnologie per gli Insegnanti di studenti di età 14-18 anni
(Modulo esperimenti)
ottenere un materiale con una nuova funzione. Nella produzione del formaggio, l’alterazione delle
micelle di caseina attraverso processi specifici (es. il trattamento con la chimosina o la fermentazione
con i batteri dell’acido lattico) porta a diversi prodotti (formaggio, yogurt ecc.). Questo è esattamente il
concetto delle nanotecnologie: progettare nuovi materiali con nuove funzioni a partire dalla
manipolazione della loro organizzazione molecolare.
Le ricerche che hanno portato a questi risultati sono state finanziate dal Settimo Programma Framework della Comunità
Europea (FP7/2007-2013), contratto di concessione n° 233433
Pagina 7 di 7