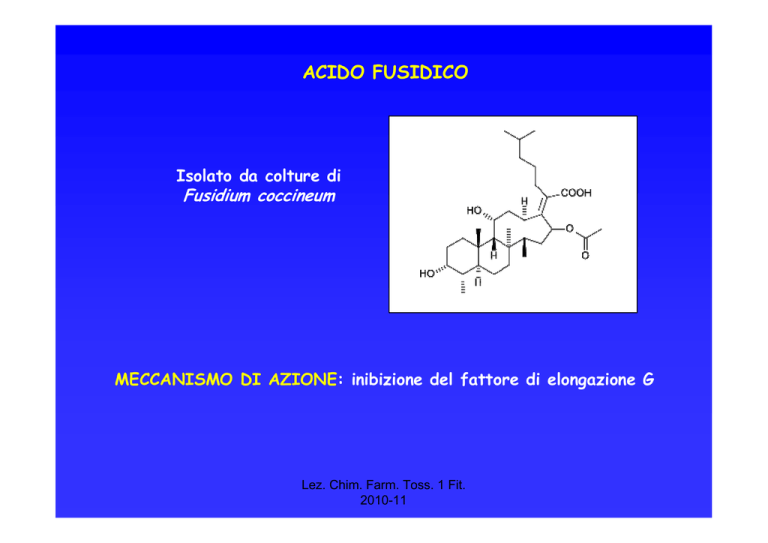
ACIDO FUSIDICO
Isolato da colture di
Fusidium coccineum
MECCANISMO DI AZIONE: inibizione del fattore di elongazione G
Lez. Chim. Farm. Toss. 1 Fit.
2010-11
MECCANISMO DI AZIONE DELL’ACIDO FUSIDICO
Linezolid
Fattori di
iniziazione
30S
30S &
mRNA
70S
Complesso
Iniziale
mRNA
50S
Terminazione
Peptidi
Puromicina
fMet-tRNA
Ciclo di
prolungamento
Lincosamidi
Macrolidi
Tetracicline
Cloramfenicolo
Aminoglucosidi
Streptogramine
Lez. Chim. Farm. Toss.
1 Fit.FUSIDICO
ACIDO
2010-11
Fattori di
prolungamento
SPETTRO D’AZIONE DELL’ACIDO FUSIDICO
Cocchi Gram + : S. epidermidis, S. aureus (anche MRSA)
Bacilli Gram + P. acnes, Corinebacterium
Anaerobi Gram + e Gram -: Bacteroides, C. difficile
Cocchi Gram -: N. gonnorrhoeae e meningitidis
Chlamidie, Mycoplasmi
Nessuna attività su Pseudomonas, Enterobatteri
UTILIZZO TERAPEUTICO
Infezioni cutanee, articolari, ossee e polmonari da Stafilococchi
(MRSA) in associazione con altri antibiotici
Infezioni da C. difficile
Infezioni cutanee da Corinebacterium
Lez. Chim. Farm. Toss. 1 Fit.
2010-11
SOMMINISTRAZIONE: orale, topica ed endovenosa
DIFFUSIONE TISSUTALE: buona su tutti i tessuti con eccezione
della prostata e liquor
t1/2: 5.5 h
ELIMINAZIONE
esclusivamente biliare in forme inattive
METABOLISMO
Elevato (95%) 4 metaboliti principali (dicarbossilico, chetonico,
idrossilico, glucuronide)
RESISTENZA
Mutazioni del fattore di elongazione (cromosomiche)
TOSSICITA’ ED EFFETTI COLLATERALI
Intolleranze gastroenteriche
Colestasi
Flebiti
Lez. Chim. Farm. Toss. 1 Fit.
Non somministrare in pazienti immunodepressi
e in gravidanza
2010-11
TETRACICLINE
H3C
Cl
H3C
CH3
N
OH
OH
C NH2
OH
OH
O
OH
O
Clortetraciclina
Isolata da Streptomyces
aureofaciens
O
Struttura 3D della Clortetraciclina
Lez. Chim. Farm. Toss. 1 Fit.
2010-11
MECCANISMO DI AZIONE DELLE TETRACICLINE
Legandosi alla subunità 30S inibiscono la sintesi proteica
impedendo l’ancoraggio del aminoacil t-RNA sul sito A
le tetracicline si legano al sito ribosomiale complessandosi con
ioni metallici
Debole inibizione della sintesi proteica sui ribosomi 80S
Azione Batteriostatica
Penetrazione cellulare: attraverso le porine (OmpF, OmpC)
complessandosi con cationi metallici mentre il passaggio
attraverso la membrana citoplasmatica avviene per trasporto
attivo
Lez. Chim. Farm. Toss. 1 Fit.
2010-11
CORRELAZIONE STRUTTURA-ATTIVITA’
H3C
R5
8
R4
9
10
11
OH
5
4
12a
1
6
7
12
O
N
R2
R3
CH3
OH
OH
OH
3
2
CONHR1
O
Requisiti fondamentali per l’attività
•OH sul C-3
•Il gruppo dimetilamminco in 4
•Sistema cheto-enolico in 11,12, 12a
•Sistema enolico in 1 e 3
•La funzione carbossamidica in 2
•Sono possibili sostituzioni sull’anello aromatico e sui carboni C-5, C-6
Lez. Chim. Farm. Toss. 1 Fit.
2010-11
SPETTRO D’AZIONE DELLE TETRACICLINE
Cocchi Gram+(aerobi e anaer.)
Staphylococcus sp, Streptococcus sp Peptococcus
sp, Peptostreptococcus sp
Bacilli Gram+(aerobi e anaer.)
B. anthracis, C. diphteriae, L. monocytogenes,
Propionibacterium sp, Cl. perfringes
Cocchi GramBacilli GramEnterobacteriaceae
altri Gram- fermentanti
altri Gram- non fermentanti
N. gonorrhoeae, N. mengitidis
Salmonella sp, Shigella sp, Yersinia sp
H. influenzae, H. ducreyi F. tularensis, P. multocida,
V. cholerae
Bordetella pertussis, Br. melitensis, Ps. mallei, Ps.
pseudomallei
ALTRI MICRORGANISMI
Spirochete
Rickettsie
Chlamydia
Mycoplasmi
T. pallidum, T. pertenue, B. recurrentis
Coxiella, Rickettsia
Chlamydia
M. pneumoniae
Lez. Chim. Farm. Toss. 1 Fit.
2010-11
IMPIEGO TERAPEUTICO
Attualmente l’impiego delle tetracicline è limitato a:
•H. ducreyi
•Brucella
•V. colerae
•Yersinia pestis
•Rickettsie
•Mycoplasmi
•Clamydia
•Propionibacterium acnes
Lez. Chim. Farm. Toss. 1 Fit.
2010-11
SOMMINISTRAZIONE E ASSORBIMENTO
L’assorbimento gastro-enterico è variabile tra il 95% (Dossiciclina) e il
30% (Clortetraciclina)
L’assorbimento è ridotto dalla presenza di ioni metallici (Mg, Al, Ca, Fe)
E’ possibile la somministrazione parenterale
La somministrazione topica è riservata alle infezioni oculari
La diffusione tissutale è elevata in tutti i tessuti compresi quelli ossei. Le
tetracicline non passano la barriera emato-encefalica
METABOLIZZAZIONE e ELIMINAZIONE
Scarsa per quasi tutte le tetracicline (fa eccezione la clortetraciclina)
L’eliminazione è in gran parte renale. Una piccola percentuale viene
eliminata per via biliare
Lez. Chim. Farm. Toss. 1 Fit.
2010-11
EFFETTI COLLATERALI
•Colite pseudomembranosa
•Colorazione dei denti
•Malformazioni ossee e fetali (sono consigliate a bambini con età >
8anni)
•Fotosensibilizzazione
•Possibile formazione di anidroderivati con epatotossicità
H3C
R5
R4
OH
H
H3C
CH3
N
R2
R5
R4
H
CH3
N
R2
OH
OH
CONHR1
OH
OH
O
OH
-H2O
OH
O
Lez. Chim. Farm. Toss. 1 Fit.
2010-11
CONHR1
OH
O
OH
O
RESISTENZA
Permeabilità:alterazione delle porine (ompF) e alterazione dello
strato lipopolissacaridico
Efflusso: eliminazione del farmaco nell’ambiente extracellulare
tramite proteine codificate da trasposoni e plasmidi
Ridotta affinità
ribosomiale S 10
del
bersaglio:
alterazione
Lez. Chim. Farm. Toss. 1 Fit.
2010-11
della
proteina
FARMACI
H3C
R5
8
R4
9
10
11
OH
5
4
12a
1
6
7
12
O
N
R2
R3
CH3
OH
OH
OH
3
2
CONHR1
O
TETRACICICLINE DI 1a GENERAZIONE
R1 = H; R2 = H; R3 = OH; R4 = CH3; R5 = Cl CLORTETRACICLINA
R1 = H; R2 = OH; R3 = OH; R4 = CH3; R5 = H OSSITETRACICLINA
R1 = H; R2 = H; R3 = OH; R4 = CH3; R5 = H TETRACICLINA
Sono tutte tetracicline naturali isolate da Streptomyces
Lez. Chim. Farm. Toss. 1 Fit.
2010-11
TETRACICLINE SEMISINTETICHE
A. Farmaci con modifiche che non interessano il gruppo carbossamidico
B. Farmaci con modifiche che interessano il gruppo carbossamidico
H3C
H
H3C
H
CH3
N
OH
OH
CONH2
OH
OH
O
OH
O
DOSSICLINA (BASSADO®)
Elevato assorbimento per os (liposolubile)
Elevata diffusione tissutale
Ridotta capacità di chelare il Ca++
t1/2 = 20 h
Impiegata anche nella profilassi della malaria
Lez. Chim. Farm. Toss. 1 Fit.
2010-11
MINOCICLINA (MINOCIN®)
Superiore assorbimento per os rispetto
alla dossiciclina
Elevata diffusione tissutale
Utilizzata anche per l’acne
Da evitare la somministrazione in pazienti
con insufficenza renale
t1/2 = 18 h
H3C
CH3
H3C
CH3
N
N
OH
CONH2
OH
O
OH
OH
O
B. Farmaci con modifiche che interessano il gruppo carbossamidico
ROLITETRACICLINA (BRISTACIN®)
Somministrazione parenterale (scarso
assorbimento per os)
t1/2 = 8 h
H3C
N
OH
H3C
CH3
OH
C NH CH2 N
OH
OH
O
Lez. Chim. Farm. Toss. 1 Fit.
2010-11
OH
O
O
TETRACICLINE DI 3a GENERAZIONE
GLICILCICLINE
VANTAGGI: maggiore potenza e resistenza all’efflusso rispetto alle tetracicline di
vecchia generazione
H3C
CH3
N
R
OH
R1
O
N
R2
NH
C NH2
OH
OH
O
OH
O
O
Struttura generale delle glicilcicline
Lez. Chim. Farm. Toss. 1 Fit.
2010-11
TIGECICLINA (TYGACIL®)
H3C
H3C
CH3
CH3
N
N
OH
O
H3C
H3C
NH
NH
CH3
C NH2
OH
OH
O
OH
O
O
La TIGECICLINA è stata approvata dalla FDA nel 2005 per il trattamento di:
•Infezioni complicate dei tessuti molli e della cute
•Infezioni complicate intraddominali
Uso esclusivo ospedaliero
Lez. Chim. Farm. Toss. 1 Fit.
2010-11
INTERAZIONI CON IL SITO RECETTORIALE DELLA SUBUNITA’ 30 S
Lez. Chim. Farm. Toss. 1 Fit.
2010-11