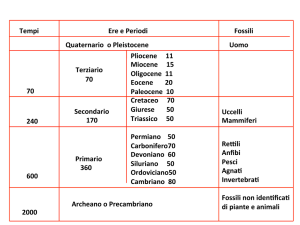
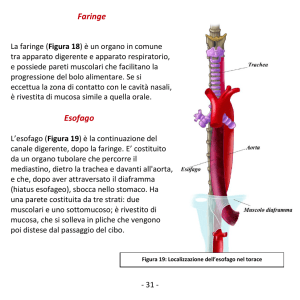
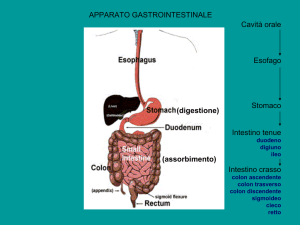
IL TUMORE DELL’ESOFAGO
Cenni di epidemiologia: il carcinoma dell’esofago rappresenta la settima causa di
morte per cancro in tutto il mondo, a testimonianza della sua elevata letalità
nonostante la sua non elevata incidenza.
La caratteristica epidemiologica più importante del carcinoma esofageo è la grande
variabilità di incidenza e distribuzione nelle diverse aree geografiche: aree
geografiche ad elevata incidenza sono spesso circondate da aree ad incidenza
significativamente più bassa, testimoniando la probabile presenza di fattori di rischio
ambientali non ancora ben conosciuti. Raro in Europa e negli Stati Uniti, ove
rappresenta l’1% di tutte le neoplasie maligne, presenta la sua maggiore incidenza
mondiale nelle regioni del Kazakistan nell’ex Unione Sovietica, il nord-est dell’Iran
nella regione del Mar Caspio, in Cina, Portorico e Singapore, ove la mortalità è
anche elevata.
Negli ultimi 20 anni, tuttavia, nel Nord America e nei paesi occidentali c’è stato un
notevole cambiamento nell’epidemiologia del carcinoma esofageo, caratterizzato sia
da un notevole aumento della sua incidenza che da un’aumentata prevalenza
dell’adenocarcinoma della giunzione esofago-gastrica rispetto al carcinoma
epidermoide del terzo medio e distale. Le cause che sottendono a questa modifica
epidemiologica sono tuttora sconosciute.
Il tumore dell’esofago colpisce principalmente il sesso maschile con un rapporto 3:1,
i soggetti di razza nera con un rapporto di 4:1 e, generalmente, soggetti di età
avanzata. Nelle donne l’aumento dell’incidenza negli ultimi anni è associato ad un
più levato consumo di sigarette.
Tumore raro nei soggetti con un’età inferiore ai 25 anni, l’incidenza aumenta
progressivamente nella fascia d’età compresa fra 45-55 anni; l’età media di
insorgenza, nell’uomo e nella donna, è di 66 anni.
La variante squamocellulare è 6 volte più frequente nei maschi neri rispetto ai
bianchi, mentre l’adenocarcinoma è 3 volte più frequente nei maschi bianchi rispetto
ai neri.
Il 15% dei carcinomi esofagei origina dal terzo superiore dell’esofago, il 50% dal
terzo medio e il rimanente 35% dal terzo inferiore; in quest’ultima sede è prevalente
l’adenocarcinoma, in particolare associato all’esofago di Barret.
Esiste un’incidenza relativamente alta di neoplasie primitive (cavità orale, faringe,
laringe, polmoni), sincrone (1,3%) o metacrone (4-9%) associate al carcinoma
esofageo per fattori di rischio comuni: possono riscontrarsi lesioni esofagee sincrone
(“skip lesions”) fino a 8 cm di distanza dal tumore primitivo per diffusione linfatica
sottomucosa.
Etiologia: fattori predisponenti al carcinoma epidermoide sono un’elevata
assunzione di alcool, un notevole uso di tabacco, oppure carenze nutrizionali di
vitamine e minerali, mentre l’adenocarcinoma della giunzione esofago-gastrica
origina più frequentemente su un esofago di Barret. In particolare:
l’alcool aumenta il rischio di carcinoma squamoso dell’esofago, ma non quello
dell’adenocarcinoma;
i fumatori hanno un rischio 5-10 volte superiore rispetto ai non fumatori ed il
rischio è strettamente connesso al numero di sigarette consumate ed agli anni di
abitudine al fumo;
il rischio di sviluppare un carcinoma squamoso dell’esofago nei soggetti che
consumano contemporaneamente bevande alcooliche e sigarette aumenta fino a
100 volte, poiché i cancerogeni contenuti nelle bevande alcooliche e nelle
1
sigarette si amplificano a vicenda, determinando un maggior aumento di lesioni
critiche al DNA ed una riduzione della capacità ripartiva dei sistemi di controllo.
Nella genesi del tumore esofageo sono implicati anche fattori genetici: la tilosi,
patologia trasmessa in maniera autosomica dominante e caratterizzata da
ipercheratosi palmare e plantare congenita e papillomi esofagei, è associata ad un
notevole aumento del rischio di carcinoma esofageo, che si sviluppa in oltre il 90%
dei soggetti entro il 65esimo anno di età.
In molte patologie benigne dell’esofago, come il megaesofago, l’esofagite da
reflusso, la stenosi peptica, le stenosi da caustici, le esofagiti batteriche e micotiche
ed i diverticoli esofagei, il rischio di insorgenza del carcinoma esofageo è aumentato.
La patogenesi comune a tutte queste condizioni sarebbe la presenza di una flogosi
cronica della mucosa esofagea che, attraverso i vari gradi di displasia, porterebbe poi
al carcinoma invasivo.
La displasia dell’epitelio esofageo è l’unica lesione pre-neoplastica conosciuta. La
displasia viene generalmente classificata in tre gradi: lieve, moderata e grave,
secondo la gravità delle anomalie citologiche presenti. La displasia lieve può
regredire e non necessariamente progredire verso la displasia grave ed il carcinoma
invasivo, mentre è stata documentata la progressione della displasia moderata. La
displasia grave viene considerata, a tutti gli effetti, un carcinoma in situ a causa delle
gravi alterazioni cellulari.
Per quanto riguarda il rischio di insorgenza dell’adenocarcinoma dell’esofago
inferiore e del cardias, oltre alla pregressa gastroresezione per ulcera gastrica e
all’alcalinizzazione del contenuto gastrico, merita una trattazione a parte la presenza
di esofago di Barret. L’esofagite peptica predispone all’insorgenza di questa
patologia caratterizzata dalla sostituzione dell’epitelio squamoso non cheratinizzato
che normalmente riveste l’esofago distale con epitelio colonnare metaplastico, sul
quale si può sviluppare la neoplasia; si può riscontrare la presenza di uno o di tutti i
seguenti tipi: epitelio gastrico di tipo fundico, epitelio giunzionale e metaplasia
intestinale. La displasia ed il carcinoma insorgono solo in presenza di metaplasia
intestinale.
I tumori esofagei benigni, come i leiomiomi ed i polipi, non vengono considerati a
rischio significativo di cancerizzazione: si ritiene, piuttosto, che si tratti di patologia
maligna sin dall’inizio, erroneamente classificata come benigna.
La sindrome di Plummer-Vinson, caratterizzata da esofagite, anemia ipocromica e
deficienza di vitamina B, è associata ad un elevato rischio di carcinoma epidermoide
dell’esofago cervicale. Anche il morbo celiaco è associato ad un aumento del rischio
di carcinoma esofageo, probabilmente dovuto alle multiple carenze vitaminiche e
nutrizionali dovute al malassorbimento.
Numerosi studi, infine, hanno messo in evidenza l’importanza della dieta e delle
carenze nutrizionali nell’insorgenza del carcinoma esofageo: l’assunzione di frutta e
verdura, l’arricchimento della dieta con betacarotene, vitamina E e selenio sembrano
svolgere un ruolo protettivo, un carente stato nutrizionale sembra incrementare il
rischio.
Anatomia patologica: circa il 15% dei carcinomi esofagei sono localizzati a livello
dell’esofago cervicale, il 20% all’esofago toracico superiore, il 30% all’esofago
medio ed il 35% all’esofago inferiore.
L’aspetto macroscopico del carcinoma esofageo viene così classificato:
2
vegetante (60%): risultanti dalla proliferazione di masse neoplastiche a grande
sviluppo endoluminale; hanno larga base di impianto, cospicuo volume, superficie
irregolare ed ampie zone di necrosi;
ulcerato (44%): sono meno frequenti dei precedenti e si presentano sotto forma di
ulcerazione neoplastica a bordi rilevati, con l’asse di ulcerazione che è sempre
orientato secondo l’asse longitudinale dell’esofago;
infiltrante (15%): a prevalente sviluppo intramurale, spesso circonfereziale e
stenosante.
Questi diversi aspetti macroscopici sono, a volte, combinati fra loro. Non si
attribuisce importanza prognostica significativa all’aspetto macroscopico, come
invece era in passato.
Dal punto di vista istopatologico si distinguono due istotipi principali:
1. carcinoma epidermoide o squamocellulare: origina dall’epitelio malpighiano
dell’esofago ed è il più frequente (80% circa); il grado di differenziazione viene
classificato in tre livelli:
G1: ben differenziato;
G2: moderatamente differenziato;
G3: scarsamente differenziato.
Varianti istologiche del carcinoma epidermoide vanno considerati:
i rari carcinomi mucosi, tutti ben differenziati;
i carcinosarcomi, che sono, invece, scarsamente differenziati;
2. adenocarcinoma: si ritiene prenda origine dalle ghiandole esofagee sottomucose
o da isole ectopiche di epitelio gastrico isolate nella mucosa epidermoide. Solo se
l’adenocarcinoma è circondato da mucosa epidermoide può essere considerato di
origine esofagea ed è raro. Gli adenocarcinomi dell’esofago inferiore sono quasi
sempre di origine della regione cardiale o da un esofago di Barret e vanno trattati
come i carcinomi del cardias. Varianti istologiche dell’adenocarcinoma sono:
i carcinomi adenocistici ed i muco epidermoidi, entrambi ben
differenziati;
il carcinoma adenosquamoso, che unisce strutture ghiandolari ed
epidermoidi.
I carcinomi indifferenziati o anaplastici sono rari e comprendono una varietà a
piccole cellule (oat cell) ed una a grandi cellule; queste forme istologiche dimostrano
una maggiore tendenza a metastatizzare per via linfatica ed ematica. I melanomi
maligni sono rarissimi, spesso polipoidi e pigmentati.
Anche i tumori maligni non epiteliali sono molto rari: i sarcomi esofagei sono, in
genere, di aspetto polipoide o vegetante ed in forma istologica di fibrosarcoma,
leiomiosarcoma o rabdomiosarcoma.
Evoluzione naturale: la displasia viene considerata la lesione iniziale della mucosa
esofagea che darà origine al carcinoma invasivo in un variabile intervallo di tempo.
L’evoluzione a carcinoma invasivo richiede, in media, 3-5 anni ed è irreversibile. La
sopravvivenza del paziente affetto da carcinoma in situ non trattato è, in media, di
circa 6 anni. I sintomi compaiono, nella massima parte, solo in presenza di un
carcinoma invasivo, infiltrante la parete esofagea, in una fase avanzata della storia
naturale della neoplasia. La sopravvivenza media del paziente affetto da carcinoma
invasivo non trattato è inferiore ad un anno. Nella fase finale di sviluppo della
neoplasia si assiste alla diffusione extraesofagea locoregionale per infiltrazione degli
organi vicini, e dei linfonodi regionali, e a distanza per la comparsa di metastasi. A
questo stadio la sopravvivenza media è di soli 4 mesi. La sopravvivenza globale dei
pazienti affetti da carcinoma esofageo è inferiore al 10% a 5 anni.
3
Vie di diffusione: il carcinoma dell’esofago diffonde attraverso le seguenti vie:
per continuità all’interno della parete esofagea in direzione prossimale e distale
attraverso i vasi linfatici della sottomucosa;
per contiguità alle strutture adiacenti come l’albero tracheobronchiale ed il
mediastino;
per via linfatica la diffusione avviene precocemente e, al momento della diagnosi,
si calcola che circa il 70% dei casi abbia già metastasi linfonodali loco-regionali;
per via ematogena le metastasi sono più tardive di quelle linfonodali ed
interessano prevalentemente il polmone ed il fegato, mentre più rare sono quelle
cerebrali e surrenali che.
Stadiazione: la stadiazione più comunemente accettata è quella TNM dalla UICCAJC. Il carcinoma dell’esofago, indipendentemente dall’istotipo, può interessare
vaste aree di superficie mucosa ed è spesso multifocale all’esordio, probabilmente
come risultato di una carcinogenesi di area. Nonostante gli adenocarcinomi possano
interessare estese aree di mucosa e sottomucosa, soprattutto nei soggetti con lunghi
segmenti di esofago di Barret, ai fini della stadiazione sono presi in considerazione
solo la profondità di penetrazione nella parete esofagea e lo stato linfonodale.
L’esofago, situato posteriormente alla trachea ed al cuore, origina dall’ipofaringe,
attraversa il mediastino posteriore e si congiunge allo stomaco attraverso un’apertura
del diaframma chiamata iato.
Dal punto di vista istologico l’esofago è costituito da quattro tonache: mucosa,
sottomucosa, muscolare (o muscolare propria) ed avventizia. Non è presente la
sierosa.
Ai fini descrittivi e di stadiazione l’esofago viene suddiviso in quattro regioni, che
dovrebbero essere sempre indicate e riportate separatamente, poiché la storia naturale
del carcinoma dell’esofago ed il suo trattamento variano in base alle divisioni
anatomiche:
1. esofago cervicale: inizia a livello del margine inferiore della cricoide e termina
all’entrata nel torace (incavo sternale), circa 18 cm a partire dall’arcata dentale
(in particolare dagli incisivi superiori);
2. esofago toracico superiore: si estende dall’entrata nel torace sino all’altezza
della biforcazione tracheale, circa 24 cm a partire dall’arcata dentale;
4
3. esofago toracico medio: si estende dalla biforcazione tracheale fino all’esofago
distale, appena sopra la giunzione esofago-gastrica, circa 32 cm a partire
dall’arcata dentale;
4. esofago toracico inferiore: lungo circa 3 cm, questa porzione include anche il
tratto intra-addominale del viscere e la giunzione esofago-gastrica, localizzata a
circa 40 cm a partire dall’arcata dentale.
La maggior parte degli adenocarcinomi origina dalla giunzione esofago-gastrica ed
interessano sia l’esofago distale che lo stomaco prossimale. Esiste controversia su
come distinguere i carcinomi dello stomaco prossimale che coinvolgono la giunzione
esofago-gastrica dagli adenocarcinomi dell’esofago distale e della giunzione
esofago-gastrica che si estendono inferiormente fino ad interessare il cardias. In
assenza di una coesistente mucosa di Barret tale distinzione può essere complessa.
Siewer ha proposto di classificare le neoplasie della giunzione esofago-gastrica in tre
tipi, I, II e III, in base al grado di invasione dell’esofago o dello stomaco; questa
classificazione, però, necessita ancora di ulteriori conferme al fine di determinare se
sia attendibile ai fini della stadiazione e della prognosi. Nella pratica clinica le
neoplasie che originano nella zona compresa fra la giunzione esofago gastrica ed il
cardias e che hanno solo un minimo (cm 2 o meno) interessamento dell’esofago,
vengono considerate come carcinomi primitivi dello stomaco.
Parametro T: questo parametro viene classificato secondo la profondità di
infiltrazione parietale.
Tx – tumore primitivo non definibile
T0 – tumore primitivo non evidenziabile
Tis – carcinoma in situ
T1 – tumore che infiltra la lamina propria o la sottomucosa;
T2 – tumore che infiltra la muscolare propria
T3 – tumore che infiltra l’avventizia
T4 – tumore che infiltra le strutture adiacenti
Per i tumori limitati allo stato mucoso (in situ o intramucoso) e sottomucoso si parla
anche di Early Esophageal Cancer; essi rappresentano, complessivamente, l’1% di
tutte le forme tumorali esofagee e se ne distinguono quattro tipi:
1. protundente (9%): lesione saliente, con aspetto papillare peduncolato o
vegetante;
2. superficiale (44%): lesione a placca con una piccola erosione, può divenire
circonferenziale (forma superficiale diffusa);
3. depresso (36%): lieve depressione mucosa con aspetto erosivo o ulcerativo e
margini irregolari;
4. occulto (11%): area di mucosa scura translucida.
5
Parametro N: la denominazione dei linfonodi regionali varia a seconda che si
consideri una neoplasia dell’esofago cervicale, dell’esofago toracico o della
giunzione esofago-gastrica:
1. linfonodi regionali per l’esofago cervicale: scalenici, giugulari interni,
cervicali, periesofagei, sopraclaveari;
2. linfonodi regionali per l’esofago intratoracico: (superiore, medio ed inferiore):
periesofagei superiori (sopra la vena azygos), sottocarenali, periesofagei inferiori
(sotto la vena azygos), mediastinici, perigastrici (esclusi i linfonodi celiaci);
3. linfonodi della giunzione EG: esofagei inferiori (sotto la vena azygos),
diaframmatici, pericardi ali, gastrici sinistri, celiaci.
L’interessamento di linfonodi più distanti (come quelli cervicali o del tronco celiaco
per le neoplasie intratoraciche) è, attualmente, considerato come metastasi a distanza
(M1a). Recenti studi suggeriscono, tuttavia, che un esteso interessamento linfonodale
è associato ad una migliore sopravvivenza rispetto alle metastasi viscerali, con un
possibilità di cura intorno al 100% dopo resezione chirurgica. In base a ciò è stato
suggerito di classificare le metastasi nei linfonodi distanti come N2 piuttosto che
come M1a, anche se tale modifica della classificazione richiede ulteriori studi.
Nel passato, per indicare le sedi dei linfonodi metastatici è stata frequentemente
utilizzata la nomenclatura citata. Più recentemente è stata sviluppata ed utilizzata una
mappa linfonodale dell’esofago che estende la nomenclatura ed il sistema di
numerazione utilizzato per la stadiazione dei carcinomi non a piccole cellule del
polmone. Tale mappa permette una più precisa identificazione dei linfonodi
interessati.
6
Parametro M: il fegato, i polmoni e la pleura sono le sedi più frequenti di metastasi
a distanza. Occasionalmente la neoplasia può estendersi per contiguità alle strutture
mediastiniche prima che sia evidente una metastasi a distanza, ciò succede
frequentemente per le neoplasie dell’esofago intratoracico che possono estendersi
direttamente all’aorta, alla trachea ed al pericardio.
Per il carcinoma dell’esofago cervicale viene definito M1 il coinvolgimento dei
linfonodi al di fuori della regione cervicale e sottoclaveare
MX – metastasi a distanza non valutabili
M0 – metastasi a distanza assenti
M1 – metastasi a distanza presenti
Tumori dell’esofago toracico inferiore: per i carcinomi dell’esofago toracico
inferiore il coinvolgimento dei linfonodi al di fuori della regione toracica inferiore
viene definito:
M1a – metastasi nei linfonodi celiaci
M1b – altre metastasi a distanza
7
Tumori dell’esofago medio toracico: per i carcinomi dell’esofago medio toracico
viene definito M1b una metastasi in qualsiasi linfonodo non regionale e/o a distanza;
pertanto:
M1a – non applicabile
M1b – metastasi ai linfonodi non regionali e/o ad altre sedi distanti
Tumori dell’esofago toracico superiore: per i carcinomi dell’esofago toracico
superiore l’interessamento dei linfonodi al di fuori di quelli regionali viene definito:
M1a – metastasi nei linfonodi cervicali
M1b – altre metastasi a distanza
8
La classificazione TNM del carcinoma esofageo comprende quattro stadi: più estesa
è la malattia, più alta è la cifra e tanto più avanzato è lo stadio.
Sintomatologia: il carcinoma esofageo nelle fasi iniziali è asintomatico e può essere
diagnosticato occasionalmente in seguito ad accertamenti eseguiti per altre patologie
o per la presenza di sintomi aspecifici. Questo spiega come la diagnosi sia spesso
tardiva: i sintomi, infatti, compaiono quando la neoplasia infiltra già i 2/3 della
circonferenza esofagea oppure quando occupa il lume dell’esofago alterandone la
funzione.
La disfagia è il sintomo più comune, presente in oltre l’80% dei casi: inizialmente
lieve e limitata ai cibi solidi, si aggrava in genere lentamente e, nel corso di settimane
o mesi, si estende ai liquidi fino a diventare totale. A volte si verificano episodi acuti
di disfagia per l’arresto del bolo alimentare in corrispondenza della stenosi
neoplastica. Sintomi associati alla disfagia sono il rigurgito alimentate e la
scialorrea. Il calo ponderale è presente nel 40% dei casi ed è causato
dall’ipoalimentazione conseguente alla disfagia ed all’anoressia. Il dolore toracico
retrosternale irradiato al dorso, spesso aggravato dalla deglutizione, è presente nel
20-30% dei casi ed indica, in genere, la presenza di un’infiltrazione mediastinica. La
disfonia può essere causata dalla paralisi di una corda vocale, in genere la sinistra,
perché il decorso intorno all’arco aortico del nervo laringeo inferiore sinistro ne
rende più facile l’infiltrazione da parte nella neoplasia o delle metastasi linfonodali
paratracheali. La tosse, la dispnea, le broncopolmoniti recidivanti ed altri sintomi
respiratori sono causati dalla compressione o dall’infiltrazione della trachea e dei
9
bronchi. Anche il rigurgito alimentare dovuto ad una stenosi serrata può causare gli
stessi sintomi. Qualora si sia formata una fistola esofago-aerea la tosse diviene
parossistica ad ogni deglutizione.
L’esame clinico non rivela in genere alterazioni patognomoniche. Il calo ponderale e
la compromissione dello stato generale di salute sono, in genere, i segni più evidenti.
Raramente sono presenti metastasi linfonodali palpabili in regione sovraclaveare o
latero-cervicale.
Diagnosi: in genere il primo esame che viene eseguito è una radiografia delle prime
vie digestive, che fornisce indicazioni sulla sede e sul tipo di lesione esofagea e sulla
presenza di patologie concomitanti. L‘esame deve comprendere uno studio accurato
del passaggio faringo-esofageo e di tutto l’esofago. Le neoplasie esofagee
superficiali sono difficili da visualizzare ed appaiono alla radiografia come lievi
irregolarità della superficie mucosa, che in corrispondenza può risultare ipomobile.
Lo studio radiologico mostra elevata sensibilità nelle forme tardive e bassa
specificità nelle forme precoci. Molto chiaro, invece, è l’aspetto radiologico del
carcinoma esofageo invasivo, che si presenta come un difetto irregolare della parete
esofagea, spesso circonfereziale e stenosante, che assume forma vegetante, ulcerata o
infiltrante. L’angolazione dell’asse esofageo può far sospettare un’infiltrazione
mediastinica.
L’esame endoscopico è indispensabile in tutti i casi: ha elevata specificità e
sensibilità e consente la precisazione istologica mediante l’esecuzione di biopsie
multiple mirate. Tutte le lesioni messe in evidenza dall’esofagoscopia devono essere
sia biotipizzate che valutate con brushing, in quanto la valutazione cito-istologica
raggiunge un’accuratezza diagnostica vicina al 100%, superiore sia alla sola citologia
che alla sola istologia.
Utile alla valutazione della profondità parietale di invasione della neoplasia e
dell’interessamento dei linfonodi regionali è l’ecografia endoscopica, che giunge ad
un’accuratezza nella determinazione di T dell’85% e dell’interessamento linfonodale
del 79%, consentendo anche di effettuare agoaspitati eco guidati dei linfonodi loco
regionali, la cui positività può costituire una controindicazione all’intervento
chirurgico con intento radicale.
Per una corretta stadiazione del paziente è necessaria una radiografia standard del
torace ed una TAC del torace e dell’addome superiore, per valutare l’estensione
locoregionale della malattia (invasione tracheobronchiale, invasione dell’aorta,
presenza di linfoadenopatie mediastiniche e sottodiaframmatiche) e la presenza di
eventuali metastasi ad organi addominali.
La RMN ha mostrato, in alcune esperienze, sensibilità e specificità superiori alla
TAC nella valutazione dell’infiltrazione del mediastino e del cuore.
I pazienti con una neoplasia esofagea del terzo medio e del terzo superiore devono
essere sottoposti a broncoscopia, al fine di escludere l’invasione tracheobronchiale.
La PET ha dimostrato una buona sensibilità per la stadiazione TNM pre-trattamento
radiochemioterapico o pre-chirurgia, per la valutazione della risposta ai trattamenti
combinati chemio-radioterapici, per la diagnosi di malattia al IV stadio.
Attualmente la TAC collo, mediastino ed addome rimane l’esame indispensabile per
la stadiazione di T ed N, per la rivalutazione pre e postoperatoria, nella fase posttrattamento radioterapico adiuvante per pazienti R1 ed R2.
Tra i requisiti essenziali per un trattamento radio chemioterapico con finalità
neoadiuvante, adiuvante o palliativo sono importanti la corretta valutazione della
funzionalità respiratoria e dello stato nutrizionale, in particolar modo nei pazienti con
perdita di peso >10% negli ultimi tre mesi.
10
Terapia: lo scopo della terapia del carcinoma esofageo è duplice: prolungare la
sopravvivenza e migliorare la sintomatologia e la qualità della vita. L’intervento
chirurgico di resezione esofagea rappresenta ancora oggi il trattamento di scelta del
carcinoma dell’esofago, in quanto consente una rapida terapia palliativa della
disfagia, ripristinando il transito alimentare e, nello stesso tempo, offre la migliore
possibilità di lunga sopravvivenza come singola modalità terapeutica. La terapia
multimodale, chemio-radio-chirurgica potrebbe migliorare la prognosi ed è già la
terapia di scelta nei casi di stadio avanzato.
Terapia chirurgica: la selezione dei pazienti candidati all’intervento chirurgico di
resezione esofagea deve essere effettuata valutando sia la stadiazione della
neoplasia e la sua resecabilità che le condizioni generali del paziente ed il rischio
operatorio. Quest’ultimo, infatti, è spesso molto alto a causa delle scadenti
condizioni generali di molti pazienti, le frequenti patologie associate ed il peso
dell’intervento di esofagectomia, che spesso necessita di laparotomia, toracotomia
e cervicotomia simultanee. Complessivamente circa il 60% dei pazienti può essere
sottoposto ad intervento chirurgico di resezione esofagea. Le vie di accesso per il
carcinoma dell’esofago sono spesso multiple: laparo- e toracotomia destra per le
neoplasie localizzate all’esofago toracico medio ed inferiore; toraco-laparo- e
cervicotomia per le neoplasie dell’esofago toracico superiore; laparo- e
cervicotomia con esofagectomia a torace chiuso per i pazienti che non possono
tollerare la toracotomia per l’elevato rischio respiratorio. La scelta della tecnica
chirurgica dipenderà soprattutto dalla sede della neoplasia esofagea.
Indipendentemente dalla via di accesso considerata e dalla sede della neoplasia
tutti gli interventi chirurgici che abbiano intento di radicalità oncologica devono
soddisfare alcuni principi per quanto riguarda l’estensione della resezione
esofagea e della linfoadenectomia. La resezione esofagea deve essere sempre
estesa almeno 6 cm a monte del margine macroscopico della neoplasia per la
tendenza del carcinoma esofageo a diffondere per via linfatica intramurale. La
linfoadenectomia locoregionale deve essere effettuata a livello dell’addome
superiore, nella regione della piccola curva gastrica e del tripode celiaco, e a
livello latero-cervicale e sovraclaveare se la neoplasia è localizzata all’esofago
cervicale. Questa estensione della linfoadenectomia è giustificata dalla tendenza
del carcinoma dell’esofago a metastatizzare per via linfatica, ed è indispensabile
per un’adeguata stadiazione post-chirurgica, poiché la presenza di metastasi
linfonodali è il più importante fattore prognostico conosciuto. Le casistiche
pubblicate riportano dati molto diversi in termini di percentuale di resecabilità, di
complicanze post-operatorie e di sopravvivenza. Attualmente i gruppi che hanno
più esperienza in chirurgia dell’esofago riportano una mortalità post-operatoria
del 5-10%. Le complicanze più gravi sono in genere quelle polmonari e le fistole
anastomotiche. La sopravvivenza a 5 anni dopo intervento di esofagectomia con
intento di radicalità oncologica varia dal 15 al 30%, e dipende soprattutto dallo
stadio della neoplasia. Infatti le neoplasie che infiltrano solo parzialmente la
patere esofagea e non hanno metastasi linfonodali (T1, N0 e T2, N0) hanno una
sopravvivenza a 5 anni che supera il 60%, mentre in presenza di infiltrazione di
tutta la parete e con metastasi linfonodali (T3, N1) la sopravvivenza a 5 anni
scende al 5%. Questi dati dimostrano i buoni risultati ottenibili con l’intervento
chirurgico in casi selezionati. La sede di recidiva dopo intervento di
esofagectomia è sia locoregionale che a distanza. Il carcinoma dell’esofago
toracico superiore ha una tendenza elevata alla recidiva locale ed una prognosi
significativamente peggiore rispetto alle altre localizzazioni. Recenti studi
11
sembrano indicare che la chemioterapia e, soprattutto la chemio-radioterapia
preoperatorie possono migliorare la sopravvivenza a lungo termine almeno in
alcuni stadi della neoplasia. In particolare questo trattamento preoperatorio si è
rilevato utile nei casi localmente avanzati (T4), in cui un intervento chirurgico
curativo è stato possibile solo dopo la riduzione del volume della massa tumorale.
La radioterapia e la chemioterapia post-operatorie non hanno, invece, ancora
dimostrato alcun miglioramento in termini di sopravvivenza;
Radioterapia: da sola viene in genere ritenuta poco efficace come trattamento con
intento curativo del carcinoma dell’esofago. Non vi sono, in letteratura, studi
validi ed un confronto non è proponibile per i migliori risultati ottenibili con
l’associazione di chemio- e radioterapia. Il campo d’irradiazione comprende
l’esofago e le stazioni linfonodali secondo la localizzazione della neoplasia. Il
carcinoma epidermoide è più sensibile dell’adenocarcinoma, per il quale è
necessario un dosaggio superiore. Le complicanze del trattamento radiante
possono essere la perforazione della neoplasia e le fistole esofago-aeree,
l’esofagite attinica e la tossicità polmonare, spinale e cardiaca. La brachiterapia
endoluminale, introdotta di recente, sembra poter migliorare i risultati, almeno
palliativi della radioterapia tradizionale;
Chemioterapia: i primi tentativi di chemioterapia del carcinoma dell’esofago
risalgono agli anni ’70 con risultanti molto scadenti. I risultati migliori si sono
ottenuti con alcuni schemi di polichemioterapia, che hanno una percentuale di
risposta intorno al 40% ed una durata di risposta di pochi mesi, senza alcun
miglioramento dimostrabile della sopravvivenza, al prezzo di una non trascurabile
tossicità renale, ematologica e gastrointestinale;
Terapia combinata (chemio- radioterapia associate alla chirurgia): il razionale
dell’associazione di radio- e chemioterapia si basa sull’effetto radio
sensibilizzante di alcuni farmaci chemioterapici, oltre all’effetto dei singoli
trattamenti. L’associazione con la chirurgia nei trattamenti combinati multimodali
è la più promettente terapia del carcinoma esofageo. Studi iniziati a partire dagli
anni ’80 hanno dimostrato un aumento della resecabilità ed anche della
sopravvivenza nei pazienti che rispondono al trattamento. Il trattamento
combinato è indicato anche in caso di carcinoma localmente avanzato, T4,
giudicato non operabile al momento della diagnosi;
Terapia palliativa: almeno il 40% dei pazienti affetti da carcinoma esofageo non
possono essere sottoposti ad un trattamento chirurgico o combinato con intento
curativo, a causa dell’estensione della neoplasia o per le loro condizioni generali.
L’obiettivo principale della terapia palliativa è quello di migliorare la disfagia e
favorire la ripresa dell’alimentazione. Le tecniche più applicate sono
l’esofagectomia palliativa, l’esofago-gastrostomia, l’applicazione di stent esofagei
e la laserterapia. Gli interventi chirurgici di resezione palliativa e di bypass della
stenosi sono indicati solo in casi molto selezionati, a causa dell’elevato rischio di
complicanze. Migliori risultati possono essere ottenuti mediante procedure
endoscopiche di applicazione di endoprotesi esofagee che, però, non possono
essere applicate in caso di stenosi esofagee insondabili, che richiederanno invece
il ricorso ad una gastrostomia o digiunostomia di alimentazione. Nel caso di
neoplasie esofagee superficiali, limitate alla mucosa ed alla sottomucosa, in
pazienti non operabili per l’elevato rischio operatorio, la laserterapia
fotodinamica, associata alla radioterapia, può ottenere l’eradicazione della
neoplasia.
12
13