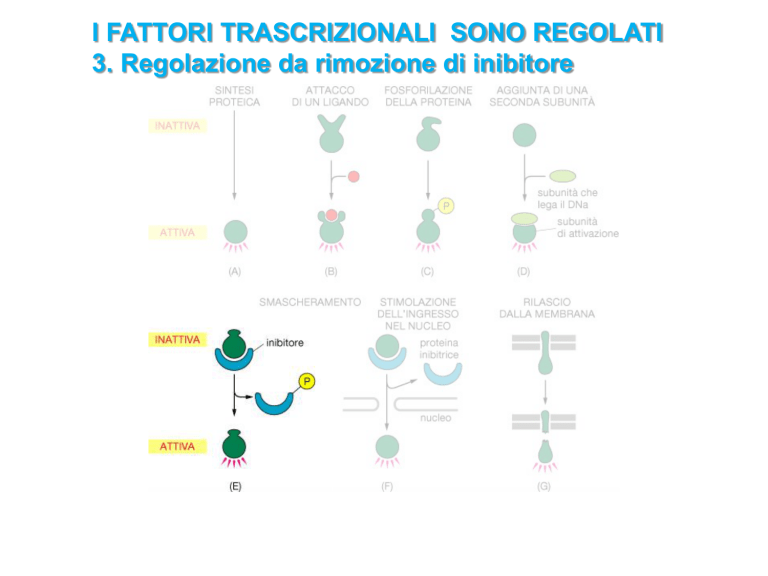
I FATTORI TRASCRIZIONALI SONO REGOLATI
3. Regolazione da rimozione di inibitore
IL FATTORE TRASCRIZIONALE NFkB
Famiglia di proteine molto conservate
che comprende 5 membri.
La famiglia comprende 2 sottofamiglie:
I) le proteine Rel: RelA (p65),RelB, c.Rel
II) le proteine NFkB (p105, p100)
Le proteine NFkB (p105, p100)
vanno incontro a proteolisi
generando le proteine p50 e
p52 che formano il dimero e le
proteine IKB che si legano al
dimero e lo inibiscono.
IL DOMINIO RHD
C-TERM
N-TERM
LA FORMAZIONE DEL DIMERO
La formazione del dimero è necessaria
per l’attività trascrizionale.
Ciascuna subunità interagisce con metà
del sito di legame.
Si possono formare differenti dimeri
(omo e etero)
Il più comune e abbondante è il dimero
p65/p50
IL FATTORE TRASCRIZIONALE NFkB
ILb
antigens
INFLAMMATION
CELL GROWTH
IMMUNITY
APOPTOSIS
LPS
BAFF
Nello stato inattivo NF-κB è
localizzato nel citoplasma
complessato con la proteina
inibitoria IKB.
Attraverso il segnale tradotto
da un recettore di membrana
viene attivata la proteina
chinasi IKK che fosforila IKB.
IKB fosforilata viene
ubiquitinata, si dissocia dal
NFkB e viene degradata dal
proteasoma.
NF-kB libero dall’inibitore
espone il segnale di
localizzazione nucleare e può
essere traslocato nel nucleo
dove si lega al suo specifico
RE. Il complesso DNA/NF-kB
recluta co-attivatori e la RNA
polimerasi e attiva la
trascrizione dei geni target
NFkB PUO’ ESSERE ATTIVATO DA UNA VARIETA’ DI STIMOLI
NF-κB is a central regulator in stress response The NF-κB signaling pathway can be
activated by numerous stimuli as listed in the blue . In response to these different
stimuli NF-κB transcriptionally regulates hundreds of genes, the generalized
categories of which are listed in the red circles.
NFkB: infiammazione, resistenza all’insulina e obesità
L’obesità causa infiammazione e insulino-resistenza
L’obesità induce cambiamenti nel metabolismo del tessuto adiposo che, attraverso un
circuito autocrino e paracrino , risultano in infiammazione localizzata e insulinoresistenza (IR). Attraverso il sistema endocrino questo stato si propaga ai tessuti distanti.
NFkB: infiammazione, resistenza all’insulina e obesità
ADIPOCITI
PRE-ADIPOCITI
CELLULE DENDRITICHE
IL-6,
IL-6,
ADIPONECTINE
LEPTINA
MCP-1
FFA
ADIPONECTINA
FFA
LINFOCITI T
CITOTOSSICI
MACROFAGI
IL-6,
TNF-a
IL-1b
L’espansione del tessuto adiposo è
accompagnato da cambiamenti
nell’espressione di citochine e
chemochine, ipossia, morte
cellulare, infiltrazione di cellule del
sistema immunitario e deregolazione
del metabolismo degli acidi grassi.
Gli adipociti maturi secernono IL-6,
MCP-1 (monocyte chemoattractant
protein), leptina, e adiponectina che
possono agire con meccanismo
autocrino, paracrino o endocrino per
regolare l’omeostasi del glucosio e
dei lipidi.
L’aumento di espressione di MCP-1
promuove l’infiltrazione di monociti
nel tessuto adiposo che
differenziano in macrofagi del
tessuto adiposo (ATM). Questi ultimi
secernono ulteriori chemochine e
citochine creando un circolo vizioso
che favorisce la creazione di un
ambiente pro-infiammatorio.
NFkB: infiammazione, resistenza all’insulina e obesità
L’infiltrazione dei macrofagi determina un
aumento di secrezione di TNF-α, che a sua
volta attiva sia la lipolisi che NF-κB negli
adipociti. Inoltre, gli acidi grassi liberi
(FFA) che si producono con la liposisi negli
adipociti a loro volta attivano NF-κB sia
nei macrofagi che negli adipociti.
Il secondo segnale di attivazione è dovuto
a molecole rilasciate da cellule
danneggiate e stress ossidativo che
attivano il pathway di JNK.
L’espressione dei geni target di NF-κB e
JNK determinano una disattivazione della
via di trasduzione del segnale del
recettore dell’insulina (IRS1 ->AKT)
I FATTORI TRASCRIZIONALI SONO REGOLATI
3. Regolazione da modificazioni covalenti
REGOLAZIONE DA MODIFICAZIONI COVALENTI : la proteina CREB
La struttura primaria di CREB rivela una
regione centrale di 60 aminoacidi KID (kinaseinducible domain), che contiene il sito di
fosforilazione della chinasi PKA.
Il dominio KID è fiancheggiato da due domini
glutamine-rich (Q1 e Q2). Nella regione CTerm è localizzato il dominio di dimerizzazione
leucine zipper (bZIP).
Il dominio Q2 promuove l’espressione dei geni
target attraverso l’interazione con la
subunità TAFII130 del complesso TFIID
ATTIVAZIONE DI CREB
ADENILATO CICLASI
Adenylyl cyclase (AC) structure. The ACs can be
divided into 5 major domains: the NH2 terminus, the
first transmembrane cluster (TM1, blue cylinders),
the first cytoplasmic loop comprised of C1a (red)
and C1b (black), the second transmembrane
cluster (TM2, blue cylinders) with extracellular Nglycosylation sites, and the second cytoplasmic
loop comprising C2a (orange) and C2b (black). C1a
and C2a are highly conserved catalytic ATP-binding
regions, which dimerize to form the catalytic site.
C1b and C2b domains are less conserved.
c-AMP signaling main features
I livelli intracellulari di cAMP sono regolati dal bilancio delle attività dell’Adenilato
ciclasi (AC) e della Fosfodiessterasi (PDE). Per entrambi gli enzimi esistono molte
isoforme che differiscono nel loro pattern di espressione e di regolazione.
Esistono 9 isoforme di AC e 12 isoforme di PDE che differiscono per il loro pattern
di espressione e meccanismo di regolazione
AC is regulated by G-proteins, so called
because they bind guanine phosphates.. The
G-proteins involved with AC are composed of
three different
subunities: alpha, beta and gamma.
For the most part, the alpha piece of the G-protein
interacts with AC. There are two types of Gproteins that can affect the AC: stimulatory Gproteins (Gs) or inhibitory G-proteins (Gi).
L’attività delle ACs e PDEs sono regolate positivamente o negativamente da altri
sistemi di segnalazione come il Calcio (attraverso la calmodulina, la calmodulinachinasi II, e calcineurina), subunità delle proteine G, fosfolipidi inositolici,
(attraverso PKC) e recettori tirosina-chinasi (attraverso ERK e PKB).
c-AMP signaling main features: PKA
I principali targets del c-AMP sono: protein kinase A (PKA), the GTP-exchange
protein EPAC e cyclic-nucleotide-gated ion channels.
L’azione di PKA è mediata da proteine chiamate AKAPs (PKA-anchoring
proteins) che determinano la specificità della trasduzione del segnale del
cAMP portando PKA in prossimità dei suoi substrati.
I FATTORI TRASCRIZIONALI SONO REGOLATI
4. Regolazione da rilascio da membrana
REGOLAZIONE DA RILASCIO DA MEMBRANA: il fattore SREBP
Nell’uomo sono state identificate
tre proteine nella famiglia,
denominate SREBP-1a, 1c e
SREBP-2.
Tutte le proteine della famiglia
SREBP hanno una struttura
tripartita simile che consiste di:
1) un dominio di legame al DNA
N-terminale di circa 400
aminoacidi che ha una struttura
HLH
2) una regione centrale di circa
80 aa idrofobica che contiene
due segmenti transmembrana
3) una regione regolatoria Cterminale
REGOLAZIONE DA RILASCIO DA MEMBRANA: il fattore SREBP
Attivazine mediante proteolisi controllata
L’attivazione avviene in 2 steps
che sono regolati dagli steroli:
S1P: una prima proteasi taglia
SREBP nel sito 1 che si trova nel
mezzo del loop che si affaccia
nel lume rompendo il legame
covalente tra le due regioni
transmembrana
S2P:una seconda proteasi taglia
il frammento N-Terminale
all’interno del dominio
transmembrana rilasciando il
dominio N-terminale maturo nel
citosol
S1P è sotto lo stretto controllo
degli steroli












