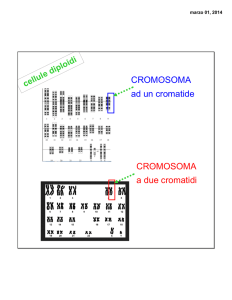
Cariotipo umano
1956
Accertamento del no. di cromosomi, i 23 cromosomi dell’assetto
aploide vengono suddivisi in 7 gruppi (A-G) sulla base delle
dimensioni e della posizione del centromero
1970
Introduzione delle tecniche di bandeggio: diventa possibile
individuare i singoli cromosomi
Braccio corto = p
Braccio lungo = q
Le bande vengono numerate con numeri progressivi
dal centromero verso i telomeri
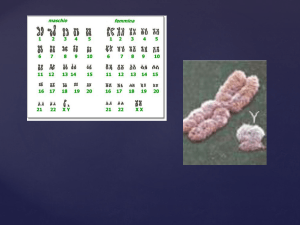
Cariotipo umano di un individuo di sesso maschile
Cariotipo umano di un individuo di sesso femminile
Bandeggio di
un cromosoma
umano a
diversi livelli
di risoluzione
UN PO’ DI NOMENCLATURA
46, XX
46, XY
cariotipo normale femminile
cariotipo normale maschile
Anomalie di numero
45, X
47, XX +21
47, XXX
Anomalie di struttura
delezioni
46, XY, del(4)(p16.3)
46, XX, del(5)(q13q33)
inversioni
46, XY, inv(11)(p11p15)
duplicazioni
46,XX, dup(1)(q22q25)
inserzioni
46, XX, ins(2)(p13q21q31)
traslocazioni reciproche
46, XX, t(2;6)(q35;p21.3)
traslocazioni Robertsoniane
45, XY, der(14;21)
Genoma umano aploide
ca. 3000 Mb (= 3 x 109 bp)
Cromosoma X
ca. 155 Mb pari al 5% del
genoma aploide, contiene
più di 1000 geni molti dei
quali housekeeping
Cromosoma Y
ca. 60 Mb pari al 2% del
genoma aploide, contiene
qualche decina di geni per
lo più coinvolti nella
formazione del testicolo e
nella produzione di
spermatozoi
Due zone di omologia X-Y poste alle due estremità dei cromosomi, vengono
indicate con la sigla PAR (Pseudo Autosomal Region)
PAR1 (o primaria) estremità del braccio corto, è grande ca. 2.6 Mb
PAR2 (o secondaria) estremità del braccio lungo, è grande ca. 320 Kb
Queste due regioni, durante la meiosi maschile, si appaiano e vanno incontro
a ricombinazione
PAR1
PAR2
Perché si è ipotizzato l’esistenza di un meccanismo di
compensazione del dosaggio genico (o più precisamente della
differenza di dosaggio genico)?
1) Le aneuploidie dei cromosomi sessuali, a differenza di quelle a
carico degli autosomi, sono compatibili con la vita, e, in alcuni
casi, non comportano fenotipi anormali
47, XXX femmine normali, talvolta sterili
47, XXY (sindrome di Klinefelter) maschi sterili, talvolta con lieve
ritardo mentale
45, X0 (sindrome di Turner), statura inferiore alla media, sterilità, altre
anomalie di sviluppo generalmente non gravi
48, XXXX o XXXY sintomatologia più grave delle precedenti, ma
comunque condizione compatibile con la vita
2) La quantità di prodotto genico di geni del cromosoma X è
uguale in maschi e femmine, nonostante il fatto che i maschi
abbiamo una sola copia del gene e le femmine due
Esempio attività enzimatica della G6PD (Glucosio-6-Fosfato
Deidrogenasi)
Nei mammiferi, a differenza che in altri organismi (es. Drosophila), la
compensazione del dosaggio genico è raggiunta attraverso l’inattivazione
di uno cromosoma X nelle cellule somatiche che ne contengono due
In cellule con aneuploidie dei cromosomi sessuali viene mantenuto attivo
un solo cromosoma X, questo spiega il fenotipo pressoché normale di
soggetti con cromosomi sessuali in eccesso o in difetto
Agli inizi degli anni ’60 Mary Lyon ed Ernest Beutler sono arrivati in modo
indipendente a dimostrare l’esistenza dell’inattivazione del cromosoma X
Beutler
studio del gene Gd nell’uomo
Lyon
studio di un gene che controlla il colore del pelo nel topo
L’inattivazione è:
casuale (in media il 50% delle cellule inattiva l’X ereditato dal padre
e il 50% quello ereditato dalla madre)
mantenuta clonalmente (le cellule figlie mantengono lo stesso
pattern di inattivazione della cellula madre)
precoce
Caratteristiche del cromosoma X trascrizionalmente inattivo:
mantiene attive alcune regioni (le due PAR ed altri geni
interspersi in regioni inattive)
assume un aspetto eterocromatico in interfase (corpo di Barr)
acquista le caratteristiche del DNA inattivo (metilazione dei
residui di Citosina, ipoacetilazione degli istoni, replicazione del
DNA nella tarda fase S)
In cellule euploidi o con aneuploidie dei cromosomi sessuali, in
interfase sono visibili 0, 1, 2 o 3 corpi di Barr a seconda del numero
di cromosomi X presenti nella cellula
Il corpo di Barr è stato
scoperto alla fine degli anni
’40 e, quando è stata scoperta
l’inattivazione del
cromosoma X, si è ipotizzato
che potesse essere
l’espressione morfologica
dell’X inattivo
Corpo di Barr struttura
eterocromatica visibile in
interfase addossato alla parete
interna della membrana
nucleare
Nucleo di una
cellula in interfase
con 1 corpo di
Barr
Nucleo di una
cellula in interfase
con 3 corpi di Barr
Come avviene l’inattivazione?
Processo multi-step:
1) ‘conteggio’ dei cromosomi X presenti nella cellula (anche
rispetto agli autosomi);
2) ‘scelta’ del(dei) cromosoma(i) X da inattivare, uno per ogni
assetto diploide;
3) inizio dell’inattivazione;
4) sua diffusione alla quasi totalità del cromosoma;
5) mantenimento dello stato inattivo
l’inattivazione non è sequenza-specifica (sequenze autosomiche
traslocate sull’X possono essere inattivate)
Tutte queste funzioni sono mediate da sequenze di
DNA che si trovano nella regione Xq13 e da loci
autosomici
La regione Xq13 contiene quindi l’X-Inactivation Center
(XIC), questa regione è stata suddivisa in sottoregioni
coinvolte nei singoli step del processo di inattivazione
inizio anni ’90 identificazione del primo gene coinvolto
nell’inattivazione
XIST (X Inactive Specific Transcript)
è l’unico gene espresso solo dal cromosoma X inattivo
codifica un RNA senza ORF di ca. 17 Kb che sembra rivestire
il cromosoma X inattivo
Attualmente sono stati identificati altri geni necessari per il
processo di inattivazione, ma le basi molecolari di questo
fenomeno non sono ancora completamente note
L’inattivazione è sempre casuale?
NO si osserva deviazione dalla casualità quando uno dei
cromosomi X della cellula porta una copia del gene XIST
(necessario per dare inizio all’inattivazione) non funzionante
o quando si ha una traslocazione bilanciata X-autosoma. In
questi casi l’inattivazione è in origine casuale, ma le cellule
che inattivano l’X coinvolto nella traslocazione inattiveranno
anche geni autosomali e questo le renderà selettivamente
svantaggiate rispetto alle altre cellule
Pattern di inattivazione nelle cellule della linea germinale:
entrambi i cromosomi X degli oogoni sono attivi, l’unico
cromosoma X degli spermatogoni è inattivo
L’inattivazione del cromosoma X è
responsabile della grande variabilità
clinica delle malattie dovute a geni che
mappano su questo cromosoma la
gravità del fenotipo clinico dipenderà
dalla proporzione di cellule che hanno
mantenuto attivo il cromosoma X con
l’allele mutante
Imprinting genetico
Espressione differenziale di materiale
genetico a seconda che esso sia stato
trasmesso dal padre o dalla madre. I geni
soggetti a imprinting sono presenti in
duplice copia, ma di essi viene espressa una
sola copia
Espressione monoallelica di geni
biallelici
Concetto contrario alle leggi di Mendel
secondo le quali l’origine materna o
paterna di un’informazione non ne influenza
l’espressione (equivalenza degli incroci
reciproci)
Geni ‘imprintati’ nel padre sono silenziati
durante la spermatogenesi la copia
fornita dal padre non viene espressa,
rimane attiva solo quella fornita dalla
madre
Geni ‘imprintati’ nella madre sono silenziati
durante la oogenesi la copia fornita dalla
madre non viene espressa, rimane attiva solo
quella fornita dal padre
pedigree di una malattia dovuta ad un gene soggetto a
imprinting silenziato durante la oogenesi (è attiva solo la
copia fornita dal padre)
il rapporto maschi : femmine tra gli affetti è 1:1, una
femmina malata non trasmette MAI la malattia, che può
ricomparire però nei suoi nipoti (figli dei suoi figli maschi)
PROVE DELL’ESISTENZA DELL’IMPRINTING
esperimenti di trapianti di pronuclei nel topo: creazione di
zigoti androgenetici e ginogenetici
zigoti ginogenetici
2n cromosomi TUTTI di
derivazione femminile
embrioni abortivi – strutture
extraembrionarie pressoché assenti,
embrione quasi normale
zigoti androgenetici
2n cromosomi TUTTI di
derivazione maschile
CONTROLLI
zigoti normali ottenuti
con trasferimento di
pronuclei
2n cromosomi, n forniti da
un maschio e n da una
femmina
embrioni abortivi – iperplasia del
trofoblasto, embrione pressoché assente
embrioni normali – la manipolazione di per
sé non impedisce il normale sviluppo
PROVE DELL’ESISTENZA DELL’IMPRINTING
NELL’UOMO
Esistono due patologie umane paragonabili agli zigoti
ginogenetici e androgenetici:
teratomi, 2n cromosomi forniti SOLO dalla madre
mole idatiforme, 2n cromosomi forniti SOLO dal padre
I triploidi (3n cromosomi = 69) sono tutti abortivi, ma il
fenotipo dei 2nP1nM è diverso da quello dei 2nM1nP, nei
primi si osserva un’iperplasia delle strutture
extraembrionarie e assenza dell’embrione vero e proprio,
viceversa, nei secondi si hanno strutture extraembrionarie
quasi assenti e embrione pressoché normale
Alcune disomie cromosomiche uniparentali (UPD)
(entrambi i cromosomi di una coppia forniti dallo stesso
genitore) hanno effetti fenotipici diversi dettati dal sesso
del genitore che ha fornito la coppia di cromosomi
Si stima che nell’uomo i geni soggetti a
imprinting siano dell’ordine di 200, si trovano
sulle seguenti regioni cromosomiche:
6, 7q, 11p, 14q, 15q11-q13, 20
molto spesso i geni soggetti a imprinting
sono riuniti in cluster contenenti geni
‘imprintati’ nella madre e geni ‘imprintati’ nel
padre
i due cluster omologhi mostrano
metilazione differenziale (ma non sempre la
metilazione è a carico dell’allele non espresso)
nei cluster sono in genere presenti sia geni
strutturali (il loro prodotto finale è una
catena polipeptidica) sia geni che producono
RNA non codificanti
L’imprinting deve essere risettato ad ogni generazione
Sindrome di Beckwith-Wiedemann (BWS) (1)
Malattia dovuta a un gene soggetto a imprinting nella
madre (è attiva solo la copia fornita dal padre) causata da
acquisizione di funzione. Il gene mappa in 11p15
P
M
P
M
P
M
Nei soggetti normali è espressa solo la
copia paterna
La duplicazione sul
cromosoma paterno ha
come conseguenza un
raddoppiamento del
prodotto genico ed
insorgenza della malattia
La duplicazione sul
cromosoma materno è
senza conseguenze perché
la copia sovrannumeraria
non viene espressa
Sindrome di Beckwith-Wiedemann (BWS) (2)
Una mutazione nel centro di imprinting
impedisce il silenziamento del gene in cis
P
M
P
M
La mutazione è sul cromosoma
paterno non si hanno conseguenze
fenotipiche perché la copia che non
può essere spenta è comunque
destinata ad essere espressa
La mutazione è sul cromosoma
materno l’individuo è malato
perché ha due copie attive del gene
Sindrome di Prader-Willi (PWS) - malattia dovuta ad
assenza della funzione del ‘gene’ PWS (si tratta di vari
geni che per semplicità vengono qui considerati come un
unico gene), ‘gene’ soggetto ad imprinting nella madre
(è espressa solo la copia fornita dal padre) che
mappa in 15q11-13
Sindrome di Angelman (AS) - malattia dovuta ad assenza
della funzione del gene AS, gene soggetto ad
imprinting nel padre (è espressa solo la copia fornita
dalla madre) che mappa in 15q11-13, cioè nella
STESSA regione del ‘gene’ PWS
Entrambe le malattie possono essere dovute a:
1. delezione dell’intera regione cromosomica 15q11-13;
2. disomia uniparentale (UPD) (materna nella PWS,
paterna nella AS);
3. errore di imprinting;
4. solo per la sindrome di Angelman: mutazione nella
copia materna del gene AS
P
M
P
M
P
M
PWS
AS
Pattern di espressione nel
soggetto normale: sono
espressi il ‘gene’ PWS del
cromosoma paterno ed il
gene AS del cromosoma
materno
La delezione è sul
cromosoma Paterno
assenza della funzione del
‘gene’ PWS, si ha Sindrome di
Prader-Willi
La delezione è sul
cromosoma Materno
assenza della funzione del
gene AS, si ha Sindrome di
Angelman
P
PWS
AS
PWS
AS
P
M
M
P
PWS
AS
M
P
M
PWS
AS
Disomia Uniparentale (UPD)
Paterna assenza
funzionale del gene AS
Sindrome di Angelman
UPD Materna assenza
funzionale del ‘gene’ PWS
Sindrome di Prader-Willi
mutazione nel centro di imprinting
sul cromosoma P che non può
essere risettato e viene trasmesso
con un’impronta di tipo Materno
assenza funzionale del gene PWS
Sindrome di Prader-Willi
mutazione nel centro di imprinting
sul cromosoma M che non può
essere risettato e viene trasmesso
con un’impronta di tipo Paterno
assenza funzionale del gene AS
Sindrome di Angelman
UPD = UniParental Disomy = disomia
uniparentale entrambi gli omologhi di una
coppia vengono ereditati dallo stesso genitore
Non si ha un’alterazione quantitativa rispetto al
normale, ma per quel particolare cromosoma
l’informazione genetica proviene da un solo
genitore
Le UPD sono in genere dovute a recupero di una
trisomia (un embrione trisomico che in una fase
estremamente precoce dello sviluppo perde un
membro della tripletta di omologhi)