Principali difficoltà nello studio dei caratteri genetici
nell’uomo
Non si possono programmare gli incroci
Il tempo di generazione dello sperimentatore è
uguale al tempo di generazione della specie oggetto
di studio
Le fratrie sono di piccole dimensioni
Vantaggi
Per l’uomo le conoscenze ‘mediche’ (anatomia,
fisiologia, patologia ecc.) sono molto più avanzate
rispetto a quelle sugli altri organismi
Anche fenotipi molto rari è difficile che sfuggano
all’osservazione
Lo studio dei caratteri mendeliani nell’uomo
nell’uomo viene effettuato attraverso lo studio dei
pedigree
Non sempre è facile dimostrare l’ereditarietà
genetica di un carattere membri della stessa
famiglia oltre a condividere una certa quota del loro
patrimonio genetico condividono anche l’ambiente
(alimentazione, stile di vita, interessi, ecc.) e non
sempre è possibile avere informazioni dettagliate e
complete sui rapporti di parentela e sul fenotipo dei
vari membri di una famiglia
Albero genealogico o pedigree figura che rappresenta
in modo schematico individui con almeno un ascendente in
comune, i loro discendenti, i loro coniugi e le relazioni di
parentela che intercorrono tra di essi
Possono essere utilizzati:
per accertare le modalità di trasmissione di un
carattere ereditario
nella consulenza genetica (es. per calcolare il
rischio di generare figli affetti o il rischio di
sviluppare una determinata malattia genetica)
sono fondamentali per la mappatura genetica
Se si utilizzano i pedigree per stabilire le modalità di
trasmissione di un carattere genetico è importante
considerare la frequenza con cui si presenta nella
popolazione il carattere in esame
se un CARATTERE è RARO possiamo assumere che
sia entrato nel pedigree una sola volta
viceversa per CARATTERI COMUNI tale
assunzione non può essere fatta
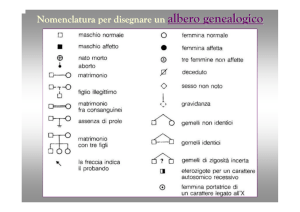
SIMBOLI USATI PER LA COSTRUZIONE DEI
PEDIGREE
Il probando è l’individuo attraverso cui si è arrivati allo studio di
quel pedigree, viene indicato con una freccia
Ogni individuo è identificato in modo non ambiguo da una coppia di
numeri (un numero romano ed uno arabo)
PRINCIPALI MODALITA’ DI TRASMISSIONE DI UN
CARATTERE MENDELIANO
autosomica dominante
autosomica recessiva
X-linked dominante
X-linked recessiva
Y-linked
mitocondriale
EREDITA’ AUTOSOMICA DOMINANTE
EREDITA’ AUTOSOMICA RECESSIVA
EREDITA’ X-LINKED RECESSIVA
EREDITA’ X-LINKED DOMINANTE
Tra gli affetti il rapporto maschi:femmine è 1:2
EREDITA’ Y-LINKED
trasmissione maschio-maschio
non si conoscono (e probabilmente non esistono) patologie legate
a geni del cromosoma Y (escluse quelle legate alla fertilità)
FATTORI CHE COMPLICANO L’ANALISI DI
PEDIGREE
penetranza incompleta – La penetranza è la percentuale di individui
che hanno il genotipo-malattia e che sono affetti.
Affermare che una malattia genetica è a penetranza incompleta equivale a
dire che esiste una certa quota di individui che non manifestano la
malattia pur avendo il genotipo-malattia.
Esempio 1. malattia AD con una penetranza dell’80%
100 soggetti Aa, 80 sono malati e 20 sono sani
Esempio 2. malattia AR con una penetranza del 70%
100 soggetti aa, 70 sono malati e 30 sono sani
La penetranza incompleta è una caratteristica
maggiormente frequente nelle malattie AD
Il motivo per cui individui con il genotipo-malattia
non sono malati può essere:
influenza dell’ambiente
azione di altri geni (gene principale + geni
modificatori)
ESEMPIO DI MANCATA PENETRANZA
madre e figlia di II-2 presentano la stessa patologia possiamo escludere
che si tratti di mutazione fresca
ETEROGENEITÀ GENETICA (eterogeneità di locus)
malattie clinicamente uguali possono essere dovute a
mutazioni in geni diversi
Esempi classici sono la sordità non sindromica e l’albinismo
Altri esempi:
• sindrome di Ehlers-Danlos (lassità di pelle e legamenti) se ne
conoscono varie forme clinicamente indistinguibili ma
geneticamente distinte (eredità AD, AR e X-linked recessiva);
•
molte altre collagenopatie;
•
alfa e beta talassemie
Quando si cerca di stabilire la modalità di trasmissione di
una particolare malattia o si vuole mappare il genemalattia bisogna tenere presente questa possibilità e
considerare che in pedigree diversi la patologia può
essere causata da mutazioni in geni diversi
ESEMPIO DI COMPLEMENTAZIONE NELL’UOMO
(Sordità autosomica recessiva)
ETEROGENEITÀ CLINICA (eterogeneità
allelica)
mutazioni diverse dello stesso gene causano
malattie diverse
talvolta la differenza è quantitativa (es. Fibrosi
cistica con e senza insufficienza
pancreatica; distrofia di Duchenne e di
Becker);
altre volte è qualitativa (alleli diversi dello
stesso gene causano patologie molto
diverse (es. insensibilità agli androgeni e
atrofia muscolo-spino-bulbare)
ESPRESSIVITA’ VARIABILE
individui portatori dello stesso allele
malattia presentano caratteristiche cliniche e
gravità diverse
INSORGENZA TARDIVA
penetranza dipendente dall’età
1
probabilità
0,8
0,6
0,4
0,2
0
0
20
40
età (anni)
60
80
I
II
1
2
3
4
III
II-1, II-3 e II-4 non hanno ricevuto l’allele
malattia o non hanno ancora manifestato la
malattia?
malattia X-linked dominante letale nei maschi
in alcuni casi si osserva poliabortività
il rapporto sessi è alterato ma, a causa delle piccole dimensioni delle
famiglie umane, generalmente è difficile dimostrarlo
malattia X-linked recessiva: mutazione fresca
o segregazione di un allele malattia ?
Mosaicismo
Presenza in un individuo di due linee cellulari
geneticamente diverse ma derivanti da un unico
zigote
Mosaicismo somatico
Mosaicismo germinale
Mosaicismo somatico e germinale
Mosaicismo funzionale nelle femmine dovuto
ad inattivazione del cromosoma X
Le malattie X-linked dominanti in genere mostrano,
nelle femmine, una notevole variabilità di
espressione dovuta alla diversa percentuale di
cellule che hanno inattivato il cromosoma X con
l’allele mutante
L’inattivazione del cromosoma X può anche essere
responsabile dell’insorgenza di malattie X-linked
recessive in femmine portatrici.
pedigree di un carattere autosomico recessivo comune
carattere X-linked comune: apparente trasmissione maschio-maschio
esempio: daltonismo, freq. del carattere nei maschi 0.08 (q), freq. di
femmine portatrici 0.147 (2pq), quindi la probabilità di un matrimonio
maschio daltonico x femmina portatrice = 0.08 x 0.147 = 0.012
EREDITA’ MITOCONDRIALE
IMPRINTING MATERNO