Unità 3
Le molecole della cellula
Unità 3
Le molecole della cellula
Obiettivi
Capire il ruolo centrale del carbonio
nella costruzione delle molecole organiche
Capire che la complessità delle biomolecole
deriva dell’assemblaggio di molecole piccole
(i monomeri) simili tra loro
Conoscere la struttura e le funzioni principali
di: carboidrati, lipidi, proteine, acidi nucleici
Comprendere in che modo le interazioni tra
le varie molecole guidano i processi biologici
In apertura: Lattosio, sì o no?
Latte e latticini sono cibi
nutrienti, ricchi di proteine e
minerali
Per milioni di persone, però, i
benefici di questi alimenti sono
accompagnati da problemi:
sono infatti intolleranti al
lattosio, lo zucchero principale
del latte
Copyright © 2009 Pearson Education, Inc.
3
In apertura: Lattosio, sì o no?
Copyright © 2009 Pearson Education, Inc.
Per assorbire il lattosio, le cellule dell’intestino tenue
devono produrre un enzima, la lattasi, in grado di
accelerare la demolizione del lattosio
4
In apertura: Lattosio, sì o no?
Copyright © 2009 Pearson Education, Inc.
Chi è intollerante al lattosio produce una quantità
insufficiente di lattasi
5
In apertura: Lattosio, sì o no?
La maggior parte degli esseri umani non produce
lattasi in età adulta
La capacità di digerire da adulti è dovuta a una
mutazione genetica
9000 anni fa, questa
mutazione si diffuse
tra le popolazioni
del nord Europa,
quando iniziarono ad
allevare bestiame
da latte
Copyright © 2009 Pearson Education, Inc.
6
Lezione 1
IL CARBONIO, LO “SCHELETRO”
DELLA VITA
7
3.1 La diversità delle molecole che caratterizzano
la vita si fonda sulle proprietà del carbonio
Quasi tutte le molecole sintetizzate dalle cellule
sono composte da atomi di carbonio legati tra loro
e con atomi di altri elementi
– Queste molecole a base di carbonio sono chiamate
composti organici
– Un atomo di carbonio può formare fino a quattro legami
– In questo modo può formare ramificazioni in quattro
direzioni
8
3.1 La diversità delle molecole che caratterizzano la
vita si fonda sulle proprietà del carbonio
Il metano (CH4) è una delle molecole organiche più
semplici
– Quattro atomi di idrogeno sono legati a un atomo di
carbonio mediante quattro legami covalenti
– Ognuno dei quattro trattini nella formula di struttura
rappresenta una coppia di elettroni condivisa
9
Formula
di struttura
Modello a sfere
e bastoncini
modello
molecolare
Metano
I quattro legami del carbonio puntano verso i vertici
di un immaginario tetraedro
10
3.1 La diversità delle molecole che caratterizzano la
vita si fonda sulle proprietà del carbonio
Il metano e i composti costituiti esclusivamente da
carbonio e idrogeno sono chiamati idrocarburi
– Gli atomi di carbonio, legati a quelli di idrogeno,
si uniscono tra loro formando catene di varia lunghezza
11
3.1 La diversità delle molecole che caratterizzano la
vita si fonda sulle proprietà del carbonio
La catena di atomi di carbonio in una molecola
organica è chiamata scheletro carbonioso
– Gli scheletri carboniosi possono essere lineari oppure
ramificati
– Composti con la stessa formula molecolare, ma con
struttura diversa sono chiamati isomeri
12
Etano
Lunghezza.
La catena carboniosa varia in lunghezza
Butano
Ramificazione.
2-Butene
Le catene carboniose possono avere
doppi legami in diverse posizioni
Cicloesano
Anelli.
Isobutano
La catena carboniosa può essere lineare
o ramificata
1-Butene
Doppi legami.
Propano
Benzene
La catena carboniosa può disporsi ad anello
13
Etano
Lunghezza
Propano
Le catene carboniose possono
avere diverse lunghezze
14
Butano
Ramificazioni
Isobutano
La catena carboniosa può essere
lineare o ramificata
15
1-Butene
Doppi legami
2-Butene
La catena carboniosa può
contenere doppi legami
in diverse posizioni
16
Cicloesano
Anelli
Benzene
La catena carboniosa può disporsi
ad anello
17
3.1 La diversità delle molecole che caratterizzano la
vita si fonda sulle proprietà del carbonio
Check
Perché gli isomeri hanno la stessa formula
molecolare (ovvero lo stesso tipo e numero
di atomi) ma proprietà differenti?
18
3.2 Gruppi chimici caratteristici contribuiscono
a determinare le proprietà dei composti organici
Le proprietà esclusive di ogni composto organico
dipendono da
– Dimensioni e forma del suo scheletro carbonioso
– Gruppi di atomi (gruppi funzionali) a esso legati
I gruppi funzionali influenzano in modo specifico
l’esito delle reazioni chimiche
19
3.2 Gruppi chimici caratteristici contribuiscono
a determinare le proprietà dei composti organici
I composti che contengono gruppi funzionali polari
tendono a essere idrofili (“amanti dell’acqua”)
– Sono dunque solubili in acqua, una condizione
essenziale per esplicare il loro importante ruolo nei
processi vitali
20
3.2 Characteristic chemical groups help determine
the properties of organic compounds
I gruppi funzionali sono
– Gruppo ossidrilico OH: un atomo di idrogeno legato a
un atomo di ossigeno
– Gruppo carbonilico: un atomo di carbonio è legato
un atomo di ossigeno da un doppio legame
– Gruppo carbossilico: un atomo di carbonio unito a un
atomo di ossigeno, con un doppio legame, e a un
gruppo ossidrilico, con un legame semplice
– Gruppo amminico: un atomo di azoto legato a due
atomi di idrogeno e a uno scheletro carbonioso
– Gruppo fosfato: costituito da un atomo di fosforo
legato a quattro atomi di ossigeno
21
22
23
24
3.2 Gruppi chimici caratteristici contribuiscono
a determinare le proprietà dei composti organici
Un esempio di composti simili che differiscono solo
per i gruppi funzionali è quello di due ormoni
sessuali:
– L’estradiolo è l’ormone sessuale femminile
– Il testosterone è l’ormone sessuale maschile
– Nonostante differiscano solo per i gruppi funzionali sono in
grado di guidare lo sviluppo dei caratteri sessuali maschili o
femminili
25
Estradiolo
Leonessa
Testosterone
Leone
26
Estradiolo
Leonessa
27
Testosterone
Leone
28
3.2 Gruppi chimici caratteristici contribuiscono
a determinare le proprietà dei composti organici
Check
Tra i seguenti gruppi funzionali, quali non
contengono carbonio?
Carbonilico
Carbossilico
Fosfato
Metilico
Ossidrilico
Amminico
29
3.3 Le cellule sintetizzano molti tipi di grandi
molecole a partire da un numero limitato
di molecole più piccole
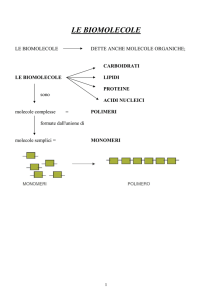
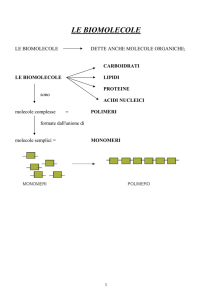
Le grandi molecole biologiche si dividono in
quattro classi principali
– Carboidrati
– Lipidi
– Proteine
– Acidi nucleici
30
3.3 Le cellule sintetizzano molti tipi di grandi
molecole a partire da un numero limitato
di molecole più piccole
Date le notevoli dimensioni, queste molecole sono
indicate dai biologi come macromolecole
Le cellule sintetizzano la maggior parte delle
macromolecole unendo molecole più piccole in
catene chiamate polimeri
Le unità che costituiscono i polimeri sono chiamate
monomeri
31
3.3 Le cellule sintetizzano molti tipi di grandi
molecole a partire da un numero limitato
di molecole più piccole
La cellula sintetizza una grande varietà di polimeri
partendo da un numero ridotto di monomeri
– Le proteine sono costruite utilizzando solo venti
amminoacidi diversi, mentre per il DNA bastano quattro
basi azotate
I monomeri utilizzati dalle cellule sono comuni
a tutti gli organismi
32
3.3 Le cellule sintetizzano molti tipi di grandi
molecole a partire da un numero limitato
di molecole più piccole
Le cellule uniscono i monomeri per “costruire” i
polimeri mediante reazioni di condensazione
Per demolire i polimeri, le cellule compiono una
reazione di idrolisi
Queste reazioni necessitano dell’aiuto di enzimi,
proteine specializzate che accelerano le reazioni
chimiche cellulari
33
Polimero a catena breve
Monomero
libero
34
Polimero a catena breve
Monomero
libero
Reazione
di disidratazione
Polimero più lungo
35
36
Idrolisi
37
3.3 Le cellule sintetizzano molti tipi di grandi
molecole a partire da un numero limitato
di molecole più piccole
Check
Con quali reazioni gli amminoacidi che fanno parte
delle proteine di un formaggio vengono riassemblati
per formare le proteine del nostro corpo?
38
Lezione 2
I CARBOIDRATI
39
3.4 I monosaccaridi sono i carboidrati più semplici
I carboidrati sono una classe di molecole di
dimensioni molto varie
– Dalle piccole molecole dello zucchero sciolto nelle
bibite…
– … alle grandi molecole di amido, un polisaccaride
presente nella pasta e nelle patate
40
41
3.4 I monosaccaridi sono i carboidrati più semplici
In genere la formula molecolare di un
monosaccaride è un multiplo della semplice
formula CH2O
Diversi monosaccaridi differiscono solo nella
disposizione degli atomi (sono isomeri)
– Differenze apparentemente trascurabili come queste
conferiscono agli isomeri proprietà diverse
I monosaccaridi, in particolare il glucosio, sono il
principale combustibile chimico della cellula
42
Glucosio
(un aldoso)
Fruttosio
(un chetoso)
43
Formula
di struttura
Formula
semplificata
Struttura
semplificata
44
3.4 I monosaccaridi sono i carboidrati più semplici
Check
Scrivi la formula molecolare di un monosaccaride con
tre atomi di carbonio
45
3.5 Le cellule formano i disaccaridi unendo due
monosaccaridi
La cellula sintetizza i disaccaridi a partire da due
monosaccaridi con una reazione di condensazione
– Il disaccaride più comune è il saccarosio, costituito da
glucosio e fruttosio
46
3.5 Le cellule formano i disaccaridi unendo due
monosaccaridi
Check
Il lattosio, il disaccaride del latte, è costituito da
glucosio e galattosio. La formula di entrambi questi
monosaccaridi è C6H12O6
– Qual è la formula molecolare del lattosio?
47
Glucosio
Glucosio
48
Glucosio
Glucosio
Maltosio
49
3.6 Lo sciroppo di mais ad alto contenuto
di fruttosio può essere uno dei responsabili
dell’obesità?
COLLEGAMENTO
salute
Dall’idrolisi dell’amido si ottiene glucosio, che in parte può
essere convertito in fruttosio per ottenere un dolcificante
più gustoso del solo glucosio
Questo dolcificante, conosciuto come sciroppo di mais ad
alto contenuto di fruttosio (high-fructose corn syrup o
HFCS), è contenuto in molti prodotti industriali
– Sembra che l’incidenza di diabete di tipo 2 e di malattie croniche
associate all’aumento di peso sia cresciuta quando è aumentato il
consumo di HFSC
– Secondo gli scienziati un eccessivo consumo di dolcificanti e grassi
insieme a una ridotta attività fisica favoriscono l’aumento di peso
50
51
3.7 I polisaccaridi sono lunghe catene di
monosaccaridi
I polisaccaridi sono polimeri di monosaccaridi
– Sono usati dagli organismi come depositi di energia o
come composti strutturali
52
3.7 I polisaccaridi sono lunghe catene di
monosaccaridi
Amido: polisaccaride di riserva energetica nelle
piante; è costituito da monomeri di glucosio
Glicogeno: polisaccaride di riserva energetica
degli animali; è costituito da monomeri di glucosio
Cellulosa: è il polimero di glucosio con cui sono
costituite le pareti cellulare nelle piante
Chitina: è un polisaccaride con cui insetti e
crostacei costruiscono il proprio esoscheletro
53
3.7 I polisaccaridi sono lunghe catene di
monosaccaridi
Quasi tutti i carboidrati sono idrofili a causa dei
numerosi gruppi ossidrilici presenti nei monomeri
da cui sono formati
54
Granuli di amido
in cellule di patata
Granuli
di glicogeno
nel tessuto
muscolare
AMIDO
Monomero
di glucosio
GLICOGENO
CELLULOSA
Fibrille di cellulosa nella parete
di una cellula vegetale
Legami idrogeno
Molecole
di cellulosa
55
Granuli di amido
in cellule di patata
AMIDO
Monomero
di glucosio
56
Granuli
di glicogeno
nel tessuto
muscolare
GLICOGENO
57
CELLULOSA
Fibrille di cellulosa nella parete
di una cellula vegetale
Legami idrogeno
Molecole
di cellulosa
58
3.7 I polisaccaridi sono lunghe catene di
monosaccaridi
Check
Amido e cellulosa sono due polisaccaridi di origine
vegetale; quali sono le somiglianze e le differenze tra
i due?
59
Lezione 3
I LIPIDI
60
3.8 I grassi sono lipidi impiegati principalmente
per immagazzinare energia
I lipidi sono composti idrofobi (“temono l’acqua”)
importanti per immagazzinare energia
– Contengono il doppio di energia di un polisaccaride
I grassi (trigliceridi) sono lipidi costituiti da
glicerolo e acidi grassi
61
62
3.8 I grassi sono lipidi impiegati principalmente per
immagazzinare energia
Gli acidi grassi si legano al glicerolo per
condensazione formando i trigliceridi
– Un trigliceride contiene una molecola di glicerolo legata
a tre acidi grassi
63
Glicerolo
Acido grasso
64
65
3.8 I grassi sono lipidi impiegati principalmente per
immagazzinare energia
Alcuni acidi grassi contengono doppi legami
– Per questo si formano pieghe nella catena carboniosa
– Sono detti insaturi perché hanno un numero di atomi
di idrogeno inferiore agli acidi grassi privi di doppi
legami (saturi)
– Le pieghe degli acidi grassi insaturi impediscono alle
molecole di compattarsi e di solidificare a temperatura
ambiente
66
3.8 I grassi sono lipidi impiegati principalmente per
immagazzinare energia
Check
Che cosa sono i grassi?
67
3.9 I fosfolipidi e gli steroidi sono lipidi che svolgono
una grande varietà di funzioni
I fosfolipidi sono strutturalmente simili ai trigliceridi
e sono componenti fondamentali della cellula
– Sono i costituenti principali della membrana cellulare,
formata da un doppio strato di fosfolipidi
– Le “teste” idrofile, costituite dal gruppo fosfato sono rivolte
verso l’ambiente acquoso interno ed esterno
– Le “code” idrofobe, costituite dagli acidi grassi, sono
raggruppate nel mezzo
68
Teste
idrofile
Acqua
Code
idrofobe
Acqua
69
3.9 I fosfolipidi e gli steroidi sono lipidi che svolgono
una grande varietà di funzioni
Gli steroidi sono lipidi il cui scheletro carbonioso è
costituito da quattro anelli uniti tra loro
– Il colesterolo è un importante steroide presente nelle
membrane delle cellule animali
– È anche il materiale di partenza per sintetizzare altri
steroidi, tra cui gli ormoni sessuali
70
71
3.9 I fosfolipidi e gli steroidi sono lipidi che svolgono
una grande varietà di funzioni
Check
Perché gli ormoni sessuali umani sono considerati
lipidi?
72
3.10 Gli steroidi anabolizzanti costituiscono un
grave rischio per la salute
Gli steroidi anabolizzanti sono varianti
sintetiche del testosterone, che determinano uno
sviluppo della muscolatura e delle ossa
– Possono essere utilizzati a fini terapeutici
– In ambito sportivo sono sfruttati (illegalmente) per
potenziare le prestazioni, ponendo gli atleti in serio
pericolo
73
74
Lezione 4
LE PROTEINE
75
3.11 Le proteine svolgono un ruolo fondamentale
in molte strutture e funzioni cellulari
Una proteina è un polimero costituito da
monomeri chiamati amminoacidi
– Ogni proteina ha una struttura tridimensionale unica
che corrisponde a una specifica funzione
76
3.11 Le proteine svolgono un ruolo fondamentale
in molte strutture e funzioni cellulari
Gli enzimi sono proteine che agiscono da
catalizzatori nella cellula
Le proteine strutturali si trovano nei peli dei
mammiferi e nelle fibre di tessuti connettivi come i
tendini e i legamenti
Le proteine contrattili come l’actina e la miosina
si trovano nei muscoli
Le proteine di difesa, come gli anticorpi,
contribuiscono a combattere le infezioni
77
3.11 Le proteine svolgono un ruolo fondamentale in
molte strutture e funzioni cellulari
Le proteine regolatrici (o proteine-segnale)
sono ormoni e altri messaggeri che contribuiscono
a coordinare le attività dell’organismo
Le proteine-recettore si trovano all’interno delle
membrane cellulari e favoriscono il riconoscimento
di particolari molecole
Le proteine di trasporto spostano le sostanze
nel corpo
78
79
3.11 Le proteine svolgono un ruolo fondamentale in
molte strutture e funzioni cellulari
Check
Quale, tra le macromolecole indicate, non è una proteina?
– Emoglobina
– Colesterolo
– Ovalbumina
– Lattasi
– Actina
80
3.12 Le proteine sono costituite da amminoacidi
legati mediante legami peptidici
Tutti gli amminoacidi contengono un gruppo
amminico e un gruppo carbossilico
– Questi sono uniti da un legame covalente a un atomo di
carbonio centrale, chiamato carbonio alfa
– Al carbonio alfa sono legati anche un atomo di idrogeno
e il gruppo R, o catena laterale
81
Gruppo
amminico
Gruppo
carbossilico
82
3.12 Le proteine sono costituite da amminoacidi
legati mediante legami peptidici
Gli amminoacidi possono essere divisi in idrofili e
idrofobi
– Quelli con un gruppo R polare sono idrofili
– Quelli con un gruppo R apolare sono idrofobi
83
Leucina (Leu)
Apolare idrofobo
Serina (Ser) Acido aspartico (Asp)
Polari idrofili
84
3.12 Le proteine sono costituite da amminoacidi
legati mediante legami peptidici
Gli amminoacidi (monomeri) sono uniti per
formare le catene polipetidiche (polimeri)
– Ciò avviene tramite una reazione di disidratazione
guidata da un enzima
– Il gruppo carbossilico di un amminoacido si lega al
gruppo amminico di quello successivo, liberando una
molecola di acqua
– Il legame covalente risultante si chiama legame peptidico
85
Gruppo
Gruppo
carbossilico amminico
Amminoacido
Amminoacido
86
Gruppo
Gruppo
carbossilico amminico
Amminoacido
Legame
peptidico
Reazione
di disidratazione
Amminoacido
Dipeptide
87
3.12 Le proteine sono costituite da amminoacidi
legati mediante legami peptidici
Check
Che cosa accomuna la sintesi di un dipeptide con
quella di un polisaccaride?
88
3.13 La forma specifica di una proteina determina
la sua funzione
La sequenza di amminoacidi che compongono un
polipeptide fa sì che esso assuma una particolare
forma
La forma di una proteina determina la sua specifica
funzione
89
Tasca
90
Tasca
91
3.13 La forma specifica di una proteina determina la
sua funzione
Alterando la forma di una proteina si modifica
anche la sua funzionalità
– Attraverso la denaturazione le catene polipeptidiche si
svolgono e la proteina perde la propria forma
– La denaturazione delle proteine può essere causata da
una variazione della concentrazione salina o del pH
92
3.13 La forma specifica di una proteina determina la
sua funzione
Check
Perché una proteina denaturata non funziona più
normalmente?
93
3.14 Nella forma di una proteina si distinguono
quattro livelli strutturali
esplorando
Una proteina può avere quattro livelli di struttura
– Struttura primaria
– Struttura secondaria
– Struttura terziaria
– Struttura quaternaria
94
3.14 Nella forma di una proteina si distinguono
quattro livelli strutturali
esplorando
La struttura primaria di una proteina è
rappresentata dalla sequenza di amminoacidi
– La corretta sequenza è precisamente definita dal
patrimonio genetico della cellula
– Anche un leggero cambiamento nella struttura primaria
della proteina può avere effetti sulla forma complessiva
della molecola e sulla sua funzione
95
3.14 Nella forma di una proteina si distinguono
quattro livelli strutturali
esplorando
La struttura secondaria di una proteina è
rappresentata dall’avvolgimento o dal ripiegamento
di parti del polipeptide
– L’avvolgimento a elica della catena polipeptidica
determina la formazione di alfa eliche
– Un particolare tipo di ripiegamento porta invece al
foglietto ripiegato (o foglietto beta)
– Queste strutture si formano grazie a legami idrogeno che si
formano a intervalli regolari lungo la catena polipeptidica
96
Le ghiandole addominali
del ragno producono
le fibre della ragnatela,
costituite da una proteina
fibrosa ricca di foglietti beta
Le fibre radiali, rigide,
contribuiscono a fissare
la forma della ragnatela
Le fibre concentriche,
usate per catturare le prede,
sono elastiche
e conferiscono resistenza
a vento, pioggia, aggressioni
97
Catena
polipeptidica
Collagene
98
3.14 Nella forma di una proteina si distinguono
quattro livelli strutturali
esplorando
La struttura terziaria è la forma tridimensionale
complessiva assunta da un polipeptide
– Solitamente la struttura terziaria di un polipeptide deriva
dalle interazioni tra i gruppi R dei suoi amminoacidi
– La forma di una proteina può essere ulteriormente
stabilizzata da legami covalenti chiamati ponti
disolfuro
99
3.14 Nella forma di una proteina si distinguono
quattro livelli strutturali
esplorando
Molte proteine sono costituite da due o più
polipeptidi (subunità) che, associandosi,
costituiscono una struttura quaternaria
– Il collagene è una proteina fibrosa con subunità
elicoidali avvolte a formare una tripla elica più spessa
– Questa struttura quaternaria conferisce alle fibre di
collagene una grande resistenza alla trazione
100
Struttura primaria
Amminoacidi
101
Struttura primaria
Amminoacidi
Legame
idrogeno
Struttura secondaria
Alfa elica
Foglietto beta
102
Struttura primaria
Amminoacidi
Legame
idrogeno
Struttura secondaria
Alfa elica
Foglietto beta
Struttura terziaria
Polipeptide
(singola subunità
di transtiretina)
103
Struttura primaria
Amminoacidi
Legame
idrogeno
Struttura secondaria
Alfa elica
Foglietto beta
Struttura terziaria
Polipeptide
(singola subunità
di transtiretina)
Struttura quaternaria
Transtiretina,
con le sue quattro
subunità identiche
104
Amminoacidi
Struttura primaria
105
Amminoacidi
Legame
idrogeno
Alfa elica
Foglietto beta
Struttura secondaria
106
Polipeptide
(singola subunità
di transtiretina)
Struttura terziaria
107
Transtiretina,
con le sue quattro
subunità identiche
Struttura quaternaria
108
3.14 Nella forma di una proteina si distinguono
quattro livelli strutturali
esplorando
Check
Una mutazione genetica può alterare la struttura
primaria di una proteina. In che modo ciò potrebbe
incidere anche sulla funzione della proteina
interessata?
109
Lezione 5
ACIDI NUCLEICI
110
3.15 Gli acidi nucleici sono polimeri di nucleotidi
coinvolti nella formazione delle proteine
Gli acidi nucleici (polinucleotidi) sono polimeri
costituiti da monomeri detti nucleotidi
– I nucleotidi sono composti da tre parti
– Uno zucchero a cinque atomi ci carbonio: ribosio per l’RNA,
desossiribosio per il DNA)
– Un gruppo fosfato
– Una base azotata
111
Base
azotata
(adenina)
Gruppo
fosfato
Zucchero
112
3.15 Gli acidi nucleici sono polimeri di nucleotidi
coinvolti nella formazione delle proteine
Le basi azotate del DNA sono:
– Adenina
– Timina
– Guanina
– Citosina
Le basi azotate dell’RNA sono:
– Adenina
– Uracile
– Guanina
– Citosina
113
3.15 Gli acidi nucleici sono polimeri di nucleotidi
coinvolti nella formazione delle proteine
Gli acidi nucleici si formano quando più nucleotidi
si uniscono tramite condensazione
Il gruppo fosfato di un nucleotide si lega allo
zucchero del monomero successivo
– Il risultato è uno scheletro di unità zucchero-fosfato, da
cui si proiettano le basi azotate
114
Nucleotide
Scheletro
zucchero-fosfato
115
3.15 Gli acidi nucleici sono polimeri di nucleotidi
coinvolti nella formazione delle proteine
Il DNA ha una configurazione a doppia elica: due
polinucleotidi avvolti a spirale l’uno intorno all’altro
– Le due catene sono tenute unite dai legami idrogeno si
formano tra le basi azotate appaiate
– A si appaia sempre con T
– C si appaia sempre con G
L’RNA, solitamente, è costituito da un unico
filamento polinucleotidico
116
Coppia
di basi
azotate
117
3.15 Gli acidi nucleici sono polimeri di nucleotidi
coinvolti nella formazione delle proteine
Check
In che modo RNA e DNA cooperano a livello
funzionale?
118
3.16 La tolleranza al lattosio è un evento recente
nell’evoluzione umana
alla luce dell’evoluzione
La maggior parte degli esseri umani smette di sintetizzare
l’enzima lattasi nella prima infanzia
La capacità di continuare a produrlo anche in età adulta è
diffusa nelle popolazioni di origini nordeuropee
Questo carattere è diventato comune in questo gruppo
perché vantaggioso per la sopravvivenza
Nel clima nordeuropeo, gli esseri umani dovevano sfruttare
risorse alimentari non vegetali, tra cui latte e i latticini
I portatori di un’alterazione genetica che permetteva di
continuare a produrre la lattasi in età adulta risultavano
avvantaggiati: perciò l’alterazione si diffuse e fu
tramandata
119
120
3.16 La tolleranza al lattosio è un evento recente
nell’evoluzione umana
alla luce dell’evoluzione
Check
Il caso dell’intolleranza al lattosio coinvolge tre delle
quattro classi principali di macromolecole organiche.
Quali sono?
121