Malattie Mitocondriali
Malattie legate al cromosoma X
Massimo Zollo
5000 fenotipi umani
Mendeliani:
50% tratti autosomici dominanti
36% autosomici recessivi
10% X linked
di 5000 caratteri , 4000 sono associati
a malattie umane per 600 sono state
identificate una o piu’ mutazioni
responsabili di malattia!
Mitocondrio….
mtDNA
16569 coppie di basi
e possiede 37 geni
Le funzioni del mitocondrio
Il mitocondrio è in grado di svolgere molteplici funzioni.
La più importante tra esse consiste nell'estrarre energia dai substrati organici
che gli arrivano per produrre un gradiente ionico che
viene sfruttato per produrre ATP.
Gli altri processi in cui il mitocondrio interviene sono:
1) l'apoptosi e la morte neuronale da tossicità da glutammato,
2) regolazione del ciclo cellulare,
3) regolazione dello stato redox della cellula,
4) sintesi dell'eme,
5) sintesi del colesterolo,
6) produzione di calore.
La produzione di energia
utilizzando i principali prodotti della glicolisi: il piruvato ed il NADH.
Essi vengono sfruttati in due processi:
il ciclo di Krebs e la fosforilazione ossidativa.
• Sono gli organuli deputati alla
respirazione cellulare aerobica
(Combustione di glucosio fino a CO2 +
H2O con produzione di ATP)
• Si trovano in tutte le cellule eucariotiche
• Sono più numerosi nelle cellule
metabolicamente attive (fino a 1000
negli epatociti)
• Hanno lunghezza 2-8μm
• Possono cambiare forma
• Si replicano per divisione
matrix
cristae
intermembrane
space
inner
membrane mitochondrion
outer
membrane
• Hanno Membrana Esterna, liscia, permeabile
alle sostanze piccole
• Membrana Interna, selettivamente
permeabile
• Tra le due membrane c’è lo spazio
intermembranoso
• La membrana interna si ripiega nelle creste
mitocondriali che si estendono nella matrice
(compartimento circondato dalla membrana
interna)
matrix
cristae
intermembrane
space
inner
membrane mitochondrion
outer
membrane
• Nella matrice si trovano gli enzimi che
degradano le molecole alimentari
• Nelle creste l’energia chimica delle molecole
alimentari viene trasformata in ATP
• Nei mammiferi un mitocondrio ha 5-10 molecole
di DNA circolare (1% del DNA totale) che è
ipermutabile
• I mitocondri sono coinvolti nell’ apoptosi (PCD)
matrix
cristae
intermembrane
space
inner
membrane mitochondrion
outer
membrane
Apoptosi o morte cellulare programmata
Kerr and Searle (1972) termine col quale si
indica la caduta delle foglie dagli alberi o dei
petali dai fiori
necrosi
-processo passivo e
degenerativo
-degradazione “random”
della cromatina
-rigonfiamento e
rottura dei mitocondri
-rottura del
plasmalemma con
conseguente rilascio di
materiale intracellulare
(compreso proteasi)
-stimolazione di una
reazione infiammatoria
apoptosi
-condensazione
-esposizione di
componenti nascoste del
plasmalemma
-disgregazione del
nucleolo, taglio della
lamina, degradazione
oligonucleosomale della
cromatina
-granuli periferici di
cromatina
-blebbing e formazione
dei corpi apoptotici che
verranno fagocitati
COSA SI CONOSCE OGGI…..
Trans-splicing
CARATTERISTICHE dell’ mtDNA
• POLIPLASMIA
• ETEROPLASMIA
• EFFETTO SOGLIA
• SEGREGAZIONE MITOTICA
• EREDITÀ MATERNA
POLIPLASMIA
In ogni cellula sono presenti molti mitocondri ed ogni mitocondrio
contiene multiple copia del suo genoma (eccetto piastrine e ovulo non
fertilizzato) migliaia di copie mtDNA / cell.
Durante la divisione cellulare i mitocondri vengono distribuiti
casualmente alle cellule figlie e quindi la genetica mitocondriale è più
simile alla genetica di popolazione che alla genetica mendeliana.
ETEROPLASMIA
In tessuti normali tutte le copie di mtDNA sono identiche omoplasmia.
Nel caso di una mutazione del mtDNA questa può colpire tutte le copie
oppure essere presente solo in una percentuale di genomi eteroplasmia.
Generalmente i polimorfismi neutrali sono omoplasmici mentre la maggior
parte delle mutazioni-malattia sono eteroplasmiche eteroplasmia
cellulare o mitocondriale?
EFFETTO SOGLIA
L’espressione clinica delle mutazioni del mtDNA è
determinata dalla relativa proporzione wild type / mutato in
un determinato tessuto; è necessario un numero minimo di
copie per danneggiare il metabolismo energetico di un
determinato organo o tessuto (valore relativo e non assoluto)
(SNC, cuore, muscolo, rene e ghiandole esocrine) (bilancio
energetico).
SEGREGAZIONE MITOTICA
Durante la divisione cellulare la proporzione di genomi
mutati può variare per deriva nelle cellule figlie, con
conseguente cambiamento fenotipico.
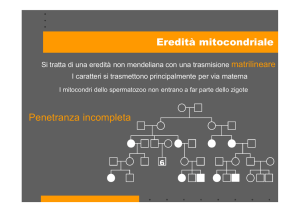
EREDITÀ MATERNA
Virtualmente tutti i mitocondri dello zigote derivano dall’oocita e perciò la
modalità di trasmissione delle mutazioni mt differisce dalla trasmissione
mendeliana classica:
madre portatrice trasmissione a tutta la progenie, ma solo le figlie femmine
possono trasmettere la mutazione ai loro figli.
Eteroplasmia + effetto dose eccezioni fenotipiche all’eredità matrilineare.
Ereditarietà mitocondriale
DIFETTI DEL DNA MITOCONDRIALE
1) sostituzioni nucleotidiche
cag cac agc ac
gtc gtc gtc Tt
2) A-delezioni / B- inserzioni
A cag --- agc ac
gtc --- gtc tt
B
cag cag -agc ac
gtc gtc Cgtc tt
SOSTITUZIONI NUCLEOTIDICHE
Generalmente associate a patologie neurologiche ed oftalmologiche.
Leber’s Hereditary Optic Neuropathy (LHON)
Cecità ad insorgenza tardiva dovuta alla morte del nervo ottico è generalmente
determinata da un cambio arg-his (np 11778) presente in omoplasmia nella
maggioranza dei pazienti, ma può essere determinata da numerose altra mutazioni a
carico dei complessi per il trasporto degli elettroni, talora anche in combinazione: la
probabilità di cecità aumenta negli individui con mutazioni più gravi o nella
combinazione di mutazioni diverse.
Neurogenic muscle weakness, Ataxia and Retinite Pigmentosa (NARP)
Retinite pigmentosa, atassia, convulsioni, demenza, debolezza muscoli prossimali di
origine neurogena, neuropatia sensitiva e ritardo nello sviluppo è determinata da
un cambio leu-arg (np 8993) nell’ATPasi6; tale mutazione è sempre presente in
eteroplasmia e la gravità dei sintomi è correlata alla percentuale del DNA mutante.
PAUSA
rilassiamo i mitocondri….
Glycolysis occurs in the
cytosol of cells.
Pyruvate enters the
mitochondrion to be
metabolized further.
Mitochondrial
Compartments:
matrix
cristae
intermembrane
space
inner
membrane mitochondrion
outer
membrane
The matrix contains Pyruvate Dehydrogenase, enzymes
of Krebs Cycle, and other pathways, e.g., fatty acid
oxidation & amino acid metabolism.
The outer membrane contains large VDAC channels,
similar to bacterial porin channels, making the outer
membrane leaky to ions & small molecules.
Pyruvate Dehydrogenase
H3C
O
O
C
C
pyruvate
HSCoA
O
O
H3C
NAD+ NADH
C
S
CoA
+ CO2
acetyl-CoA
Pyruvate Dehydrogenase, catalyzes oxidative
decarboxylation of pyruvate, to form acetylCoA.
Mitocondrio
umano
COX1
COX2
COX3
Evoluzione
Tecniche Forensiche
MalattieMITO
http://www.webalice.it/prati_50/malattiemito.htm
•
•
•
•
•
•
•
•
•
•
•
•
•
•
•
•
•
•
•
•
•
•
•
•
•
•
•
•
•
•
Malattia Di Alpers - Polidistrofia cerebrale progressiva infantile. Sindrome Di Barth - Cardiomiopatia Infantile Mortale.
Mancanza Della Carnitina: Malattie con disturbo della demolizione degli acidi grassi - Codice di esenzione: RCG070 Carenza della CPT (carnitin-palmitin-trasferasi)
Mancanza Del Complesso I - carenza di NADH deidrogenasi (NADH-CoQ riduttasi).
Mancanza Del Complesso II - Carenza di succinato deidrogenasi.
Mancanza Del Complesso III - Carenza di Ubiquinone-citocromo c ossidoriduttasi.
Mancanza Del Complesso IV/Mancanza Del Cox –
Mancanza Complessa Di V - Mancanza del Trifosfato di adenosina Synthase:Sindrome della oftalmoplegia esterna progressiva cronica.
CPEO - Sindrome Esterna Progressiva Cronica Di Oftalmoplegia: Eredità mendeliana - materna - sporadica .
MELAS - Codice di esenzione: RN0710 KSS - sindrome di Kearns-Sayre (spodadica) - Codice di esenzione: RF0020 NARP Inizio: Infanzia - eredità materna Codice di esenzione: RF0030
MILS - Sindrome di Leigh ereditata per via matrilineare Codice di esenzione: RF0030
MERFF - Epilessia mioclonica, con le fibre ragged-rosse - Eredità materna o sporadica - Codice di esenzione: RF0020 Sindrome di Pearson: Eredità sporadica - Inizio: Infanzia - Codice di esenzione: RN1600 MDS La sindrome da deplezione del DNA mitocondriale - Codice di esenzione: RN0710 MNGIE : - Codice di esenzione: RN0710 Mancanza di CPT I
Mancanza di CPT II
Acidosi lattica :
LCAD - Mancanza A catena lunga Della Deidrogenasi Dell'Acilico-CoA
Sindrome di Leigh: da http://www.telethon.it/
Codice di esenzione: RF0030
LHON
La neuropatia ottica ereditaria di Leber (LHON)
Malattia Di Luft : Sintomi: Ipermetabolismo,
Mancanza Della Carbossilasi Del Piruvato :
Mancanza Della Deidrogenasi Del Piruvato :
Malattia di Alzheimer: il cinque per cento circa dei malati anziani presenta la stessa mutazione del DNA mitocondriale
La sindrome da deplezione del DNA mitocondriale (MDS)
DISORDINI
•
MITOCONDRIALI
a)Mutazioni puntiformi situate in geni codificati tRNA
• - Epilessia mioclonica con fibre Regged
Red (MERRF) -neuromuscolare comprende epilessia,
atassia progressiva., ipostenia ed ipotrofia muscolare, sordità e
demenza.
Transizione A>G nel gene per il tRNA-Lys
• - Encefalomiopatia mitocondriale,
acidosi lattica ed episodi tipo stroke
(MELAS o MALAS) difetti di crescita, acidosi lattica
persistente, episodi di vomito,
tRNA-Leu (UUR),
DISORDINI
MITOCONDRIALI
• b)Mutazioni puntiformi situate in geni che
codificano subunità proteiche degli enzimi
mitocondriali.
• Atrofia ottica di Leber (LHON)
ereditarietà materna -perdita della visione
centrale bilaterale-mutazioni puntiformi a
carico del geni che codificano subunità
proteiche degli enzimi mitocondriali
Leber’s Hereditary Optic Neuropathy (LHON)
Cecità ad insorgenza tardiva dovuta alla morte del nervo ottico è generalmente
determinata da un cambio arg-his (np 11778) presente in omoplasmia nella
maggioranza dei pazienti, ma può essere determinata da numerose altra mutazioni a
carico dei complessi per il trasporto degli elettroni, talora anche in combinazione: la
probabilità di cecità aumenta negli individui con mutazioni più gravi o nella
combinazione di mutazioni diverse.
DISORDINI
MITOCONDRIALI
• Neuropatia, Atassia e Retinite
Pigmentosa (NARP) Retinite pigmentosa,
cecità, atassia, crisi epilettiche-mutazioni
nel gene per la subunità 6 del complesso
V (ATPase 6).
DISORDINI
MITOCONDRIALI
• DELEZIONI SPORADICHE
• Sindrome di Kearns-Sayre (KSS) difetto di
conduzione cardiaca, sindrome celebrale, elevato contenuto proteiconel liquido
cerebrospinale (> 100 mg/dl).
• Miopatia oculare pura (OM)
• Sindrome di Pearson- tessuti emopoietici, il pancreas
esocrino, il fegato e i reni. Il quadro più tipico è quello di una anemia
macrocitica, accompagnata da neuropenia e trombocitopenia
DISORDINI
MITOCONDRIALI
• DELEZIONI MULTIPLE
• Delezione multipla ed ereditarietà autosomica
dominante -della D-loop ed il tratto corrispondente ai geni per l’ATPasi 6 e 8.
• DEPLEZIONE DI DNA MITOCONDRIALE
• Miopatia mitocondriale infantile fatale
associata a deplezione del mtDNA -Marcata ipotonia
muscolare, ptosi, oftalmoplegia-deficit di citocromo b ed aa3 nel tessuto
muscolare.
• Epatopatia mitocondriale infantile fatale
associata a delezione del mtDNA.
Malattia di Alzheimer: il cinque per cento circa dei malati anziani
presenta la stessa mutazione del DNA mitocondriale
•
Alzheimer’s disease is the most common cause of dementia. The
disease is age-sensitive, afflicting about 3% of people between 65 to 74
years of age, and rising to an incidence of nearly 50% in those over
age 85.
• The classification of diabetes mellitus as Type 1 and 2 was
changed in 1997 from the old classification of Insulindependent diabetes mellitus (IDDM) and Non-insulindependent diabetes mellitus (NIDDM).
L’atassia di Friedreich
esempio di malattia mitocondriale
(OMIM 229300)
• Autosomica recessiva
• Incidenza: 1/30000-1/50000 nati vivi (Italia:
1/22000-1/25000). Frequenza minore nelle
popolazioni asiatiche e africane
• Insorgenza solitamente prima dei 20 anni
atassia e scoliosi (varianti rare: insorgenza fino
a 50 anni o entro la prima decade di vita)
• Durata della vita ridotta
Alterazioni biochimiche e
cellulari
• Alterazioni mitocondriali:
- attività aconitasi ed enzimi dei complessi I-III
della catena respiratoria (N.B. enzimi che
contengono un gruppo Fe-S)
- accumulo di ferro intramitocondriale
- perdita di DNA mitocondriale
• fosfolipidi nella corteccia cerebellare e
occipitale
• Perdita neuronale nel midollo spinale, nella
corteccia e nel cervelletto
Manifestazioni cliniche
• Atassia, nistagmo,
disartria, segno di
Babinski, spasticità,
debolezza delle estremità
inferiori, alterazioni
sensoriali, riduzione o
perdita dei riflessi
tendinei, riduzione o
assenza dei potenziali
somatosensoriali
• Anomalie scheletriche:
scoliosi e piede cavo
• Anomalie cardiache:
cardiomiopatia ipertrofica,
stenosi muscolare
subaortica, dilatazione
del ventricolo sinistro,
alterazioni della
contrattilità cardiaca
• Anomalie endocrine:
diabete mellito
• Alterazioni sfinteriche
EREDITARIETA’ LEGATA AL SESSO
Eredità X-Linked recessiva
• l’ individuo affetto è più frequentemente un maschio
• i maschi affetti sono comunemente nati da genitori sani
– la malattia viene ereditata dalla madre che è portatrice
sana (eterozigote) e può avere parenti maschi affetti
• le femmine portatrici sono fenotipicamente normali
(asintomatiche)
– in media, 1 su 4 figli è affetto
• in media il 50% dei maschi di una fratria è affetto
• NON vi è trasmissione da padre a figlio maschio
– ma un matrimonio di un maschio affetto con una
femmina portatrice può simulare una trasmissione da
maschio a maschio
Eredità X-Linked dominante (rara)
• generalmente le femmine sono affette il doppio delle
volte dei maschi
– certe malattie sono letali nel maschio emizigote
• le femmine sono spesso affette più lievemente e con
più variabilità dei maschi
– dovuto all’inattivazione del cromosoma X (o
Lyonizzazione)
• padri affetti possono avere solo figlie femmine affette
ma non figli maschi affetti
• in media il 50% di tutti i figli di una madre affetta
saranno affetti
Eredità Y-Linked (rara)
• solo gli individui maschi sono affetti
• trasmissione diretta da padre a figlio
– cromosoma Y
• i figli maschi affetti avranno sempre un padre affetto
– a meno che sia insorta una nuova mutazione
• per esempio nei geni che inducono la
differenziazione di un embrione in un maschio, che
esprimono fattori spermatogenetici, gli antigeni minori
dell’istocompatibilità (HY)
Analisi di alberi genealogici:
eredità X-linked recessiva
Il gene che dà la malattia è trasmesso dal cromosoma X: dalle madri
passa ai figli maschi e alle figlie, e dai padri alle figlie ma non ai figli
maschi
– i maschi non affetti non hanno il gene che dà la malattia (non possono
essere portatori)
– la madre di un figlio maschio affetto è portatore obbligato, a meno che
il figlio abbia una nuova mutazione
– mutazioni nuove sono comune per molte malattie recessive X- linked
– tutte le figlie di un padre affetto ed il 50% delle figlie di na madre
portatrice, sono portatrici
– discendendo di generazione in generazione nell’albero genealogico
sulla linea femminile, il rischio di essere portatrice si dimezza ad ogni
generazione
Eredità X-linked recessiva
normale (XHY) x portatrice sana (XHXh)
50% femmine, normali
50% femmine, portatrici
50% maschi, normali
50% maschi, affetti
Eredità X-linked dominante
affetti (XBY) x normali (XbXb)
100% femmine, affette
100% maschi, normali
normali (XbY) x affette (XbXB)
50% femmine, normali
50% femmine, affette
50% maschi, normali
50% maschi, affetti
Eredità Y-linked dominante
affetti (X Y) x normali (X X)
100% femmine, normali
100% maschi, affetti
EMOFILIA