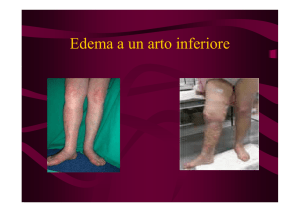
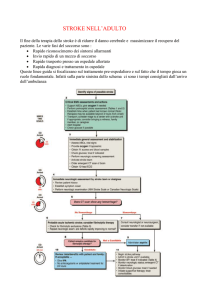
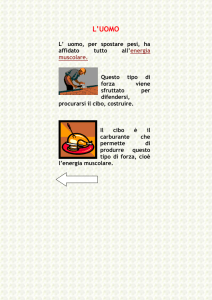
EUR MED PHYS 2008;44(Suppl. 1 to No. 3)
Recupero della forza muscolare dopo precoce mobilizzazione
passiva nel paziente emiplegico
E. CARRARO1, S. MASIERO1, G. ROSATI2, C. FERRARO1
Introduzione
1Scuola
La perdita di destrezza nell’uso dell’arto superiore rappresenta
uno dei principali fattori di disabilità persistente post-ictus1. Si è stimato che circa il 20% dei pazienti non recuperano completamente
l’uso funzionale dell’arto superiore e che il recupero è parziale
nell’85% dei casi2. Una grave invalidità e una marcata limitazione
nelle attività della vita quotidiana persiste in circa il 35% di tutti i
pazienti post-stroke. L’outcome motorio conseguente ad un trattamento convenzionale è povero, con una percentuale di pazienti
compresa tra il 30 e il 60% che, nonostante la terapia convenzionale,
non riacquistano un uso funzionale del loro arto paretico3,4. Infatti,
dei soggetti sopravvissuti allo stroke, dal 30% al 66% continuano ad
avere disabilità motoria all’arto superiore per più di 6 mesi5,6.
Secondo le linee guida SPREAD, nelle fasi precoci dell’ictus è indicato effettuare una intensa mobilizzazione passiva quotidiana degli arti
paretici o plegici in tutto il range di movimento delle articolazioni6.
Inoltre, da alcuni studi risulta che il precoce intervento di mobilizzazione dell’arto superiore paretico/plegico nel paziente post-ictus rappresenta il fattore maggiormente correlato con il ritorno al proprio domicilio entro sei settimane dall’evento ictale. Nella clinica, l’esercizio di
mobilizzazione passiva (ROM) è una componente standard di trattamento ed è considerato efficace a prevenire contratture.
Recenti studi clinici hanno dimostrato che la mobilizzazione passiva altera lo stato inibitorio del sistema nervoso centrale e conseguentemente le risposte comportamentali dei soggetti8,9.
Immediatamente dopo uno stroke, la riduzione della forza muscolare è dovuta alla perdita di input discendenti dal pool di motoneuroni spinali per la diminuita attivazione delle unità motorie, mentre sei
mesi dopo uno stroke, la riduzione della forza è dovuta anche ad una
diminuzione di un’area settoriale trasversa10 e al disuso11. Inoltre, l’effetto dell’allenamento alla forza può dipendere dal livello iniziale di
deficit della forza. In una review, Ada et al.12 raccomandano di inserire interventi diretti a stimolare il rinforzo muscolare come parte della
riabilitazione stessa dello stroke, soprattutto nei primi sei mesi.
È stato evidenziato come la debolezza muscolare (intesa come
perdita di abilità a generare una forza di intensità normale) sia il
maggiore contribuente alla limitazione dell’attività motoria13-17. Studi
che confrontano il grado di danno neurologico con l’attività, riportano un alto grado di correlazione maggiore tra la forza e l’attività,
rispetto ad altri tipi di danno18-21. Conseguentemente, si è cercato di
implementare l’allenamento alla forza come parte integrante della
riabilitazione post-stroke; Gli interventi potrebbero includere la stimolazione elettrica, il biofeedback, la ri-educazione muscolare in
aggiunta agli esercizi di resistenza progressiva.
Vol. 44 - Suppl. 1 to No. 3
di Specializzazione in Medicina Fisica e Riabilitazione,
Università degli Studi di Padova, Padova;
2Dipartimento di Innovazione Meccanica e Gestionale,
Università degli Studi di Padova, Padova
In questo lavoro, presentiamo la nostra esperienza con NEuroREhabilitation-roBOT (NeReBot), un apparecchio robotico progettato
e costruito presso il Dipartimento di Innovazione Meccanica e
Gestionale dell’Università di Padova per il trattamento dell’arto superiore post-stroke22. Diversamente dagli altri robot descritti in letteratura, NeReBot è un’interfaccia aptica a cavi che può essere utilizzata
al letto del paziente con l’obiettivo di poter trattare soggetti poststroke in fase acuta. Dal punto di vista meccanico l’apparecchio è
costituito da una struttura mobile in acciaio, comprendente un basamento a struttura aperta a forma di C, una colonna regolabile in
altezza e bracci orizzontali regolabili in angolazione. Sulla struttura
sono collocati inoltre tre motori in corrente continua e a tensione di
50V, un PC, una minitastiera e un monitor LCD, due scatole all’interno delle quali sono inseriti dispositivi elettronici di controllo. Si utilizzano per la mobilizzazione dell’arto tre cavi in nylon che convertono il moto rotatorio dei tre motori in corrente continua in una
traiettoria spaziale per l’arto del paziente. L’avambraccio del paziente
è posto su un’ortesi in materiale termoplastico, la quale è agganciata
ai tre cavi con un sistema di sgancio magnetico che interviene nel
caso in cui la trazione superi un valore di sicurezza per il paziente.
Mediante l’utilizzo di un software, appositamente sviluppato, l’apparecchio è in grado di acquisire le posizioni spaziali dell’arto superiore che il medico sceglie come punti della traiettoria da compiere
durante la terapia. In seguito l’apparecchio ripete ciclicamente la
traiettoria spaziale derivante da interpolazione dei punti acquisiti
con possibilità di selezionare diverse velocità. NeReBot è stato programmato per effettuare movimenti (flesso-estensione, ab-adduzione, prono-supinazione) dell’arto superiore (spalla e gomito), simulando un trattamento hand-over-hand.
Lo scopo del nostro studio pilota è stato quello di verificare se
una precoce terapia con NeReBot riduce la debolezza e favorisce il
recupero della forza muscolare di pazienti post-stroke con arto
superiore plegico/paretico.
Materiali e metodi
Sono stati reclutati 20 soggetti (età media: 69,5 anni; SD 12,5),
con emiplegia/paresi da lesione vascolare cerebrale (ischemica o
emorragica) recente (entro una settimana dall’ictus).
EUROPA MEDICOPHYSICA
1
CARRARO
RECUPERO DELLA FORZA MUSCOLARE DOPO PRECOCE MOBILIZZAZIONE PASSIVA NEL PAZIENTE EMIPLEGICO
Tabella I. – Sono rappresentati i guadagni in forza (media e SD) dei muscoli considerati durante il follow-up di 240 giorni nel gruppo sperimentale e nel gruppo di controllo (MRC= Medical Research Council).
Effetti del trattamento
MRC deltoide
MRC bicipite
MRC tricipite
MRC pronatori
MRC supinatori
Dopo 15 gg
GS
GC
p
0,80±1,13
0,40±0,51
0,413
0,30±0,82
0,40±0,69
0,755
0,30±0,82
0,50±0,85
0,656
0,60±0,96
0,90±1,22
0,585
0,60±0,96
0,90±1,32
0,764
0,20±0,78
0,50±0,70
0,284
0,10±0,87
0,40±0,84
0,359
Dopo 30 gg
GS
GC
p
1,80±1,31
0,80±0,78
0,072
1,50±1,30
0,70±0,90
0,101
1,50±1,23
0,90±1,12
0,205
0,88±0,88
1,98±1,92
0,783
1,33±1,00
1,56±1,99
0,784
1,51±1,51
0,98±0,98
0,697
1,41±1,47
0,62±0,87
0,634
Dopo 90 gg
GS
GC
p
2,40±1,17
1,30±0,94
0,032
2,30±1,56
1,20±1,22
0,050
2,10±1,52
1,30±1,16
0,227
1,06±1,06
1,55±1,59
0,260
1,65±1,28
1,73±1,59
0,613
1,90±1,37
1,30±0,89
0,293
1,58±1,58
0,93±0,83
0,348
Dopo 240 gg
GS
GC
p
3,25±1,16
1,50±0,92
0,007
2,38±1,72
1,50±1,41
0,055
2,38±1,75
1,63±1,76
0,255
2,71±1,38
1,78±1,48
0,161
2,50±1,41
1,63±1,50
0,303
1,88±1,15
1,13±0,99
0,829
1,75±1,66
1,25±1,03
0,421
I criteri di esclusione allo studio erano: a) instabilità cardiovascolare (grave ipertensione arteriosa non controllabile farmacologicamente, grave coronaropatia, etc.); b) presenza di gravi deficit cognitivi (eminattenzione spaziale, afasia globale); c) comparsa di marcata
e precoce spasticità (≥ 3 sec. la scala di Ashworth); d) età superiore
a 85 anni.
I pazienti sono stati randomizzati in 2 gruppi: 10 soggetti erano
assegnati al gruppo sperimentale (GS) che riceveva terapia tradizionale e robot-terapia, i rimanenti al gruppo di controllo (GC) che era
trattato solo con terapia tradizionale. Tutti i soggetti reclutati ricevevano la stessa dose di trattamento riabilitativo standard (in termini di
minuti/die) basato sul concetto Bobath. Il GS è stato sottoposto in
aggiunta ad un programma di trattamento supplementare all’arto
superiore con NeReBot, iniziando entro la prima settimana dallo
stroke e comprendeva un tempo di trattamento di 40 minuti al giorno (suddiviso in due fasi di 20 minuti) per una durata di 4 settimane. All’inizio di ogni sessione, il terapista cercava di identificare la
traiettoria ottimale e le posizioni di riposo per ciascun paziente da
far eseguire al robot, personalizzando secondo il recupero individuale per sfruttare pienamente le abilità motorie residue del paziente e provvedere alla stimolazione multisensoriale. Il robot assisteva e
guidava l’avambraccio e la mano del paziente e ripeteva l’esercizio
secondo le impostazioni date dal team di riabilitazione, secondo il
grado di disabilità del paziente: tutte le sessioni di trattamento consistevano di una sequenza di compiti motori seguiti da una breve fase
di riposo. All’inizio di ogni sessione di terapia, veniva esaminato il
braccio plegico per individuare il recupero della funzione motoria, il
dolore o altre complicanze. Nella prima settimana il paziente era di
solito in posizione supina (sul letto) e gli esercizi quotidiani includevano ripetizioni passive lungo traiettorie semplici (es. elevazione del
braccio); appena possibile il paziente veniva posto seduto su una
sedia o su una sedia a rotelle, legato bene con una cintura di sicurezza per limitare movimenti di torsione del tronco e prevenire possibili cadute. L’insieme degli esercizi da effettuare con l’arto plegico,
si faceva progressivamente più complesso a questo stadio (ad es,
includeva movimenti circolari).
All’entrata nello studio dei pazienti, venivano registrate le caratteristiche dei soggetti (età, sesso, lato della paresi, tipo ed insorgenza
2
MRC flessori dita MRC estensori dita
dello stroke, patologie concomitanti). I risultati erano valutati a
distanza di 1, 3 e 8 mesi dall’ictus con la Medical Research Council
(MRC)23 che valuta il recupero della forza muscolare e con Modified
Ashworth Scale (MAS)24 per evidenziare eventuali variazioni del
tono muscolare.
Le caratteristiche dei pazienti nel gruppo di controllo e in quello
sperimentale sono stati comparati usando il test del Chi-quadro (per
dati nominali) o il test della T di Student per variabili indipendenti
(dati continui). Abbiamo utilizzato il test U di Man-Whitney per evidenziare una differenza significativa tra i guadagni medi nei punteggi della forza muscolare (MRC) nei due gruppi. La significatività statistica è stata posta a p≤0,05. per l’analisi statistica è stato usato il
programma SPSS version 11,5 (SPSS, Inc., Chicago, IL).
Risultati
Il GS ed il GC erano comparabili per età, sesso, fattori di rischio
(ipertensione, diabete, familiarità, cardiopatie, depressione, obesità,
dislipidemie), tipo di stroke (tutti ischemici) e valutazioni cliniche
pre-trattamento. I risultati ottenuti dalla valutazione clinica dopo 1, 3
e 8 mesi dall’inizio del trattamento con NeReBot sono rappresentati
nella tabella I. Nessuna variazione significativa tra i due gruppi era
riscontrata a carico del tono muscolare alla MAS in tutto il follow-up
considerato.
Durante la terapia con NeReBot, non si sono verificate complicanze o effetti indesiderati nei pazienti.
Conclusioni
Dalla valutazione effettuata con la MRC, il GS mostra un significativo incremento della forza del muscolo deltoide a 3 e 8 mesi e del
bicipite brachiale a 3 mesi ed incrementi sebbene non statisticamente significativi, in altri muscoli (tricipite brachiale, supinatori e flessori del polso) rispetto al GC. La scala di Ashworth, modificata da
Bohannon e Smith, non ha rilevato significative variazioni del tono
muscolare tra i due gruppi a dimostrazione che la mobilizzazione
passiva anche se effettuata in fase acuta non influenza l’insorgenza o
il peggioramento della spasticità di un paziente emiplegico.
I nostri risultati, seppur preliminari, sembrano confermare che
un’intensa e precoce mobilizzazione passiva nel soggetto con pare-
EUROPA MEDICOPHYSICA
October 2008
RECUPERO DELLA FORZA MUSCOLARE DOPO PRECOCE MOBILIZZAZIONE PASSIVA NEL PAZIENTE EMIPLEGICO
si/plegia post-ictus può produrre significativi benefici motori utilizzabili nel percorso riabilitativo. Rimane ancora da determinare quale
sia il regime ottimale di esercizio con robot efficace a migliorare la
funzione motoria dopo uno ictus.
In conclusione, riteniamo che sulla base dei nostri dati preliminari un’intensa e precoce mobilizzazione passiva debba essere considerata parte integrante dell’intervento riabilitativo nei pazienti con
emiparesi/emiplegia post-ictus.
Bibliografia
1. Burke D. Spasticity as an adaptation to pyramidal tract injury. Adv Neurol 1988;47:401-8.
2. Gowland C, de Bruin H, Basmajian J, Plews N, Nurcea I. Agonist and
antagonist activity during voluntary upper limb movement in patients
with stroke. Phys Ther 1992;72:624-63.
3. Gowland C. Recovery of motor function following stroke: Profile and
predictors. Physiother Can. 1982;34:77-84.
4. Kwakkel G, Kollen BJ, Wagenaar RC. Therapy impact on functional recovery in stroke rehabilitation: A critical review of the literature. Phys
1999;85377-91.
5. Richards L, Pohl P. Therapeutic interventions to improve upper extremity
recovery and function. Clin Geriatr Med 1999;15::819-32.
6. Stroke Prevention and Educational Awareness Diffusion (SPREAD). The
Italian guidelines for stroke prevention and treatment. Milano: Ed.
Hypephar Group, 2003.
7. Liebesman JL, Cafarelli E. Physiology of range of motion in human joints:
A critical review. Crit Rev Phys Rehabil Med. 1994;6:131-60.
8. Lewis GN, Byblow WD. Modulations in corticomotor excitability during
passive upper-limb movement: Is there a cortical influence? Brain Res.
2002;943:263-75.
9. Hogan N, Krebs HI, Rohrer B, Palazzolo JJ, Dipietro L, Fasoli SE, Stein J,
Hughes R, Frontera WR, Lynch D, Volpe BT. Motions or muscles? Some
behavioral factors underlying robotic assistance of motor recovery. J
Rehabil Res Dev 2006;43:605-18.
10. Ryan AS, Dobrovolny CL, Smith GV, Silver KH, Macko RF. Hemiparetic
muscle atrophy and increased intramuscular fat in stroke patients. Arch
Phys Med Rehabil 2002;83:1703-7.
11. Hara Y, Akaboshi K, Masakado Y, Chino N. Physiologic decrease of single thenar motor units in the F-response in stroke patients. Arch Phys
Med Rehabil 2000;81:418-23.
Vol. 44 - Suppl. 1 to No. 3
CARRARO
12. Ada L, Dorsch S, Canning CG. Strengthening interventions increase
strength and improve activity after stroke: a systematic review. Aust J
Physiother 2006;52:241-8.
13. Bohannon RW, Andrews AW. Correlation of knee extensor muscle torque
and spasticity with gait speed in patients with stroke. Arch Phys Med
Rehabil. 1990;71:330-3.
14. Boissy P, Bourbonnais D, Carlotti MM, Gravel D, Arsenault BA. Maximal
grip force in chronic stroke participants and its relationship to global
upper extremity activity. Clinic Rehabil 1999;13:354-62.
15. Chae J, Yang G, Park BK, Labatia I. Muscle weakness and cocontraction
in upper limb hemiparesis: relationship to motor impairment and physical disability. Neurorehabil Neural Repair 2002;16:241-8.
16. Kim CM, Eng JJ. The relationship of lower-extremity muscle torque to
locomotor performance in people with stroke. Phys Ther 2003;83:49-57.
17. Mercier C, Bourbonnais D. Relative shoulder flexor and handgrip
strength is related to upper limb function after stroke. Clin Rehabil 2004;
18:215-21
18. Bohannon RW, Warren ME, Cogman KA. Motor variables correlated with
the hand-to-mouth maneuver in stroke patients. Arch Phys Med Rehabil
1991;7:682-4.
19. Canning C, Ada L, Adams R, O’Dwyer NJ. Loss of strength contributes
more to physical disability after stroke than loss of dexterity. Clin Rehabil
2004;18:300-8.
20. Lin S. Motor function and joint position sense in relation to gait performance in chronic stroke patients. Arch Phys Med Rehabil 2005;86:197203
21. Nadeau S, Arsenault AB, Gravel D, Bourbonnais D. Analysis of the clinical factors determining natural and maximal gait speeds in adults with a
stroke. Am J Phys Med Rehabil 1999;78:123-30.
22. Fanin C, Gallina P, Rossi A, Zanatta U, Masiero S. Nerebot: a wire-based
robot for neurorehabilitation. Proceedings of the 8th International Conference on Rehabilitation Robotics, Seoul, Korea,2003; pp. 23-7.
23. Medical Research Council. Aids to the examination of the peripheral nervous system. London: Her Majesty’s Stationery Office; 1976. Memorandum no. 45.
24. Bohannon RW, Smith MB. Interrater reliability of a modified Ashworth
scale of muscle spasticity. Phys Ther 1987;67:206-7.
25. Fasoli SE, Krebs HI, Stein J, Frontera WR, Hogan N. Effects of robotic
therapy on motor impairment and recovery in chronic stroke. Arch Phys
Med Rehabil. 2003;84:477-82.
EUROPA MEDICOPHYSICA
3