
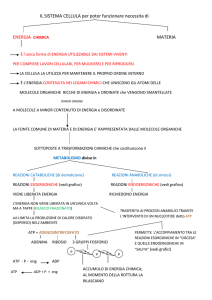
Il metabolismo è la somma di tutte le trasformazioni
chimiche che avvengono in un organismo o in una cellula
Il catabolismo è l’insieme delle reazioni che portano alla scissione di
molecole complesse (ricche di energia) in sostanze più semplici (povere di
energia). Rilascia energia
Nutrienti contenenti
energia
Carboidrati
Grassi
Proteine
Molecole complesse
Carboidrati
Grassi
Proteine
Attività cellulari
Prodotti di scarto
poveri di energia
CO2
H2O
NH3
catabolismo
E
anabolismo
Molecole semplici
L’anabolismo è l’insieme delle reazioni che portano alla formazione di
molecole complesse a partire da molecole più semplici. Richiede energia
Adenosin-trifosfato ATP
legame anidridico:legame tra due acidi
cariche negative che si respingono
legami
anidridici ad
alto contenuto
energetico
ATP
ADP + Pi
ADP + Pi
ATP
∆G –7.3 kcal/mol
∆G +7.3 kcal/mol
respirazione
cellulare
C6H12O6
glucosio
+
6 CO2
6O2
fotosintesi
+
6 H2O
luce
∆G = -686 Kcal/mol
Reazioni cataboliche
∆G < 0
ATP
Reazioni anaboliche
∆G > 0
Composto ad alto
contenuto energetico
L’ATP immagazzina temporaneamente l’E libera e la rende
disponibile per le reazioni successive
Le reazioni di ossidazione dei composti organici consistono in
reazioni di deidrogenazione cioè nella sottrazione di due atomi
di idrogeno
L’ossidazione di un alcool
primario forma un’aldeide
L’ossidazione di un’aldeide
(idrata) forma un acido
carbossilico
L’ossidazione di un alcool
secondario forma un chetone
L’ossidazione di un alcool
terziario non avviene
Ciò che cambia è il rapporto H/O
prodotti di
rifiuto ossidati
substrati
ridotti
6
6
Acido oleico
-
fosforilazione a
livello dei substrati
ATP
e
e-
NH3 e -
NADH e FADH2
trasportatori di elettroni
sotto forma di atomi di idrogeno
CO2
I trasportatori di idrogeno: NAD+
Nicotin Adenin Dinucleotide
H+ ione idrogeno
non ha più l’elettrone
H atomo di idrogeno
ha il suo elettrone
prodotti di
rifiuto ossidati
substrati
ridotti
6
CO2
6
Acido oleico
e-
-
fosforilazione a
livello dei substrati
ATP
e
NH3 e -
NADH e FADH2
trasportatori di elettroni
sotto forma di atomi di idrogeno
e½
O2 + 2e- +2H+
mitocondri
Catena
respiratoria
NAD+ e FAD
ossidati
ADP+P
H2O
ATP
accettore finale
di elettroni
C6H12O6
+
glucosio
6 CO2
6O2
+
6 H2O
∆G = -686 Kcal/mol
catena
respiratoria
glicolisi
piruvato
deidrogenasi
ciclo di Krebs
32 molecole di ATP = 237 Kcal/mol
40%
Il frazionamente in più passaggi metabolici permette il
recupero di una notevole quantità di energia
Schema generale del
metabolismo cellulare
proteine
polisaccaridi
trigliceridi
aminoacidi
monosaccaridi
acidi grassi
e glicerolo
STADIO 2:
Ossidazione delle unità semplici
ad acetilCoA accompagnata dalla
produzione di limitate quantità
di NADH e
di ATP nel citoplasma
glucosio
citoplasma
glicolisi
STADIO 1:
Scissione di
macromolecole a unità
semplici
ATP
NADH
piruvato
acetilCoA
Ciclo
di
Krebs
membrana
mitocondriale
STADIO 3:
Completa ossidazione
dell’acetilCoA ad CO2 e H2O
accompagnata dalla produzione
di grandi quantità di NADH,
FADH2 e di ATP nei mitocondri
Potere riducente
NADH, FADH2
ATP
O2
NH3
Fosforilazione
ossidativa
membrana
plasmatica
βossidazione
ATP
ATP
H2 O
Prodotti di rifiuto
CO2
Acetil CoA
Legame tioestere
Unità
acetile
legame ad
alta energia
di idrolisi
carboidrati
lipidi
proteine
acetilCoA
acidi grassi
ossidazione
corpi chetonici
aminoacidi
Come è fatta una via metabolica?
A
E1
B
E2
C
E3
D
Le reazioni sono catalizzate, cioè accelerate, da speciali
proteine dette enzimi
Accelerazione di velocità da parte di enzimi
Enzima
Velocità
non enzimatica
Velocità
enzimatica
Chimotripsina
4x10-9
4x10-2
107
Lisozima
3x10-2
5x10-1
2x108
Fumarasi
2x10-8
2x10-3
3x1011
b-Amilasi
3x10-9
1x10-3
3x1011
3x10-10
3x10-4
1014
10-15
10-2
1017
Ureasi
Fosfatasi alcalina
Accelerazione
di velocità
Gli enzimi sono catalizzatori di natura proteica
accelerano solo reazioni spontanee non apportano
energia alla reazione
non alterano l’equilibrio della reazione
prendono parte alla reazione ma si ritrovano
fine immodificati
alla
sono efficaci a concentrazioni minime rispetto alle
concentrazioni dei substrati
sono molto specifici, in quanto catalizzano solo
alcuni tipi di reazioni chimiche
Gli enzimi accelerano solo le reazioni termodinamicamente
possibili
reazione esoergonica ∆G negativo
G
G
A+B
C+D
Ma come fanno ad avvenire le reazioni termodinamicamente
impossibili?
reazione endoergonica ∆G positivo
G
C+D
A+B
Accoppiando le reazioni endoergoniche
a reazioni esoergoniche
reazione 1
reazione 2
somma
A+b
e+d
C+d
f+b
∆G1>0
∆G2<0
A+e
C+f
∆G1+∆
∆G2
Una reazione esoergonica, come la scissione dell’ATP,
fornisce l’energia necessaria a una reazione endoergonica
Gli enzimi accelerano le reazioni chimiche abbassando l’energia di
attivazione (fanno diminuire l’energia libera del complesso
attivato)
Effetto della concentrazione del substrato
velocità della reazione
reazione catalizzata
reazione non catalizzata
concentrazione del substrato [S]
Struttura degli enzimi
enzima
substrato
sito attivo
complesso enzima/substrato
In genere il sito attivo rappresenta meno
del 5% della superficie di un enzima
Meccanismo di azione degli enzimi
prodotti
substrato
sito attivo
complesso
enzima/substrato
enzima
E + S
[ES]
complesso
enzima/prodotti
enzima
[E P]
E + P
L’attività enzimatica si studia determinando la velocità (V)
con cui decorre la reazione in presenza di enzima (E)
d[P]
V=
d[S]
V=-
dt
dt
Effetto della concentrazione del substrato
velocità della reazione
reazione catalizzata
reazione non catalizzata
concentrazione del substrato [S]
Effetto della concentrazione del substrato
Struttura degli enzimi
apoenzimasito attivo
substrato
+
coenzima
oloenzima
I coenzimi sono molecole
organiche a basso peso
molecolare derivate da
vitamine
Caratteristiche degli enzimi
• La loro attività è influenzata dalle condizioni
ambientali
• Funzionano al meglio a valori particolari di
temperatura, pH e concentrazione salina
Effetto della temperatura
37°C = optimum di temperatura
Come viene regolata una via metabolica?
A
E1
B
E2
C
E3
D
Le vie metaboliche vengono regolate controllando l’attività
dell’enzima che catalizza una delle prime reazioni della via
Meccanismi di regolazione dell’attività enzimatica
Regolazione della sintesi
Le cellule regolano la produzione degli enzimi a seconda delle
necessità e le reazioni avvengono solo se sono presenti gli
enzimi che le catalizzano
Inibitori
I
S
Inibizione competitiva
l’inibitore ha una
struttura simile al
substrato e compete
con il substrato per il
legame sul sito attivo
I
E
I
Inibizione non
competitiva
l’inibitore si lega a un
sito diverso dal sito
attivo inducendo un
cambiamento
conformazionale
dell’enzima
Meccanismi di regolazione dell’attività enzimatica
Regolazione della sintesi
Le cellule regolano la produzione degli enzimi a seconda delle
necessità e le reazioni avvengono solo se sono presenti gli
enzimi che le catalizzano
Inibitori
Modificazione covalente irreversibile
Gli enzimi sono sintetizzati in forma inattiva e vengono attivati
mediante scissione di uno più legami peptidici
Modificazione covalente irrreversibile
Attivazione della chimotripsina
Meccanismi di regolazione dell’attività enzimatica
Regolazione della sintesi
Le cellule regolano la produzione degli enzimi a seconda delle
necessità e le reazioni avvengono solo se sono presenti gli
enzimi che le catalizzano
Inibitori
Modificazione covalente irreversibile
Gli enzimi possono essere prodotti in forma inattiva ed essere
attivati mediante scissione
Modificazione covalente reversibile
Gli enzimi possono essere modulati attraverso processi di
fosforilazione/defosforilazione
Modificazione covalente reversibile
ATP
ADP
proteina chinasi
E
E
CH2OH
CH2O fosfatasi
Pi
H2O
Pi = H3 PO4
acido fosforico
Pi
Comunicazione endocrina
L’ormone viene secreto
da una ghiandola
endocrina
L’ormone viaggia nel
circolo sanguigno e
raggiunge la cellula
bersaglio dove
esplicherà la sua azione
L’ormone riconosce la cellula bersaglio, poiché essa possiede un recettore
specifico per l’ormone stesso
Un recettore è una proteina che lega l’ormone con altissima affinità
Esistono due classi di ormoni a seconda della
loro natura chimica e del meccanismo d’azione
Ormoni idrofilici:
idrofilici
ormoni proteici (TSH, GH, ACTH, insulina, ecc.)
peptidici (ADH o vasopressina, ossitocina)
ormoni fenolici (adrenalina, nor-adrenalina)
Recettori di membrana
Non possono attraversare la membrana cellulare
Ormoni idrofobici:
idrofobici
Recettori intracellulari
ormoni steroidei (corticosteroidi, progestinici,
ormoni sessuali maschili e femminili)
ormoni tiroidei (T3 e T4)
acido retinoico
Possono attraversare la membrana cellulare
Meccanismo d’azione degli ormoni idrosolubili
Hanno un’azione molto rapida e per breve tempo
Meccanismo d’azione degli ormoni liposolubili
Hanno un’azione più lenta e prolungata nel tempo










![(Microsoft PowerPoint - Bioenergetica [modalit\340 compatibilit\340])](http://s1.studylibit.com/store/data/001091089_1-c31cee3923ca787caf520f2384eef8ca-300x300.png)
