UTILIZZO DELLA SPETTROMETRIA DI MASSA PER LA GENOTIPIZZAZIONE
DEGLI ADENOCARCINOMI POLMONARI
Nicole Carlessi1, Eleonora Bonaparte1, Rossella Falcone1, Silvia Tabano1, Silvia Sirchia2,
Leda Paganini1, Chiara Pesenti1, Sara Giangiobbe1, Michele Ciboddo1, Silvano Bosari1, Monica Miozzo1
1
Dipartimento di Fisiopatologia Medico-Chirurgica e dei Trapianti. UO di Patologia Molecolare, Fondazione IRCCS Ca’ Granda Ospedale Maggiore Policlinico, Milano
2
Dipartimento di Scienze della Salute, Università degli Studi di Milano, Milano
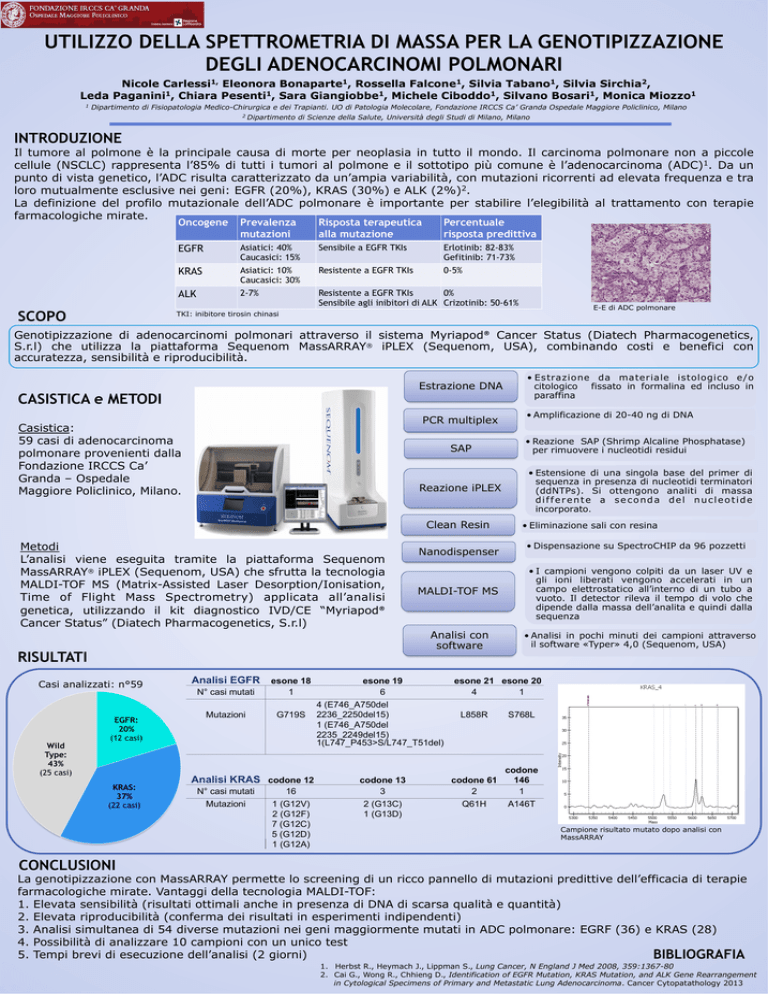
INTRODUZIONE
Il tumore al polmone è la principale causa di morte per neoplasia in tutto il mondo. Il carcinoma polmonare non a piccole
cellule (NSCLC) rappresenta l’85% di tutti i tumori al polmone e il sottotipo più comune è l’adenocarcinoma (ADC)1. Da un
punto di vista genetico, l’ADC risulta caratterizzato da un’ampia variabilità, con mutazioni ricorrenti ad elevata frequenza e tra
loro mutualmente esclusive nei geni: EGFR (20%), KRAS (30%) e ALK (2%)2.
La definizione del profilo mutazionale dell’ADC polmonare è importante per stabilire l’elegibilità al trattamento con terapie
farmacologiche mirate.
SCOPO
Oncogene
Prevalenza
mutazioni
Risposta terapeutica
alla mutazione
Percentuale
risposta predittiva
EGFR
Asiatici: 40%
Caucasici: 15%
Sensibile a EGFR TKIs
Erlotinib: 82-83%
Gefitinib: 71-73%
KRAS
Asiatici: 10%
Caucasici: 30%
Resistente a EGFR TKIs
0-5%
ALK
2-7%
Resistente a EGFR TKIs
0%
Sensibile agli inibitori di ALK Crizotinib: 50-61%
E-E di ADC polmonare
TKI: inibitore tirosin chinasi
Genotipizzazione di adenocarcinomi polmonari attraverso il sistema Myriapod® Cancer Status (Diatech Pharmacogenetics,
S.r.l) che utilizza la piattaforma Sequenom MassARRAY® iPLEX (Sequenom, USA), combinando costi e benefici con
accuratezza, sensibilità e riproducibilità.
Estrazione DNA
CASISTICA e METODI
PCR multiplex
Casistica:
59 casi di adenocarcinoma
polmonare provenienti dalla
Fondazione IRCCS Ca’
Granda – Ospedale
Maggiore Policlinico, Milano.
SAP
Reazione iPLEX
Clean Resin
Metodi
L’analisi viene eseguita tramite la piattaforma Sequenom
MassARRAY® iPLEX (Sequenom, USA) che sfrutta la tecnologia
MALDI-TOF MS (Matrix-Assisted Laser Desorption/Ionisation,
Time of Flight Mass Spectrometry) applicata all’analisi
genetica, utilizzando il kit diagnostico IVD/CE “Myriapod®
Cancer Status” (Diatech Pharmacogenetics, S.r.l)
RISULTATI
Casi analizzati: n°59
Analisi EGFR
N° casi mutati
Mutazioni
esone 18
1
G719S
Analisi KRAS codone 12
N° casi mutati
16
Mutazioni
1 (G12V)
2 (G12F)
7 (G12C)
5 (G12D)
1 (G12A)
Nanodispenser
• Reazione SAP (Shrimp Alcaline Phosphatase)
per rimuovere i nucleotidi residui
• Estensione di una singola base del primer di
sequenza in presenza di nucleotidi terminatori
(ddNTPs). Si ottengono analiti di massa
differente a seconda del nucleotide
incorporato.
• Eliminazione sali con resina
• Dispensazione su SpectroCHIP da 96 pozzetti
MALDI-TOF MS
Analisi con
software
• Analisi in pochi minuti dei campioni attraverso
il software «Typer» 4,0 (Sequenom, USA)
4 (E746_A750del
2236_2250del15)
1 (E746_A750del
2235_2249del15)
1(L747_P453>S/L747_T51del)
2 (G13C)
1 (G13D)
• Amplificazione di 20-40 ng di DNA
• I campioni vengono colpiti da un laser UV e
gli ioni liberati vengono accelerati in un
campo elettrostatico all’interno di un tubo a
vuoto. Il detector rileva il tempo di volo che
dipende dalla massa dell’analita e quindi dalla
sequenza
esone 19
6
codone 13
3
• Estrazione da materiale istologico e/o
citologico fissato in formalina ed incluso in
paraffina
esone 21 esone 20
4
1
L858R
S768L
codone
146
codone 61
2
1
Q61H
A146T
Campione risultato mutato dopo analisi con
MassARRAY
CONCLUSIONI
La genotipizzazione con MassARRAY permette lo screening di un ricco pannello di mutazioni predittive dell’efficacia di terapie
farmacologiche mirate. Vantaggi della tecnologia MALDI-TOF:
1. Elevata sensibilità (risultati ottimali anche in presenza di DNA di scarsa qualità e quantità)
2. Elevata riproducibilità (conferma dei risultati in esperimenti indipendenti)
3. Analisi simultanea di 54 diverse mutazioni nei geni maggiormente mutati in ADC polmonare: EGRF (36) e KRAS (28)
4. Possibilità di analizzare 10 campioni con un unico test
5. Tempi brevi di esecuzione dell’analisi (2 giorni)
BIBLIOGRAFIA
1. Herbst R., Heymach J., Lippman S., Lung Cancer, N England J Med 2008, 359:1367-80
2. Cai G., Wong R., Chhieng D., Identification of EGFR Mutation, KRAS Mutation, and ALK Gene Rearrangement
in Cytological Specimens of Primary and Metastatic Lung Adenocarcinoma. Cancer Cytopatathology 2013