Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
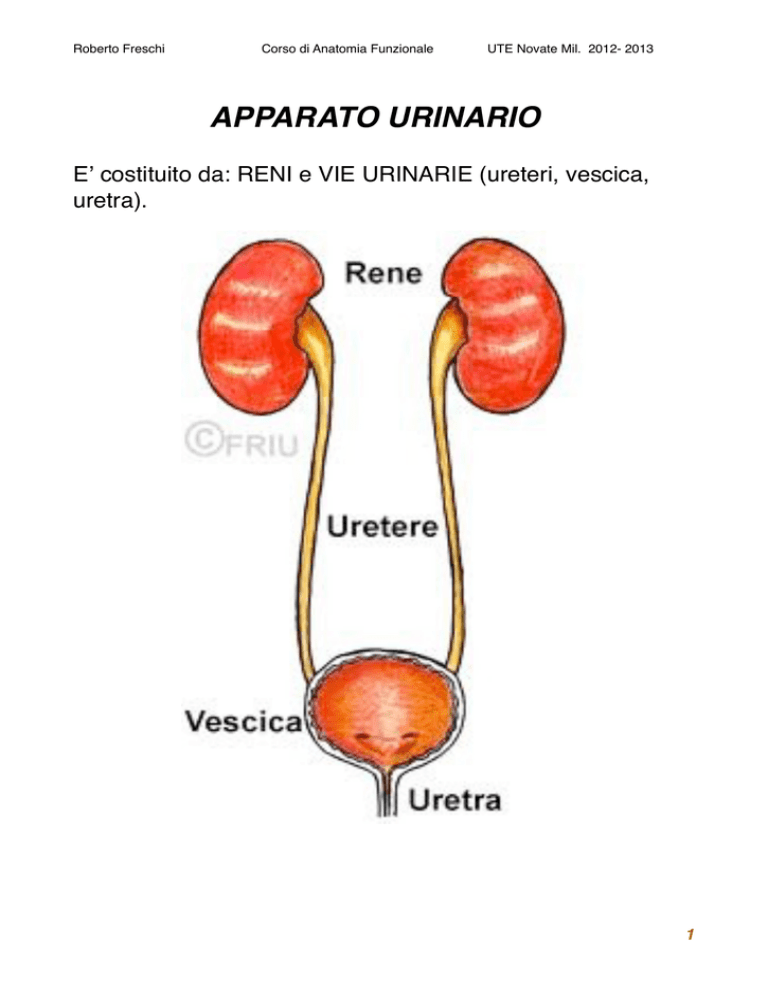
APPARATO URINARIO
Eʼ costituito da: RENI e VIE URINARIE (ureteri, vescica,
uretra).
1
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
RENI
Dove si trovano?
I due reni sono situati a lato della colonna vertebrale, allʼaltezza delle ultime
vertebre toraciche e delle prime dorsali.
Il rene destro è più basso del sinistro di circa 2 cm., per il rapporto con il
fegato che - sviluppandosi - lo spinge più in basso.
Alloggiano nelle logge renali e sono retroperitoneali (si trovano, cioè dietro al
peritoneo che tappezza la parete posteriore della cavità addominale).
2
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
Come sono fatti?
Hanno forma a fagiolo appiattito, colore rosso-bruno e consistenza
abbastanza dura.
Nellʼadulto, pesano in media 150- 160 g.
La lunghezza media è di 12 cm., la larghezza 6.5 cm., lo spessore 3 cm.
La superficie è generalmente liscia e regolare, ma può presentare solchi, che
delimitano territori corrispondenti ai singoli lobi (rene lobato).
Nei reni si distinguono: una faccia anteriore (guarda in avanti ed un poco
lateralmente), una faccia posteriore (guarda indietro ed un poco allʼinterno),
un polo superiore (arrotondato), un polo inferiore (appuntito), un margine
laterale (convesso) ed un margine mediale (concavo).
3
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
Il margine mediale presenta, nel suo mezzo, una sorta di fessura verticale
lunga 3-4 cm., che da passaggio a vasi sanguigni e linfatici, ai nervi ed alla
pelvi (o bacinetto) renale: prende il nome di ilo renale.
Lʼimmagine, in sezione, mostra lʼilo renale (Hilum) ed il bacinetto (Pelvis). Si noti anche,
al di sopra del polo superiore, la presenza della ghiandola surrenale.
4
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
Il rene è uno degli organi più altamente differenziati del corpo umano. Alla
conclusione dello sviluppo embrionario, sono circa 30 i diversi tipi cellulari
che vanno a formare una moltitudine di capillari di filtrazione e di nefroni
segmentati con lʼinterstizio che li avvolge.
Questa complessità cellulare modula (=regola, controlla) una gran varietà di
processi fisiologici.
Le funzioni endocrine, la regolazione della pressione sanguigna, il trasporto di
acqua e sostanze in essa disciolte, lʼequilibrio acido-base, la eliminazione dei
metaboliti dei farmaci sono alcuni esempi del complesso meccanismo di funzione
renale.
Si rende a questo punto necessario approfondire la conoscenza della struttura
interna (e microscopica) del rene, presupposto fondamentale per comprenderne il
funzionamento.
In sezione, in ogni rene si distinguono 2 porzioni: corticale e midollare.
5
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
La corticale è la più periferica, situata sotto la capsula renale; forma gli archi
corticali e si insinua tra le porzioni midollari (piramidi) come colonne renali (vedi
figura precedente).
Contiene:
• corpuscoli renali.
• tubuli contorti
• raggi midollari (costituiti da anse di Henle e collettori), cioè tubuli a decorso radiale dalla
base delle piramidi verso la periferia.
La midollare è la porzione più interna, formata da 10- 12 piramidi con base allʼesterno ed
apice verso lʼilo. Lʼapice si apre in un calice minore.
Contiene:
• porzioni spesse delle anse di Henle.
• collettori.
La funzione escretoria si esplica attraverso il nefrone (che è lʼunità funzionale renale).
Ogni rene contiene circa 1 milione di nefroni.
Il rene è un insieme di nefroni che operano in parallelo.
6
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
Dedichiamoci ora alla comprensione di come è fatto e funziona il NEFRONE, che abbiamo
definito come lʼunità funzionale del rene e che abbiamo identificato nella figura
precedente.
IL NEFRONE
Ha il compito di formare lʼurina (funzione uropoietica).
Ogni nefrone è costituito da:
• Un corpuscolo renale (di Malpighi): è costituito da 2 elementi principali: la
capsula di Bowman (formazione sferica, con un polo vascolare ed un polo
urinifero) ed il glomerulo renale (lʼinsieme dei capillari che collegano, avvolti a
gomitolo, lʼarteriola afferente a quella efferente).
7
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
• Un tubulo renale, che può essere, a sua volta, diviso in tre porzioni e
funzioni diverse: il tubulo prossimale (o di 1° ordine), lʼansa di Henle, il
tubulo distale (o di 2° ordine).
I tubuli renali, lunghi 30-40 mm., iniziano a fondo cieco con unʼestremità dilatata
(disposta come un calice intorno ad un gomitolo di capillari sanguigni) e terminano,
dopo un decorso assai complicato, confluendo con altri tubuli, nel sistema dei dotti
escretori.
8
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
Ogni nefrone opera mediante processi di filtrazione, riassorbimento,
concentrazione e secrezione, che avvengono con caratteristiche specifiche
nelle varie sezioni del nefrone:
1. Glomerulo> ultrafiltrazione
2. Tubulo prossimale> riassorbimento (obbligatorio) acqua, sodio, cloro
ecc.
3. Ansa di Henle> concentrazione urine
4. Tubulo distale e dotto collettore> riassorbimento (facoltativo) acqua,
sodio, cloro ecc.
I nefroni si distinguono in:
• Nefroni corticali: rappresentano lʼ85% di tutti i nefroni. Sono caratterizzati da un
corpuscolo renale più piccolo -situato nella parte periferica della corticale- e da un
tubulo più breve.
• Nefroni iuxtamidollari (= vicini alla midollare): sono forniti di un corpuscolo renale
più voluminoso e localizzato vicino alla midollare e da un tubulo assai più lungo.
Rispetto ai precedenti, presentano unʼarteriola efferente che forma non solo una
rete capillare attorno ai tubuli, ma anche una serie di anse vascolari (vasa recta)
che discendono nella midollare, circondano i dotti collettori ed i tratti ascendenti
dellʼansa di Henle. Questi vasi sono molto importanti perchè, oltre a consentire il
ritorno alla corticale del sangue, forniscono ossigeno e nutrienti ai segmenti
tubulari, trasportano ai tubuli le sostanze che devono essere secrete, riportano
nella circolazione generale lʼacqua ed i soluti che devono essere riassorbiti e
partecipano al meccanismo di concentrazione/ diluizione delle urine.
9
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
La figura illustra schematicamente la struttura di un nefrone. Notare la c.d. ansa di
Henle: è la porzione del tubulo renale che, formando unʼansa, collega il tubulo contorto
prossimale al tubulo contorto distale; si approfonda nella massa renale, attraversando tutta
la midollare del rene fino alla sua estremità interna. In ogni ansa si distingue un ramo
discendente ed uno ascendente. Insieme ai vasa recta, svolge una parte attiva nella
funzione del rene, soprattutto nella concentrazione dellʼurina.
10
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
Riassumendo e schematizzando, abbiamo appreso che lʼunità funzionale
del rene è il nefrone, in cui avviene la filtrazione del sangue e la produzione
di urina.
Il nefrone è costituito da glomerulo, capsula di Bowman, tubulo renale
(distinto nei suoi diversi tratti).
Il glomerulo è costituito da una fitta rete di capillari, che originano e ricevono
sangue arterioso da una arteriola, lʼarteriola afferente.
Dopo essere passato attraverso i capillari, il sangue esce dal glomerulo
tramite unʼaltra arteriola, lʼarteriola efferente.
Il glomerulo è costituito, quindi, da un gomitolo di capillari intercalati tra due
arteriole che costituiscono una struttura (rete mirabile arteriosa) caratteristica
del glomerulo renale (negli altri tessuti il sistema capillare è sempre
interposto tra unʼarteriola ed una venula).
Il diametro dellʼarteriola afferente è maggiore di quella efferente, per cui nei
capillari che costituiscono il glomerulo il sangue viene ultrafiltrato (filtrato
sotto pressione) e dai capillari glomerulari fuoriescono acqua, sali minerali,
zuccheri, cataboliti e tutte le sostanze di piccole dimensioni; la parte
corpuscolata del sangue (globuli rossi, bianchi e piastrine), la maggior parte
delle proteine e le sostanze di grandi dimensioni rimangono nel sangue che
rimane nei capillari e giunge allʼarteriola efferente.
Tutto il liquido filtrato attraverso la parete dei capillari del glomerulo
costituisce lʼurina primitiva, che contiene i cataboliti (= sostanze di rifiuto) ma
anche sostanze utili (acqua, sali minerali, zuccheri) e viene raccolto dalla
capsula di Bowman e convogliato nel tubulo renale.
11
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
Il primo tratto del tubulo renale, il tubulo contorto prossimale, si trova, insieme
con il glomerulo, nella zona corticale del rene.
Dal tubulo prossimale il liquido passa nellʼansa di Henle, che si approfonda
nella zona midollare.
Dopo essere passato attraverso lʼansa di Henle, il liquido entra nel tubulo
contorto distale che -come il prossimale- è situato nella zona corticale.
A livello del tubulo renale avviene il riassorbimento, attivo e passivo, di molti
dei materiali presenti nellʼurina primitiva (acqua, zuccheri, sali minerali), che
ritornano quindi nel sangue che scorre nella fitta rete di capillari che circonda
il tubulo renale e si forma lʼurina definitiva, che viene inviata nei dotti
12
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
collettori, da qui nei calici renali e quindi, attraverso le pelvi e gli ureteri, nella
vescica.
Quotidianamente, i nostri reni producono circa 180 litri di urina primitiva, che
viene quindi in gran parte riassorbita (oltre il 90%) per portare ad una
produzione quotidiana media di urina di 1,5 litri.
Lʼurina è costituita per circa il 95% da acqua, per il 2.5% circa da urea e, per
il resto, da sali minerali, creatinina, acido urico ed altre sostanze di rifiuto.
LA FILTRAZIONE GLOMERULARE
La filtrazione glomerulare è determinata essenzialmente dal gradiente di
pressione idrostatica attraverso la parete del capillare glomerulare (= differenza
di pressione tra i due lati della membrana di parete del capillare).
Si oppone invece alla filtrazione la pressione oncotica allʼinterno del lume
capillare (determinata dalla concentrazione delle proteine plasmatiche non
filtrate).
Dal momento che la pressione oncotica aumenta con il progredire nel capillare
glomerulare, la forza di filtrazione si riduce a zero al passaggio nellʼarteriola efferente.
Molti fattori, in prevalenza emodinamici, intervengono -in condizioni
fisiologiche- alla regolazione della filtrazione glomerulare.
Esistono, ad esempio, meccanismi di autoregolazione capaci di regolare il
tono (muscolare) sia dellʼarteriola afferente che di quella efferente:
13
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
Il riflesso miogenico: è mediato dal sistema neurovegetativo e rappresenta la prima
linea difensiva dalle fluttuazioni del flusso sanguigno renale (se stirato dallʼaumento
pressorio sistemico, il muscolo liscio delle arteriole afferenti risponde contraendosi; in
questo modo aumenta la resistenza al flusso, riducendo la quantità di sangue che
attraversa lʼarteriola e con essa la pressione idrostatica esercitata sulle pareti dei capillari
glomerulari > si riduce la velocità di filtrazione. Viceversa, se diminuisce la pressione
arteriosa sistemica, il muscolo arteriolare si rilassa ed il vaso si dilata in maniera
massimale; aumenta così il flusso di sangue allʼinterno del glomerulo e con esso anche la
pressione idrostatica glomerulare e la velocità di filtrazione).
Il feedback tubulo-glomerulare: le variazioni di flusso del liquido che attraversa il
tratto finale dellʼansa di Henle ed il tratto iniziale del tubulo distale influenzano la velocità
di filtrazione glomerulare. Nellʼansa di Henle avvengono processi di riassorbimento di
acqua, cloro e sodio. La particolare struttura ripiegata del nefrone fa sì che la porzione
finale dellʼansa di Henle passi fra le arteriole afferenti ed efferenti. In questa regione, tra le
due strutture si stabilisce una relazione strutturale e funzionale tale da costituire un vero e
proprio ʻapparatoʼ, definito apparato iuxtaglomerulare. Nei punti in cui vengono in
contatto, sia le pareti arteriolari che quelle del tubulo hanno una struttura modificata che
permette loro di influenzarsi reciprocamente. In particolare, la struttura tubulare modificata
è costituita da una placca di cellule detta macula densa, mentre la parete adiacente
dellʼarteriola afferente contiene cellule muscolari lisce specializzate, dette cellule
iuxtaglomerulari, capaci di secernere renina, ormone proteolitico con effetti ipertensivi.
14
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
Quando le cellule della macula densa captano un aumento della quantità di cloro
(espressione di un aumento della velocità di filtrazione glomerulare) segnalano alle cellule
iuxtaglomerulari di ridurre la secrezione di renina e di contrarre lʼarteriola afferente.
In questo modo aumenta la resistenza al flusso offerta dallʼarteriola afferente e la
pressione idrostatica a valle -cioè nel glomerulo- diminuisce (assieme alla velocità di
filtrazione glomerulare).
Nella condizione opposta, cioè in caso di riduzione della quantità di cloro a livello della
macula densa, tali cellule segnalano alle cellule iuxtaglomerulari di aumentare la quantità
di renina, e allʼarteriola afferente di dilatarsi, riducendo le proprie resistenze; di
conseguenza, si ha un aumento della velocità di filtrazione.
Il controllo della resistenza delle arteriole afferenti ed efferenti è regolato
anche da fattori sistemici.
Dʼaltronde, una delle principali funzioni del rene è quella di regolare la
pressione arteriosa sistemica, per cui è importante che i glomeruli
recepiscano eventuali variazioni della pressione arteriosa sistemica ed
adeguino la VFG di conseguenza.
Tali variazioni vengono trasmesse al rene per via endocrina o nervosa.
Il controllo nervoso della velocità di filtrazione glomerulare (VGF) è affidato a neuroni
simpatici che innervano sia lʼarteriola afferente che quella efferente.
Di conseguenza, una forte attivazione del simpatico, conseguente -per esempio- ad una
forte emorragia o ad una severa disidratazione, determina una contrazione delle arteriole
afferenti ed efferenti, riducendo sia la VGF che il flusso di sangue ai reni. In questo modo,
si cerca di preservare al massimo il volume idrico.
Il controllo endocrino della VFG è affidato a diversi ormoni. Oltre allʼadrenalina
circolante, i cui effetti vasocostrittori sono stati appena descritti, la resistenza arteriolare
viene aumentata anche dallʼangiotensina II.
In questʼultimo caso, la vasocostrizione riguarda soprattutto le arteriole efferenti, per cui
lʼaumento pressorio nei capillari glomerulari aumenta la VFG.
Tra le sostanze vasodilatatorie che si oppongono allʼeffetto vasocostrittore del sistema
nervoso simpatico e dellʼangiotensina II, ricordiamo alcune prostaglandine (PGE2, PG12,
Bradichinina), che riducono la resistenza al flusso offerta soprattutto dalle arteriole
afferenti. Ne consegue un aumento della VFG.
\
15
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
Un rene normalmente funzionante ha come scopo principale, attraverso
numerosi processi cellulari, quello di mantenere lʼomeostasi corporea (cioè la
condizione dʼequilibrio interno degli organismi, che deve mantenersi anche al
variare delle condizioni esterne, attraverso meccanismi autoregolanti).
Eʼ intuitivo quanto possa avere importanza, a questo proposito, lʼequilibrio
idrosalino, in buona parte di competenza del rene.
EQUILIBRIO IDRO- SALINO
La quantità di acqua corporea è regolata a 2 livelli:
• Nel sistema nervoso centrale si trova il “centro della sete”, stimolato tutte le volte
che rischiamo disidratazione.
• Nel rene: la quantità di urina eliminata dal rene è infatti proporzionale alla
percentuale di acqua presente nel plasma e nellʼorganismo.
Nella capsula di Bowman scorrono 180 litri di filtrato al giorno, mentre nel tratto
finale del tubulo prossimale tale volume scende a 54 litri/die.
In questo primo tratto, vengono infatti riassorbite grandi quantità di acqua, così
come avviene nelle porzioni successive. Grazie allʼefficace processo di
riassorbimento, al termine del dotto collettore esce soltanto 1,5 litri di liquido al
giorno (sotto forma di urine).
Per capire come il rene interviene nella regolazione del bilancio idrico, occorre
considerare un ulteriore fattore, rappresentato dallʼosmolarità del liquido presente
nei tubuli.
Lʼosmolarità esprime la concentrazione dei soluti in una soluzione (nel nostro caso nel
liquido presente in sede tubulare), sottolineando il numero delle particelle in essa disciolte,
indipendentemente dalola carica elettrica e dalle dimensioni.
Lʼosmolarità dipende pertanto dalla somma dei soluti (sodio, cloro, calcio, glucosio,
aminoacidi ecc.) contenuti nella pre-urina.
Lʼosmolarità è espressa in osmoli per litro o, quando la soluzione è particolarmente diluita,
in milliosmoli per litro: il suo valore esprime la concentrazione della soluzione, ma non dice
alcunché sulla natura delle particelle in essa contenute.
Di riflesso, due soluzioni con uguale osmolarità avranno lo stesso contenuto numerico di
particelle, la stessa pressione osmotica e la stessa temperatura di congelamento ed
ebollizione (pH, conducibilità elettrica e densità potrebbero essere differenti, perchè
dipendono dalla natura chimica dei soluti e non dal loro numero).
16
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
I liquidi fisiologici, presenti dentro e fuori le cellule, hanno unʼosmolarità pari a 300
milliosmoli, che ritroviamo anche nel filtrato presente nella capsula di Bowman.
Alla fine del tubulo contorto prossimale, il volume di liquido si riduce, ma
lʼosmolarità rimane invariata poichè lʼacqua segue i soluti riassorbiti ed il loro
rapporto rimane inalterato.
Nel tubulo prossimale vengono riassorbiti il glucosio, le vitamine, gli
aminoacidi, molti sali e quel poʼ di proteine che sono riuscite a passare.
Lungo lʼansa di Henle, al contrario, non solo si riduce il volume del filtrato, ma
diminuisce sensibilmente anche lʼosmolarità (-66%); di conseguenza, i soluti
divengono meno concentrati, o più diluiti che dir si voglia.
La branca discendente dellʼansa di Henle è permeabile allʼacqua -che viene
riassorbita- ma non ai soluti; è questo il motivo per cui il volume diminuisce e la
concentrazione dei soluti aumenta.
Nella branca ascendente dellʼansa di Henle, la parete è impermeabile allʼacqua, la
cui uscita è quindi impedita, e possiede delle ʻpompeʼ per espellere i sali.
Questo sistema è particolarmente efficiente, tanto che alla fine dellʼansa ritroviamo
un liquido particolarmente diluito (18 l/die), pronto per entrare nel tubulo distale.
Dal tubulo distale in poi, la permeabilità della parete tubulare è regolata
attivamente, in base alle richieste fisiologiche, da un ormone, chiamato
antidiuretico o vasopressina, il cui nome ci fa già intuire la sua azione:
liberato dallʼipofisi posteriore, è in grado di ridurre la diuresi (eliminazione di
urina).
La vasopressina viene secreta ogni volta che lʼacqua scarseggia, per informare i
reni dello stato di disidratazione dellʼorganismo.
In risposta allʼormone, il rene interviene attivamente e, rendendo permeabili
allʼacqua le pareti degli ultimi tratti del nefrone, riduce i volumi escreti, aumentando
quelli riassorbiti.
In assenza di vasopressina (diabete insipido), il soggetto è costretto ad eliminare 18 litri di
urina al giorno e -di conseguenza- ad assumere almeno 20 litri di liquidi con la dieta.
17
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
Alla fine del dotto collettore, dovʼé presente lʼurina che sarà eliminata,
lʼosmolarità varia da 50 a 1200 milliosmoli. Lʼurina, quindi, può essere molto
diluita (quando si beve in eccesso) o molto concentrata (quando si é
disidratati).
Lʼaldosterone ha un effetto analogo sul riassorbimento dei sali minerali
(soprattutto del sodio).
18
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
Il sangue che giunge al glomerulo non viene completamente filtrato, ma circa
lʼ80% ritorna subito in circolo senza subire alcuna filtrazione.
Se così non fosse, lʼimportante quantitativo di sangue, con il suo carico di
cellule e di proteine non filtrabili, rischierebbe di intasare il “setaccio”,
compromettendo lʼintera funzionalità renale.
Per questo motivo, lʼorganismo preferisce filtrare piccole quantità di sangue
alla volta.
19
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
Prendiamo ora in considerazione, a titolo esemplificativo, il ʻpercorsoʼ del
glucosio a livello renale.
RIASSORBIMENTO DEL GLUCOSIO
Il glucosio, in virtù delle sue ridotte dimensioni, viene rapidamente filtrato a livello
glomerulare; per questo motivo, la sua concentrazione nel filtrato è identica a quella
del plasma.
Dopo essere stato filtrato, il glucosio viene prontamente riassorbito nel tubulo
prossimale, dove si trovano cellule epiteliali simili a quelle intestinali (dotate di
microvilli). Questa operazione è abbastanza complessa:
il glucosio viene captato da specifici trasportatori, capaci di legare
contemporaneamente una molecola di sodio ed una di glucosio e di trasportarli
insieme nel citoplasma delle cellule che costituiscono la membrana esterna del
tubulo renale; a questo livello, una pompa sodio-potassio provvede a riportare
allʼesterno il sodio, mentre un trasportatore (GLUT 4) compie la medesima
operazione con lo zucchero (riversandolo nellʼinterstizio tra tubuli e capillari).
In condizioni fisiologiche, questi trasportatori riescono a recuperare tutto il glucosio,
ma, dal momento che il loro numero è limitato, quando le concentrazioni dello
zucchero nel filtrato salgono eccessivamente, un poʼ di glucosio sfugge al
riassorbimento.
Quando tutti questi trasportatori sono legati ad una molecola di glucosio (saturati),
lʼoriginale e diretta proporzionalità tra glucosio filtrato e glucosio riassorbito viene
quindi perduta.
Questo fenomeno si manifesta in corrispondenza della cosiddetta soglia renale,
che equivale ad una glicemia di 300 mg/dl.
Una volta superato tale limite, la concentrazione di glucosio riassorbito non può più
aumentare, anche se la concentrazione nel filtrato continua a crescere.
Di conseguenza, inizierà ad aumentare la concentrazione dello zucchero nelle
urine.
Il limite di 300 mg di glucosio per decilitro di sangue é in realtà un valore teorico; in pratica,
la soglia renale è molto più bassa (180 mg/dl).
Ciò in relazione al fatto che non tutti i nefroni -lavorano singolarmente, sono lʼunità
funzionale del rene- sono ugualmente abili nel recuperare il glucosio, a causa della
variabilità del numero dei trasportatori.
20
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
Eʼ sufficiente che uno solo dei nefroni perda una molecola di glucosio che questa si ritrovi
nelle urine, dando origine ad una condizione nota come glicosuria.
La presenza di glucosio nelle urine é molto pericolosa, poichè questo zucchero richiama
notevoli quantità dʼacqua, disidratando lʼorganismo; inoltre, facilitando la proliferazione
batterica, aumenta lʼincidenza di infezioni delle vie urinarie.
21
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
INVECCHIAMENTO E RENE
• Il flusso di sangue al rene si riduce gradualmente da 1200 ml/min allʼetà di
30-40 anni a 600 ml/min allʼetà di 80 anni. Ciò in rapporto alla perdita di massa
renale (atrofia) ed a quella -selettiva- dei vasi della corticale.
• La velocità di filtrazione glomerulare (GFR), misurata con la clearance della
creatinina si riduce dopo i 30-40 anni, di circa 8 ml/min/1.73 mq/decennio, in
circa i 2/3 di persone anziane non nefropatiche o non in terapia
antipertensiva. Oltre allʼinvecchiamento, avrebbero importanza anche i rialzi
pressori.
• La massa renale si riduce gradualmente ed il peso del rene diminuisce da
250-270 g. a circa 30 anni, a 180-200 g. a circa 70 anni. La perdita di
massa é soprattutto corticale, mentre la midollare viene relativamente
risparmiata. Il numero di glomeruli si riduce più o meno parallelamente alla
riduzione del peso del rene. Aumenta la percentuale dei glomeruli sclerotici,
provocando la riduzione della superficie disponibile per la filtrazione.
• A livello dei tubuli renali, compaiono diverticoli nelle porzioni distali del
nefrone, che raggiungono il numero di circa 3 per tubulo attorno ai 90 anni.
Questi diverticoli possono trasformarsi in cisti da ritenzione, il cui riscontro
nellʼanziano è frequente (ed il significato clinico sconosciuto).
• Le pareti dei vasi renali di grosso calibro subiscono alterazioni sclerotiche,
mentre i vasi di calibro inferiore sembrano esserne risparmiati.
• La funzione tubulare scompare in interi nefroni con il passare degli anni,
seguendo il declino della GFR.
• La soglia renale di glicosuria aumenta con lʼetà: quindi, di solito, in un
paziente diabetico più anziano, il glucosio compare nelle urine a un livello di
glicemia più elevato rispetto ad un diabetico più giovane.
• La capacità massima di concentrazione delle urine diminuisce per una
incapacità relativa a mantenere il gradiente osmotico nella porzione midollare del
rene.
22
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
MALATTIE RENALI
Introduzione
La funzione di reni normali si manifesta attraverso molteplici meccanismi, il
cui scopo è di mantenere lʼomeostasi corporea.
Una qualsivoglia alterazione di queste funzioni può condurre ad una
costellazione di anomalie addirittura interferenti con la sopravvivenza.
Le manifestazioni cliniche di queste alterazioni dipendono dalla fisiopatologia
del danno renale e vengono spesso identificate inizialmente come un insieme
di sintomi, di riscontri abnormi di dati fisici e di laboratorio che -spesso solo in
un secondo tempo- rendono possibile lʼidentificazione di specifiche sindromi
o malattie.
Queste sindromi renali possono essere espressione di una malattia sistemica
o di una specifica e primitiva malattia renale.
Sono tipici indicatori di una patologia renale:
1. Azotemia: un suo incremento depone per una riduzione del GFR
(filtrazione glomerulare).
2. Alterazioni del sedimento urinario: globuli rossi e bianchi, cilindri e cristalli
allʼesame
standard delle urine.
23
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
3. Proteinuria: la presenza di proteine nelle urine prova lʼavvenuta -anomalaescrezione di proteine del siero.
4.Alterazioni del volume urinario: oliguria (=poche urine), anuria (=assenza di
urine), poliuria (=molte urine).
5.Presenza di ipertensione e/o di espansione del volume liquido corporeo
(edema)*.
6.Alterazioni del quadro elettrolitico.
7.In alcuni casi febbre e dolore.
________________________________
* Edema: abnorme aumento della quantità del liquido contenuto nelle cellule e/o negli
spazi intercellulari e negli interstizi dei tessuti. Può trattarsi di una condizione locale limitata cioè ad un determinato distretto dellʼorganismo- oppure di una condizione
generalizzata, che si accompagna anche a versamento di liquido nelle cavità sierose
(pleure, peritoneo) > in questo caso si parla di anasarca. I tessuti edematosi appaiono
tumefatti, pallidi e -nel caso dei tessuti sottocutanei- facilmente identificabili perché,
comprimendo la zona con un dito, vi rimane impressa per qualche tempo una fossetta
corrispondente alla zona di pressione (segno della fovea).
Cominciamo ora ad affrontare la descrizione delle principali patologie renali,
cercando di utilizzare i criteri più recentemente proposti -ed approvati- dalla
comunità scientifica internazionale.
24
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
Danno renale acuto (Acute Kidney Injury > AKI)
Eʼ la nuova dizione di quella che era lʼ insufficienza renale acuta ed indica una
improvvisa compromissione della funzionalità renale, che si manifesta con la ritenzione di
sostanze azotate (azotemia) e di altre sostanze normalmente eliminate dal rene.
LʼAKI non è una singola malattia, bensì raggruppa un gruppo eterogeneo di condizioni con
comuni tratti diagnostici (azotemia e creatininemia elevate, spesso associate ad una
riduzione di volume delle urine).
LʼAKI può presentare gradi differenti di gravità, dallʼasintomatica alla rapidamente fatale.
Le ragioni che hanno portato a mutare il nome dellʼInsufficienza renale acuta in AKI sono
diverse:
• Il termine insufficienza riflette solo una parte dei possibili danni clinici di un rene. In più di
una situazione, il danno renale non trova riscontro che in una modesta alterazione di
funzionalità.
• Nondimeno, un danno modesto può (e succede spesso) influire negativamente sulla
prognosi nel lungo periodo, determinando gravi insufficienze (che spesso richiedono la
dialisi).
LʼAKI complica il 5-7% dei ricoveri ospedalieri urgenti ed il 30% di quelli in
Terapia Intensiva (in cui il rischio di morte supera il 50%).
LʼAKI rappresenta pure una delle complicanze più frequenti, nei paesi in via
di sviluppo, particolarmente nella correzione delle patologie diarroiche,
infettive (come malaria e leptospirosi) e nelle catastrofi naturali (terremoti).
LʼAKI è aumentata di incidenza, negli USA, di più di 4 volte dal 1988; è
stimata una incidenza annuale di 500 per 100.000 individui (superiore a
quella dellʼictus).
Le cause di AKi sono convenzionalmente suddivise in 3 categorie:
1. Azotemia pre-renale
2. Malattia intrinseca renale
3. Ostruzione post-renale
25
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
AZOTEMIA PRE- RENALE
Eʼ la più comune. Eʼ identificata da un aumento di azotemia o creatininemia
conseguenti ad una riduzione del flusso e della pressione di perfusione
renale, che normalmente garantiscono una normale filtrazione a livello del
glomerulo.
I quadri clinici più comunemente responsabili di azotemia pre-renale sono:
• Lʼipovolemia: ʻvolemiaʼ è sinonimo di volume sanguigno circolante (quindi della
quantità complessiva di sangue presente allʼinterno del sistema circolatorio) che è
mediamente di circa 5 litri. ʻIpovolemiaʼ significa riduzione della volemia. Si può
verificare per emorragie (interne od esterne), perdite di acqua e sali da reni o
intestino o dalla cute (é il caso delle grandi ustioni).
• La riduzione della gittata cardiaca
• Farmaci capaci di interferire con i meccanismi di autoregolazione renale:
soprattutto i FANS e gli inibitori dellʼangiotensina (usati come anti-ipertensivi).
Per definizione, lʼazotemia pre-renale NON implica la presenza di danno
renale ed è rapidamente reversibile una volta che si sia ripristinata una
normale perfusione.
Ciò non significa che non possa coesistere con altre forme di AKI e che,
soprattutto se protratta, non possa determinare un danno ischemico al rene
(di solito una necrosi tubulare acuta).
26
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
MALATTIA INTRINSECA RENALE
Le cause più comuni di danno renale intrinseco sono rappresentate da:
• Sepsi: é una infezione generalizzata a tutto lʼorganismo, determinata dal passaggio in
circolo di batteri provenienti da focolai infettivi localizzati in altre sedi. Nei soli USA si
registrano più di 700.000 casi di sepsi allʼanno; lʼAKI intrinseco ne complica più
del 50%, aumentando di molto il rischio morte. La sepsi è anche una importante
causa di AKI intrinseco nei paesi in via di sviluppo. Il meccanismo attraverso cui la
sepsi fa danno è solitamente di tipo emodinamico (ridotta filtrazione glomerulare,
anche in assenza di una chiara ipotensione), specie se in presenza di un danno
tubulare. La sepsi può causare danno endoteliale (cioè della parete dei vasi
capillari), portando a trombosi dei piccoli vasi, ad attivazione di globuli bianchi che
-depositandosi- possono danneggiare le cellule tubulari renali.
• Ischemia: i reni sani, anche se rappresentano solo lo 0.5% della massa
corporea, ricevono il 20% della portata cardiaca ed utilizzano il 10% dellʼossigeno.
I reni sono anche, nella loro midollare, una delle regioni meno irrorate -a causa
dellʼarchitettura dei vasi sanguigni deputati a fornire ossigeno e nutrienti ai tubulie, di conseguenza, più sensibili e vulnerabili da danni ischemici. Sono poi le
interazioni tra globuli bianchi ed endotelio dei piccoli vasi a determinare processi
infiammatori capaci di ridurre il flusso locale (in strutture metabolicamente assai
importanti).
Eʼ pur vero che lʼischemia di per sé non è sufficiente, di solito, a causare un signi
ficativo danno renale, come testimoniano i casi di clampaggio dellʼaorta sopra-re=
nale o di arresto cardiaco.
Nella clinica, lʼAKI da ischemia é appannaggio di pazienti affetti da malattie renali
croniche od in età avanzata; oppure, di casi in cui lʼevento ischemico sia concomi
tante a sepsi, farmaci vasoattivi o nefrotossici, traumi, ustioni e pancreatiti.**
_______________________________________________
** Ustioni e pancreatiti acute: condizionano cospicue perdite di liquidi extravascolari e, di
solito, un maggior rischio di sepsi così come di infezioni polmonari. La massiccia
somministrazione di liquidi, necessaria nellʼintervento rianimatorio, può aumentare di molto
(oltre i 20 mmHg) la pressione allʼinterno dellʼaddome, determinando la compressione
della vena renale ed unʼulteriore riduzione del filtrato glomerulare.
27
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
28
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
OSTRUZIONE POST-RENALE
Si realizza quando il flusso dellʼurina, normalmente unidirezionale, sia
acutamente bloccato (parzialmente o totalmente): la pressione aumenta così
in senso retrogrado e può arrivare ad interferire con la filtrazione glomerulare.
Lʼostruzione può essere causata da un danno -anatomico o funzionale- a
qualsiasi livello, dal bacinetto renale alla punta dellʼuretra.
Perché lʼostruzione produca danno, in un individuo sano è necessario sia
completa e bilaterale.
Eventi classicamente responsabili di ostruzione post-renale sono:
•
•
•
•
•
•
A livello di collo vescicale, patologie -benigne o maligne- della prostata.
“Vescica neurologica **”
Coaguli di sangue, calcoli.
Cateteri vescicali ostruiti.
Infiltrati della parete dellʼuretere (neoplasie).
Compressioni estrinseche degli ureteri: ascessi, tumori addominali, sequele di interventi
chirurgici.
29
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
______________________________________
* Vescica neurologica: la vescica è un contenitore le cui funzioni sono regolate da precisi
meccanismi, che presuppongono lʼinvio di un continuo flusso di informazioni verso
strutture nervose (posizionate a livello di midollo spinale, tronco cerebrale e corteccia
cerebrale). Da queste strutture nervose partono segnali -eccitatori od inibitori- indirizzati
verso le componenti muscolari di vescica, uretra ecc., volti a consentire lo svuotamento
(o lʼaccumulo) di urina. Una patologia neurologica che colpisca uno dei centri di controllo
ha come conseguenza una incoordinazione del meccanismo, che si riflette in una
disfunzione neurogenica dello svuotamento (ritenzione, incontinenza, vascica
automatica).
Lʼinstaurarsi di un AKI post-renale implica alterazioni emodinamiche scatenate dal
brusco innalzarsi della pressione allʼinterno dei tubuli renali.
Allʼaumento della pressione nei tubuli, corrisponde inizialmente un periodo di
iperemia (per la dilatazione delle arteriole) seguito dalla vasocostrizione intrarenale
(per stimolo chimico, da angiotensina, vasopressina ed altri). Ciò induce una ridotta
perfusione dei glomeruli e, quindi, una ridotta filtrazione glomerulare.
30
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
MALATTIE CRONICHE DEL RENE (Chronic Kidney
Disease)
Si comprende, in questa dizione, una grande varietà di situazioni, il cui punto
comune è di associarsi ad una funzionalità renale abnorme ed a una
progressiva riduzione della filtrazione glomerulare.
Fisiopatologia
Duplice il meccanismo alla base di una malattia renale cronica:
1. Quello legato alla causa specifica: alterazioni renali geneticamente determinate,
deposizione di immunocomplessi ed infiammazione in alcuni tipi di
glomerulonefriti, esposizione a tossine in certe malattie dei tubuli ecc.).
2. Quelli conseguenti alla riduzione della massa renale, indipendentemente dalla
causa specifica: per esempio, lʼipertrofia e la maggior capacità filtrante dei
nefroni sopravvissuti. Con il passar del tempo, questi meccanismi di adattamento
iniziale possono divenire controproducenti, dal momento che sia lʼaumento di
pressione che di flusso possono sconvolgere lʼarchitettura del glomerulo,
condizionandone la
sclerosi e la perdita di
funzionalità.
31
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
Fattori di rischio
Eʼ molto importante identificare i fattori di rischio per CKD, persino in soggetti
con normale grado di filtrazione glomerulare (GFR).
I principali sono:
• Ipertensione
• diabete
• malattie autoimmuni
• età avanzata
• origini Africane *
• storia famigliare di malattie renali
• un episodio pregresso di danno renale acuto
• presenza di proteinuria, sedimento urinario anomalo ed alterazioni strutturali
dellʼapparato urinario.
___________________________________
* Genetica: nelle popolazioni di origine Africana dellʼovest, alcune patologie renali hanno
una frequenza anche di 7 volte superiore a quella degli americani di origine ispanica.
Studi recenti hanno consentito di spiegarlo con la presenza di sequenze di DNA varianti
nei loci correlati alle suddette malattie.
Le malattie renali croniche vengono classificate partendo dal GFR (grado di
filtrazione glomerulare).
*
Il calcolo del GFR avviene utilizzando complesse formule matematiche, che
tengono conto di:
1. Creatininemia
2. Età
3. Sesso
4. Razza
5. Peso corporeo
Il GFR viene espresso in mL/minuto per 1.73 mq di superficie corporea.
32
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
Il GFR diminuisce di circa 1 ml/min/1.73 mq per anno con lʼavanzare dellʼetà,
passando dai valori massimi (circa 120 ml/die/1,73 mq della terza decade) a quelli
medi (70 ml) dei 70 anni.
Il GFR medio è più basso nelle donne che nei maschi.
**
Il dosaggio dellʼalbumina nelle urine delle 24 ore è pure uno strumento utile per
controllare il danno a carico dei nefroni ed anche la risposta alla terapia, specie
nelle glomerulopatie croniche.
La persistenza nelle urine di più di 17 milligrammi di albumina per grammo di creatinina
(nel maschio adulto) e di 25 mg (nella femmina adulta) viene solitamente considerata
significativa di danno renale cronico.
Si chiama microalbuminuria la presenza di minime quantità di albumina nelle urine, che
non possono essere misurate secondo le comuni metodiche di laboratorio. Il riscontro di
microalbuminuria é un buon test di screening precoce per le malattie renali (ed anche per
la presenza di una malattia micro-vascolare, cioè dei piccoli vasi, in generale).
Le malattie renali croniche, in base al GFR, vengono classificate in 6
differenti stadi, con crescente grado di gravità e conseguente diversa
prognosi.
33
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
Nei primi 2 stadi, di solito mancano sintomi connessi al decremento del GFR.
Possono, peraltro, essere presenti sintomi della malattia renale sottostante (edemi
in pazienti con sindrome nefrosica, ipertensione in pazienti con rene policistico
ecc.).
Se il GFR si riduce come negli stadi 3-4, si rendono progressivamente evidenti
segni clinici e di laboratorio da CKD.
Virtualmente sono interessati tutti gli apparati, ma le complicanze più evidenti sono:
• Anemia e connessa spiccata faticabilità.
• Perdita di appetito con progressiva malnutrizione.
• Alterazioni nel metabolismo di calcio, fosforo, sodio, potassio e nellʼequilibrio acido-base.
Se il paziente progredisce sino allo stadio 5, vi è accumulo di sostanze tossiche,
che condizionano una significativa interferenza nelle attività quotidiane, nella
percezione di benessere, nello stato nutrizionale: via via fino alla c.d. sindrome
uremica, che può condurre a morte se non si interviene con dialisi o trapianto.
34
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
Epidemiologia
Eʼ stato stimato che almeno il 6% della popolazione USA adulta ha una CKD in
Stadio 1 e 2; un ulteriore 4.5% in Stadio 3 e 4.
Riportiamo ora le 5 cause più frequenti di danno renale cronico, che -per la
popolazione USA ed Europea- comprendono il 90% dei casi:
1. Malattia glomerulare diabetica.
2. Glomerulonefrite.
3. Nefropatia ipertensiva, comprensiva della Glomerulopatia primaria con
ipertensione e della malattia renale vascolare ischemica.
4. Rene policistico (autosomico dominante).
5. Altre nefropatie cistiche e tubulointerstiziali.
Quadro di nefropatia diabetica
Anche se i valori di azotemia e creatininemia vengono usati per quantificare le
capacità escretorie del rene, lʼaccumulo di queste due molecole di per sé non da
ragione dei molti segni e sintomi che caratterizzano la sindrome uremica degli
stadi più avanzati di malattia renale cronica.
Sono centinaia le tossine che si accumulano, insieme ad altre categorie di prodotti azotati
(composti guanidinici, urati, poliamidi, fenoli ecc.) ed alle cosiddette ʻmolecole medieʼ (in
relazione al peso molecolare) che possono aumentare morbilità e mortalità.
Nella sindrome uremica, va poi considerato che non viene compromessa solo la
funzione escretoria del rene: vengono, ad esempio, alterate o soppresse molte
35
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
delle funzioni endocrine e metaboliche, di normale competenza renale, con il
risultato di anemia, malnutrizione, dismetabolismi di grassi, proteine e carboidrati.
Anche i livelli di molti ormoni (paratormone, insulina, glucagone, steroidi, vitamina
D ed ormoni sessuali) cambiano a seguito della ritenzione urinaria, della minor
degradazione e dellʼabnorme regolazione.
Potremmo proseguire con numerosi altri esempi. Vale forse la pena di sintetizzare,
in 3 punti, le ʻsfereʼ di disfunzione nella sindrome uremica:
1. Quelle conseguenti allʼaccumulo di tossine, che normalmente vengono eliminate
dal rene, inclusi i prodotti del metabolismo proteico.
2. Quelle conseguenti alla perdita di altre funzioni renali, come il bilancio idroelettrolitico e la regolazione ormonale.
3. La progressiva infiammazione sistemica e le sue conseguenze vascolari e
nutrizionali.
Eʼ praticamente impossibile, in questo contesto e con i tempi di cui
disponiamo, addentrarci nelle singole problematiche, sia cliniche che di
indagine.
I pazienti con malattia renale cronica devono essere affidati alle competenze
dello specialista (Nefrologo) che orienterà il proprio intervento
• nel trattamento della malattia di base: correzione dellʼiperglicemia (diabete),
farmaci immunomodulanti (glomerulonefrite), nuove terapie ritardanti la citogenesi
(rene policistico).
• nellʼottimizzazione del ʻtimingʼ (= tempo di intervento) terapeutico, specifico o no, in
relazione alla diminuzione della filtrazione glomerulare. Basti pensare che il
peggioramento del GFR può essere conseguenza di fattori o processi in sovrapposizione
(ipertensione non controllata, infezioni delle vie urinarie, esposizione a farmaci
nefrotossici od a mezzi di contrasto iodato ecc.), che possono essere reversibili.
• nel cercare di rallentare la progressione della malattia cronica: riducendo
lʼipertensione allʼinterno del glomerulo e la perdita di proteine.
• nel cercare di rallentare la progressione della malattia renale diabetica: controllo
di glicemia ed ipertensione, restrizione proteica.
• nel contrastare le possibili complicanze: scelta e dosaggio di molti farmaci, anche
di uso comune.
• nella preparazione a dialisi o trapianto.
36
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
Ci occuperemo ora delle principali malattie renali, per comodità concettuale
distinguendole in:
• Glomerulopatie
• Malattie tubulari o tubulopatie
• Malattie da infezione delle vie urinarie
• Malattie vascolari renali
• Nefrolitiasi
• Neoplasie
1. Glomerulopatie
Con questo nome si indica un gruppo di malattie infiammatorie del rene, che
colpiscono le strutture funzionali più importanti del tessuto renale, i glomeruli.
Nellʼinsorgenza delle glomerulopatie sono implicati diversi meccanismi
immunologici (mezzi che rappresentano il sistema di difesa dellʼorganismo
nei confronti di sostanze ʻestraneeʼ) non ancora completamente chiariti.
I processi patologici a carico dei glomeruli possono essere innescati:
• da una abnorme risposta del sistema immunitario a molecole estranee (antigeni)
con deposizione nel rene di complessi antigene-anticorpo (i c.d.
immunocomplessi).*
• da una risposta anticorpale dellʼorganismo a certe molecole glomerulari, che sono
erroneamente riconosciute come ʻestraneeʼ. **
37
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
Le glomerulopatie si distinguono in primitive (che si presentano come malattie a sé
stanti: é il caso delle glomerulonefriti) oppure secondarie (quando fanno parte di
malattie più complesse: ad esempio, diabete, collagenopatie, malattie sistemiche).
Acute sono le patologie glomerulari che si instaurano in settimane o pochi mesi,
croniche quelle che impiegano mesi od anni.
________________________________________
* Immunocomplessi circolanti: gli antigeni nel siero con cui possono combinarsi gli
anticorpi possono essere il DNA (ad esempio nel Lupus), prodotti batterici (ad esempio,
Streptococchi o Treponema P.), prodotti virali (virus dellʼepatite B e C), antigeni malarici
(Plasmodio della Malaria), antigeni tumorali (ad esempio, CEA).
**Autoanticorpi: anticorpi diretti contro normali antigeni glomerulari o antigeni che si
sono “impiantati” nel glomerulo, formando complessi immuni ʻin situʼ.
38
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
Gli immunocomplessi, sia quelli che si formano in circolazione che quelli che
si formano ʻin situʼ con gli antigeni da impianto, producono aggregati
granulari, la cui localizzazione glomerulare dipende da carica, quantità,
affinità per lʼantigene, solubilità, dimensione, efficienza dei meccanismi di
rimozione e da fattori emodinamici.
39
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
Il sito della reazione anticorpale nel glomerulo é molto importante nella
presentazione clinico-patologica della malattia:
• La deposizione degli antigeni nello spazio sub-endoteliale* o nel mesangio**
innesca solitamente una risposta nefritica, richiamando globuli bianchi e piastrine.
• La deposizione degli antigeni nello spazio subepiteliale innesca una risposta
nefrosica, cioé con scarso infiltrato infiammatorio.
• La risposta infiammatoria é più grave se il deposito é sub-endoteliale, in quanto
allʼinfiltrazione leucocitaria fa seguito la proliferazione delle cellule endoteliali e del
mesangio.
_____________________________________
* Spazio subendoteliale: lʼendotelio è una sottilissima lamina che tappezza la parete
interna dellʼapparato circolatorio in tutte le sue diverse sezioni (cavità cardiache, arterie,
capillari, vene, vasi linfatici) ed é a diretto contatto con il sangue. Eʼ costituito da uno
strato di cellule molto appiattite, che poggiano su una membrana a struttura fibroelastica, con funzioni di supporto. Nei vasi capillari di alcuni organi (tra cui il rene),
lʼendotelio presenta delle fenestrature, regolarmente distribuite, chiuse da una
membrana sottile. Tali fenestrature rappresentano la sede ove avviene la diffusione nei
40
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
tessuti di acqua e sostanze nutritive. Lo spazio al di sotto dellʼendotelio, costituito dal
restante spessore della parete vascolare, prende nome di sub-endoteliale.
** Mesangio: allʼinterno del glomerulo, il mesangio é lʼinsieme di particolari cellule
(mesangiali), disposte attorno ai capillari, che avvolgono insinuandosi tra endotelio e
membrana basale. Hanno capacità contrattile, per cui -contraendosi e rilasciandosi,
possono regolare il calibro dei capillari glomerulari: contraendosi, riducono lʼafflusso di
sangue allʼinterno del glomerulo, con conseguente riduzione della filtrazione renale e
quindi della escrezione di acqua, sodio ed altre sostanze.
Queste cellule hanno un ruolo anche nei meccanismi dellʼinfiammazione e dellʼimmunità.
In più, sono dotate di attività fagocitaria nei confronti di proteine, immunocomplessi ed
altro.
Posizione del mesangio allʼinterno del corpuscolo renale
5a indica il mesangio intraglomerulare
Rappresentazioneschematica, in sezione, del mesangio (M)
e di tre capillari (C).
41
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
Glomerulonefriti acute (Sindromi nefritiche acute)
La presentazione clinica classica é fondata su:
• Ipertensione.
• Ematuria (=sangue nelle urine).
• Presenza di cilindri ematici .*
• Piuria (=globuli bianchi nelle urine).
• Proteinuria, da lieve a modesta.
Se il danno infiammatorio del glomerulo é esteso, si può avere:
• Riduzione del filtrato glomerulare
• Aumento dellʼazotemia.
• Ritenzione idro-salina.
_________________________________
* Cilindri ematici: sono strutture di forma cilindrica che si possono osservare al
microscopio nel sedimento dellʼurina di persone affette da malattie renali. La forma é
dovuta al fatto che cellule (in questo caso globuli rossi), più o meno degenerate, si
accumulano nei tubuli renali, producendo formazioni compatte che ricalcano lo stampo
interno del tubulo stesso.
42
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
Cause e principali quadri clinici delle glomerulonefriti
acute
1. Glomerulonefrite post-streptococcica
Eʼ il prototipo delle glomerulonefriti acute proliferative endocapillari (v. sopra).
La sua incidenza é drammaticamente diminuita nei paesi sviluppati, ove può
ormai essere considerata sporadica e dove colpisce tipicamente lʼetà avanzata,
specie se vi sono altre condizioni debilitanti .
Nei paesi sottosviluppati di solito colpisce bambini tra i 2 ed i 14 anni, con
maggior frequenza maschi.
Infezioni di cute o gola da Streptococco beta emolitico, in particolare di tipo M, di
solito precedono la malattia glomerulare: di 2-6 settimane quelle cutanee
(Impetigine *), di 1-3 settimane quella faringea.
_______________________________________
*Impetigine: é causata normalmente dalla Stafilococco Aureo, ma anche dallo
Streptococco beta emolitico. Eʼ unʼinfezione acuta che colpisce la pelle, generalmente del
viso e degli arti. Compaiono inizialmente vesciche ripiene di liquido chiaro su viso, braccia
e gambe; le vesciche successivamente si rompono e si forma una crosta gialla o brunogiallastra, che si stacca facilmente. La pelle adiacente alla crosta può arrossarsi e
provocare forte prurito.
Eʼ una malattia molto comune tra i bambini in età prescolare ed una cattiva igiene é un
rilevante fattore di rischio.
Il contagio avviene per contatto con le lesioni cutanee o con le secrezioni nasali del
malato.
Se non adeguatamente curata, lʼimpetigine può provocare infezioni più pericolose a carico
degli organi interni, rene su tutti.
43
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
La glomerulonefrite post-streptococcica è una malattia immunomediata, che
coinvolge:
• Antigeni streptococcici.
• Immunocomplessi circolanti.
• Attivazione del complemento**.
___________________________________________
** Complemento: il sistema del complemento, insieme agli anticorpi, é un elemento
essenziale del sistema immunitario di difesa contro gli agenti infettivi. Eʼ costituito da una
ventina di proteine circolanti e di membrana, capaci di interagire reciprocamente e con le
membrane cellulari. Lʼattivazione a cascata di queste proteine -che convenzionalmente
vengono chiamate componenti- è alla base di attività biologiche varie, come la lisi (=
distruzione) cellulare, batterica o virale. Le proteine del sistema del complemento si
introducono nelle membrane degli agenti patogeni, virus o batteri che siano,
“bucandole” (inducendo la formazione di pori che portano alla lisi).
Ogniqualvolta, poi, viene attivato il complemento, si ha anche il reclutamento di varie
cellule immunocompetenti, quali monociti, macrofagi, linfociti.
44
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
Lʼattivazione del complemento, secondo la c.d. via classica -cui si riferisce la figuradipende dallʼinterazione di 3 proteine del sistema (C1, C4, C2) con il complesso antigeneanticorpo. Inizia, a questo punto, una cascata di reazioni chimiche -su cui, ovviamente,
non ci dilunghiamo- che hanno come tappa ultima la fissazione alla membrana del battere
e la sua distruzione.
Nelle 2 immagini, schematizzata la formazione dei pori nelle
membrane degli agenti infettanti ad opera delle proteine del
complemento e la conseguente perdita della capacità di re=
golare il passaggio dei liquidi extracellulari.
45
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
La diagnosi di glomerulonefrite post-streptococcica assai raramente richiede
il ricorso alla biopsia.
Vi sono dati di laboratorio assai caratteristici che bastano a comprovare la
diagnosi (accanto, ovviamente, ai dati clinici):
• Diminuzione (specie nella prima settimana di malattia) delle frazioni C3 del
complemento, con C4 normali.
• Fattori reumatoidi positivi (40%), crioglobuline ed immunocomplessi circolanti
(60-70%).
• Colture positive per lo Streptococco si rinvengono in non più del 10% dei casi, ma
altre titolazioni (ad esempio, degli anticorpi anti-DNAasi) pesano nella conferma
della diagnosi.
La terapia prevede il trattamento antibiotico per le infezioni streptococciche
(ai pazienti ed a tutti coloro che vivono accanto) e le eventuali misure di
supporto (controllo di ipertensione, edemi ecc.).
La prognosi é buona (meno dellʼ1% dei bambini ha problemi renali residui).
Maggiori i rischi negli anziani (soprattutto se lʼazotemia è superiore a 60).
46
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
2. Glomerulonefrite associata ad endocardite
Rappresenta una complicanza tipica dellʼendocardite batterica subacuta*, specie in
pazienti che non vengono trattati per lungo tempo ed hanno emocolture negative.
________________________
* Nelle forme acute, di solito non si ha glomerulonefrite, dal momento che gli immunocomplessi
che la determinano impiegano di solito 10-14 giorni a svilupparsi ed in questo lasso di tempo il
paziente riceve un trattamento adeguato.
Eʼ causata dalla deposizione nel rene di immunocomplessi circolanti, con
attivazione del complemento.
I sintomi tipici sono rappresentati da:
•
•
•
•
Ematuria (macro o microscopica).
Piuria.
Proteinuria (di modesta entità).
Rapida compromissione della funzionalità renale (raramente).
La terapia si fonda sullo sradicamento dellʼinfezione con un trattamento
antibiotico di 4-6 settimane, che -quanto più precocemente eseguito- limita le
complicanze renali, migliorando nettamente la prognosi.
47
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
3. Nefrite lupica
Rappresenta una comune e seria complicanza del Lupus Eritematoso
Sistemico, più grave nelle adolescenti afro-americane.
Dal 30 al 50% dei pazienti affetti da Lupus presentano manifestazioni cliniche di malattia
renale già al tempo della diagnosi; il 60% degli adulti e lʼ80% dei bambini sviluppa
alterazioni renali in un momento qualsiasi del decorso della loro malattia.
La nefrite lupica è conseguente alla deposizione di immuno-complessi circolanti,
capaci di attivare la cascata di reazioni del complemento, con relativi danni (ma
anche con infiltrati leucocitari, attivazione di fattori della coagulazione e liberazione
di varie citochine*).
________________________________
* Citochine: sono proteine di piccole dimensioni, prodotte da vari tipi di cellule, che
trasmettono messaggi in grado di attivare funzioni specializzate come la riproduzione, la
differenziazione e la morte cellulare. Le citochine prodotte dal sistema immunitario (cioè
da macrofagi e linfociti) sono dette linfochine o interleuchine. Ne è un esempio
lʼimportante famiglia degli Interferoni, che inducono le cellule a resistere ad infezioni
virali.
48
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
Si riconoscono diverse lesioni istologiche della nefrite lupica, classificate in 6 classi
dallʼOrganizzazione Mondiale della Sanità:
1. Lesioni minime.
2. Proliferazione delle cellule del mesangio.
3. Nefrite focale (proliferazione endo- ed extra-capillare, con depositi focali subendoteliali di
immunocomplessi).
4. Nefrite diffusa (proliferazione endo- ed extracapillare diffusa, con depositi subendoteliali
diffusi ed alterazioni diffuse del mesangio).
5. Nefrite membranosa (assottigliamento delle membrane basali con depositi subendoteliali
diffusi).
6. Nefrite sclerotica (sclerosi globale di quasi tutti i capillari glomerulari).
In genere, la prognosi è peggiore nei pazienti in classe 4 e 5, buona per le classi 1
e 2, intermedia per la classe 3.
Va però sottolineato che il lupus è una malattia imprevedibile, per cui è difficile
valutare una prognosi a lungo termine sul risultato di una sola biopsia iniziale.
I sintomi della nefrite lupica, accanto a quelli della malattia di base, variano per
numero ed intensità a seconda della Classe in cui si colloca il paziente.
• Proteinuria e conseguente formazione di edemi.
•
•
•
•
•
•
Ematuria.
Ipertensione.
Funzionalità renale compromessa.
Anticorpi anti-DNA
Bassi livelli di complemento.
Cellule ʻa castoneʼ **nel sedimento urinario.
___________________________________
** Cellule a castone: particolare morfologia tipica delle neoplasie epiteliali ghiandolari
(adenocarcinomi di derivazione gastrica, intestinale o mammaria). Eʼ possibile identificare
cellule -in tal caso neoplastiche- che presentano un grosso vacuolo omogeneo che
occupa tutto il citoplasma, spingendo e deformando il nucleo contro la membrana
cellulare. Questo materiale è muco ed è sensibile a specifiche colorazioni (PAS). Queste
cellule ad anello con castone possono evidenziarsi anche in patologie non tumorali, quali,
ad esempio, in corso di versamenti cavitari o di nefrite lupica.
49
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
La terapia della nefrite lupica è differente, come ovvio, a seconda della
stadiazione.
Si fonda principalmente su due tipologie di farmaci -i cortisonici e gli
immunosoppressori- spesso usati in associazione e per periodi prolungati di
tempo.
Nei casi più gravi, raggiunti dal 20% dei pazienti, sono necessari dialisi e/o
trapianto di rene.
Il trapianto viene eseguito di solito dopo 6 mesi di malattia stabilizzata ed ha
risultati sovrapponibili a quelli di trapianti eseguiti per altre patologie.
Doveroso, per chiarezza e completezza, a questo punto, un richiamo a quelle che
sono le nozioni fondamentali sulla malattia di base di questa particolare forma di
nefrite, il Lupus Eritematoso Sistemico (LES).
Malattia ad eziologia sconosciuta, che colpisce più facilmente il sesso femminile (9 su 10),
di età compresa soprattutto tra i 20 ed i 50 anni.
Nel corso della malattia, vengono
danneggiati numerosi tessuti ad opera di
immunocomplessi di origine patologica.
Dallʼinterazione tra la predisposizione genetica (in parte responsabile di una anormale
regolazione immunitaria) e fattori ambientali (tra questi, sicuramente dimostrati i raggi UV)
deriverebbe una risposta patologica da parte del sistema immunitario, caratterizzata da
una iperattività dei linfociti B e T, che i normali meccanismi di autocontrollo immunitario
non sono in grado di sopprimere. Farebbe seguito la formazione di immunocomplessi,
che si depositano nei tessuti e scatenano una reazione di tipo infiammatorio responsabile
del danno di vari organi.
In effetti, il LES è caratterizzato dalla produzione di una grande quantità di autoanticorpi
diretti contro le molecole dellʼorganismo stesso, soprattutto contro strutture che fanno
parte del nucleo delle cellule: anticorpi anti-muscolo liscio (presenti nel 30% dei casi),
anticorpi anti-nucleo, anti-DNA (molto frequenti ma poco specifici), e poi autoanticorpi
contro le strutture intracitoplasmatiche, i fattori della coagulazione, le cellule del sangue e
contro antigeni presenti su numerosi organi e tessuti.
La malattia può presentarsi con sintomi diversi, non sempre tutti contemporaneamente
presenti.
Accanto a quelli sistemici (debolezza, malessere, febbre, perdita di appetito, nausea e
perdita di peso, talora diffuso ingrossamento linfoghiandolare) possono comparire segni e
sintomi indicativi dei danni dʼorgano che la malattia provoca, a carico di:
• Sistema muscolo-scheletrico: dolori articolari e muscolari, poliartriti, miositi.
• Cute: eritema a farfalla, fotosensibilità, ulcere orali, lupus discoide.
50
Roberto Freschi
•
•
•
•
•
•
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
Ematologico: anemia, leucopenia, piastrinopenia.
Neurologico: disturbi cognitivi, convulsioni, psicosi.
Cardiopolmonare: pleurite, pericardite, miocardite, infarti miocardici, endocardite).
Renale: glomerulonefrite acuta.
Oculare: congiuntivite, xeroftalmia.
Gastrointestinale
Il tipico eritema a farfalla del volto
51
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
4. Malattia anti-membrana-basale-del-glomerulo (anti-GBM)
Pur trattandosi di malattia rara, questa particolare glomerulonefrite (che può
presentarsi in soggetti che sviluppano auto-anticorpi diretti contro la
membrana basale del glomerulo) assume particolare rilievo clinico quando si
associa (frequentemente) ad emorragia polmonare. In tale evenienza, prende
il nome di Sindrome di Goodpasture.
La Sindrome di Goodpasture ha unʼincidenza fino ad 1 caso per milione di
popolazione per anno.
Colpisce caratteristicamente due fasce di età:
• Maschi tra 20 e 30 anni.
• Maschi e femmine tra 60 e 70 anni.
Nel gruppo più giovane, la malattia solitamente si manifesta in modo esplosivo con:
•
•
•
•
•
Emottisi
Anemia acuta
Febbre
Problemi respiratori
Ematuria
Nel gruppo più anziano, la malattia si presenta più spesso con un prolungato
periodo di danno renale (la presentazione con oliguria è associata a peggior prognosi).
Diagnosi
Metodica di elezione è la biopsia renale, i cui aspetti sono caratteristici.
Spesso dosabili (nel siero e nella biopsia) gli anticorpi anti GMB.
Terapia
La terapia convenzionale include una combinazione di plasmaferesi * e di
immunosoppressori .
52
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
<<<<<<<<<<
Schema di un glomerulo: le frecce <<<<< indicano la membrana basale
glomerulare (MBG), verso cui sono diretti gli anticorpi.
Nella foto sotto, lʼimmagine al microscopio di una biopsia renale, ove è
ben visibile la proliferazione della membrana basale.
<<<<<<<
53
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
_______________________________
* Plasmaferesi: è una procedura terapeutica (chiamata anche aferesi o plasmaexchange) che permette la separazione della componente liquida del sangue (il plasma)
dalla componente cellulare e la rimozione di sostanze in esso presenti. Il paziente è
collegato alla macchina attraverso 2 accessi venosi, che permettono da un lato il prelievo
dei sangue da depurare e dallʼaltro la contemporanea reinfusione del sangue depurato,
in un ciclo continuo.
•
•
•
•
Si possono così rimuovere dal circolo sanguigno diverse sostanze, quali:
Immunoglobuline
Immunocomplessi circolanti
Tossine
Metaboliti
Non ci soffermiamo, forzatamente, su altri quadri di glomerulonefrite (sono
numerosi: Nefropatia da IgA, Glomerulonefrite membranoproliferativa o
mesangioproliferativa), per occuparci di un altro, importante capitolo delle
malattie renali, la Sindrome Nefrosica.
54
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
Sindrome nefrosica
Più che di una malattia vera e propria, si tratta di un complesso di sintomi,
caratterizzato da abbondante eliminazione di proteine attraverso le urine
(proteinuria), edemi e versamenti nelle cavità sierose, riduzione delle
proteine nel plasma sanguigno (ipoproteinemia) e, frequentemente, anche
da aumento dei lipidi e del colesterolo nel sangue (iperlipemia,
ipercolesterolemia).
Senza una diagnosi ed una terapia tempestive, ognuno di questi sintomi può
arrecare danno ai glomeruli, sino a determinare una riduzione della filtrazione
glomerulare, provocando insufficienza renale.
Possono essere causa di sindrome nefrosica diverse condizioni, che schematicamente- richiamiamo:
• Glomerulopatia a lesioni minime (Minimal Change Disease): è responsabile del
70-90% di sindromi nefrosiche del bambino e solo del 10-15% di quelle dellʼadulto. La
malattia si presenta di solito come una malattia renale primitiva, anche se può essere
associata a parecchie altre condizioni (Hodgkin, allergie, uso di FANS). Viene chiamata
ʻa lesioni minimeʼ o addirittura ʻniente lesioniʼ , perchè volume e struttura glomerulare
sono normali alla microscopia ottica; è la microscopia elettronica che evidenzia la
lesione caratteristica e cioè la scomparsa dei podociti* delle cellule epiteliali viscerali. Si
ritiene possa esserne causa una citochina circolante (vedi nota precedente a pag. 48).
Per avere una dimensione del problema, si ha una perdita media di 10 grammi di
albumina nel giro di 24 ore. Caratteristico il decorso con remissioni spontanee e ricadute.
Terapia di prima scelta e provata efficacia quella steroidea.
___________________________________________
* Podociti: sono cellule altamente differenziate. Si trovano nel nefrone, allʼinterno della
Capsula di Bowman, appaiono come elementi stellati, con il corpo voluminoso e rigonfio
che sporge nello spazio capsulare e con prolungamenti (i processi maggiori), che
abbracciano -come i tentacoli di una piovra- i capillari glomerulari. Dai processi maggiori
si stacca un numero notevole di prolungamenti sottili e brevi, che prendono il nome di
pedicelli o piedi terminali. I pedicelli sono leggermente dilatati alla loro estremità, in
corrispondenza della quale aderiscono alla superficie esterna della lamina basale dei
capillari glomerulari.
55
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
56
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
• Glomerulosclerosi segmentaria e focale: si riferisce ad un tipo di lesione renale
caratterizzato da ʻcicatriciʼ di alcuni -ma non di tutti- i glomeruli (focale) e,
allʼinterno dei glomeruli interessati, di solo parte di essi (segmentaria). Eʼ patologia
in aumento, rappresentando la terza causa più comune di sindrome nefrosica dellʼadulto
(20-30%), nei maschi di razza nera (50%). Vi sono dati indicanti che un fattore circolante
funga da mediatore dellʼaumento della permeabilità glomerulare alle proteine, assieme
ad altre sostanze responsabili della sclerosi (cicatrizzazione). La malattia inizia nei
glomeruli iuxtamidollari (i più profondi), il che da ragione della scarsa rispondenza delle
biopsie (spesso effettuate più superficialmente). I sintomi sono ematuria, ipertensione,
proteinuria (di qualsiasi entità) sino allʼinsufficienza renale. La terapia si basa sugli
steroidi (non sempre vi è sensibilità) e sugli immunosoppressori.
>>>
57
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
• Glomerulonefrite membranosa: è responsabile di circa il 30% delle sindromi
nefrosiche dellʼadulto (tra i 30 ed i 50 anni in particolare e con un rapporto 2:1 tra
maschi e femmine). Rara nellʼinfanzia, è la causa più comune delle sindromi
nefrosiche dellʼanziano. Frequenti le associazioni: tumori maligni (30%, mammellapolmone- colon), infezioni (epatite B, malaria), malattie reumatiche (Lupus, artrite
reumatoide). La biopsia renale dimostra un ispessimento della membrana basale del
glomerulo, uniforme e diffuso. Questo ispessimento è dovuto alla deposizione di
immunocomplessi sul versante epiteliale della membrana basale. La deposizione di
immunocomplessi produce lʼinnesco di mediatori dellʼinfiammazione ed una reazione
della membrana basale con estroflessioni che inglobano lʼimmunocomplesso. Questa
glomerulonefrite si segnala per il più elevato numero di complicanze trombotiche (vene
renali, vene profonde degli arti, embolia polmonare). Terapia: dei sintomi (ipertensione,
edemi) + steroidi e/o immunosoppressori.
58
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
• Nefropatia diabetica: è la causa più frequente di insufficienza renale cronica
negli USA (45% dei pazienti in dialisi) ed è descritta in grande aumento in tutto il
mondo. La maggioranza (90%) dei diabetici con nefropatia ha diabete tipo 2. Sono
considerati fattori di rischio iperglicemia, ipertensione, dislipidemia, fumo di sigarette,
precedenti famigliari di nefropatia, fattori genetici. Le alterazioni morfologiche renali
compaiono entro i primi 2 anni dal manifestarsi del diabete e consistono tipicamente in
un assottigliamento della membrana basale glomerulare e dalla espansione del
mesangio (vedi nota pag.41) per accumulo della sua matrice. Frequenti anche le
alterazioni vascolari. Allo stadio iniziale, la malattia prevede la comparsa nelle urine di
anormali livelli di albumina (meno di 30 mg./die); tale condizione viene definita
microalbuminuria. In assenza di interventi terapeutici specifici, circa lʼ80% dei pazienti
presenta un incremento nellʼescrezione urinaria di albumina che, in una parte di essi,
può arrivare ad eliminare più di 500 mg. di albumina nelle 24 ore: è lo stadio (in genere
dopo 15-20 anni) della nefropatia conclamata. Con la comparsa della proteinuria
clinica, si assiste ad una riduzione graduale ma progressiva della funzione renale, che
porta, nel corso degli anni, allʼinsufficienza renale terminale ed alla necessità della
dialisi. Numerosi studi hanno dimostrato che la progressione della nefropatia diabetica
può essere rallentata da alcuni interventi, la cui efficacia risulta maggiore se attuati ad
uno stadio precoce: controllo glicemico, controllo dellʼipertensione, dieta ipoproteica.
59
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
• Malattie da depositi glomerulari: una disfunzione delle plasmacellule* che si
trovano a produrre una eccessiva quantità di immunoglobuline a catena leggera
porta talora alla formazione di depositi glomerulari (o tubulari) responsabili di
grave proteinuria e di insufficienza renale. Lo stesso vale per lʼaccumulo di
frammenti proteici di amiloide **, presenti in molte malattie infiammatorie.
______________________________________
* Plasmacellule: sono cellule del sistema immunitario. Sono presenti nei tessuti sede di
processi infiammatori cronici, ma anche nel midollo osseo, nella mucosa del tubo
digerente e delle vie respiratorie, nei linfonodi. In condizioni normali non si vedono nel
sangue periferico. Le plasmacellule derivano dai linfociti B nel corso delle reazioni di
difesa immunitaria dellʼorganismo; quando vengono a contatto con antigeni, la loro
attività consiste nella sintesi di proteine, e precisamente di immunoglobuline, cioè di
anticorpi circolanti.
** Amiloide: proteina fibrillare a basso peso molecolare, che si accumula, localmente od
in modo diffuso, in organi o tessuti, formando depositi che sono alla base della amiloidosi.
Circa il 10% dei depositi di amiloide è costituito dalla proteina C reattiva, proteina
normalmente presente nel sangue, che aumenta negli stati infiammatori.
60
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
La deposizione di immunoglobuline o di sostanza amiloide possono causare una
sindrome nefrosica, che -in circa il 40-60% dei pazienti- progredisce sino alla dialisi.
La biopsia del rene (o del fegato) è diagnostica nel 90% dei casi.
Nel caso dellʼamiloidosi, nel 70% si può fare diagnosi con la biopsia del grasso
periombelicale.
I depositi di amiloide sono distribuiti lungo i vasi sanguigni e nelle regioni
mesangiali del rene.
61
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
RENE POLICISTICO
Rappresenta la malattia ereditaria a-rischio-vita più diffusa nel mondo, oltre che
una causa tra le più frequenti di insufficienza renale.
La forma autosomica dominante* circa il 90% dei casi) è vista prevalentemente
negli adulti, mentre quella recessiva ** più spesso nei bambini.
Il rene policistico, nella forma dominante, è una malattia sistemica, che origina da
mutazioni di 2 geni, denominati PKD-1 (cromosoma 16) e PKD-2 (cromosoma 4).
Lʼeterogeneità fenotipica *** è una caratteristica del Rene Policistico dellʼadulto.
Lʼincidenza è di 1 su 400-1000.
Gli individui colpiti sono spesso asintomatici sino alla 4°-5° decade.
I sintomi di presentazione sono solitamente rappresentati da:
•
•
•
•
•
•
Dolori lombari.
Ematuria.
Infezioni delle vie urinarie.
Comparsa di ipertensione.
Masse addominali.
Aumento della creatininemia.
_________________________________________
* Ereditarietà autosomica dominante: il carattere appare in tutte le generazioni, ogni
individuo colpito ha di norma un genitore affetto. Sono affetti sia maschi che femmine e
trasmettono il carattere con eguale probabilità ai figli di entrambi i sessi. Ogni filio di un
genitore affetto ha il rischio del 50% di essere affetto. Membri non affetti della famiglia
non trasmettono il carattere ai figli.
** Ereditarietà recessiva: il carattere si manifesta nel figlio solo nel caso riceva dai
entrambi i genitori lo stesso fattore.
*** Eterogeneità fenotipica: definisce il fenomeno per cui mutazioni in loci genetici
diversi possono avere lo stesso effetto fenotipico (= lʼinsieme di tutto ciò che appare, cioè
di tutte le caratteristiche osservabili di un organismo vivente).
62
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
Lʼevoluzione è solitamente lentamente progressiva nellʼarco dei 10-20 anni che
seguono la diagnosi. Lʼinsufficienza renale si manifesta nel 60% dei casi, attorno
allʼetà di 70 anni: aumenterebbero il rischio di danno renale lʼetà alla diagnosi (quanto più
giovane), la razza (rischi maggiori per i neri), il sesso (maschi) e lʼipertensione. Esiste
inoltre una correlazione stretta tra le dimensioni renali misurate con la Risonanza
Magnetica e la velocità di deterioramento della funzionalità renale.
La diagnosi è molto spesso precoce, dal momento che lo screening viene richiesto
da chi sa di avere un genitore affetto. Si fonda su:
• Ecografia: documenta la presenza di cisti, numerose e di varia dimensione, nei reni ma
anche -talvolta- nel fegato.
• TAC: è certamente più sensibile nello screening della fase pre-sintomatica nei pazienti
più giovani.
• Risonanza Magnetica: sicuramente la metodica più sensibile. Viene utilizzata anche
per una corretta misurazione delle dimensioni del rene.
63
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
• Test genetico: lo studio della mutazione dei geni è, per ora, la prova più accurata,
quando le cisti non possono essere riscontrate -perché non abbastanza grandimediante lʼesplorazione con ecografia o TAC. Eʼ molto costoso.
Cosa sono le “cisti” che caratterizzano questa malattia?
Una cisti nel rene comincia con un rigonfiamento di un nefrone (non
necessariamente di tutti), in un punto qualsiasi.
Circa il 70% delle cisti si stacca dal nefrone quando sono ancora minuscole (circa 2 cm. di
diametro).
Nel tempo, le cisti si allargano, si riempiono di liquido (limpido o contenente sangue o
globuli bianchi).
La ricerca ha dimostrato che concorrono almeno tre elementi alla formazione delle cisti:
1. Proliferazione delle cellule: le cellule della parete della cisti si riproducono con velocità
superiore alle cellule normali del rene. Ciò fa sì che le cisti crescano in ampiezza.
2. Secrezione cellulare: la secrezione è un modo per formare il liquido. Nella formazione
della cisti, sono le stesse cellule di parete a possedere questa capacità.
3. Anormale membrana basale: è il sottilissimo strato di tessuto su cui poggiano le cellule
della cisti. Nel Rene <policistico dellʼadulto, tale strato è più spesso del normale ed ha
una struttura anomala.
In generale, le cisti provocano problemi per le loro dimensioni e lo spazio che
occupano.
64
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
La terapia: nessun trattamento si è rivelato efficace nel prevenire la crescita delle
cisti o lʼinsufficienza renale.
Raccomandato il trattamento dellʼipertensione, con preferenza -tra i farmaci- degli
ACE-inibitori (se ne sta studiando lʼazione diretta proprio su crescita dimensionale
del rene e sulla riduzione del filtrato glomerulare).
In caso di infezioni delle cisti -renali od epatiche- la scelta di elezione è sul Bactrim
o sui fluorochinolonici (entrambi liposolubili e quindi dotati di una elevata
penetrazione nelle cisti).
Il dolore può richiedere il drenaggio percutaneo, laparoscopico o chirurgico della
cisti.
In caso di conclamato danno renale, la dialisi ha risultati, in genere, superiori a
quelli di altri malati dializzati per altre cause.
Quelli che vanno incontro a trapianto, soprattutto se le cisti sono voluminose od
infette, possono richiedere, prima, la nefrectomia (asportazione chirurgica dei reni)
bilaterale. La sopravvivenza dopo il trapianto, in questi pazienti -pur essendo
paragonabile a quella dei trapiantati per altra causa- rimane a rischio per le complicanze
extrarenali della malattia, che possono interessare fegato, cuore, intestino ed altri organi:
•
•
•
•
Cisti epatiche (60-70% dei casi).
Prolasso della valvola mitralica (26%).
Aneurismi dei vasi intracranici (5- 10%).
Ernie, sia inguinali che ombelicali.
Nuovi farmaci allo studio: sono numerosi. Ne citiamo alcuni:
• Somatostatina: sarebbe in grado di interferire con i meccanismi di formazione del liquido
allʼinterno delle cisti, rallentandone la formazione.
• Sirolimus: è un immuno-soppressore utilizzato nella terapia anti-rigetto nei trapianti.
Sembrerebbe in grado di ridurre la crescita delle cellule che formano la cisti renale,
riducendone quindi la formazione.
• Tolvaptan: è un diuretico, accreditato della capacità di ridurre la formazione del liquido
allʼinterno delle cisti.
65
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
Il rene policistico nella forma autosomico recessiva è primariamente
patologia dellʼinfanzia.
Lʼincidenza è di 1 caso ogni 20.000 nati.
In tutte le famiglie in cui si riscontra, la patologia è dovuta a mutazioni in un gene
chiamato PKHD1, che si trova sul cromosoma 6, che condizionano la formazione di
dilatazioni (cisti) del tubulo collettore.
66
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
Eʼ quindi evidente che le due patologie (Autosomal Dominant Pollycistic Kidney
Disease > ADPKD e Autosomal Recessive Polycistic Kidney Disease > ARPKD)
hanno basi genetiche diverse ed anche decorsi clinici e morfologici diversi e ben
distinguibili.
La presentazione clinica della forma recessiva è molto variabile. Sono tuttavia
disponibili alcuni dati:
• Fino al 50% dei neonati affetti muore di ipoplasia polmonare*, conseguenza di
oligoidramnios** da severa malattia renale intrauterina.
• Quasi lʼ80% di quelli che sopravvivono è ancora in vita allʼetà di 10 anni, ma -in 1/3 dei
casi- con una severa insufficienza renale.
• I reni appaiono aumentati di volume già alla nascita.
• Eʼ compromessa la capacità di concentrare le urine, a testimonianza della compromessa
funzionalità dei tubuli renali.
• Lʼipertensione si manifesta nei primi anni di vita.
La diagnosi è principalmente ecografica (rivela reni ipoecogeni ingranditi) e può
essere fatta in utero dopo 24 settimane di gestazione. N.B.: le cisti si rendono visibili
solo dopo la nascita.
Non esiste una terapia specifica. Una terapia intensiva neonatale, il trattamento
dellʼipertensione, la dialisi ed il trapianto renale possono consentire la
sopravvivenza sino allʼetà adulta. Una possibile complicanza -la fibrosi epatica***- può
rendere necessario anche un trapianto di fegato.
_____________________________________
* Ipoplasia polmonare: è una patologia polmonare congenita caratterizzata da assenza
completa o ridotto sviluppo di uno o più lobi polmonari.
** Oligoidramnios: condizione patologica della gravidanza, caratterizzata dalla
diminuzione del liquido amniotico al di sotto di 500 ml. La carenza di liquido può essere
associata ad anomalie dellʼapparato urinario fetale, poiché le urine rappresentano uno dei
costituenti principali del liquido amniotico.
67
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
*** Fibrosi epatica: significa accumulo di tessuto ʻcicatrizialeʼ nel fegato. Si può
osservare in quasi tutte le condizioni di danno cronico del fegato. Nel fegato normale, la
matrice è una sorta di delicata impalcatura, che si trova tra le varie cellule, che sostiene e
separa dai vasi sanguigni, permettendo in maniera ottimale gli scambi di informazioni e
metabolici. In corso di fibrosi, la matrice del fegato cambia le sue caratteristiche, sia in
senso qualitativo che quantitativo, a scapito delle altre cellule ʻnobiliʼ.
68
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
Malattie tubulo-interstiziali del rene
Lʼinfiammazione o la fibrosi dellʼinterstizio* renale e lʼatrofia del comparto tubulare
sono conseguenza comune delle malattie del glomerulo o dei vasi renali.
Distinto da questi fenomeni secondari è un gruppo di malattie che primariamente
interessano tubuli ed interstizio, con relativo risparmio di glomeruli e vasi.
Tali malattie vengono suddivise in acute e croniche, classificate come:
1. Nefriti Interstiziali Acute
2. Nefriti tubulo-interstiziali croniche
_______________________________________
* Interstizio renale: è il tessuto connettivo lasso che occupa gli spazi compresi tra i
corpuscoli renali, i tubuli ed i vasi sanguigni. Scarso nella corticale, aumenta
progressivamente in quantità procedendo nella midollare.
1. Nefriti Interstiziali Acute
Nella maggior parte dei casi si presentano con una insufficienza renale acuta.
Lʼacuzie in questo gruppo di malattie può essere determinata da infiltrati
infiammatori particolarmente aggressivi, che portano ad edema interstiziale, danno
delle cellule dei tubuli e compromissione del flusso tubulare, per franca ostruzione
dei tubuli ad opera di calcoli, detriti cellulari o cristalli.
Il dolore al fianco, se presente, è dovuto alla distensione della capsula renale.
Esistono quattro cause fondamentali:
1. Farmaci: antibiotici (sulfonamidi, chinolonici, penicilline, vancomicina, eritromicina,
rifampicina) ed antivirali (acyclovir), FANS, diuretici, antiepilettici, inibitori di pompa ecc.
2. Infezioni: sia virali che batteriche.
3. Malattie autoimmuni: lupus, Sjogren, nefrite interstiziale con uveite ecc.
4. Malattie ostruttive acute: mieloma, nefropatia acuta da fosfati o da urati.
69
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
Attualmente, la nefrite interstiziale acuta è sempre più spesso correlata ad una
reazione allergica a farmaci.
Nefrite interstiziale allergica
La percentuale di positività alla biopsia di nefriti interstiziali allergiche non supera il 15%
dei casi di insufficienza renale acuta non altrimenti spiegata.
Eʼ questo un dato probabilmente sottostimato: farmaci potenzialmente nefrotossici, infatti,
vengono continuamente identificati ed empiricamente sospesi in pazienti con
creatininemia aumentata (con beneficio per il paziente, ma senza il conforto di una
diagnosi bioptica).
Quadro clinico: la presentazione classica di questa nefrite - febbre, eruzione
cutanea, eosinofilia*, danno renale con oliguria dopo 7-10 giorni di trattamento con
meticillina od altri antibiotici betalattamici**- è ormai eccezione più che regola.
Più spesso. i pazienti scoprono casualmente valori elevati di creatininemia o hanno
sintomi correlabili con una insufficienza renale acuta. Citiamo solo alcuni casi
atipici:
• Nei casi da FANS, febbre, eruzione cutanea ed eosinofilia sono rari, mentre è comune
un danno renale acuto con cospicua proteinuria.
• La reintroduzione in terapia di rifampicina, dopo un periodo senza trattamento, può
indurre una insufficienza renale particolarmente severa e rapida.
• Farmaci quali gli inibitori di pompa e gli antiretrovirali determinano quadri più insidiosi,
che portano ad un danno tubulo-interstiziale progressivo.
70
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
_____________________________________
* Eosinofilia: i granulociti eosinofili sono cellule (globuli bianchi) del sistema immunitario,
così chiamate perchè, al loro interno, presentano delle granulazioni che si colorano con un
colorante particolare chiamato eosina, che li fa apparire di un colore rosato. Vengono
prodotti dal midollo osseo e sono importanti nella risposta immunitaria, soprattutto nei
confronti dei parassiti e nelle reazioni allergiche.
** Antibiotici betalattamici: sono una classe di antibiotici che impediscono la sintesi
della parete cellulare dei batteri. Derivano il nome di betalattamici dalla loro struttura
chimica (il betalattame. anello a 4 atomi che forma unʼammide ciclica). Rientrano in questa
categoria le penicilline, le cefalosporine ed altri antibiotici (aztreonam, meropenem).
La terapia di queste nefriti si basa principalmente sulla sospensione del farmaco
nefrotossico.
Il danno renale, peraltro, può non essere del tutto reversibile, in rapporto al tempo di
esposizione ed al grado di atrofia tubulare e fibrosi interstiziale che si sono creati.
La terapia steroidea può accelerare la guarigione del danno renale, senza peraltro
modificarne la sopravvivenza.
71
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
Nefrite acuta associata ad infezioni
Solo un breve riferimento, per tenere distinta questa forma dalla pielonefrite
batterica (che generalmente non causa una insufficienza renale acuta, fatti salvi i
casi in cui colpisce entrambi i reni o causa uno shock settico)
Attualmente, questa forma di nefrite acuta la si vede spesso in pazienti
immunocompromessi ed, in particolare, in alcune categorie di trapiantati renali.
Nefrite interstiziale acuta nelle collagenopatie
Prenderemo in esame, a titolo esemplificativo, 3 di queste:
* Sindrome di Sjogren
Eʼ una malattia autoimmune sistemica, che colpisce le ghiandole esocrine -specie le
lacrimali e le salivari- con la tipica sintomatologia di secchezza di occhi e bocca (“sindrome
secca”).
Può accompagnarsi ad una infiltrazione linfocitaria di differenti organi e tessuti, tra cui
polmoni e reni.
A livello renale, la nefrite interstiziale è la manifestazione più comune, che può esitare in
una modesta insufficienza renale.
72
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
** Nefrite tubulo-interstiziale con uveite
Eʼ malattia autoimmune, di cui non si conosce la causa. Responsabile del 5% dei casi di
nefrite acuta interstiziale, colpisce più le donne (3:1), con unʼetà media di insorgenza
attorno ai 15 anni.
La sintomatologia è tipicamente caratterizzata da febbre, da una uveite* dolorosa,
spesso bilaterale e da un coinvolgimento renale di tipo interstiziale (quasi sempre
responsabile della diagnosi). Vi sono poi perdita di appetito e di peso corporeo, dolori
addominali ed articolari.
La diagnosi è spesso di esclusione, fondata sullʼassociazione dellʼuveite con un
incremento di creatinina e VES, presenza di globuli bianchi nelle urine (con urinocoltura
sterile), modesta proteinuria con negative le sierologie più comuni per patologie
autoimmuni.
La terapia si basa su cortisonici orali. Il ricorso ad immunosoppressori può essere
giustificato dalla prevenzione delle recidive.
___________________________________
* Uveite: è unʼinfiammazione dellʼuvea. Lʼuvea è la tonaca vascolare dellʼocchio. Eʼ divisa
in 3 parti: iride (anteriore, posta davanti al cristallino,con la forma di un anello piatto che
circonda la pupilla), corpo ciliare (intermedio) e coroide (posteriore). Ha principalmente
una funzione vascolare e di nutrimento del bulbo.
Iride
Corpo
(g)
ciliare (f)
Coroide (d)
73
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
***Nefrite interstiziale nel Lupus
Una reazione infiammatoria a livello dellʼinterstizio renale spesso accompagna le
lesioni del glomerulo negli stadi più avanzati di nefrite lupica (vedi pag. 48-51).
Possono essere presenti anche depositi di immunocomplessi a livello tubulare nel
50% dei casi.
Occasionalmente, i sintomi da nefrite tubulo-interstiziale possono essere prevalenti
su quelli glomerulari.
Tubulopatie ostruttive
Una insufficienza renale acuta può manifestarsi quando cristalli di vario tipo si
depositano nelle cellule dei tubuli o nellʼinterstizio, ostruendo i tubuli stessi.
Lʼinsufficienza renale che si determina è oligurica (accompagnata, cioè da una
contrazione del volume delle urine) ed è spesso accompagnata da dolore al fianco
(causato dallʼostruzione tubulare).
Ne sono spesso causa i farmaci (sulfadiazina -nella cura della toxoplasmosi-, indinavir HIV- ed anche acyclovir -se somministrato endovena per casi gravi di herpes). Cristalli di
tali farmaci sono ritrovati nelle urine.
Unʼaltra causa è rappresentata dallʼostruzione acuta dei tubuli (ma anche dei dotti
collettori, della pelvi ed anche degli ureteri) da parte di cristalli di acido urico. Ciò più
di frequente si manifesta come risultato dellʼiperuricemia massiva che consegue a terapie
antitumorali dei linfomi i dei mielomi.
74
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
2. Nefriti tubulo-interstiziali croniche
Il miglioramento delle condizioni lavorative e di salute pubblica, insieme alla messa
al bando degli analgesici contenenti fenacetina (Optalidon!!) ha portato ad una
drammatica caduta nellʼincidenza della nefrite interstiziale cronica da esposizione a
metalli pesanti (piombo e cadmio su tutti) e da analgesici. Oggi, la nefrite
interstiziale cronica è più spesso conseguenza di una ischemia renale oppure
secondaria ad una glomerulonefrite.
Nella casistica, hanno importanza anche alcune anomalie di sviluppo o malattie
ereditarie, come il reflusso vescico-uretrale e conseguente nefropatia da reflusso o
come la nefropatia falciforme.
In tutti questi casi, nulla si può fare sul danno renale instaurato, ma lʼulteriore
deterioramento della funzionalità renale può essere prevenuto o almeno rallentato,
trattando lʼipertensione a livello glomerulare, che è quasi sempre presente in
queste situazioni.
Eʼ evidente, quindi, lʼimportanza di scoprire precocemente i pazienti a rischio, per
proteggerli da una insufficienza renale grave.
Nefropatia da reflusso
La nefropatia da reflusso è una conseguenza di un reflusso vescico-ureterale presente
nella prima infanzia.
Denominata in passato ʻpielonefrite cronicaʼ in quanto considerata conseguenza di
infezioni ricorrenti delle vie urinarie nellʼinfanzia, è stato dimostrato invece che il flusso
retrogrado dellʼurina dalla vescica in uno o entrambi gli ureteri e reni dipende da valvole
uretero-vescicali mal posizionate o incompetenti.
Un reflusso ad alta pressione di urina sterile compromette lo sviluppo normale dei reni.
Se si associano infezioni delle vie urinarie, soprattutto nella prima infanzia, il risultato è un
processo infiammatorio che tende a cronicizzare con successiva formazione di cicatrici nel
tessuto interstiziale e di atrofia tubulare.
La perdita di nefroni porta allʼipertrofia dei glomeruli rimanenti ed eventuale loro
secondaria insufficienza.
Questa nefropatia spesso non dà sintomi specifici (viene diagnosticata, spesso, a fronte
dellʼalterazione di esami eseguiti routinariamente -proteinuria, sedimento urinario poveroo in occasione di una gravidanza).
Se il rene interessato è solo uno, lʼipertensione può essere lʼunico sintomo. Quando sono
invece interessati entrambi i reni, la malattia procede inesorabilmente verso anni di grave
insufficienza renale.
75
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
La diagnosi, nellʼadulto, è possibile anche solo con una ecografia, che caratteristicamente
mostra reni piccoli, con limiti irregolari, corticali assottigliate e regioni di ipertrofia
compensatoria.
Terapia: mantenere la sterilità delle urine nellʼinfanzia limita la cicatrizzazione
dellʼinterstizio. Il re-impianto chirurgico degli ureteri in vescica è efficace solo se molto
precoce, eseguito cioè prima che si sia instaurato un qualche danno renale.
76
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
Nefropatia da drepanocitosi*
In questa malattia, lʼevidenza di una compromessa funzionalità dei tubuli può
rendersi evidente nellʼinfanzia o nella prima adolescenza come poliuria da diminuita
capacità di concentrazione o da acidosi tubulare renale anche di molti anni
pregressa.
La presenza di microalbuminuria in un bambino affetto da drepanocitosi deve costituire
motivo di allarme ed indicazione alla consultazione di un nefrologo e/o allʼavvio di una
terapia con basse dosi di ACE-inibitori.
Una ischemia determinata dallʼaccumulo dei globuli rossi alterati nei vasi della midollare
renale può causare la necrosi della papilla, che si manifesta con una ematuria
macroscopica e con unʼostruzione ureterale.
______________________________
* Drepanocitosi: La drepanocitosi o anemia falciforme è una malattia genetica del
sangue, caratterizzata da anemia cronica e da episodi dolorosi più o meno frequenti in
varie parti del corpo, causati dallʼocclusione dei vasi sanguigni. I globuli rossi prendono
forma ʻa falceʼ, invece della forma normale a disco. Ciò succede perchè, nella
drepanocitosi, le alterazioni avvengono nel gene che dirige la produzione
dellʼemoglobina; danno origine ad una forma anomala di emoglobina (chiamata
emoglobina S), le cui molecole tendono facilmente ad aggregarsi fra loro, formando dei
microscopici filamenti allʼinterno del globulo rosso.
Questi globuli rossi sono incapaci di scorrere normalmente allʼinterno dei capillari (dove i
globuli rossi normali passano grazie alla loro elasticità) e quindi tendono a bloccarsi,
ostruendo il vaso.
77
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
78
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
Tra le nefropatie tubulo-interstiziali, citiamo aneddoticamente altre forme:
• Da analgesici: derivanti dallʼuso protratto di preparati contenenti fenacetina
(vietata negli USA dal 1983 ed abbandonata dallʼuso in Italia), aspirina e caffeina.
La concentrazione del farmaco a livelli tossici nella parte midollare del rene determina
necrosi papillare e successiva insufficienza renale.
• Da erbe cinesi: descritta per la prima volta in giovani donne cinesi, che
assumevano -a scopo dimagrante- preparati di erboristeria, che contenevano
lʼacido aristolochico. Tale sostanza, presente in diversi rimedi della medicina
tradizionale cinese, oltre che nefrotossica, aumenta significativamente il rischio di cancro
alla vescica.
Il fiore dellʼAristolochia, da cui si deriva lʼacido .
• Balcanica: nelle città balcaniche situate attorno agli affluenti del Danubio è
endemica una nefropatia tubulo-interstiziale cronica che, recentemente, è stata
correlata, oltre che con altre sostanze tossiche, con lʼacido aristolochico frutto di
una contaminazione della preparazione del grano.
• Da sali di Litio: lʼuso dei sali di litio per il trattamento delle psicosi maniacodepressive può causare diversi danni renali, il più comune dei quali è il diabete
insipido nefrogeno (poliuria e polidipsia). Meno frequente la nefrite
tubulointersiziale cronica, comunque appannaggio di chi ha fatto un uso prolungato
(oltre i 10-20 anni) di litio e con esperienza ripetuta di livelli tossici.
79
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
Malattie vascolari del rene
La vascolarizzazione del rene è insolitamente complessa, con un flusso
arteriolare alla corticale certamente superiore alle esigenze metaboliche, ma
coerente con la funzione primaria di organo di filtrazione.
Una volta assicurato il sangue ai glomeruli nella corticale, i vasi (postglomerulari) portano sangue ai segmenti più profondi della midollare, da cui
dipende il trasporto dei soluti a vari livelli del tubulo. Questi vasi postglomerulari trasportano meno sangue, mantenendo le regioni profonde -ad elevata
richiesta di ossigeno- al limite dellʼipossia.
Le patologie vascolari che possono costituire una minaccia alla
vascolarizzazione del rene includono:
• Aterosclerosi dei grossi vasi.
• Malattie fibromuscolari.
• Malattie emboliche.
• Malattie infiammatorie.
• Malattie ematologiche.
80
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
Stenosi dellʼarteria renale
Le cause che determinano unʼocclusione dei grossi vasi arteriosi possono
essere:
• Una compressione estrinseca del vaso.
• Una displasia fibromuscolare: rara malattia vascolare sistemica, ad eziologia (=causa)
sconosciuta, caratterizzata da alterazioni delle cellule muscolari lisce e del tessuto
fibroelastico della parete di arterie di medio e piccolo calibro. Le alterazioni, bene
evidenziabili allʼangiografia, consistono in restringimenti trasversali alternati a dilatazioni
focali “a corona di rosario”. La malattia colpisce prevalentemente donne tra i 15 ed i 50
anni. Eʼ di riscontro nel 3-5% dei donatori di rene.
• La malattia aterosclerotica: è lʼevenienza più comune.
Qualsiasi alterazione in grado di ridurre la pressione di perfusione a livello
renale può attivare meccanismi il cui scopo sia quello di ristabilire detta
pressione, a costo di sviluppare una ipertensione sistemica.
Dato che il ristabilire normali pressioni di perfusione renale può rendere
reversibile questo meccanismo, la stenosi dellʼarteria renale viene
correntemente considerato una causa secondaria di ipertensione
specificamente trattabile.
La stenosi dellʼarteria renale è abbastanza comune (come arteriosclerotica 6.8%
al di sopra dei 65 anni, con tendenza alla progressione -anche fino allʼocclusione totalenei 5 anni successivi), con spesso solo modeste implicazioni emodinamiche.
81
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
Quando i livelli di stenosi (= restringimento) dellʼarteria renale si fanno critici,
determinano una ridotta pressione di perfusione, che:
• Attiva il sistema renina-angiotensina*
• Riduce lʼescrezione di sodio
• Attiva vie simpatiche adrenergiche**
Lʼinsieme di questi eventi porta allo stabilirsi di una ipertensione, caratterizzata da:
• Dipendenza iniziale dallʼangiotensina.
• Valori pressori con grande variabilità.
• Rapido danno degli organi-bersaglio: ipertrofia del ventricolo sinistro del cuore, fibrosi
renale.
_______________________________________
* Sistema renina-angiotensina: la renina è un enzima prodotto ed immagazzinato a
livello delle cellule iuxtaglomerulari del rene (= lʼinsieme di alcune strutture microscopiche
situate al polo vascolare del glomerulo. Sono cellule che formano una specie di manicotto
attorno allʼarteriola afferente, a contatto anche con una parte del tubulo distale -vedi immagine
sottostante).
82
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
La renina viene rilasciata ogniqualvolta si verifichi una diminuzione della pressione di
perfusione renale, a livello dellʼapparato iuxtaglomerulare.
Lʼangiotensina è una proteina che stimola la vasocostrizione (aumentando la pressione).
In caso di bassa pressione, stimola il surrene a produrre aldosterone, che aumenta la
ritenzione idrica e quindi la pressione. Oltre alle funzioni citate, è anche un potente
ormone, sintetizzato dal fegato in forma di angiotensinogeno.
La renina coverte lʼangiotensinogeno in angiotensina I, che a sua volta viene convertito in
Angiotensina II, ad opera dellʼenzima di conversione ACE (Angiotensin-Converting
Enzyme), presente principalmente a livello dei capillari polmonari.
LʼAngiotensina II è un potente vasocostrittore: la costrizione delle arteriole afferenti al
glomerulo, ma anche quelle efferenti. Se così non fosse, si avrebbe una diminuzione del
flusso sanguigno a livello del glomerulo, che viene invece bilanciata dalla costrizione delle
arteriole efferenti.
Sempre lʼAngiotensina II, a livello del surrene, causa il rilascio di aldosterone.
LʼAldosterone è un ormone che agisce a livello del sistema nervoso centrale,
aumentando il senso della sede e di appetito per il salato.
A livello dei tubuli renali, favorisce il riassorbimento del sodio dallʼurina.
A livello dellʼipotalamo, favorisce il rilascio dellʼormone antidiuretico (o Vasopressina) che,
a livello del tubulo collettore del rene, favorisce il riassorbimento dellʼacqua.
Tutti questi effetti hanno lo scopo di aumentare la quantità di liquido nel sangue e,
conseguentemente, la sua pressione.
83
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
• Vie simpatiche adrenergiche: il sistema nervoso vegetativo è costituito, nella sua
complessità, di 2 componenti, quella del simpatico e quella del parasimpatico.
Il simpatico utilizza come neurotrasmettitori lʼadrenalina e la noradrenalina (da cui il nome
di ʻadrenergicoʼ).
Tra le sue molte funzioni, il simpatico stimola lʼapparato iuxtaglomerulare del rene a
produrre renina.
Inoltre: aumenta la pressione arteriosa, contrae i vasi sanguigni cutanei e viscerali (fatta
eccezione per cuore e polmoni) ecc.
84
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
La diagnosi di stenosi dellʼarteria renale può effettuarsi con diverse metodiche:
1. Doppler: poco costoso, è fortemente dipendente dallʼesperienza e dalla competenza
dellʼoperatore.
2. Angiografia in Risonanza Magnetica: molto costoso, fornisce immagini ottime, ma il
gadolinio (mezzo di contrasto paramagnetico) non può essere usato in caso di
compromessa funzione renale. La presenza eventuale di stent genera artefatti.
3. Angio TAC: di costo relativamente minore, fornisce ottime immagini, senza artefatti da
stent, ma il mezzo di contrasto è potenzialmente nefrotossico.
4. Arteriografia: considerata gold standard per la diagnosi, viene eseguita solitamente con un
programma di interventistica. Comporta rischi sia per tossicità del mezzo di contrasto che per
complicanze legate alla procedura (embolie, dissezione della parete vasale)
Immagine AngioTAC: stenosi arteria renale destra
85
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
La terapia della documentata stenosi dellʼarteria renale può essere medica (basata
essenzialmente sullʼuso di farmaci ACE-inibitori) o chirurgica (angioplastica).
Angioplastica percutanea: consiste nellʼintroduzione di un catetere nel vaso stenotico,
che viene gonfiato in corrispondenza del restringimento, in modo da ripristinare il normale
d i a m e t r o d e l v a s o e permettere un incremento del flusso sanguigno.
Posizionamento di stent: pur essendo questa metodica efficace nel ristabilire il flusso
renale, il recupero della funzionalità renale è circoscritto al 25% dei casi, mentre rimane
invariata nel 50% e peggiora nei restanti.
86
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
Trombosi della vena renale
La trombosi delle vene renali può manifestarsi:
I.
Dolore, spontaneo od evocato, al fianco, ematuria, proteinuria e rapida
compromissione della funzionalità renale.
II. In maniera del tutto silente (qualche volta scoperta facendo indagini dopo
unʼembolia polmonare).
La vena renale sinistra è quella più comunemente interessata, anche se nei
2/3 dei casi la trombosi è bilaterale.
Le cause di questa patologia sono riconducibili a 3 capitoli:
1. Danno endoteliale: può essere provocato da omocistinuria*, interventi chirurgici (sia
endovasali che addominali).
2. Stasi venosa: per disidratazione (specie nei maschi e nella popolazione pediatrica),
per compressione da patologie retroperitoneali (come la fibrosi o come tumori
addominali).
3. Stati di ipercoagulabilità: nella sindrome da anticorpi antifosfolipidi**, nella sindrome
nefrosica o nella carenza di proteina C ed S, di antitrombina o di fattore V di Leyden***;
in presenza di disseminazione neoplastica o di uso di contraccettivi orali.
87
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
___________________________________
* Omocistinuria: malattia rara, ereditaria (recessiva), che colpisce il metabolismo della
metionina, per carenza di un enzima- vitamina B6 dipendente. Ciò comporta lʼaccumulo
di omocisteina, responsabile di molti sintomi, con netta maggior frequenza di fenomeni
trombotici, sia arteriosi che venosi.
• Anticorpi antifosfolipidi: sono un gruppo di autoanticorpi diretti verso una
combinazione di fosfolipidi e proteine plasmatiche. Comprendono gli anticardiolipina
(aCL), gli antibeta2glicoproteina1 (antibeta2GPI) ed il lupus anticoagulant (LAC). Questi
anticorpi, con meccanismi non del tutto chiariti, favoriscono uno spostamento
dellʼequilibrio coagulativo in senso pro-trombotico. La Sindrome da anticorpi
antifosfolipidi è una condizione clinica associata alla predisposizione a trombosi
arteriose e venose (ed a aborti spontanei), caratterizzata da trombocitemia (= carenza di
piastrine) ed alla presenza in circolo dei suddetti anticorpi.
• Proteina C ed S, antitrombina III ecc.: sono proteine che funzionano da inibitori
fisiologici della coagulazione, impedendo lʼeccessiva estensione nella formazione di un
trombo. Per questo, una carenza di uno di questi ʻanticoagulanti naturaliʼ facilita
lʼinsorgenza delle trombosi.
Facilità alla trombosi per ridotta Proteina C attivata
88
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
La diagnosi si fonda su 3 tipi di indagine:
1. Ecodoppler
2. TAC-angiografia: è la metodica più precisa, vicina al 100%.
3. RNM-angiografia: altra metodica ad elevata precisione, ma decisamente più costosa
ed in più richiede sedazione nei pazienti in età pediatrica.
La terapia della trombosi venosa renale è quella anticoagulante, unita -ove
possibile- al trattamento della causa.
Nei casi più gravi, può essere presa in considerazione la trombolisi endovascolare*,
via via fino alla nefrectomia, in prevenzione delle complicanze più rischiose.
__________________________________
* Trombolisi endovascolare: metodica che consiste nellʼiniezione di un bolo di farmaci
anticoagulanti intra-trombosi. Presuppone il raggiungimento, con una sonda angiografica,
del luogo dellʼostruzione vasale. Vantaggiosa perché può rappresentare, oltre che un
mezzo terapeutico, un utile mezzo diagnostico (smascherando la presenza di lesioni
stenosanti che possono essere allʼorigine dellʼevento acuto). Il rischio maggiore è
rappresentato dalle emorragie, specie nei pazienti più anziani.
89
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
CALCOLOSI RENALE
(Nefrolitiasi)
I calcoli renali rappresentano uno dei problemi urologici più frequenti.
Negli USA, circa il 13% degli uomini ed il 7% delle donne ne soffre almeno
una volta nella vita e, nel mondo industrializzato, le percentuali sono in
aumento.
Il calcolo è una massa solida formata dalla aggregazione di cristalli che
possono essere presenti nelle urine. I cristalli, aggregandosi, crescono di
dimensioni formando i calcoli, la cui grandezza può essere molto variabile, da
un granello di sabbia ad una pallina da golf.
I calcoli sono costituiti da ossalato o fosfato di calcio nel 75-85% dei casi, da
fosfato di ammonio e magnesio (struvite) -di solito correlati ad infezioni delle
vie urinarie- da acido urico (10-15%) o da cistina (1%).
90
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
Sintomi: dal momento che i calcoli si sviluppano sulla superficie della papilla
renale o allʼinterno dei dotti collettori, non necessariamente generano sintomi.
La presenza di calcoli asintomatici è spesso di riscontro collaterale in corso di
indagini radiologiche addominali svolte per altri motivi.
I calcoli sono una causa comune di isolata ematuria.
I calcoli divengono sintomatici quando entrano nellʼuretere o quando occludono la
giunzione uretero-pelvica, causando dolore ed ostruzione al deflusso urinario.
In teoria, un calcolo può attraversare lʼuretere senza causare sintomi, ma la regola è che
tale transito genera dolore e sanguinamento.
Il dolore inizia gradualmente, di solito in corrispondenza del fianco, aumentando
progressivamente di intensità nei 20-60 minuti successivi, quando raggiunge unʼintensità
tale da richiedere il ricorso a narcotici per renderlo tollerabile.
Può rimanere localizzato al fianco, oppure diffondere verso il basso, anteriormente,
interessando la regione lombare, il testicolo (o la vulva).
91
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
Un calcolo nella porzione dellʼuretere prossima alla vescica può essere responsabile di
sintomi evocatori di una infezione delle vie urinarie (urgenza minzionale, disuria).
La maggior parte dei calcoli di diametro inferiore a 0.5 cm. transita spontaneamente.
La diagnosi si fa soprattutto con la TAC spirale*, che consente di individuare la
presenza anche di calcoli non radiopachi (come quelli di acido urico), non necessita
di mezzo di contrasto e può servire alla diagnosi di altre patologie fonte di dolore
attribuito ai calcoli renali.
Lʼecografia non ha la medesima sensibilità della TAC.
____________________________________
* TAC spirale: permette lʼacquisizione veloce di immagini piuttosto nitide e poco sensibili
ai movimenti cardiaci e respiratori. Il lettino non si muove più solamente tra una
scansione e lʼaltra, ma si trova in movimento continuo insieme al tubo generatore di
radiazioni ed ai detettori (che le raccolgono) che compiono movimenti continui ad elica
(spirale).
92
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
Cosa porta alla formazione dei calcoli?
I calcoli di solito si formano quando viene meno il delicato equilibrio tra solubilità e
precipitazione dei sali. I reni trattengono acqua, ma espellono sostanze che sono
poco solubili.
Il problema è mitigato dal fatto che le urine contengono sostanze quali pirofosfati,
citrati e glicoproteine, capaci di inibire la cristallizzazione. Quando però le urine
divengono sovrassature di materiali insolubili (o per la loro eccessiva escrezione o per
lʼeccessiva conservazione dʼacqua), i cristalli si formano, si accrescono e si
aggregano a formare il calcolo.
Alla luce di quanto detto sopra, è intuitivo quanto possa essere determinante
lʼaumento dellʼidratazione nel prevenire la formazione di calcoli od il loro
accrescimento.
Altrettanto importanti sono dieta, attività fisica ed abitudini di vita (meglio se
conoscendo la composizione dei calcoli, onde dare indicazioni più precise).
La terapia -medica o chirurgica- dipende da molti elementi:
•
•
•
•
•
•
•
localizzazione del calcolo.
estensione dellʼostruzione.
natura del calcolo.
funzionalità del rene interessato e di quello controlaterale.
presenza o assenza di infezioni delle vie urinarie.
entità del dolore e del sanguinamento.
rischi anestesiologici e chirurgici.
La terapia medica prevede lʼuso di antispastici che, rilassando la muscolatura
della parete dellʼuretere, possono agevolare il transito del calcolo.
93
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
La terapia chirurgica sta abbandonando gli interventi ʻa cielo apertoʼ per questo tipo
di malattie, sostituendoli con una triplice alternativa:
1. Litotrissia extracorporea: lʼesposizione ad onde dʼurto di rene, pelvi renale od uretere
causa la frammentazione del calcolo. Eʼ riservata ai casi in cui il calcolo sia
sufficientemente piccolo (inferiore ai 2 cm) ed una durezza non eccessiva.
2.
Nefrolitotomia percutanea: è una procedura chirurgica che consiste nel fare una
piccola incisione nella pelle, per introdurre uno strumento cavo (Nefrolitotomo) fino al
rene colpito. Eʼ lʼopzione principe per i calcoli di grosse dimensioni, che vengono
distrutti o con ultrasuoni o con raggi laser.
94
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
3. Ureteroscopia: utilizza raggi laser per colpire calcoli od un ʻcestelloʼ per rimuoverli, se
preferenzialmente localizzati nellʼuretere. Viene effettuata utilizzando uno strumento a fibre
ottiche di pochi mm (2-3) di diametro che, passando attraverso lʼuretra e la vescica, viene
introdotto e fatto risalire nellʼuretere. La percentuale di successo è al 90%.
A seconda della composizione del calcolo, si possono identificare situazioni
patologiche particolari (ad esempio: un iperparatiroidismo primario partendo da
calcoli di fosfato o di ossalato di calcio), che richiedono interventi terapeutici mirati
alla patologia di base.
95
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
INFEZIONI DELLE VIE
URINARIE
PIELONEFRITI E PROSTATITI
Oggi le infezioni delle vie urinarie rappresentano una malattia dolorosa
fortunatamente rapidamente responsiva alle moderne terapie antibiotiche. In epoca
pre-antibiotica, il problema era assai più complesso: Ippocrate, scrivendo di quella
che sembra essere stata una cistite acuta, diceva che la malattia poteva protrarsi
anche per 1 anno, prima di risolversi o -nei casi peggiori- portarsi ad interessare i
reni.
Definizioni: le infezioni del tratto urinario (UTI) possono essere asintomatiche
(infezioni subcliniche) o sintomatiche (malattia).
Il termine UTI, quindi, comprende una varietà di entità cliniche, incluse la batteriuria
asintomatica (ABU), le cistiti, le prostatiti e le pielonefriti.
La distinzione tra infezioni -quelle sintomatiche- delle vie urinarie e batteriuria asintomatica
è importante, proprio per i risvolti pratici di una corretta definizione diagnostica. Entrambe
le forme contemplano la presenza di batteri nelle vie urinarie, solitamente assieme alla
presenza di globuli bianchi nelle urine. Ma, mentre la batteriuria asintomatica non si
accompagna a sintomi riconducibili ad una infezione delle vie urinarie (e quindi, nella
maggior parte dei casi, non richiede trattamento antibiotico), le infezioni del tratto urinario
danno sintomatologia tipica (e richiedono trattamento antibiotico).
Epidemiologia: allʼinfuori dellʼetà infantile (i maschi hanno una maggiore incidenza di
anomalie congenite a carico dellʼapparato urinario e quindi una relativa maggior incidenza
di UTI) e della vecchiaia (dopo i 50 anni, lʼostruzione legata allʼipertrofia della prostata
diviene comune nei maschi, pareggiando il rischio di UTI), tra 1 e 50 anni, le infezioni
delle vie urinarie sono decisamente più frequenti nelle donne (la possibilità di
contrarre una cistite acuta è 60 volte più frequente nelle 48 ore che seguono ad un
rapporto sessuale). Trattandosi di una infezione ascendente, è chiaro che la
pielonefrite riconosce i medesimi fattori di rischio della cistite, unitamente a d una
storia materna di UTI, al diabete ed allʼincontinenza urinaria (post menopausa).
Abbastanza tipicamente (in circa il 30% delle donne) ad una infezione delle vie urinarie ne
fa seguito unʼaltra (o più di una): ciò si spiegherebbe con un “sequestro” di batteri nella
parete vescicale, anche se lʼanalisi statistica ha individuato solo nei rapporti sessuali
frequenti e nellʼuso di spermicidi le uniche cause significative (nelle donne in menopausa,
tutto ciò che ostacola un completo svuotamento della vescica).
96
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
La maggior parte dei maschi con UTI presenta unʼanomalia, anatomica o
funzionale, delle vie urinarie (più comunemente una ipertrofia della prostata). Da
sottolineare anche che la mancata circoncisione è associata ad un maggior rischio
di UTI, dal momento che lʼEscherichia Coli colonizza abbastanza caratteristicamente
glande e prepuzio, da cui poi migra verso le vie urinarie.
Cause: i batteri responsabili di UTI sono, nella stragrande maggioranza, batteri
intestinali migrati nellʼapparato urinario (nel 75-90% dei casi, lʼE. Coli).
Nel mondo, sono dimostrati aumenti delle resistenze batteriche ai comuni antibiotici
(superiori al 20% al Bactrim e tra 5-10% alla ciprofloxacina). Dal momento che le
resistenze variano a seconda delle regioni geografiche, è importante tenerne conto prima
di scegliere il farmaco da usare.
Patogenesi: il tratto urinario può essere visto come unʼunità anatomica formata da
una ininterrotta colonna di urina dallʼuretra ai reni.
Nella maggior parte dei casi, i batteri causano unʼinfezione ascendendo
dallʼuretra alla vescica e di qui ad ureteri e reni.
La presenza di batteri può non essere sufficiente allo stabilirsi di una infezione.
Entrano in gioco anche le condizioni di difesa individuali e fattori comportamentali*.
Ad esempio: in condizioni normali, molti dei batteri che entrano in vescica dopo un
rapporto sessuale vengono eliminati dalle difese immunitarie / Qualsiasi corpo estraneo
presente nelle vie urinarie (catetere, calcolo) fornisce una superficie inerte ottimale per la
colonizzazione batterica / Una minzione abnorme e-o lo svuotamento incompleto della
vescica favorisce le infezioni.
97
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
I batteri possono raggiungere le vie urinarie anche attraverso la circolazione
sanguigna: di solito, ciò accade non oltre il 2% dei casi e quasi sempre ad opera di
microrganismi particolarmente virulenti come Salmonella e Stafilococco aureo.
_____________________________________
* Fattori comportamentali: lʼ ecologia vaginale ha grande importanza. La
colonizzazione dellʼostio vaginale e della regione periuretrale da parte della flora
intestinale (E. Coli soprattutto) è il passaggio critico per il realizzarsi di una infezione delle
vie urinarie. I rapporti sessuali aumentano questo rischio di colonizzazione (e le creme
spermicide sono tossiche nei confronti della normale flora batterica vaginale). In
menopausa, i lattobacilli vaginali prima preminenti vengono progressivamente sostituiti da
batteri gram-.
Sintomatologia:
• Batteriuria asintomatica: deve essere considerata questa diagnosi quando il paziente,
in presenza di batteri nel sedimento urinario, non presenta sintomi direttamente
correlabili con una infezione delle vie urinarie. La presenza di segni o sintomi generali
quali febbre, alterate condizioni mentali ed aumento dei globuli bianchi non hanno
rilevanza, se non in seconda istanza.
• Cistite: i sintomi tipici sono rappresentati da disuria (= dolore ad urinare), pollachiuria (=
stimoli frequenti ad urinare), urgenza (= impellenza minzionale). Sono pure presenti
nocturia (= maggior bisogno di urinare durante la notte), esitazione (= presenza di una
certa latenza nel cominciare la minzione), dolenzia sovrapubica e grossolana ematuria.
La presenza di dolore al fianco od alla schiena da un lato è di solito dovuto
allʼinteressamento del tratto superiore delle vie urinarie. La presenza di febbre testimonia
di unʼestensione dellʼinfezione al rene od alla prostata.
• Pielonefrite: dolore al fianco o allʼangolo costo-vertebrale, febbre, nausea, nausea e
vomito -perlopiù ad esordio acuto- sono più o meno violenti, a seconda della gravità
dellʼinfezione. I sintomi della cistite possono non essere presenti. La febbre è certo
lʼelemento più caratteristico, con il suo schema di grossi ʻpicchiʼ che si risolvono dopo 72
ore di terapia. Può essere complicata (specie nei diabetici) da necrosi della papilla
renale o dalla formazione di ascessi nel rene.
• Prostatite: può essere acuta o cronica. La forma acuta si presenta con disuria,
pollachiuria, dolore in corrispondenza della prostata, del perineo o del bacino. Febbre e
brividi sono solitamente presenti, così come sono comuni i sintomi di ostruzione allo
svuotamento vescicale. La forma cronica, batterica, si presenta in maniera più insidiosa,
con cistiti ricorrenti, talora in associazione a dolore pelvico e perineale.
98
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
Diagnosi: in questo settore è opportuno fare chiarezza, anche e soprattutto in
funzione delle scelte terapeutiche (e relativa tempistica).
Una cistite non-complicata in una donna può essere trattata sulla semplice storia
clinica, se i sintomi sono coerenti.
In tutti gli altri casi, è opportuno muoversi partendo da:
• Stick test : solo i batteri della famiglia delle Enterobacteriaceae convertono i nitrati in
nitriti, per cui la presenza di nitriti in quantità sufficiente nelle urine è riprova della
presenza di Escherichia Coli (non dimenticando che, se il soggetto sta bevendo molto ed
urinando spesso, lo stick può avere un risultato falsamente negativo). Attualmente, il test
che più di ogni altro unisce alla rapidità, al basso costo ed alla facile interpretabilità una
ragionevole accuratezza è quello che misura lʼattività dellʼesterasi leucocitaria urinaria.
Il test esplora la presenza di questo enzima allʼinterno dei globuli bianchi: è quindi un test
di piuria (e quindi, indirettamente, della presenza di batteri).
• Esame urine: significativa la presenza di sangue (30% delle cistiti) e di globuli bianchi.
• Urinocoltura: fatta salva la necessità di una corretta raccolta del campione di urine
(rischio di contaminazione), la positività dellʼurinocoltura deve essere validata anche
dalla concentrazione dei batteri presenti. In soggetti asintomatici, deve essere di almeno
100.000 batteri, per scendere a 100/ml (donne con sintomi di cistite) e a 1000/ml (uomini
con sintomi di cistite).
99
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
CARCINOMA RENALE
Rappresenta la maggioranza (90-95%) dei tumori maligni del rene. Più rari i
sarcomi (che originano dai tessuti della capsula o delle strutture che
circondano il rene) ed il nefroblastoma o tumore di Wilms (il più tipico per lʼetà
infantile).
Origina dalle cellule dei tubuli.
Può essere bilaterale (2%).
Rappresenta il 2% di tutti i tumori, ma la sua incidenza è in costante crescita.
Nel sesso maschile si presenta con una frequenza doppia rispetto al femminile.
In Italia sono colpite ogni anno 4000 persone, 2/3 maschi.
La probabilità di sviluppare questo tumore cresce con lʼaumentare dellʼetà ed il
picco massimo di insorgenza è intorno ai 60 anni.
Fattori di rischio: il principale ed il più diffuso è il fumo di sigaretta (il numero di
sigarette fumate ogni giorno ed il numero di anni di esposizione al fumo sono direttamente
proporzionali allʼaumento di rischio di malattia).
Altro fattore di rischio è rappresentato dallʼesposizione cronica ad alcuni metalli e sostanze
particolari, quali asbesto, cadmio (contaminazione di suoli da fertilizzanti, pesci dʼoceano, acqua
potabile contaminata da tubature galvanizzate o in plastica nera, saldature lattine, batterie, cibi raffinati)
fenacetina (farmaci analgesici), torotrasto (usato in passato come mezzo di contrasto radioattivo in
radiologia) .
Esistono anche forme ereditarie, molto rare, trasmesse da un gene identificato
(VHL), che si trova sul braccio corto del Cromosoma 3.
100
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
Sintomi
La triade classica - ematuria, dolore addominale, massa palpabile in addome
o fianco - è presente nel 10-20% dei pazienti.
Altri sintomi possono essere :
•
•
•
•
Febbre
Perdita di peso
Anemizzazione
Varicocele: dilatazione delle vene del testicolo e dello scroto, per compressione o
trombosi della vena spermatica.
Il più delle volte, comunque, il carcinoma renale è di riscontro occasionale, in corso
di indagini (soprattutto TC, RMN ed ecografie) eseguite per altri motivi.
Proprio queste diagnosi precoci frutto di riscontro occasionale hanno contribuito ad
aumentare di 5 anni la sopravvivenza dei pazienti, rendendo anche possibile una chirurgia
più conservativa (nefrectomia parziale).
Anche per i tumori renali, è in uso una stadiazione secondo il sistema TNM, ove:
• T si riferisce alle dimensioni del tumore.
• N si riferisce allo stato dei linfonodi adiacenti, infiltrati o meno da cellule tumorali.
• M si riferisce alla presenza di metastasi.
101
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
Sulla base della stadiazione, si operano le scelte terapeutiche, che contemplano la
Chirurgia, più o meno radicale (eliminazione del rene malato nel caso di cancro limitato
ad un solo rene / nefrectomia parziale nei casi di diagnosi molto precoce o in quelli di
malattia bilaterale).
Le metastasi sono assai poco sensibili alla chemioterapia: risultati e speranze sono riposte
nella immunoterapia (cure che attivino il sistema immunitario del malato contro il cancro).
102
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
URETERE
Eʼ un condotto di forma tubulare, lungo 25-30 cm (lʼuretere destro è più corto
di circa 1,5 cm) e del diametro di 6-8 mm, che collega il bacinetto renale con
la vescica.
Gli ureteri, uno per lato, decorrono verticalmente ai lati della colonna vertebrale e
penetrano nel fondo della vescica ai due angoli esterni del cosiddetto trigono.
Lʼultimo tratto dellʼuretere decorre nello spessore della parete della vescica, per cui,
quando la vescica è piena, rimane chiuso: viene così impedito il reflusso dellʼurina.
La struttura anatomica dellʼuretere è identica a quella dei calici e del bacinetto
renale.
La parete è formata da tessuto muscolare liscio (le fibre muscolari -disposte
longitudinalmente e circolarmente-, contraendosi alternativamente, danno origine ai
movimenti peristaltici, che aiutano la progressione dellʼurina verso la vescica, dove
entra a fiotti).
103
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
Lʼuretere può essere interessato da processi patologici di varia natura, i più
importanti dei quali sono:
• Anomalie malformative congenite: arresto di sviluppo, duplicità*, anomalie di
sbocco**, diverticoli, dilatazioni cistiche, megauretere***).
_______________________________________
* Duplicità: durante lo sviluppo embrionale si possono generare delle malformazioni
ureterali, a causa di una anomalia dellʼabbozzo ureterale dʼorigine (arresto o mancato
sviluppo) o di divisione (in caso di una precoce ramificazione dellʼabbozzo ureterale, si
osserva uno sdoppiamento -parziale o totale- dellʼuretere).
** Anomalie di sbocco: sbocchi anomali di ureteri singoli o doppi si possono aprire
sulla parete vescicale laterale, a livello del collo vescicale, nellʼuretra femminile, a livello
dellʼapparato genitale (prostata e vescicola seminale nel maschio, utero o vagina nella
femmina) o esternamente.
*** Megauretere: abnorme aumento di calibro di uno od entrambi gli ureteri. Può essere
presente alla nascita (malformativo) od essere conseguente al ristagno dʼurina, a seguito
compressioni o comunque ostacoli al flusso.
• Processi infiammatori (ureteriti): in genere si associano ad infiammazioni del
bacinetto renale e della vescica.
• Calcolosi
• Tumori
Questi vari processi possono determinare una stenosi (= restringimento) o una
occlusione dellʼuretere, ostacolando il deflusso dellʼurina, con possibile dilatazione
delle vie urinarie a monte dellʼostacolo (sia dellʼuretere che del bacinetto renale).
104
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
VESCICA
La vescica è un organo cavo, impari e mediano, che è accolto nella piccola
pelvi, dietro e sopra la sinfisi pubica.
Nella femmina, è posta anteriormente allʼutero ed alla vagina e poggia
direttamente sul pavimento muscolare pelvico.
Nel maschio, è situata anteriormente al retto e poggia sulla base della
prostata, che la separa dal diaframma muscolare.
105
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
Riceve lo sbocco degli ureteri e comunica con lʼesterno attraverso lʼuretra.
Lʼuretra decorre attraverso un diaframma uro-genitale, costituito da muscolatura
striata (e quindi sotto controllo volontario), detto anche sfintere esterno.
Esiste poi uno sfintere interno, costituito da muscolatura liscia (e quindi
indipendente dal controllo volontario), in corrispondenza del collo vescicale (la
regione della vescica in cui si trova lʼinizio dellʼuretra).
Prende nome di trigono vescicale la parte di vescica che riceve lo sbocco degli
ureteri.
106
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
La parte ʻaltaʼ della vescica, detta fondo, costituisce il deposito dellʼurina.
Il volume vescicale è estremamente variabile: la capacità normale è
solitamente compresa tra 250-300 ml; può però arrivare, in virtù della propria
elasticità (tutta la parete dellʼorgano comprende uno strato muscolare), in
condizioni eccezionali, a 2 litri.
MINZIONE
Eʼ lʼatto riflesso, facilitato od inibito dalla volontà, consistente nellʼemissione attraverso lʼuretra- dellʼurina contenuta nella vescica.
Nellʼadulto, il riflesso inizia quando la vescica contiene 300-400 ml di urina.
La distensione delle pareti della vescica eccita i recettori da stiramento, che
trasmettono impulsi al tratto sacrale del midollo spinale. Dal midollo partono poi
impulsi che raggiungono la muscolatura dello strato più esterno della vescica
(muscolo detrusore), alla cui contrazione si deve lo svuotamento della vescica.
107
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
Affinchè la vescica si svuoti, è necessario che la pressione intravescicale aumenti sino
a superare la pressione allʼinterno dellʼuretra. Questa condizione si realizza con più
meccanismi:
• Lo sfintere interno (liscio), quello esterno (striato) ed il pavimento pelvico si rilassano.
• Il detrusore si contrae: ne consegue anche un cambiamento di forma della vescica che,
da piatta, assume una forma ad imbuto e spinge contro il pavimento pelvico.
• La pressione addominale aumenta, anche per contrazione volontaria.
CONTINENZA
Eʼ definita come il controllo volontario della minzione. In genere, si considera
normale continenza la capacità di immagazzinare lʼurina senza perdite per almeno
2 ore da svegli, ed interrompere il sonno notturno non più di una volta (prima dei 65
anni) o due volte (dopo i 65 anni).
La persona continente dovrebbe essere in grado di impegnarsi in una moderata o
intensa attività fisica senza perdere urine, e di rinviare la minzione nonostante il
desiderio di urinare.
Dovendo ora operare una scelta tra le varie patologie della vescica, voglio
dare spazio ad una situazione assai diffusa (e non sempre conosciuta e
correttamente inquadrata), quale la c.d. vescica iperattiva.
Daremo poi inevitabilmente spazio ai tumori vescicali, spesso sottostimati.
108
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
SINDROME DELLA VESCICA IPERATTIVA
Diffusa in tutto il mondo, ha un significativo impatto sulla qualità di vita di
quanti ne soffrono.
Con questo nome si intende unʼentità clinica caratterizzata da:
• Urgenza minzionale: improvviso ed irrefrenabile desiderio di urinare, difficoltà a
procrastinare la minzione.
• Incontinenza da urgenza: perdita involontaria di urina, accompagnata o preceduta
immediatamente da urgenza. Può essere presente o meno, NON rappresenta un
elemento diagnostico indispensabile.
• Pollachiuria: elevata frequenza minzionale, tanto diurna quanto notturna.
Eʼ riconducibile ad una iperattività del detrusore (il muscolo di parete della
vescica), legata a cause note (problemi neurologici) o -più spesso- ignote
(idiopatica).
Va da sé che il termine empirico di “vescica iperattiva” può essere utilizzato solo in
assenza di infezioni urinarie od altre patologie note.
I sintomi che configurano il quadro di vescica iperattiva sono presenti sia negli
uomini che nelle donne e tendono ad aumentare con lʼetà:
• Nella donna, con lʼavanzare degli anni, tendono a diminuire la capacità e la compliance*
vescicali, al pari della massima pressione di chiusura uretrale e del flusso massimo
urinario.
• Nellʼuomo si riduce il flusso massimo** ed aumenta il residuo vescicale post-minzionale.
_____________________________________
* Compliance vescicale: è il rapporto tra volume di riempimento ed aumento della
pressione del detrusore. Eʼ un indice del potere della vescica di modificare il proprio
volume in rapporto a modificazioni della pressione.
** Flusso urinario: è la velocità (misurata in ml/secondo) con cui esce lʼurina durante la
minzione volontaria. Eʼ risultante di numerose variabili indipendenti: volume vescicale,
pressione del detrusore, resistenze a livello dellʼuretra, impegno del torchio addominale,
stato psicologico del paziente, età ecc.
109
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
I possibili fattori di rischio associati con la vescica iperattiva sono:
•
•
•
•
•
•
•
•
Età
Menopausa.
Obesità.
Alterazioni della sfera cognitiva.
Precedente chirurgia uro-ginecologica.
Farmaci.
Fumo di sigaretta.
Evt. prolassi, vaginali o rettali.
Lʼapproccio terapeutico è molteplice, spaziando dalle terapie comportamentali a
quelle farmacologiche.
La terapia classica consiste nellʼuso degli antimuscarinici, efficaci ma spesso condizionanti
effetti collaterali pesanti.
Ultimamente, è stata sperimentata la cizolirtina (Mirabegron), appartenente a diversa
categoria farmacologica (il farmaco nasce come analgesico), con diversi e meno gravi
effetti collaterali.
110
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
CANCRO DELLA VESCICA
Il medesimo tipo di epitelio riveste la superficie interna del tratto dellʼapparato
urinario, che va dal bacinetto renale allʼuretere, alla vescica ed ai 2/3
prossimali dellʼuretra. Il cancro può colpire in ognuno di questi punti, con
peraltro una netta prevalenza (90%) a carico della vescica, contro lʼ8% del
bacinetto renale ed il 2% delle restanti localizzazioni.
Il tumore della vescica rappresenta circa il 3% di tutti i tumori, tre volte più
frequente negli uomini (è il 4° cancro più comune) che nelle donne (in cui occupa il
13°posto) e due volte più frequenti nei bianchi rispetto ai neri.
Eʼ più comune tra i 60 ed i 70 anni, con età media di diagnosi a 65 anni.
Una caratteristica peculiare di questi tumori è quella di un rapporto incidenza/
mortalità di 5:1. Ciò riflette la preminenza di varianti superficiali meno letali rispetto
a varianti (infiltranti) più letali e metastatizzanti.
Una volta diagnosticato, questo tipo di tumore presenta il fenomeno del
policronotropismo, della tendenza, cioè, a ripresentarsi nel tempo in punti anche
diversi, ma sempre del tratto urinario con il medesimo tipo di rivestimento epiteliale.
Fattori di rischio
• Fumo di sigaretta: contribuisce allo sviluppo del tumore nel 50% dei maschi e nel 40%
delle femmine. Il rischio di sviluppare il tumore è aumentato da 2 a 4 volte rispetto ai
non-fumatori e permane per oltre 10 anni dopo che si sia smesso di fumare.
• Esposizione cronica allʼanilina (coloranti, industria tessile) ed a farmaci (fenacetina antidolorifico-,clornafazina -antitumorale- e ciclofosfamide).
• Parassiti, come la Bilharzia e lo Schistosoma Haematobium, diffusi in paesi del terzo
mondo (Medio Oriente ed Egitto in particolare, ma anche Madagascar ed isole
dellʼOceano Indiano).
• Predisposizione genetica: esistono prove a favore di una componente genetica quale
fattore di rischio predisponente.
• Dieta: fritture e grassi consumati in grande quantità sono associati ad un aumentato
rischio.
111
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
Sintomi
I sintomi con cui si può presentare un tumore della vescica sono comuni a molte
altre malattie che colpiscono lʼapparato urinario.
La presenza di sangue nelle urine (ematuria) è sintomo che interessa lʼ80-90% dei
pazienti con tumore della vescica ed è spesso indicatore di una forma vegetante del
tumore.
Non va scordato che la vescica è la sorgente più frequente (40%) di ematuria, ma che
questo non necessariamente è sinonimo di tumore. Nel 22% dei casi si tratta di una
banale cistite. Se lʼematuria è microscopica, più probabile unʼorigine prostatica (25%).
In presenza di ematuria è quindi opportuno uno screening diagnostico delle cause, pur
sapendo che si aumenta la possibilità di diagnosticare un tumore in fase iniziale, ma che
questo non sposta le possibilità di sopravvivenza.
Dopo lʼematuria, i sintomi relativamente più frequenti sono quelli irritativi, quali la
sensazione di bruciore alla vescica quando si comprime lʼaddome, la difficoltà ed il dolore
ad urinare.
Il tumore della vescica può diffondere localmente ed a distanza per via linfatica: dapprima
ai linfonodi e successivamente -attraverso il circolo sanguigno- a polmoni, fegato ed ossa.
112
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
Diagnosi
Le procedure diagnostiche, nel caso vi sia un sospetto di cancro alla vescica, si
basano su:
1. Ecografia
2. Urografia, TAC e Risonanza Magnetica
3. Cistoscopia: lʼindagine endoscopica si effettua in anestesia. Si introduce un endoscopio
flessibile in vescica, si esplora la superficie, con la possibilità di eseguire prese bioptiche dei
tessuti sospetti, nonchè di asportare direttamente eventuali masse tumorali vegetanti.
113
Roberto Freschi
Corso di Anatomia Funzionale
UTE Novate Mil. 2012- 2013
Terapia
La scelta del trattamento è dipendente dallʼinvasione o meno, da parte del tumore,
del muscolo della parete vescicale, così come dalla sua diffusione ai linfonodi od
oltre.
• Per neoplasie di piccole dimensioni non infiltranti, lʼindicazione è alla resezione
transuretrale, seguita o meno da terapia intravescicale.
La terapia intravescicale utilizza:
1. Il bacillo di Calmette-Guerin (BCG)*, somministrato per instillazioni prima settimanali(6)
poi mensili (in media per 1 anno).
2. Chemioterapici
• Per neoplasie di maggiori dimensioni od infiltranti, si esegue la cistectomia radicale
(asportazione completa della vescica), unita a -specie se in presenza di metastasichemio- e radioterapia.
__________________________________
* Bacillo di Calmette-Guerin: è il batterio vivo attenuato (230 passaggi in un terreno
costituito da bile, glicerina e patata, per un periodo di 13 anni, dal 1908 al 1921, per
attenuarne la virulenza) utilizzato per la vaccinazione per la tubercolosi.
114