Il Programma Clinico di ELUVIA
Prof. Carlo Setacci
Professore Ordinario Università di Siena e Direttore Struttura Complessa di Chirurgia
Vascolare Policlinico Santa Maria alle Scotte, Siena.
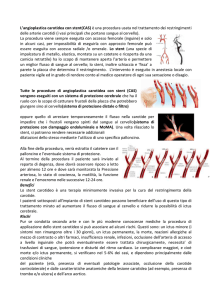
European guidelines
Destino Clinico
Primary
amputation
25%
Medical
Treatment
only
25%
Revascularization
50%
Cured
25%
Continuing
CLI
25%
Alive Amputated
25%
Dead
25%
AFS-POPLITEA NORMALE
NEI NORMALI MOVIMENTI
1.
ESTENSIONE CONTRAZIONE
2.
TORSIONE
3.
COMPRESSIONE
4.
FLESSIONE
Stent sul mercato
Bare Metal Stents
(BMS)
Uncoated stents composed of
bare metal that are
permanently placed inside the
affected artery
Constructed from a range of
metals, including nitinol,
stainless steel, cobalt
chromium, platinum
chromium
Drug-Eluting Stents
Covered Stents
BMS that are coated with a
polymeric material and
release drugs locally
Metal stent structures with
coverings composed of fabric
or graft material such as
polytetrafluoroethylene
(PTFE)
Composed of biodegradable
materials that can be
absorbed or resorbed by the
body
Graft material covering
provides a direct barrier to
tissue ingrowth and reduces
the risk of chronic
inflammation and restenosis
Bioabsorbable DES deliver
anti-proliferative agents to
prevent restenosis and
degrade over time,
eliminating concerns
regarding late-stent
thrombosis, chronic
inflammation, acute vessel
closure, and biocompatibility
Stent releases the antiproliferative or
immunosuppressive drug over
time, leaving behind the
metallic stent in the artery
Represent the future of stent
technology
Classic stent type
Either self-expanding or
balloon-expandable
Bioabsorbable
Stents (BAS)
Either self-expanding or
balloon-expandable
Either self-expanding or
balloon-expandable
Opzioni chirurgiche
Il programma Clinico di ELUVIA
Il programma Clinico di ELUVIA
Boston Scientific sta implementando un rigoroso programma
clinico che, finora, ha permesso di validare:
Stent senza farmaco: STUDIO SUPERNOVA
Stent ELUVIA con farmaco: STUDIO MAJESTIC
Studio SuperNova
Obiettivo
dello
studio
Design
dello
studio
Valutare l’efficacia e la sicurezza dello Stent Innova nel trattamento
delle lesioni femoro-poplitee
Studio prospettico, multicentrico, a singolo braccio, di non inferiorità
rispetto agli obiettivi di performance (Performance Goal) della PTA1
49 centri in USA, Canada, Europa e Giappone; 299 pazienti
Endpoints primari fissati ad 1 anno
Pazienti: Ischemia cronica arti inferiori (Rutherford 2-4) con almeno un vaso BTK
Criteri
• Tipologia Lesione: stenosi de novo, restenosi (≥70%), occlusioni
di
• Lunghezza lesione: ≥ 30 mm e ≤ 190 mm
arruolamento • Diametro del vaso: ≥ 4 mm e ≤ 7 mm
del tratto femoro-popliteo
1. Rocha-Singh KJ, Jaff MR, Crabtree TR, Bloch DA, Ansel G; VIVA Physicians, Inc. Catheter Cardiovasc Interv. 2007 May 1;69(6):910-9.
Conclusioni Studio SuperNOVA
• Lo studio ha dimostrato la sicurezza e l’efficacia
dello stent Innova nel trattamento delle lesioni
femoro-poplitee, testando lo stent su lesioni
complesse per tipologia e posizione (distale).
• Il 97.3% dei pazienti trattati ha mostrato un
miglioramento clinico valutato con la Classificazione
di Rutherford.
MAJESTIC: struttura dello studio
Obiettivo
dello
studio
Design
dello
studio
Determinare le perfomances dello stent Eluvia a rilascio di farmaco
nel trattamento delle lesioni femoro-poplitee lunghe fino a 110
mm.
Studio prospettico, multicentrico, a singolo braccio, non randomizzato.
14 centri in Europa (Austria, Belgio, Germania), Australia e Nuova Zelanda;
57 pazienti
Endpoint primario: Primary Patency a 9 mesi
Follow up a 3 anni
Pazienti: Ischemia cronica arti inferiori (Rutherford 2-4)
Criteri
• Tipologia Lesione: stenosi de novo o restenosi (≥ 70%) nella SFA nativa o nell’arteria poplitea
di
prossimale, che non abbiano subito precedenti trattamenti con DEB.
arruolamento • Lunghezza lesione: ≥ 30 mm e ≤ 110 mm
• Diametro del vaso: ≥ 4 mm e ≤ 6 mm
Conclusioni MAJESTIC
• Lo studio ha dimostrato l’efficiacia dello stent a rilascio
controllato di farmaco ELUVIA in quanto il 96.1% dei
pazienti trattati con questo stent aveva il vaso pervio a
12 mesi dalla procedura
• Il 94 % dei pazienti ha registrato un miglioramento
della sintomatologia clinica
EMINENT
Obiettivo
dello
studio
Design
dello
studio
Determinare le perfomances dello stent Eluvia a rilascio di farmaco
nel trattamento delle lesioni femoro-poplitee IN UN AMPIA
COORTE DI PAZIENTI
Studio prospettico, multicentrico, a doppio braccio, randomizzato.
centri in Europa (PI italiano)
750 pazienti
Endpoint primario: Primary Patency, and economic data
Pazienti: Ischemia cronica arti inferiori (Rutherford 2-5)
Criteri
• Tipologia Lesione: stenosi de novo o restenosi (≥ 70%) nella SFA nativa o nell’arteria poplitea
di
prossimale, che non abbiano subito precedenti trattamenti con DEB.
arruolamento
Conclusioni EMINENT…
• FIRST IN MAN 06/2016….
COMUNQUE