Prof. Giorgio Sartor
Metabolismo dei grassi
Copyright © 2001-2017 by Giorgio Sartor.
B12 - Versione 1.6.2 – Apr-17
All rights reserved.
Lipidi
• Semplici
– Sono molecole che non contengono legami
esterei o amidici
• Acidi grassi
• Colesterolo
• Complessi
– Sono derivati di acidi grassi variamente
esterificati o amidati.
• Glicerofosfolipidi e sfingosidi
• Trigliceridi
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
-2-
1
Metabolismo dei grassi
1. Demolizione dei trigliceridi
2. Catabolismo degli acidi grassi
3. Biosintesi
– degli acidi grassi e colesterolo
– dei lipidi complessi
4. Trasporto dei lipidi
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
-3-
I grassi (esteri del glicerolo)
O
H
H
C1
C2
O
H
H
C3
CH3
O
CH3
O
O
CH3
H
O
HO
N
+
CH3
CH 3
O
H 3C
O
O
HO
NH 2
R
P
O
HO
• Trigliceridi (TAG)
O
3
O
O
2
+
NH 3
CH 3
O
1
CH 3
O
CH2OH
HO
H
H 2C
OH
• Fosfolipidi
O
• Lisofosfolipidi
OH
OH
OH
OH
OH
OH
O
P
H 3C
N
O
+
O
3
O
CH3
2
CH3
OH
1
CH3
O
O
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
-4-
2
I grassi (esteri della sfingosina)
HO
HO
HO
CH3
NH2
• Sfingosina
CH3
H
N
CH3
HO
• Ceramidi
O
• Sfingomielina
HO
O
O
P
CH3
H
N
CH3
O
O
O
+
N
H3C
CH3
H3C
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
-5-
Metabolismo dei grassi
1. Demolizione dei trigliceridi
2. Catabolismo degli acidi grassi
3. Biosintesi
– degli acidi grassi e colesterolo
– dei lipidi complessi
4. Trasporto dei lipidi
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
-6-
3
Metabolismo dei grassi
• I grassi sono fra le principali fonti di
energia metabolica
Energia
(kJ·mole-1)
g/70Kg
Energia (kJ)
Grassi
37
15000
555000
Proteine
17
6000
102000
Glicogeno
(fegato)
16
120
1920
Glicogeno
(muscolo)
16
70
1120
Glucosio
16
20
360
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
-7-
Digestione dei grassi
O
C1
H
C2
C3
H
O
H
CH3
O
CH3
O
H
O
CH3
H
O
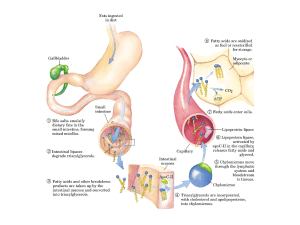
• A livello intestinale i grassi
(triacilgliceroli, TAG) sono idrolizzati in
C1 e C3 da lipasi pancreatiche mentre i
C2 sono idrolizzati da lipasi intestinali
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
-8-
4
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
-9-
Lipasi
• Catalizza l’idrolisi dei triacilgliceroli in posizione 1 e 3
formando 1,2-diacilgliceroli, 2-acilglicerolo e quindi
glicerolo
O
C1
C2
C3
H
H
O
H
CH3
O
CH3
O
H
O
CH3
H
O
O
H2O
H
H
O
H
CH3
O
CH3
O
H
OH
H
O
H2O
CH3
O
O
H
H
H
CH3
O
OH O
O
H
H2O
CH3
HO
H
H
OH
OH
OH
H
H
H
H
O
CH3
O
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 10 -
5
Lipolisi: meccanismo generale
O
O
R"
R'
R"
O
R'
O
Nu+
H
R
Nu:
H
R
O
O
H
O
R'
H
R"
O
R'
H+
Nu:
Nu
R"
O
R
H
R
H 2O
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 11 -
Triacilglicerolo lipasi EC 3.1.1.3
Ormone
(Adrenalina o glucagone)
Gα-GTP
Adenilato
ciclasi
(inattiva)
AMP
Adenilato ciclasi
(attiva)
ATP
Fosfodiesterasi
cAMP + PPi
Proteina
chinasi A
(inattiva)
Proteina
chinasi A
(attiva)
P
ATP
Fosforilasi chinasi
(b-inattiva)
ADP Fosforilasi chinasi
(a-attiva)
ATP
Fosfatasi
Pi
P
ADP Triacilglicerolo
Triacilglicerolo
lipasi
lipasi
(a-attiva)
(b-inattiva)
Fosfatasi
Pi
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 12 -
6
Triacilglicerolo lipasi EC 3.1.1.3
Insulina
Ormone
(Adrenalina o glucagone)
Gα-GTP
Adenilato
ciclasi
(inattiva)
AMP
Adenilato ciclasi
(attiva)
ATP
Fosfodiesterasi
cAMP + PPi
Proteina
chinasi A
(inattiva)
Proteina
chinasi A
(attiva)
P
ATP
ADP Fosforilasi chinasi
Fosforilasi chinasi
(b-inattiva)
• Forma “a” attiva ed
indipendente da
effettori allosterici
• Forma “b” meno attiva
e dipendente da fattori
allosterici
B12 - v. 1.6.2 © gsartor 2001-2017
(a-attiva)
Fosfatasi
Pi
Triacilglicerolo
lipasi
(b-inattiva)
ATP
P
ADP Triacilglicerolo
Fosfatasi
lipasi
(a-attiva)
Pi
Metabolismo dei grassi
- 13 -
Triacilglicerolo lipasi EC 3.1.1.3
• Triacilglicerolo lipasi
da Pseudomonas
Aeruginosa
complessata con un
omologo di un
trigliceride.
• Possiede un dominio
legante Ca++
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 14 -
7
Detergenti
• L’accessibilità dei legami esterei dei TAG è favorita dalla
presenza di sali di acili biliari che funzionano come
emulsionanti:
OH
O
H3C
Acido colico (colato)
CH3
O
CH3
O
O
R
HO
N
H
OH
CH3
B12 - v. 1.6.2 © gsartor 2001-2017
O
Acido taurocolico
O
O
R
S
O
N
H
Acido glicocolico
O
Metabolismo dei grassi
- 15 -
Fosfolipasi
O
PLD
PLC
P
H 3C
N
+
O
O
3
O
CH3
CH3
O
2
O
1
PLA2
CH3
CH3
O
O
PLA1
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 16 -
8
MECCANISMO
FOSFOLIPASI
B12 - v. 1.6.2 © gsartor 2001-2017
DESTINO DEI
PRODOTTI
Metabolismo dei grassi
- 17 -
Fosfolipasi
•
•
•
•
Fosfolipasi
Fosfolipasi
Fosfolipasi
Fosfolipasi
A1 EC 3.1.1.32
A2 EC 3.1.1.4
C EC 3.1.4.3
D EC 3.1.4.4
• Lipasi EC 3.1.1.3
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 18 -
9
Fosfolipasi A1 (EC 3.1.1.32 )
O
P
H3 C
N
O
+
O
3
O
CH3
O
2
CH3
CH3
CH3
O
1
O
O
O
O
O
P
O
+
H3C
N
CH3
O
O
O
CH
CH3 3
CH3
O
OH
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 19 -
Fosfolipasi A1
Ca++
ASP
HIS
1QD6
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 20 -
10
Meccanismo (diade catalitica)
His48
H
H
N
O
Ca++
O
H
N
O
H
O
R"
O
H
O
His48
R'
Asp99
H
N
O
H
Ca++
O
O
H
N
O
R"
O
H
H
Ca++
H
N
O
H
O
O
N
O
R'
Asp99
His48
H
O
R"
H
O
O
R'
Asp99
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 21 -
Fosfolipasi A2 (EC EC 3.1.1.4)
O
P
H3 C
N
O
+
O
3
O
CH3
O
2
CH3
CH3
CH3
O
1
O
O
O
O
P
+
H3C
N
O
CH3
O
O
O
CH
CH3 3
OH
CH3
O
O
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 22 -
11
Fosfolipasi A2
• Il lisofosfolipide è un detergente potentissimo,
• La fosfolipasi A2 è contenuta nel veleno di
serpenti (cobra), insetti (api), probabilmente
anche in invertebrati marini (spugne), l’effetto
è quello di lisare i globuli rossi attraverso
l’effetto della lisofosfatidilcolina
• Nei mammiferi è secreta dal pancreas e una
piccola quantità di lecitina viene secreta dal
fegato, e quindi idrolizzata, per aiutare la
solubilizzazione dei grassi.
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 23 -
Fosfolipasi A2
• Esistono almeno due famiglie di
PLA2:
– sPLA2: secreta, che permette l’idrolisi
dei fosfolipidi all’interfaccia, e
possiede un dominio che si lega alla
membrana (veleno delle api)
– cPLA2: citosolica, che viene utilizzata
per la produzione di acidi grassi
(arachidonato), inositolo fosfato come
messaggeri intracellulari.
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 24 -
12
Fosfolipasi A2 (EC 3.1.1.4)
1S8G
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 25 -
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 26 -
13
Diade catalitica
Ca++
ASP99
HIS48
1FXF
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 27 -
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 28 -
14
Ipotetico modo d’azione di Fosfolipasi A2 su di una micella
di fosfolipidi
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 29 -
FABS
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 30 -
15
FABS
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 31 -
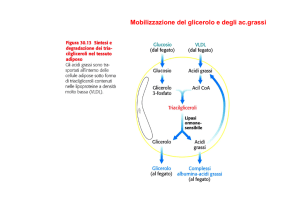
Destino dei prodotti
• Glicerolo
– Convertito in diidrossiacetonfosfato entra nella glicolisi
– La conversione è catalizzata da:
• Glicerolo fosfato deidrogenasi
• Diidrossiacetone chinasi
• Acidi grassi
– Ossidazione
• Principalmente β-ossidazione
– Produzione Acetil-CoA, NADH, FADH2
• Oppure ω-ossidazione
– Processo aspecifico che porta alla produzione di composti
idrosolubili più facili da eliminare.
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 32 -
16
Glicerolo
• L’ossidazione del glicerolo a
diidrossiacetone è
catalizzata dalla glicerolo
fosfato deidrogenasi (EC
1.1.1.6)
OH
OH
HO
O
OH
OH
NAD+
NADH
1JQ5
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 33 -
Glicerolo
OH
OH
O
O
O
OH
A TP
1UOE
B12 - v. 1.6.2 © gsartor 2001-2017
O
P
O
O
ADP
• La fosforilazione del
diidrossiacetone è catalizzata
dalla diidrossiacetone chinasi
(EC 2.7.1.29).
• Il diidrossiacetonfosfato così
formatosi è convogliato nella
glicolisi
Diidrossiacetone
Mg++
Metabolismo dei grassi
Omologo ATP
- 34 -
17
Glicerolo
OH
OH
O
O
O
OH
O
A TP
1UOE
O
P
ADP
O
• La fosforilazione del
diidrossiacetone è catalizzata
dalla diidrossiacetone chinasi
(EC 2.7.1.29).
• Il diidrossiacetonfosfato così
formatosi è convogliato nella
glicolisi
Diidrossiacetone
B12 - v. 1.6.2 © gsartor 2001-2017
Omologo ATP
Mg++
Metabolismo dei grassi
- 35 -
Lipidi
• Semplici
– Sono molecole che non contengono legami
esterei o amidici
• Acidi grassi
• Colesterolo
• Complessi
– Sono derivati di acidi grassi variamente
esterificati o amidati.
• Glicerofosfolipidi e sfingosidi
• Trigliceridi
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 36 -
18
Metabolismo dei grassi
1. Demolizione dei trigliceridi
2. Catabolismo degli acidi grassi
3. Biosintesi
– degli acidi grassi e colesterolo
– dei lipidi complessi
4. Trasporto dei lipidi
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 37 -
β-ossidazione degli acidi grassi
19
Acidi grassi
O
• Acidi grassi
saturi
18
1
O
3
2
5
4
7
6
9
8
11
10
13
12
15
17
14
16
14
16
CH3
Acido stearico (C18)
O
• Acidi grassi
insaturi
9
1
O
3
2
5
4
18
10
7
6
12
11
8
13
CH3
17
15
Acido oleico (C18∆9)
C18:1ω9
O
• Acidi grassi
polinsaturi
9
1
O
3
2
5
4
10
12
13
15
7
6
8
11
14
17
16
CH3
18
Acido linoleico (C18∆9,12)
C18:2ω6
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 39 -
β-ossidazione acidi grassi
• Una volta che i TGA sono idrolizzati ad acidi grassi questi
ultimi vengono demoliti fondamentalmente attraverso
l’ossidazione,
• Il principale meccanismo è quello della β-ossidazione che
distacca unità bicarboniose, sottoforma di Acetil-CoA,
rompendo il legame tra il Cα e il Cβ,
O
H
α
O
H
H
β
O
S
C H3
H
O
CH3
CoA
B12 - v. 1.6.2 © gsartor 2001-2017
H
α
O
H
H
β
CH3
H
Metabolismo dei grassi
- 40 -
20
β-ossidazione acidi grassi
• A seconda del numero (n) di
atomi di carbonio dell’acido
grasso di producono n/2
molecole di Acetil-CoA.
• La reazione avviene nella
matrice mitocondriale.
• Gli acidi grassi vengo attivati
attraverso la formazione di un
Acil-CoA.
• L’Acil-CoA viene trasportato
all’interno della membrana
interna mitocondriale attraverso
il sistema carnitina/acilcarnitina.
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 41 -
Attivazione degli acidi grassi
• L’attivazione degli acidi grassi
porta alla formazione di AcilCoa
• Avviene nel citoplasma ad
opera di una l’acil-CoA sintetasi
(EC 6.2.1.3).
• Il processo è endoergonico
(∆G = 31.4 kJ·mole-1)
• Viene reso spontaneo dalla
razione di idrolisi di una
molecola di ATP a AMP e PPi, il
quale fornisce un surplus di
energia convertendosi a 2Pi
attraverso una pirofosfatasi,
per un totale di -65.9 kJ·mole-1
di ATP impiegato.
B12 - v. 1.6.2 © gsartor 2001-2017
CH3
O
O
CoASH
ATP
∆G = + 31.4 kJ mol-1 ∆G = - 32.3 kJ mol-1
∆G = - 33.6 kJ mol-1
AMP + PPi
2Pi
CoA
CH3
S
O
1V25
Metabolismo dei grassi
1V26
- 42 -
21
Formazione di Acil-CoA
O
• Il meccanismo di
reazione prevede la
formazione di un
derivato intermedio
aciladenosina, legato
all’enzima, che subisce
l’attacco nucleofilo da
parte dell’atomo di
zolfo del CoA-SH.
O
P
O
ATP
O
O
P
O
P
O
O
O
N
O
O
+
n CH3
O
OH
P
O
O
O
2
O
P
HO
O
O
O
O
H
O
P
O
N
O
H3C
P
O
O
CoA
O
Pi
PPi
O
S
N
N
HO
O
Acido grasso
NH2
N
O
NH2
N
Aciladenosina
n
N
HO
N
OH
O
CoA
O
S
H3C
n
O
O
P
H3C
O
N
O
O
Acil-CoA
NH2
N
CoA
+
O
N
N
HO
S
n
O P
O
OH
AMP
O
N
O
NH2
N
Intermedio tetraedrico
N
HO
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
N
OH
- 43 -
Trasporto
• Il trasporto degli acilCoA nell’interno degli
organelli subcellulari, dove avviene
l’ossidazione degli acidi grassi, sfrutta il
sistema carnitina/acilcarnitina.
O
O
OH
N
H
H3C
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
+
CH3
CH3
- 44 -
22
Carnitina
• Il sistema carnitina/acilcarnitina è stato scoperto la
prima volta nei mitocondri.
• Esso contiene carnitina acetiltransferasi (CAT), legata
strettamente alla faccia interna della membrana interna
mitocondriale e quattro isoenzimi carnitina palmitoil
transferasi (CPT, CPT-IA nel fegato, CPT-IB nel muscolo
e altre cellule, CPT-IC nel cervello e CPT-II).
• Gli enzimi CPT-I sono localizzati nella membrana
esterna mitocondriale con le loro porzioni catalitica e
regolatoria (inibita da malonilCoA) che si affacciano
verso il lato citoplasmatico mentre CPT II è localizzata
come la CAT.
• Tale varietà isoenzimatica è legata alla diversa affinità
per i diversi gruppi acilici:
– CAT: C2-C10, CPTI: C6-C20
– CPTII: C6-C18
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 45 -
Carnitina
• Anche i perossisomi contengono una CAT,
– la carnitina octiltransferasi (CROT) che ha un’affinità
maggiore per C4-C16, è inibita da malonilCoA
– ed un’altra acilcarnitina transferasi solubile non
inibita da malonilCoA.
• Anche altre membrane (reticolo
endoplasmatico, sarcoplasmatico, membrana
nucleare e membrana plasmatica) contengono
carnitina aciltransferasi.
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 46 -
23
Trasporto nei mitocondri
Acil-CoA
Carnitina
• Il trasporto di Acil-Coa
attraverso la membrana
interna mitocondriale viene
quindi mediato dalla
carnitina attraverso tre
sistemi enzimatici:
Citoplasma
CPTI
A. Carnitina aciltransferasi I,
nel lato citoplasmatico,
Carnitina
– CAT, CPT-IA nel fegato,
CPT-IB nel muscolo e altre
cellule, CPT-IC nel cervello.
O-acilcarnitina
CoA-SH
Spazio intermembrana
B. Carnitina acilcarnitina
traslocasi (CACT), nella
membrana e
C. Carnitina aciltransferasi II,
nel lato della matrice
mitocondriale.
CACT
CPTII
Matrice
– CPT-II
O-acilcarnitina + CoA-SH
Acil-CoA
+
Carnitina
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 47 -
Trasporto nei mitocondri
Acil-CoA
Carnitina
O-acetilcarnitina
Citoplasma
CPTI
Carnitina
O-acetilcarnitina
O-acilcarnitina
CoA-SH
Carnitina
Spazio intermembrana
CACT
CACT
CPTII
CAT
Matrice
β-ossidazione
O-acilcarnitina + CoA-SH
B12 - v. 1.6.2 © gsartor 2001-2017
Acil-CoA
Acetil-CoA + Carnitina O-acetilcarnitina
+
+
Carnitina
CoA-SH
Metabolismo dei grassi
Carnitina
- 48 -
24
Trasporto nei perossisomi
• Nei perossisomi il
trasporto di Acil-Coa
attraverso la membrana
viene mediato dalla
carnitina attraverso:
CPT
solubile
Carnitina + Acil-CoA
CoA-SH + O-acilcarnitina
A. Carnitina aciltransferasi
I, nel lato
citoplasmatico,
Citoplasma
– CROT e solubile.
CROT
B. Carnitina acilcarnitina
traslocasi, nella
membrana e
C. Carnitina aciltransferasi
II, all’interno.
CACT
CPTII
Interno del perossisoma
– CPT-II
Carnitina + Acil-CoA
B12 - v. 1.6.2 © gsartor 2001-2017
CoA-SH + O-acilcarnitina
Metabolismo dei grassi
- 49 -
Carnitina aciltransferasi EC 2.3.1.7
O
OH
N
O
H 3C
+
O
CH3
+
CoA
S
CH3
Carnitina Acil
transferasi I
(lato matrice)
n
CH3
Carnitina Acil
transferasi II
(lato citoplasma)
O
O
O
O
n
N
+
CH3
CH3
+
H3C CH3
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
CoA
H
S
- 50 -
25
Carnitina aciltransferasi EC 2.3.1.7
CoA
Carnitina
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 51 -
Carnitina aciltransferasi EC 2.3.1.7
Carnitina
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 52 -
26
Carnitina aciltransferasi EC 2.3.1.7
CoA
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 53 -
Carnitina aciltransferasi EC 2.3.1.7
CoA
Carnitina
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 54 -
27
Carnitina aciltransferasi EC 2.3.1.7
CoA
Carnitina
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 55 -
β-ossidazione acidi grassi
•
•
La strategia della β-ossidazione
consiste nel generare un
nuovo carbonile in β a seguito
della rotture del legame tra Cα
e Cβ.
Tale sequenza di reazioni
produce:
–
–
–
–
•
Un Acetil-CoA
Un Acil-CoA più corto di due
unità carboniose.
Un FADH2
Un NADH
O
FAD
CoA
CH3
S
Acil-CoA (Cn)
O
CoA
O
S
CH3
CoA
3-Chetotiolasi
EC 2.3.1.16
Acil-CoA
deidrogenasi
EC 1.3.3.6
EC 1.3.99.3
EC 1.3.99.13
FADH2
CH3
S
Acil-CoA (Cn-2)
O
H
CoA
CoA-SH
CH3
S
O
O
H
CoA
La reazione procede
S
ciclicamente fino a quando
β-chetoacil-CoA
l’acil-CoA è ridotto a due unità
NADH + H+
(Acetil-CoA) o tre unità
L-3-idrossiacil-CoA
(Propionil-CoA) carboniose.
deidrogenasi
EC 1.1.1.35
NAD+
trans-∆2-enoil-CoA
CH3
H 2O
O
Enoil-CoA idratasi
EC 4.2.1.17
OH
CoA
S
CH3
L-β-idrossiacil-CoA
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 56 -
28
β-ossidazione acidi grassi
•
•
La strategia della β-ossidazione
consiste nel generare un
nuovo carbonile in β a seguito
della rotture del legame tra Cα
e Cβ.
Tale sequenza di reazioni
produce:
–
–
–
–
•
Un Acetil-CoA
Un Acil-CoA più corto di due
unità carboniose.
Un FADH2
Un NADH
O
FAD
CoA
CH3
S
Acil-CoA (Cn)
O
CoA
O
S
CH3
CoA
3-Chetotiolasi
EC 2.3.1.16
Acil-CoA
deidrogenasi
EC 1.3.3.6
EC 1.3.99.3
EC 1.3.99.13
FADH2
CH3
S
Acil-CoA (Cn-2)
O
H
CoA
CoA-SH
CH3
S
O
O
H
CoA
La reazione procede
S
ciclicamente fino a quando
β-chetoacil-CoA
l’acil-CoA è ridotto a due unità
NADH + H+
(Acetil-CoA) o tre unità
L-3-idrossiacil-CoA
(Propionil-CoA) carboniose.
deidrogenasi
EC 1.1.1.35
NAD+
trans-∆2-enoil-CoA
CH3
H 2O
O
Enoil-CoA idratasi
EC 4.2.1.17
OH
CoA
CH3
S
L-β-idrossiacil-CoA
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 57 -
β-ossidazione acidi grassi
•
•
La strategia della β-ossidazione
consiste nel generare un
nuovo carbonile in β a seguito
della rotture del legame tra Cα
e Cβ.
Tale sequenza di reazioni
produce:
–
–
–
–
•
Un Acetil-CoA
Un Acil-CoA più corto di due
unità carboniose.
Un FADH2
Un NADH
O
FAD
CoA
CH3
S
Acil-CoA (Cn)
O
CoA
O
S
CH3
CoA
3-Chetotiolasi
EC 2.3.1.16
Acil-CoA
deidrogenasi
EC 1.3.3.6
EC 1.3.99.3
EC 1.3.99.13
FADH2
CH3
S
Acil-CoA (Cn-2)
O
H
CoA
CoA-SH
CH3
S
O
O
H
CoA
La reazione procede
S
ciclicamente fino a quando
β-chetoacil-CoA
l’acil-CoA è ridotto a due unità
NADH + H+
(Acetil-CoA) o tre unità
L-3-idrossiacil-CoA
(Propionil-CoA) carboniose.
deidrogenasi
EC 1.1.1.35
NAD+
trans-∆2-enoil-CoA
CH3
H 2O
O
Enoil-CoA idratasi
EC 4.2.1.17
OH
CoA
S
CH3
L-β-idrossiacil-CoA
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 58 -
29
β-ossidazione acidi grassi
•
•
La strategia della β-ossidazione
consiste nel generare un
nuovo carbonile in β a seguito
della rotture del legame tra Cα
e Cβ.
Tale sequenza di reazioni
produce:
–
–
–
–
•
Un Acetil-CoA
Un Acil-CoA più corto di due
unità carboniose.
Un FADH2
Un NADH
O
FAD
CoA
CH3
S
Acil-CoA (Cn)
O
CoA
O
S
CH3
CoA
3-Chetotiolasi
EC 2.3.1.16
Acil-CoA
deidrogenasi
EC 1.3.3.6
EC 1.3.99.3
EC 1.3.99.13
FADH2
CH3
S
Acil-CoA (Cn-2)
O
H
CoA
CoA-SH
CH3
S
O
O
H
CoA
La reazione procede
S
ciclicamente fino a quando
β-chetoacil-CoA
l’acil-CoA è ridotto a due unità
NADH + H+
(Acetil-CoA) o tre unità
L-3-idrossiacil-CoA
(Propionil-CoA) carboniose.
deidrogenasi
EC 1.1.1.35
NAD+
trans-∆2-enoil-CoA
CH3
H 2O
O
Enoil-CoA idratasi
EC 4.2.1.17
OH
CoA
CH3
S
L-β-idrossiacil-CoA
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 59 -
β-ossidazione acidi grassi
•
•
La strategia della β-ossidazione
consiste nel generare un
nuovo carbonile in β a seguito
della rotture del legame tra Cα
e Cβ.
Tale sequenza di reazioni
produce:
–
–
–
–
•
Un Acetil-CoA
Un Acil-CoA più corto di due
unità carboniose.
Un FADH2
Un NADH
O
FAD
CoA
CH3
S
Acil-CoA (Cn)
O
CoA
O
S
CH3
CoA
3-Chetotiolasi
EC 2.3.1.16
Acil-CoA
deidrogenasi
EC 1.3.3.6
EC 1.3.99.3
EC 1.3.99.13
FADH2
CH3
S
Acil-CoA (Cn-2)
O
H
CoA
CoA-SH
CH3
S
O
O
H
CoA
La reazione procede
S
ciclicamente fino a quando
β-chetoacil-CoA
l’acil-CoA è ridotto a due unità
NADH + H+
(Acetil-CoA) o tre unità
L-3-idrossiacil-CoA
(Propionil-CoA) carboniose.
deidrogenasi
EC 1.1.1.35
NAD+
trans-∆2-enoil-CoA
CH3
H 2O
O
Enoil-CoA idratasi
EC 4.2.1.17
OH
CoA
S
CH3
L-β-idrossiacil-CoA
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 60 -
30
β-ossidazione acidi grassi
•
•
La strategia della β-ossidazione
consiste nel generare un
nuovo carbonile in β a seguito
della rotture del legame tra Cα
e Cβ.
Tale sequenza di reazioni
produce:
–
–
–
–
•
Un Acetil-CoA
Un Acil-CoA più corto di due
unità carboniose.
Un FADH2
Un NADH
La reazione procede
ciclicamente fino a quando
l’acil-CoA è ridotto a due
unità (Acetil-CoA) o tre
unità (Propionil-CoA)
carboniose.
O
FAD
CoA
CH3
S
Acil-CoA (Cn)
O
CoA
O
S
CH3
CoA
3-Chetotiolasi
EC 2.3.1.16
Acil-CoA
deidrogenasi
EC 1.3.3.6
EC 1.3.99.3
EC 1.3.99.13
FADH2
CH3
S
Acil-CoA (Cn-2)
O
H
CoA
CoA-SH
O
H
CoA
S
CH3
S
O
trans-∆2-enoil-CoA
CH3
β-chetoacil-CoA
H 2O
NADH + H+
L-3-idrossiacil-CoA
deidrogenasi
EC 1.1.1.35
NAD+
O
Enoil-CoA idratasi
EC 4.2.1.17
OH
CoA
S
CH3
L-β-idrossiacil-CoA
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 61 -
Destino dei prodotti
• I prodotti della β-ossidazione:
– Acetil-CoA e corpi chetonici: entrano nel
ciclo di Krebs per produrre equivalenti
riducenti (NADH e FADH2) che alimentano la
fosforilazione ossidativa per la produzione di
ATP.
– Un Acil-CoA più corto di due unità
carboniose: rientra nel ciclo successivo di βossidazione.
– FADH2 e NADH che alimentano la
fosforilazione ossidativa per la produzione di
ATP.
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 62 -
31
β-ossidazione acidi grassi
• In tutto quattro attività
enzimatiche catalizzano
il processo ciclico:
– Una deidrogenasi
riduce il legame CαCβ
a doppio legame,
– Una idratasi addiziona
acqua in trans per
formare un enolo
– Un’altra deidrogenasi
riduce il gruppo OH a
carbonile ed infine
– Una tiolasi permette la
rottura del legame
CαCβ per formare
Acetil-CoA e Acil-CoA
più corto di due unità.
B12 - v. 1.6.2 © gsartor 2001-2017
O
FAD
CoA
CH3
S
Acil-CoA (Cn)
O
CoA
O
S
CH3
CoA
3-Chetotiolasi
EC 2.3.1.16
Acil-CoA
deidrogenasi
EC 1.3.3.6
EC 1.3.99.3
EC 1.3.99.13
FADH2
CH3
S
Acil-CoA (Cn-2)
O
H
CoA
CoA-SH
O
H
CoA
S
CH3
S
O
trans-∆2-enoil-CoA
CH3
β-chetoacil-CoA
H 2O
NADH + H+
L-3-idrossiacil-CoA
deidrogenasi
EC 1.1.1.35
NAD+
O
Enoil-CoA idratasi
EC 4.2.1.17
OH
CoA
CH3
S
L-β-idrossiacil-CoA
Metabolismo dei grassi
- 63 -
β-ossidazione acidi grassi
• In tutto quattro attività
enzimatiche catalizzano
il processo ciclico:
– Una deidrogenasi
riduce il legame CαCβ
a doppio legame,
– Una idratasi addiziona
acqua in trans per
formare un enolo
– Un’altra deidrogenasi
riduce il gruppo OH a
carbonile ed infine
– Una tiolasi permette la
rottura del legame
CαCβ per formare
Acetil-CoA e Acil-CoA
più corto di due unità.
B12 - v. 1.6.2 © gsartor 2001-2017
O
FAD
CoA
CH3
S
Acil-CoA (Cn)
O
CoA
O
S
CH3
CoA
3-Chetotiolasi
EC 2.3.1.16
Acil-CoA
deidrogenasi
EC 1.3.3.6
EC 1.3.99.3
EC 1.3.99.13
FADH2
CH3
S
Acil-CoA (Cn-2)
O
H
CoA
CoA-SH
O
H
CoA
S
CH3
S
O
trans-∆2-enoil-CoA
CH3
β-chetoacil-CoA
H 2O
NADH + H+
L-3-idrossiacil-CoA
deidrogenasi
EC 1.1.1.35
NAD+
O
Enoil-CoA idratasi
EC 4.2.1.17
OH
CoA
S
CH3
L-β-idrossiacil-CoA
Metabolismo dei grassi
- 64 -
32
β-ossidazione acidi grassi
• In tutto quattro attività
enzimatiche catalizzano
il processo ciclico:
– Una deidrogenasi
riduce il legame CαCβ
a doppio legame,
– Una idratasi addiziona
acqua in trans per
formare un enolo
– Un’altra deidrogenasi
riduce il gruppo OH a
carbonile ed infine
– Una tiolasi permette la
rottura del legame
CαCβ per formare
Acetil-CoA e Acil-CoA
più corto di due unità.
B12 - v. 1.6.2 © gsartor 2001-2017
O
FAD
CoA
CH3
S
Acil-CoA (Cn)
O
CoA
O
S
CH3
CoA
3-Chetotiolasi
EC 2.3.1.16
Acil-CoA
deidrogenasi
EC 1.3.3.6
EC 1.3.99.3
EC 1.3.99.13
FADH2
CH3
S
Acil-CoA (Cn-2)
O
H
CoA
CoA-SH
O
H
CoA
S
CH3
S
O
trans-∆2-enoil-CoA
CH3
β-chetoacil-CoA
H 2O
NADH + H+
L-3-idrossiacil-CoA
deidrogenasi
EC 1.1.1.35
NAD+
O
Enoil-CoA idratasi
EC 4.2.1.17
OH
CoA
CH3
S
L-β-idrossiacil-CoA
Metabolismo dei grassi
- 65 -
β-ossidazione acidi grassi
• In tutto quattro attività
enzimatiche catalizzano
il processo ciclico:
– Una deidrogenasi
riduce il legame CαCβ
a doppio legame,
– Una idratasi addiziona
acqua in trans per
formare un enolo
– Un’altra deidorgenasi
riduce il gruppo OH a
carbonile ed infine
– Una tiolasi permette la
rottura del legame
CαCβ per formare
Acetil-CoA e Acil-CoA
più corto di due unità.
B12 - v. 1.6.2 © gsartor 2001-2017
O
FAD
CoA
CH3
S
Acil-CoA (Cn)
O
CoA
O
S
CH3
CoA
3-Chetotiolasi
EC 2.3.1.16
Acil-CoA
deidrogenasi
EC 1.3.3.6
EC 1.3.99.3
EC 1.3.99.13
FADH2
CH3
S
Acil-CoA (Cn-2)
O
H
CoA
CoA-SH
O
H
CoA
S
trans-∆2-enoil-CoA
CH3
β-chetoacil-CoA
H 2O
NADH + H+
L-3-idrossiacil-CoA
deidrogenasi
EC 1.1.1.35
NAD+
CH3
S
O
O
Enoil-CoA idratasi
EC 4.2.1.17
OH
CoA
S
CH3
L-β-idrossiacil-CoA
Metabolismo dei grassi
- 66 -
33
β-ossidazione acidi grassi
• In tutto quattro attività
enzimatiche catalizzano
il processo ciclico:
– Una deidrogenasi
riduce il legame CαCβ
a doppio legame,
– Una idratasi addiziona
acqua in trans per
formare un enolo
– Un’altra deidorgenasi
riduce il gruppo OH a
carbonile ed infine
– Una tiolasi permette la
rottura del legame
CαCβ per formare
Acetil-CoA e Acil-CoA
più corto di due unità.
B12 - v. 1.6.2 © gsartor 2001-2017
O
FAD
CoA
CH3
S
Acil-CoA (Cn)
O
CoA
O
S
CH3
CoA
3-Chetotiolasi
EC 2.3.1.16
Acil-CoA
deidrogenasi
EC 1.3.3.6
EC 1.3.99.3
EC 1.3.99.13
FADH2
CH3
S
Acil-CoA (Cn-2)
O
H
CoA
E il ciclo si ripete
CoA-SH
O
H
CoA
S
CH3
S
O
trans-∆2-enoil-CoA
CH3
β-chetoacil-CoA
H 2O
NADH + H+
L-3-idrossiacil-CoA
deidrogenasi
EC 1.1.1.35
NAD+
O
Enoil-CoA idratasi
EC 4.2.1.17
OH
CoA
CH3
S
L-β-idrossiacil-CoA
Metabolismo dei grassi
- 67 -
β-ossidazione acidi grassi
• In tutto quattro attività
enzimatiche catalizzano
il processo ciclico:
– Una deidrogenasi
riduce il legame CαCβ
a doppio legame,
– Una idratasi addiziona
acqua in trans per
formare un enolo
– Un’altra deidrogenasi
riduce il gruppo OH a
carbonile ed infine
– Una tiolasi permette la
rottura del legame
CαCβ per formare
Acetil-CoA e Acil-CoA
più corto di due unità.
B12 - v. 1.6.2 © gsartor 2001-2017
O
FAD
CoA
CH3
S
Acil-CoA (Cn)
O
CoA
O
S
CH3
CoA
3-Chetotiolasi
EC 2.3.1.16
Acil-CoA
deidrogenasi
EC 1.3.3.6
EC 1.3.99.3
EC 1.3.99.13
FADH2
CH3
S
Acil-CoA (Cn-2)
O
H
CoA
CoA-SH
O
H
CoA
S
CH3
S
O
trans-∆2-enoil-CoA
CH3
β-chetoacil-CoA
H 2O
NADH + H+
L-3-idrossiacil-CoA
deidrogenasi
EC 1.1.1.35
NAD+
O
Enoil-CoA idratasi
EC 4.2.1.17
OH
CoA
S
CH3
L-β-idrossiacil-CoA
Metabolismo dei grassi
- 68 -
34
Acil-CoA deidrogenasi
EC 1.3.3.6 - EC 1.3.99.3 - EC 1.3.99.13
O
FAD
CoA
CH3
S
Acil-CoA (Cn)
O
CoA
O
S
CH
• Tre enzimi solubili nella matrice
CoA
S
mitocondriale con diversa 3-Chetotiolasi
specificità per
Acil-CoA (C
EC 2.3.1.16
acidi grassi con catena idrofobica
di diversa
CoA-SH
lunghezza (corti, medi e lunghi).
O
O
CoAgruppo
• Contengono un FAD come
CH
S
prostetico.
β-chetoacil-CoA
Acil-CoA
deidrogenasi
EC 1.3.3.6
EC 1.3.99.3
EC 1.3.99.13
3
FADH2
CH3
n-2)
O
H
CoA
CH3
S
H
trans- ∆2-enoil-CoA
3
NADH +
H2 O
H+
L-3-idrossiacil-CoA
deidrogenasi
EC 1.1.1.35
NAD+
O
Enoil-CoA idratasi
EC 4.2.1.17
OH
CoA
CH3
S
L-β-idrossiacil-CoA
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 69 -
Acil-CoA deidrogenasi
EC 1.3.3.6 - EC 1.3.99.3 - EC 1.3.99.13
• Il FAD viene ridotto a FADH2, gli elettroni vengono poi
convogliati alla catena respiratoria attraverso una flavoproteina
trasportatrice di elettroni (ETF) e al CoQ per formare CoQH2.
O
CoA
CH3
S
Acil-CoA (Cn)
FAD
ETFred
CoQ
FADH2
ETFox
CoQH2
EC 1.3.3.6
EC 1.3.99.3
EC 1.3.99.13
trans-∆2-enoil-CoA
O
H
CoA
CH3
S
H
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 70 -
35
Acil-CoA deidrogenasi
EC 1.3.3.6 - EC 1.3.99.3 - EC 1.3.99.13
• Meccanismo
O
H
O
H
H
H
H
CoA
HS
S
CH3
C
H
H
CH3
H
CH 3
H
B
B
+
FAD
H
O
O
H
CoA
CH 3
H
H
CoA
S
S
C
H
H
B
B12 - v. 1.6.2 © gsartor 2001-2017
EC 1.3.3.6
1IS2
+
Metabolismo dei grassi
- 71 -
β-ossidazione acidi grassi
• In tutto quattro attività
enzimatiche catalizzano
il processo ciclico:
– Una deidrogenasi
riduce il legame CαCβ
a doppio legame,
– Una idratasi addiziona
acqua in trans per
formare un enolo
– Un’altra deidrogenasi
riduce il gruppo OH a
carbonile ed infine
– Una tiolasi permette la
rottura del legame
CαCβ per formare
Acetil-CoA e Acil-CoA
più corto di due unità.
B12 - v. 1.6.2 © gsartor 2001-2017
O
FAD
CoA
CH3
S
Acil-CoA (Cn)
O
CoA
O
S
CH3
CoA
3-Chetotiolasi
EC 2.3.1.16
Acil-CoA
deidrogenasi
EC 1.3.3.6
EC 1.3.99.3
EC 1.3.99.13
FADH2
CH3
S
Acil-CoA (Cn-2)
O
H
CoA
CoA-SH
O
H
CoA
S
CH3
S
O
trans-∆2-enoil-CoA
CH3
β-chetoacil-CoA
H2O
NADH + H+
L-3-idrossiacil-CoA
deidrogenasi
EC 1.1.1.35
NAD+
O
Enoil-CoA idratasi
EC 4.2.1.17
OH
CoA
S
CH3
L-β-idrossiacil-CoA
Metabolismo dei grassi
- 72 -
36
β-ossidazione acidi grassi
O
• Idratazione stereo specifica.
CoA
• L’enoil-CoA idratasi catalizza l’idratazione S
Acil-CoA (Cn)
O
stereospecifica al doppio legame trans
CoA
O
producendo L-idrossiacil-CoA.
S
CH3
CoA
• Esamero.
S
3-Chetotiolasi
Acil-CoA (Cn-2)
• Due enzimi:
EC 2.3.1.16
• EC 4.2.1.17: maggiore affinità per enoil-CoA a corta
CoA-SH
catena.
O
O
CoA per enoil-CoA a lunga
• EC 4.2.1.74: maggiore affinità
CH3
S
catena.
β-chetoacil-CoA
FAD
CH3
Acil-CoA
deidrogenasi
EC 1.3.3.6
EC 1.3.99.3
EC 1.3.99.13
FADH2
CH3
O
S
CH3
H
trans- ∆2-enoil-CoA
H2 O
NADH + H+
L-3-idrossiacil-CoA
deidrogenasi
EC 1.1.1.35
NAD+
O
H
CoA
Enoil-CoA idratasi
EC 4.2.1.17
EC 4.2.1.74
OH
CoA
S
CH3
L-β-idrossiacil-CoA
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 73 -
Enoil-CoA idratasi EC 4.2.1.17
Esanoil-CoA
1MJ3
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 74 -
37
Enoil-CoA idratasi EC 4.2.1.17
++
O δ−
CoA
S
H
H
H
O
H
O
CoA
R
O
O
Glu144
O
Glu164
O
S
CoA
H
O
S
H
O
H
H
O
H
H
H
R
O
CoA
O
O
S
Glu144
H
O
O
O
Glu164
H
Glu144
H
O δ−
O
O
Glu164
R
Glu144
Glu164
O R
H
O
H
O
O
Glu144
O
Glu164
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 75 -
Enoil-CoA idratasi EC 4.2.1.17
++
O δ−
CoA
S
H
H
H
O
H
O
CoA
R
O
O
Glu144
O
Glu164
O
S
CoA
H
H
O
O
S
H
O
H
H
H
H
R
O
CoA
H
O
O
O
Glu164
H
Glu144
O
O
S
Glu144
Glu164
H
O δ−
O
O
R
Glu164
O R
Glu144
H
O
H
O
O
Glu144
O
Glu164
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 76 -
38
β-ossidazione acidi grassi
• In tutto quattro attività
enzimatiche catalizzano
il processo ciclico:
– Una deidrogenasi
riduce il legame CαCβ
a doppio legame,
– Una idratasi addiziona
acqua in trans per
formare un enolo
– Un’altra deidrogenasi
riduce il gruppo OH a
carbonile ed infine
– Una tiolasi permette la
rottura del legame
CαCβ per formare
Acetil-CoA e Acil-CoA
più corto di due unità.
B12 - v. 1.6.2 © gsartor 2001-2017
O
FAD
CoA
CH3
S
Acil-CoA (Cn)
O
CoA
O
S
CH3
CoA
3-Chetotiolasi
EC 2.3.1.16
Acil-CoA
deidrogenasi
EC 1.3.3.6
EC 1.3.99.3
EC 1.3.99.13
FADH2
CH3
S
Acil-CoA (Cn-2)
O
H
CoA
CoA-SH
O
H
CoA
S
CH3
S
O
trans-∆2-enoil-CoA
CH3
β-chetoacil-CoA
H2O
NADH + H+
L-3-idrossiacil-CoA
deidrogenasi
EC 1.1.1.35
NAD+
O
Enoil-CoA idratasi
EC 4.2.1.17
OH
CoA
CH3
S
L-β-idrossiacil-CoA
Metabolismo dei grassi
- 77 -
β-ossidazione acidi grassi
• L’enzima L-3-idrossiacil-CoA deidrogenasi
catalizza
O
FAD
CoA
Acil-CoA
l’ossidazione di L-β-idrossiacil-CoA.
CH
deidrogenasi
S
EC 1.3.3.6
• È un enzima specifico per l’isomero
L. Acil-CoA (C )
O
EC 1.3.99.3
CoA
O
EC 1.3.99.13
• Il NADH prodotto entra nellaS catena
respiratoria a livello del
CH
FADH
CoA
complesso I.
CH
S
3
n
3
2
3
3-Chetotiolasi
EC 2.3.1.16
Acil-CoA (Cn-2)
O
H
CoA
CoA-SH
O
H
CoA
S
CH3
S
O
trans-∆2-enoil-CoA
CH3
β-chetoacil-CoA
H2O
NADH + H+
L-3-idrossiacil-CoA
deidrogenasi
EC 1.1.1.35
NAD+
O
Enoil-CoA idratasi
EC 4.2.1.17
OH
CoA
S
CH3
L-β-idrossiacil-CoA
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 78 -
39
L-3-idrossiacil-CoA deidrogenasi EC 1.1.1.35
CoA
S
His
O
H N
O
H
N
+
δ−
H
-
NH2
H NH2
O
NAD+
O
O
O
O
O P O P O
O
O
+
N
CH3
O
OH
HO
Glu
N
N
N
N
O
HO
H
OH
Gly
CoA
S
His
O
H N
N
H
O
N
CH3
OH
HO
Glu
O
O
O P O P O
O
O
O
N
N
NADH
O
O
O
NH2
H H NH2
+
N
N
O
OH
HO
H
Gly
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 79 -
β-ossidazione acidi grassi
• In tutto quattro attività
enzimatiche catalizzano
il processo ciclico:
– Una deidrogenasi
riduce il legame CαCβ
a doppio legame,
– Una idratasi addiziona
acqua in trans per
formare un enolo
– Un’altra deidrogenasi
riduce il gruppo OH a
carbonile ed infine
– Una tiolasi permette la
rottura del legame
CαCβ per formare
Acetil-CoA e Acil-CoA
più corto di due unità.
B12 - v. 1.6.2 © gsartor 2001-2017
O
FAD
CoA
CH3
S
Acil-CoA (Cn)
O
CoA
O
S
CH3
CoA
3-Chetotiolasi
EC 2.3.1.16
Acil-CoA
deidrogenasi
EC 1.3.3.6
EC 1.3.99.3
EC 1.3.99.13
FADH2
CH3
S
Acil-CoA (Cn-2)
O
H
CoA
CoA-SH
O
H
CoA
S
CH3
S
O
trans-∆2-enoil-CoA
CH3
β-chetoacil-CoA
H2O
NADH + H+
L-3-idrossiacil-CoA
deidrogenasi
EC 1.1.1.35
NAD+
O
Enoil-CoA idratasi
EC 4.2.1.17
OH
CoA
S
CH3
L-β-idrossiacil-CoA
Metabolismo dei grassi
- 80 -
40
β-ossidazione acidi grassi
O
FAD
CoA
CH3
S
Acil-CoA (Cn)
O
CoA
O
S
CH3
CoA
3-Chetotiolasi
EC 2.3.1.16
Acil-CoA
deidrogenasi
EC 1.3.3.6
EC 1.3.99.3
EC 1.3.99.13
FADH2
CH3
S
Acil-CoA (Cn-2)
O
H
CoA
CoA-SH
O
H
CoA
S
CH3
S
O
trans-∆2-enoil-CoA
CH3
β-chetoacil-CoA
H2O
NADH + H+
Enoil-CoA idratasi
• La chetotiolasi catalizza la scissione delO β-chetoacil-CoA.
OH
EC 4.2.1.17
CoA di carbonio più corto.
• Si produce un Acil-CoA di due atomi
CH
S
• Il ciclo ricomincia.
L-β-idrossiacil-CoA
L-3-idrossiacil-CoA
deidrogenasi
EC 1.1.1.35
NAD+
B12 - v. 1.6.2 © gsartor 2001-2017
3
Metabolismo dei grassi
- 81 -
3-Chetotiolasi EC 2.3.1.16
O
Cn
O
CoA
S
O
S
H
+
B
CoA
S
CH2
O
O
CoA
O
S
O
CH2-
CoA
S
H
+
B
H
S
S
+
B
O
O
CoA
S
S
B
B12 - v. 1.6.2 © gsartor 2001-2017
CH3
C2
Intermedio
enzima tioestere
Metabolismo dei grassi
- 82 -
41
3-Chetotiolasi EC 2.3.1.16
CoA
O
O
CoA
S
S
H
S
S
H
+
B
B
Intermedio
enzima tioestere
O
CoA
S
H
+
B
B12 - v. 1.6.2 © gsartor 2001-2017
S
Metabolismo dei grassi
Cn-2
- 83 -
3-Chetotiolasi EC 2.3.1.16
Arg
Cys
1AWF
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 84 -
42
Stechiometria
• Per ogni ciclo si producono:
– NADH che equivale a 2.5 moli di ATP prodotte nella catena
respiratoria.
– FADH2 che equivale a 1.5 moli di ATP prodotte nella catena
respiratoria.
• Per la degradazione dell’acido palmitico (C16):
CH3-(CH2)14-CO-S-CoA + 7FAD + 7NAD+ + 7H2O + 7CoASH →
→ 8CH3-CO-S-CoA + 7FADH2 + 7NADH + 7H+
7FADH2 + 10.5Pi + 10.5ADP + 3.5O2 →
7FAD + 17.5H2O + 10.5ATP 320 kJ·mol-1
7NADH + 7H+ + 17.5Pi + 17.5ADP + 3.5O2 →
7NAD+ + 24.5H2O + 17.5ATP 534 kJ·mol-1
8CH3-CO-S-CoA + 16O2 + 80Pi + 80ADP →
→ 8 CoA + 88H2O + 16CO2 + 80ATP 2440 kJ·mol-1
CH3-(CH2)14-CO-S-CoA + 108Pi +108ADP +23O2 →
→ 108ATP + 16 CO2 + 130H2O + CoASH
3294 kJ·mol-1
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 85 -
Stechiometria
• Per ogni ciclo si producono:
– NADH che equivale a 2.5 moli di ATP prodotte nella catena
respiratoria.
– FADH2 che equivale a 1.5 moli di ATP prodotte nella catena
respiratoria.
• Per la degradazione dell’acido palmitico (C16):
CH3-(CH2)14-CO-S-CoA + 7FAD + 7NAD+ + 7H2O + 7CoASH →
→ 8CH3-CO-S-CoA + 7FADH2 + 7NADH + 7H+
7FADH2 + 10.5Pi + 10.5ADP + 3.5O2 →
7FAD + 17.5H2O + 10.5ATP 320 kJ·mol-1
+
7NADH + 7H + 17.5Pi + 17.5ADP + 3.5O2 →
7NAD+ + 24.5H2O + 17.5ATP 534 kJ·mol-1
8CH3-CO-S-CoA + 16O2 + 80Pi + 80ADP →
→ 8 CoA + 88H2O + 16CO2 + 80ATP 2440 kJ·mol-1
CH3-(CH2)14-CO-S-CoA + 108Pi +108ADP +23O2 →
→ 108ATP + 16 CO2 + 130H2O + CoASH
3294 kJ·mol-1
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 86 -
43
Rendimento
• Combustione dell’acido palmitico:
CH3-(CH2)14-COOH + O2 → CO2 + H2O
∆G°’ = -9790 kJ·mol-1
• Ossidazione dell’acido palmitico e respirazione cellulare:
CH3-(CH2)14-COOH + O2 → CO2 + H2O
(108 – 2)·ATP = ∆G°’ = -3233 kJ·mol-1
Efficienza = 3233/9790 = 33%
• Produzione di 130 H2O metabolica per mole di acido
palmitico che viene β-ossidato.
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 87 -
Pari e dispari
• Dalla β-ossidazione di acidi grassi con
atomi si carbonio pari (n) si formano
n/2 acetil-CoA attraverso (n/2 – 1) cicli
di reazioni.
• Dalla β-ossidazione di acidi grassi con
atomi si carbonio dispari (n) si formano
n/2-1 acetil-CoA + 1 propionil-CoA da
(n/2-1) cicli di reazioni.
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 88 -
44
Acidi grassi dispari
D-Metilmalonil-CoA
Propionil-CoA
Acil-CoA
β-ossidazione
Propionil-CoA
carbossilasi
O
H3C
S
CoA
O
H3C
S
O
O
ATP + CO2 + H2O
Metilmalonil-CoA
epimerasi
O
n/2
H3C
CoA
S
O
O
S
Metilmalonil-CoA
mutasi
O
S
O
CoA
CH3
L-Metilmalonil-CoA
Succinil-CoA
B12 - v. 1.6.2 © gsartor 2001-2017
O
CoA
O
CoA
Metabolismo dei grassi
- 89 -
Acidi grassi monoinsaturi
Oleil-CoA (C18∆9)
cis-∆3-dodecanoil-CoA
3 x β-ossidazione
O
H3C
6
6
S
H3C
CoA
S
6
O
3
OH
H3C
S
CoA
Enoil-CoA
isomerasi
H2O
O
S
6
H3C
CoA
O
CoA
Enoil-CoA
idratasi
6 x β-ossidazione
O
H3C
6
S
CoA
trans-∆3-dodecanoil-CoA
O
6
H3C
B12 - v. 1.6.2 © gsartor 2001-2017
S
CoA
Metabolismo dei grassi
- 90 -
45
Acidi grassi polinsaturi
Linoeil-CoA (C18∆9∆12)
cis-∆3-cis-∆3-dodecanoil-CoA
O
H3C
4
3 x β-ossidazione
CoA
S
6
S
H 3C
4
O
3
H 3C
S
H 2O
O
S
4
Enoil-CoA
isomerasi
CoA
cis-∆4-decanoil-CoA
H3C
CoA
β-ossidazione Enoil-CoA
idratasi
NADPH + H+
O
H3C
CoA
4
S
trans-∆3-cis-∆6-dodecanoil-CoA
NADP+
trans-∆3-decanoil-CoA
O
H 3C
4
S
CoA
H 3C
Dienoil-CoA
reduttasi
trans-∆2-cis-∆4-decanoil-CoA
S
4
B12 - v. 1.6.2 © gsartor 2001-2017
H 3C
CoA
O
H 2O
O
5
CoA
O
S
CoA
4 x β-ossidazione
Enoil-CoA
idratasi
Metabolismo dei grassi
- 91 -
Perossisomi
• La β-ossidazione avviene in molte strutture subcellulari,
in particolare nei perossisomi.
• Sono deputati alla formazione di H2O2 che viene
utilizzata come sistema di difesa da batteri, virus, ecc.
• L’accettore di elettroni della acil-CoA ossidasi è il FAD:
FAD → FADH2
FADH2 + O2 → FAD + H2O2
2 H2O2 → H2O + O2
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 92 -
46
ω-ossidazione
• Nel reticolo endoplasmatico può avvenire la ω-ossidazione.
O
O
O
O
n
CH3
O
O
n
OH
O
n
O
• Catalizzata da enzimi che appartengono alla classe delle
ossidasi miste (CytP450, CYP)
• Provocano una idrossilazione e quindi una ossidazione.
• È un processo aspecifico che converte molecole lipofile in
prodotti più idrosolubili più facili da eliminare.
• È un processo che detossifica le cellule da molecole lipofile.
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 93 -
Struttura del CYP (1PO5)
AA basici
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 94 -
47
Struttura del CYP (1PO5)
Cys436
AA basici
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 95 -
Struttura del CYP (1PO5)
Cys436
AA basici
Cavità
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 96 -
48
Ciclo del CYP
RH (substrato)
(prodotto) ROH
Fe3+H2O
e-
Fe3+RH
Fe3+ROH
H2O
H2O
Fe2+RH
O2
FeO3+RH
NAD(P)H-citocromo
P450 reduttasi
[Fe2+O2RH]-1
e-
H2O
H+
H+
[Fe2+OOHRH]-1
[Fe2+O2RH]-2
citocromo b5
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
Meccanismo
ciclico del CYP
- 97 -
O
O
OH
H
R
H2O
O
N
N
Fe
H
H
O
N
3+
H
ROH
N
3+
N
N
H2O
RH
N
Fe
RH
N
N
Fe
N
II
N
S
S
S
N
3+
I
RH
2-
O
e-
.
+
VII
N
N
Fe
N
4+
A
N
H2O2
S
H2O
H+
HO
VI
RH
RH
H+
N
-
N
O
N
3+
2+
N
III
N
S
N
Fe
N
Fe
N
S
H
RH
2-
H+
O
N
3+
N
O
O
Fe
S
O2
RH
N
N
N
V
RH
O
O
O
3+
N
e-
Fe
N
N
N
N
S
Fe
2+
N
N
O
S
IV
N
2+
N
Fe
N
N
S
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 98 -
49
Meccanismo ciclico
del CYP
O
O
OH
H
R
P450 acquo Fe3+
(basso spin)
Lega RH
II. P450 canfora Fe3+
(alto spin)
VII
entra 1e-, riduzione
a Fe2+
III. P450 canfora Fe2+
Lega O2
VI
IV. P450 con O2
legato, equivalente
a Fe3+-O2entra 1e-, riduzione
a O22V. P450 perossido
I.
N
N
N
Fe
H
H
O
N
3+
H
ROH
H2O
O
N
Fe
N
H2O
RH
3+
N
RH
N
Fe
N
II
N
S
S
S
N
3+
N
I
O
RH
2-
e-
.
+
N
N
4+
N
Fe
A
N
H2O 2
S
H2O
H+
RH
RH
H+
HO
N
-
N
O
Fe
N
Fe
N
III
N
S
N
3+
N
2+
N
S
RH
2-
H+
O
N
O
N
3+
N
N
Fe
N
N
S
-
RH
O
O
O
Fe
N
3+
N
N
2+
N
S
e-
H
O2
RH
O
N
Fe
N
O
S
V
IV
N
N
2+
Fe
N
N
S
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
Meccanismo ciclico
del CYP
O
OH
H
R
H2O
O
N
1H+
Entra
VI. P450
idroperossido
Entra 1H+ esce
H2O
VII. P450 Fe4+ O2catione radicale
sulla proteina
si forma ROH
- 99 -
N
Fe
H
H
O
N
3+
H
ROH
N
N
N
Fe
H2O
RH
3+
N
RH
N
N
Fe
N
II
N
S
S
S
N
3+
I
O
RH
2-
e-
.
+
VII
N
N
4+
N
Fe
A
N
H2O 2
S
H2O
H+
HO
VI
RH
RH
H+
N
-
N
O
N
3+
2+
N
III
N
S
N
Fe
N
Fe
N
S
A.
L’idroperossido VI
si può formare
per reazione di II
con H2O2
H
RH
2-
H+
O
N
N
O
O
Fe
S
3+
O2
RH
N
N
N
V
O
O
O
3+
N
e-
-
RH
Fe
N
N
N
2+
N
S
Fe
N
N
O
S
IV
N
2+
N
Fe
N
N
S
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 100 -
50
Meccanismo
• L’ossigeno è legato non ad angolo retto.
• Il legame dell’ossigeno allontana il ligando
(RH) solo dopo che I due atomi di ossigeno si
sono ridotti il ligando si riavvicina. Ciò
previene la formazione di ROS.
• Gli elettroni per la riduzione dell’ossigeno so
forniti da una proteina Fe-S (P450 batterica o
mitcondriale) o da una NADPH-citocromo P450
ossidoreduttasi
FAD/FMN
dipendente
(microsomi).
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 101 -
Meccanismo generale del CYP
H2O
NADP+
NADPH + H+
CYTP450
Reduttasi
FMNH2/FADH2
CYP Fe3+
CYTP450
Reduttasi
FMN/FAD
ROH
CYP Fe2+
RH
2H+ + O2
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 102 -
51
Metabolismo dei grassi
1. Demolizione dei trigliceridi
2. Catabolismo degli acidi grassi
3. Biosintesi
– degli acidi grassi e colesterolo
– dei lipidi complessi
4. Trasporto dei lipidi
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 103 -
Biosintesi degli acidi grassi
• La sintesi degli acidi grassi segue un percorso
diverso rispetto al catabolismo:
– Le catene di acidi grassi sono costruite per addizione
di unità di due atomi di carbonio derivate dal acetilCoA.
– Le unità di acetato sono attivate dalla formazione di
malonil-CoA.
– Gli intermedi della biosintesi sono legati a SH di
proteine (proteine trasportatrici di acili, ACP) e non a
CoA-SH.
– La sintesi avviene nel citoplasma mentre la
degradazione è mitocondriale.
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 104 -
52
Biosintesi degli acidi grassi
• Negli animali la sintesi è catalizzata da una serie di
enzimi componenti del complesso acido grasso sintasi
(EC 2.3.1.85 EC 2.3.1.86) mentre nelle piante e nei
batteri gli enzimi sono separati
• La biosintesi usa come sistema redox il NADP+/NADPH
(la degradazione usa il sistema NAD+/NADH).
• L’addizione dell’unità C2 è alimentata dal ∆G negativo
della decarbossilazione del malonil-CoA.
• L’allungamento è ripetuto fino alla formazione di C16
(Acido palmitico).
• Altri enzimi catalizzano la ramificazione e
l’insaturazione.
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 105 -
Strategia
Acetil-CoA
Malonil-CoA
CO2
O
O
H3C
S
O
CoA
S
O
CoA
CO2
Acetil-ACP
O
H3 C
ACP
S
CO2
O
O
6
S
O
CH3
CoA
O
O
CH3
S
Dopo sette cicli
EC 2.3.1.85
EC 2.3.1.86
O
S
ACP
ACP
O
CH3
O
(CH2)14
NADPH
NADP+
INVERSO DELLA β-OSSIDAZIONE
H2O
NADPH
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
NADP+
- 106 -
53
Energia
• La spinta è il potere riducente del
NADPH
Acetil-CoA + 7 Malonil-CoA + 14 NADPH + 14H+ →
→ Palmitoil-CoA + 7 HCO3- + 7 CoA-SH + 14 NADP+
Formazione di esteri
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 107 -
Quindi:
• Per produrre acidi grassi, nel citoplasma servono:
– Acetil-CoA
– Malonil-CoA
• (Acetil-CoA + CO2 → Malonil-CoA)
– Equivalenti riducenti come NADPH
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 108 -
54
Il trasporto
Acido
Grasso
Acil-CoA
Acil-carnitina
β-ossidazione
Aminoacidi
Acil-carnitina
Citrato
Acetil-CoA
Ossalcetato
Acetil-CoA
Citrato
Citrato
sintasi
ATP-citrato
liasi
Ossalcetato
Citrato
Ciclo
di Krebs
NAD+
Malato
deidrogenasi
NADH
NAD+
Malato
Malato
deidrogenasi
Acidi
grassi
NADH
Malato
Malato
NADP+
CO2
Enzima
malico
ADP + Pi
NADH
Piruvato
carbossilasi
Piruvato
deidrogenasi
NAD+
NADPH
CO2
ATP
Piruvato
CO2
Piruvato
Piruvato
NADH
MATRICE
MITOCONDRIALE
LATO
CITOPLASMA
Glicolisi
NAD+
Glucosio
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 109 -
Formazione di malonil-CoA
O
H3C
O
O
S
CoA
O
+ ATP +
HO
O
Acetil-CoA
Acetil-CoA
carbossilasi
EC 6.4.1.2
O
S
CoA
+ ADP + Pi +H+
Malonil-CoA
• L’acetil-CoA carbossilasi (ACC) è un enzima biotina dipendente
che funziona in modo simile alla piruvato carbossilasi,
• Non fa parte del complesso acido grasso sintasi,
• Ha un meccanismo a ping-pong:
ATP
HCO3-
E-biotina
B12 - v. 1.6.2 © gsartor 2001-2017
ADP
Pi
Acetil-CoA
E-carbossibiotina
Metabolismo dei grassi
Malonil-CoA
E-biotina
- 110 -
55
Acetil-CoA carbossilasi (EC 6.4.1.2)
• Ha un peso molecolare da 4000 a 8000 kD è formata da
monomeri di 230 kD
• Ogni subunità contiene le attività per:
–
–
–
–
Il trasporto della carbossibiotina,
La biotina carbossilasi
La transcarbossilasi
I siti di regolazione allosterica
• La forma polimerica è attiva, i singoli monomeri non sono
attivi.
• L’equilibrio:
Monomeri inattivi ↔ polimero attivo
• È regolato dal prodotto (palmitoil-CoA) che lo sposta verso i
monomeri, mentre il citrato lo sposta verso il polimero.
• Gli effetti allosterici sono regolati dalla fosforilazione.
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 111 -
Acetil-CoA carbossilasi (EC 6.4.1.2)
• Possiede numerosi siti di fosforilazione,
• È fosforilata da una chinasi e defosforilata da una fosfatasi.
• La ACC defosforilata è attivata da bassa concentrazione di
citrato ed inibita da alta concentrazione di (grasso) acil-CoA,
al contrario la ACC fosforilata attivata da alta concentrazione
di citrato e inibita da bassa concentrazione di (grasso) acilCoA.
?
Protein chinasi
calmodulina
dipendente
P
P
23 25
Caseina
chinasi II
Protein chinasi
cAMP dipendente
Protein chinasi C
Protein chinasi
AMP dipendente
P
P P
P
29
76 77
95
Protein chinasi C
Protein chinasi
cAMP dipendente
AMP-protein chinasi
P
1
B12 - v. 1.6.2 © gsartor 2001-2017
1200
Metabolismo dei grassi
2345
- 112 -
56
Acetil-CoA carbossilasi (EC 6.4.1.2)
OH
• È un enzima a biotina
S
O
CH3
H3 C
NH
HN
O
• La biotina si lega ad una lisina nel sito attivo dell’enzima
formando un lungo braccio flessibile ad una estremità del quale
vi è il sito di carbossilazione.
Lisina
O
O
S
B12 - v. 1.6.2 © gsartor 2001-2017
NH
H
NH
HN
Sito di carbossilazione
N
CH 3
H3C
Legame
ε-peptidico
O
Metabolismo dei grassi
- 113 -
Acetil-CoA carbossilasi (EC 6.4.1.2)
ATP
• Il lungo braccio flessibile
permette il movimento
della biotina tra il sito di
carbossilazione e il sito di
decarbossilazione e
formazione del malonilCoA.
• La carbossilazione
avviene ad opera di
carbossifosfato che si
forma nel sito di
carbossilazione per
reazione di ATP e
bicarbonato.
HCO3
Biotina
Carbossifosfato
O
ADP
O
O
P
O
HN
O
NH
CH3
O
O
O
O
P
O
O
H
O
S Carbossibiotina
H3C
N
O
NH
CH3
N
H
O
O
N
O
H
N
H
O
O
N
H
N
H
S
CH3
H3C
N
O
Metabolismo dei grassi
N
O
O
B12 - v. 1.6.2 © gsartor 2001-2017
S
H3 C
O
NH
O
- 114 -
57
Acetil-CoA carbossilasi (EC 6.4.1.2)
O
O
N
H
N
H
S
CH3
H3C
CoA
• La decarbossilazione e
formazione di malonil-CoA
avviene nel secondo sito
della Acetil-CoA carbossilasi
dove si lega acetil-CoA per
formare malonil-CoA.
O
O
O
O
H3 C
O
N
N
H
H
S
CoA
S
CH3
H3C
O
O
B12 - v. 1.6.2 © gsartor 2001-2017
NH
N
O
S
HN
NH
O
O
Metabolismo dei grassi
- 115 -
Formazione di Acetil-ACP
Acetil-CoA
Malonil-CoA
CO2
O
O
H3C
S
CoA
S
O
O
S
ACP
CO2
O
O
6
S
O
CoA
CO2
Acetil-ACP
H3C
O
• La reazione è catalizzata
da [ACP]acetiltransferasi
(EC 2.3.1.38),
• Per il malonil-CoA invece
vi è una
[ACP]maloniltransferasi
(EC 2.3.1.39)
CH3
CoA
O
O
CH3
S
ACP
Dopo sette cicli
O
S
ACP
O
CH3
O
(CH2)14
NADPH
NADP+
INVERSO DELLA β-OSSIDAZIONE
H2O
NADPH
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
NADP+
- 116 -
58
Acyl Carrier Protein (ACP)
• Il legame avviene attraverso la Ser terminale
che lega il gruppo prostetico:
O
H
S
O
H
N
N
H
H
CH3
O
O
CH3
OH
O
P
ACP
O
Fosfopanteina
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 117 -
Strategia
CO2
O
H3 C
O
O
Acetil-CoA
S
CoA
S
O
CoA
Malonil-CoA
CO2
O
Acetil-ACP
H3 C
S
ACP
CO2
O
6 Malonil-CoA
CoA
S
O
CH3
β-chetoacil-ACP
sintetasi
EC 2.3.1.41
O
6
O
O
S
Palmitoil-ACP
ACP
Dopo sette cicli
S
CH3
O
(CH2)14
O
NADP+
O
CH3
O
(CH2) 14
Acetoacetil-ACP
β-chetoacil [ACP]
reduttasi
EC 1.1.1.100
ACP
S
Butirril-ACP
Acil-ACP-idrolasi
EC 3.1.2.14
ACP
Acido grasso sintasi
EC 2.3.1.85
EC 2.3.1.86
CH3
Enoil-[ACP] reduttasi
NADPH EC 1.3.1.10
NADH EC 1.3.1.9
CH3
NADPH
β-idrossibutirril
[ACP] deidratasi
EC 4.2.1.58
H
H
Palmitato
O
ACP
Crotonil-ACP
NADP+
CH3
HO
H
O
S
H2O
S
NADPH
ACP
D-idrossibutirril-ACP
(nella β-ossidazione
L-idrossienoil-CoA)
INVERSO DELLA β-OSSIDAZIONE
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 118 -
59
Acido grasso sintasi
Subunità α
• Il meccanismo è lo
stesso sia per gli
organismi superiori
che per i batteri che
le piante,
• È diversa
l’organizzazione degli
enzimi:
– Nel lievito e nelle
piante il complesso
acido grasso sintasi è
un complesso
enzimatico α6β6.
Enzima di
Condensazione
(Chetoacil-ACP-sintasi)
B-chetoacil
ACP-reduttasi
Acetiltransferasi
Maloniltransferasi
β-idrossialcil
deidratasi
Enoilreduttasi
Subunità β
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 119 -
Acido grasso sintasi
• Il meccanismo è lo stesso
sia per gli organismi
superiori che per i batteri
che le piante,
• È diversa l’organizzazione
degli enzimi:
– Negli animali è un dimero
nel quale ognuno dei
monomeri contiene le
attività enzimatiche della
catena sintetica, i
monomeri sono organizzati
testa-coda in modo tale che
il prodotto di una catena di
reazioni entra nella
successiva catena di
reazioni
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 120 -
60
Acido grasso sintasi
Ingresso
dei substrati
Tioesterasi
β-idrossialcil
deidratasi
Dominio 1:
Legame e
condensazione
dell’acile e del
malonile
B-chetoacil
ACP-reduttasi
Allungamento
della catena
Enoilreduttasi
Maloniltransferasi
Dominio 2:
Riduzione degli
intermedi
Allungamento
della catena
Acetiltransferasi
Enzima di
Condensazione
(Chetoacil-ACP-sintasi)
Dominio 3:
Rilascio del palmitato
Ingresso
dei substrati
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 121 -
Meccanismo
AT KSasi AT
C2
C2
C3
C3
ACP
ACP
C2
C3
ACP
C1
C4
C4
ACP
C3
ACP
B12 - v. 1.6.2 © gsartor 2001-2017
C2 C
3
C2
Metabolismo dei grassi
ACP
ACP
- 122 -
61
Meccanismo
3-chetoacil-ACP sintasi
AT KSasi ATMalonil transferasi
Acetil transferasi
AT
KSasi
O
MT
AT
O
O
S
H
S
C2
O
H
H
KSasi
H
CH3
O
O
C2
H3C
CoA
S
C3
S
Acetil-CoA
O
H
AT
O
O
O
C3
S
H
CoA
MT
CH3
C2
ACPACP
O
O
H
S
C3
O
O
ACP
ACP
S
H
O
MT
KSasi
O
O
O
Malonil-CoA
S
ACP
ACP
AT
MT
KSasi
O
O
S
H
AT
CH3
H
O
H2O
H
H
MT
KSasi
O
S
H
NADPH
NADP+
S
NADP+
NADPH
C4
O
C2
ACP
C3
O
ACP
ACP
B12 - v. 1.6.2 © gsartor 2001-2017
S
H
O
O
O
CH3
O
S
ACP
C2 C
3
O
H
MT
KSasi
CH3
O
C4
O
AT
O
S
O
CH3
MT
KSasi
O
CO2
H
H
AT
C1
H
ACP
ACP
S
O
O
S
ACP
ACP
O
Metabolismo dei grassi
- 123 -
Meccanismo
3-chetoacil-ACP sintasi
Acetil transferasi
Malonil transferasi
AT
MT
KSasi
O
H
AT
O
S
H
H
KSasi
O
O
S
MT
AT
O
O
O
O
H3C
O
H
CoA
S
S
Acetil-CoA
O
H
S
H
H
CH3
O
O
CoA
O
S
ACP
S
O
O
H
O
CH3
MT
KSasi
O
ACP
O
Malonil-CoA
S
ACP
AT
KSasi
O
H
MT
O
S
H
CH3
AT
KSasi
O
H2O
H
H
MT
AT
O
O
S
H
H
CO2
H
CH3
KSasi
S
NADP+
NADPH
ACP
NADP+
NADPH
O
H
CH3
O
MT
KSasi
S
O
O
O
CH3
O
H
O
S
O
ACP
S
ACP
B12 - v. 1.6.2 © gsartor 2001-2017
AT
O
H
O
O
O
MT
S
Metabolismo dei grassi
O
S
ACP
O
- 124 -
62
Allungamento della catena
• L’allungamento della catena procede come inverso della
β-ossidazione dell’acile attraverso legame con CoA.
• A differenza della β-ossidazione l’enoil-CoA reduttasi usa
il NADPH invece del FADH2.
O
H3C
S
CoA
H
S
CoA
NADH + H+
O
R
O
S
CoA
O
R
OH
S
Tiolasi
Acil-CoA (Cn)
L-β-idrossiacil-CoA
NAD+
CoA
S
H
L-β-idrossiacil-CoA
deidrogenasi
β-chetoacil-CoA
O
R
Enoil-CoA
idratasi
NAPD+
H2O
NADPH + H+
O
H
O
R
S
R
CoA
Enoil-CoA
reduttasi
Acil-CoA (Cn+2)
CoA
S
CoA
H
α−β-trans-enoil-CoA
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 125 -
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 126 -
63
Mono insaturazione
• La singola insaturazione viene inserita nella catena acilica nel
processo di allungamento della catena del Acil-ACP.
• Nell’E. Coli agisce una β-idrossidecanoil-ACP idratasi che
elimina una molecola d’acqua dal D-b-idrossidecanoil-ACP
intermedio.
• Negli eucarioti la reazione avviene attraverso un’ossidazione
del prodotto finale (stearoil-CoA, C18) ad opera di O2 nel
reticolo endoplasmatico.
H 2O
1/2 O2
O
O
H3 C
16
S
H3 C
CoA
Stearoil-CoA (C18)
B12 - v. 1.6.2 © gsartor 2001-2017
7
S
7
CoA
Oleil-CoA (C18∆9)
Metabolismo dei grassi
- 127 -
Mono insaturazione
• La singola insaturazione viene inserita nella catena acilica nel
processo di allungamento della catena del Acil-ACP.
• Nell’E. Coli agisce una β-idrossidecanoil-ACP idratasi che
elimina una molecola d’acqua dal D-b-idrossidecanoil-ACP
intermedio.
• Negli eucarioti la reazione avviene attraverso un’ossidazione
del prodotto finale (stearoil-CoA, C18) ad opera di O2 nel
reticolo endoplasmatico.
2H+
NADH + H+
Cyt b5
reduttasi
(Fe++)
2 Cyt b5
(Fe++)
Desaturasi
(Fe+++)
O
H3C
7
7
S
CoA + H2O
Oleil-CoA (C18∆9)
NAD+
Cyt b5
reduttasi
(Fe+++)
2 Cyt b5
(Fe+++)
Desaturasi
(Fe++)
O
H3C
16
S
CoA
+ 1/2 O2 + 2H+
Stearoil-CoA (C18)
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 128 -
64
Poli insaturazione
O
O
Linoleato (C18- ∆9, 12)
CoA-SH + ATP
• La gestione degli acidi
grassi polinsaturi (PUFA)
è diversa nei diversi
organismi, quindi i
processi sono diversi a
seconda dell’organismo.
• Nei mammiferi:
Acil-CoA
sintetasi
AMP + PPi
O
S
CoA
Linoleil-CoA (C18- ∆9, 12-CoA)
Desaturazione
2H+
S
C18- ∆6, 9, 12-CoA
CoA
O
Malonil-CoA
Allungamento
CO2 + CoASH
S
C20- ∆8, 11, 14-CoA
CoA
O
Desaturazione
2H+
O
S
CoA
Arachidonoil-CoA (C20- ∆5, 8, 11, 14 -CoA)
H2O
CoASH
O
O
Arachidonato (C20- ∆5, 8, 11, 14)
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 129 -
Controllo e regolazione della biosintesi
• L’acetil-CoA ha un ruolo centrale della regolazione del
metabolismo degli acidi grassi e dei glucidi.
• L’acetil-CoA carbossilasi è regolata allostericamente dal
citrato (attivatore) e dagli acil-CoA (inibitore).
• Il malonil-CoA agisce invece come inibitore del trasporto
di Acil-CoA all’interno dei mitocondri a livello della
formazione dell’acil-carnitina.
• Vi è poi un azione di controllo a livello di interazione tra
gli organi mediata dagli ormoni attraverso le cascate
enzimatiche attivate dal cAMP.
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 130 -
65
Controllo e regolazione della biosintesi
Acido
Grasso
Acil-CoA
Acil-carnitina
β-ossidazione
Aminoacidi
Acil-carnitina
ACC
Citrato
Acetil-CoA
Ossalacetato
Citrato
sintasi
Acetil-CoA
Citrato
Malonil-CoA
ATP-citrato
liasi
Ossalacetato
Citrato
Ciclo
di Krebs
NADH
Malato
deidrogenasi
NADH
NAD+
Malato
deidrogenasi
Acil-CoA
NAD+
Malato
Malato
Malato
NADP+
CO2
Enzima
malico
ADP + Pi
NADH
Piruvato
carbossilasi
Piruvato
deidrogenasi
NAD+
NADPH
CO2
ATP
Piruvato
CO2
Piruvato
MATRICE
MITOCONDRIALE
Piruvato
NADH
LATO
CITOPLASMA
Glicolisi
NAD+
Glucosio
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 131 -
Controllo e regolazione della biosintesi
Ormone
(Adrenalina o glucagone)
Gα-GTP
Adenilato
ciclasi
(inattiva)
AMP
Adenilato ciclasi
(attiva)
ATP
Fosfodiesterasi
cAMP + PPi
Proteina
chinasi A
(inattiva)
Proteina
chinasi A
(attiva)
P
ATP
Fosforilasi chinasi
(b-inattiva)
Pi
ADP Fosforilasi chinasi
(a-attiva)
Fosfatasi
Acetil-CoA
Carbossilasi
(attiva a basso citrato)
ATP
ADP
Fosfatasi
P
Acetil-CoA
Carbossilasi
(attiva ad
alto citrato)
Pi
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 132 -
66
Metabolismo dei grassi
• Demolizione dei trigliceridi
• Catabolismo degli acidi grassi
• Biosintesi
– degli acidi grassi e colesterolo
– dei lipidi complessi
• Trasporto dei lipidi
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 133 -
Lipidi
• Semplici
– Sono molecole che non contengono legami
esterei o amidici
• Agidi grassi
• Colesterolo
• Complessi
– Sono derivati di acidi grassi variamente
esterificati o amidati.
• Glicerofosfolipidi e sfingosidi
• Trigliceridi
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 134 -
67
Colesterolo
• Il colesterolo appartiene alla
famiglia degli steroidi,
H 3C
H3 C
• È un componente fondamentale
delle membrane biologiche,
H 3C
CH3
H
CH3
H
H
H
HO
• È il precursore nella sintesi
degli acidi biliari (acido colico,
acido taurocolico, acido
glicocolico) e della sintesi degli
ormoni steroidei (testosterone,
estradiolo, progesterone) e
della vitamina D3.
CH3
H
CH3
HO
H
H
H
CH3
CH3
CH3
H
• Viene sintetizzato
prevalentemente nelle cellule
epatiche a partire da acetilCoA.
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 135 -
Biosintesi del colesterolo
• Viene sintetizzato nelle cellule epatiche a partire da
acetil-CoA per formare 3-R-mevalonato.
O
H3C
S
CoA
H
S
O
S
CoA
CoA
S
H 3C
O
H3C
O
CoA
H
S
3-idrossi-3-metil
glutaril-CoA
HMG-CoA
CoA
OH
O
O
H3C
CoA
S
Tiolasi
O
Acetoacetil-CoA
I riduzione
II riduzione
NAPD+
NADPH + H+
O
OH
CH3
O
H
H
O
OH
NAPD+
OH
CH3
OH
S
H
CoA
Intermedio legato
all'enzima
3-R-mevalonato
H
B12 - v. 1.6.2 © gsartor 2001-2017
CoA
NADPH + H+
HMG-CoA reduttasi
O
S
CH3
HMG sintasi
Acetil-CoA (Cn)
O
S
CoA
Metabolismo dei grassi
- 136 -
68
HMG reduttasi EC 1.1.1.34
• È una glicoproteina di
membrana del reticolo
endoplamatico,
• Il suo peso molecolare è
di 97 kD,
• Il sito attivo è rivolto
verso il citoplasma.
• È anch’essa regolata dal
sistema protein chinasi.
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 137 -
HMG reduttasi EC 1.1.1.34
• È una glicoproteina di
membrana del reticolo
endoplamatico,
• Il suo peso molecolare è
di 97 kD,
• Il sito attivo è rivolto
verso il citoplasma.
• È anch’essa regolata dal
sistema protein chinasi.
HMG
CoA
NADP
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 138 -
69
HMG reduttasi EC 1.1.1.34
• Viene inibita dalle
statine, usate come
farmaci per ridurre
elevati livelli di
colesterolo.
Mevastatina
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 139 -
Controllo e regolazione della biosintesi del colesterolo
Ormone
(Adrenalina o glucagone)
Gα-GTP
Adenilato
ciclasi
(inattiva)
AMP
Adenilato ciclasi
(attiva)
ATP
Fosfodiesterasi
cAMP + PPi
HMG-CoA reduttasi
chinasi chinasi (inattiva)
HMG-CoA reduttasi
chinasi chinasi (attiva)
P
ATP
ADP HMG-CoA reduttasi
HMG-CoA reduttasi
chinasi (inattiva)
3-R-mevalonato
Pi
chinasi (attiva)
Fosfatasi
specifica
HMG-CoA
reduttasi
(attiva)
HMG-CoA
B12 - v. 1.6.2 © gsartor 2001-2017
Pi
Metabolismo dei grassi
P
ATP
ADP
Fosfatasi
specifica
HMG-CoA
reduttasi
(inattiva)
- 140 -
70
Biosintesi del colesterolo
• Il mevalonato viene convertito in squalene attraverso
l’allungamento con unità isoprenoidi.
O
OH
O
ADP + Pi + CO2
2ADP
2ATP
ATP
O
H
CH3
H
OH
3-R-mevalonato
Mevalonato
chinasi
Fosfomevalonato
chinasi
O
OH
H
H
CH3
O
O
P
O
P O
O
O
O
5-pirofosfo-3-R-mevalonato
Pirofosfomevalonato
carbossilasi
O
O
CH3 H
H2C
H
O
P
P O
O
O
O
Isopentenilpirofosfato
Isopentenilpirofosfato
isomerasi
Isopentenilpirofosfato
Pi
Isopentenilpirofosfato
Pi
CH3
O
O
CH3 H
H 3C
H
O
P
O
O
H3C
Geranilpirofosfato
CH3
CH3
H
O
H
O
P
O
O
P O
O
Dimetilallilpirofosfato
O
O
CH 3 H
H3 C
O
O
CH3 H
P O
O
P
O
O
NADPH + H+
P O
O
NAPD+ + 2Pi
Farnesilpirofosfato
CH3
Allungamento testa-coda
di unità isoprenoidi
CH3
CH 3
CH3
H3C
CH3
B12 - v. 1.6.2 © gsartor 2001-2017
CH3
CH3
Squalene
Metabolismo dei grassi
- 141 -
Biosintesi del colesterolo
• Lo squalene viene convertito in colesterolo attraverso
monossigenasi e ciclasi.
Squalene-2,3-epossido
Squalene
H3 C
CH3
H3 C
CH3
CH3
CH3
CH3
CH3
CH3
CH3
H 3C
CH3
CH3
Squalene
monossigenasi
O
CH3
H+
2,3-ossidosqualene
lanosterolo ciclasi
CH3
H3 C
CH3
CH3
H3 C
CH3
CH3
CH3
7-deidrocolesterolo
CH3
20 tappe
CH3
CH3
HO
CH3
H3 C
CH3
Lanosterolo
CH3
Molte
tappe
HO
H3 C
Colesterolo
H3 C
CH3
CH3
CH3
CH3
CH3
CH3
CH3
CH3
CH3
HO
HO
Desmosterolo
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 142 -
71
Destino del colesterolo
• Il colesterolo può:
– entrare nella costituzione delle membrane,
– essere convertito in esteri del colesterolo e trasportato dalle
lipoproteine alle cellule bersaglio
– essere sorgente per la sintesi degli ormoni steroidei e gli
acidi biliari.
H 3C
C o les te ro lo
C H3
CH3
IN C O R PO R A ZIO N E
N ELLE M EM B R A N E
CH3
ORMONI
ST ER O ID EI
CH3
CH3
ACIDI
B ILIAR I
HO
O
R
S
C oA
A c il- C o A c o le s t e ro lo
a c ilt ra n s fe ra s i
(A CA T)
H3C
C H3
CH3
CH3
CH3
LIP O PR O T EIN E
O
C H3
R
O
E s te r i d e l c o le s t e ro lo
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 143 -
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 144 -
72
Metabolismo dei grassi
1. Demolizione dei trigliceridi
2. Catabolismo degli acidi grassi
3. Biosintesi
– degli acidi grassi e colesterolo
– dei lipidi complessi
4. Trasporto dei lipidi
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 145 -
Lipidi
• Semplici
– Sono molecole che non contengono legami
esterei o amidici
• Agidi grassi
• Colesterolo
• Complessi
– Sono derivati di acidi grassi variamente
esterificati o amidati.
• Glicerofosfolipidi e sfingosidi
• Trigliceridi
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 146 -
73
Glicerofosfolipidi
• Sono esteri di acidi grassi e glicerolo
R OH
R O
O
+
R'
O
CH2OH
HO
R'
O
+ H2O
O
H
+
CH2OH O
CH2OH
HO
H
C
H2
B12 - v. 1.6.2 © gsartor 2001-2017
O
O
+ H2O
Metabolismo dei grassi
- 147 -
Acido fosfatidico
• È il prototipo dei fosfolipidi,
• Si ottiene per esterificazione del glicerolo con due catene di
acidi grassi (in C1 e C2) e di acido fosforico (in C3):
O
P
O
3
O
O
O
2
H3C
O
H 3C
1
O
O
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 148 -
74
Biosintesi dell’acido fosfatidico
Diidrossiacetonfosfato
• L’acido fosfatidico viene
sintetizzato a partire da
glicerolo-3-P e acil-ACP.
• Negli eucarioti la
sorgente è il
diidrossiacetonfosfato
Glicerolo-3-fosfato
NADH + H+
OH
NAD+
Glicerolo-3-fosfato
deidrogenasi
O
P
Diidrossiaceton
fosfato
aciltransferasi
CoA
R
O
O
R
o
S
CoA R
Glicerolo-3-fosfato
aciltransferasi
o
H S
CoA
H S
CoA
O
NADPH + H+
O
OH
O
O
O
S
S
ACP
H S
ACP
O
NAPD+
O
R
R
O
OH
Acil-diidrossiaceton
fosfato reduttasi
O
P
OH
OH
Glicerolo
chinasi
O
O P
O
O
O
ATP
OH
O
O
Glicerolo
ADP
OH
1-acil-glicerolo-3-fosfato
O
O
O
O
P
O
O
1-acil-diidrossiacetonfosfato
o
O
O
S
S
1-acilglicerolo
aciltransferasi
CoA
R
R
o
H S
CoA
ACP
H S
ACP
O
O
R
O
Acido fosfatidico
O
R
O
O
P
O
B12 - v. 1.6.2 © gsartor 2001-2017
O
Metabolismo dei grassi
- 149 -
Fosfolipidi
• Nei fosfolipidi la funzione acida libera del
gruppo fosfato è esterificata con un alcool:
– Colina
HO
N
+
CH3
CH3
O
H3C
– Serina
O
O
HO
NH2
– Etanolamina
R
HO
– Inositolo
O
3
O
O
2
+
NH3
– Glicerolo
P
O
O
1
O
CH2OH
HO
H
H2C
OH
CH3
CH3
O
OH
OH
OH
OH
OH
OH
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 150 -
75
Fosfatidilcolina
• Un esempio di glicerofosfolipide molto
presente nelle membrane biologiche è la
fosfatidilcolina dove la funzione acida libera
del gruppo fosfato è esterificata con la colina.
O
P
O
H3C
CH
CH3 3
N
+
O
3
O
O
2
CH3
O
1
CH3
O
O
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 151 -
Biosintesi di fosfolipidi
O O
• Negli eucarioti i
trigliceridi e i fosfolipidi
provengono dall’acido
fosfatidico.
• Il legame degli
aminoalcoli al
diacilglicerolo viene
effettuato attivando gli
aminoalcoli fosforilati con
Citidina trifosfato (CTP).
• I triacilgliceroli si
formano dal
diacilglicerolo per
trasferimento di un acile
dal acil-CoA.
Etanolamina
O
Colina
P
Acido fosfatidico
+
NH3
Etanolamina
chinasi
O
O
ADP
R
P
ADP
P
O
H2O
O O
Acido fosfatidico
fosfatasi
Pi
CTP:fosfocolina
citidiltransferasi
NH3
CTP
PPi
ADP
Diacilglicerolo
chinasi
ATP
CTP:fosfoetanolamina
citidiltransferasi
N
+
P
O
PPi
O
CDPetanolamina
O
+
NH3
P
CDP-colina
1,2,-diacilglicerolo
fosfocolina
transferasi
O
CMP
S
CoA
O
H S
R
O
O
O
O
O
O
R
O
CH3
CH3
O
O
O
R
R
O
R
O
R
Fosfatidilcolina
R
Metabolismo dei grassi
+
N
P
O
CoA
O
CH3
O O
Diacilglicerolo
aciltransferasi
O
O
CH3
CH3
Diacilgliecrolo
R
O O
+
CDPcolina
R
O
N
O O
R
CDP-etanolamina
1,2,-diacilglicerolo
fosfoetanolamina
transferasi
CMP
CH3
P
O
O
O O
CH3
CH3
O
Citidina
O
NH3
+
CTP
OH
O
Citidina
CH3
CH 3
ATP
Fosfocolina
O
CH3
R
+
O O
+
Colina
chinasi
O
Fosfoetanolamina
O
Fosfatidiletanolamina
B12 - v. 1.6.2 © gsartor 2001-2017
N
O
ATP
O
CH 3
HO
O
HO
Triacilgliecrolo
- 152 -
76
Biosintesi di fosfatidilserina
• Nei mammiferi la sintesi
di fosfatidilserina avviene
attraverso la scambio
con etanolamina.
O O
O
+
NH3
P
O
Fosfatidiletanolamina
O
O
O
CO2
R
O
R
O
O
HO
O
HO
Fosfatidilserina
decarbossilasi
(mitocondri)
O
NH3+
NH3+
Enzima di scambio
delle basi
(reticolo endoplasmatico)
HO
HO
NH3+
NH3+
O O
O
O
P
O H3N
+
O
O
O
O
Fosfatidilserina
R
O
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
R
- 153 -
Metabolismo dei grassi
1. Demolizione dei trigliceridi
2. Catabolismo degli acidi grassi
3. Biosintesi
– degli acidi grassi e colesterolo
– dei lipidi complessi
4. Trasporto dei lipidi
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 154 -
77
Complessi lipoproteici
• I lipidi circolano negli organismi sottoforma di complessi
lipoproteici:
• Gli acidi grassi sono coniugati con l’albumina
• I triacilgliceroli, i fosfolipidi, il colesterolo ed i suoi esteri
sono trasportati come lipoproteine.
Densità
(g/ml)
Diametro
(nm)
HDL (High Density Lipoprotein)
1.063-1.210
5-15
LDL (Low Density Lipoprotein)
1.019-1.063
18-28
IDL (Intermediate Density
Lipoprotein)
1.006-1.019
25-50
VLDL (Very Low Density Lipoprotein)
0.950-1.006
30-80
Chilomicroni
< 0.950
100-500
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 155 -
Complessi lipoproteici
• I lipidi circolano negli organismi sottoforma di complessi
lipoproteici:
• Gli acidi grassi sono coniugati con l’albumina
• I triacilgliceroli, i fosfolipidi, il colesterolo ed i suoi esteri
sono trasportati come lipoproteine.
Proteine
Colesterolo
Fosfolipidi
Triacilgliceroli
HDL (High Density
Lipoprotein)
LDL (Low Density
Lipoprotein)
IDL (Intermediate
Density Lipoprotein)
VLDL (Very Low Density
Lipoprotein)
Chilomicroni
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 156 -
78
Complessi lipoproteici
• Le lipoproteine vengono sintetizzate nel fegato e
nell’intestino (chilomicroni).
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 157 -
Complessi lipoproteici
• Le lipoproteine vengono sintetizzate nel fegato e
nell’intestino (chilomicroni).
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 158 -
79
Complessi lipoproteici
Apoproteina
PM
A-1
28.000
A-2
8.700
Concentrazione
nel plasma
(mg/100ml)
90-120
30-50
Distribuzione
Proteina principale nelle HDL
Si trova come dimero nelle
HDL
B-48
240.000
<5
B-100
500.000
80-100
Proteina principale nelle LDL
Solo nei chilomicroni
C-1
7.000
4-7
Nei chilomicroni, VLDL, IDL,
HDL
C-2
8.800
3-8
Nei chilomicroni, VLDL, IDL,
HDL
C-3
8.800
8-15
Nei chilomicroni, VLDL, IDL,
HDL
D
32.500
8-10
Nelle HDL
E
34.100
3-6
B12 - v. 1.6.2 © gsartor 2001-2017
Nei chilomicroni, VLDL, IDL,
HDL
Metabolismo dei grassi
- 159 -
Complessi lipoproteici
• La sintesi delle
apoproteine, dei
fosfolipidi, del
triacilglicerolo, del
colesterolo e dei suoi
esteri avviene nel
reticolo
endoplasmatico,
• L’assemblaggio dei
componenti nelle
prelipoproteine
avviene nel RE e
queste vengono
trasferite nel Golgi.
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 160 -
80
Complessi lipoproteici
• Nel Golgi alle
preliproproteine
vengono aggiunti i
fosfolipidi e, forse,
gli esteri del
colesterolo.
• Le vescicole di
secrezione
contenenti le
lipoproteine
migrano verso la
membrana
plasmatica dove
• Si fondono con essa
e rilasciano nel
circolo le
lipoproteine.
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 161 -
Produzione e rilascio
• Le lipoproteine
circolanti vengono
internalizzate dalle
cellule bersaglio.
• Esse vengono
riconosciute da uno
specifico recettore
(Low Density
Lipoprotein
Receptor) che media
il processo.
B12 - v. 1.6.2 © gsartor 2001-2017
Metabolismo dei grassi
- 162 -
81
Crediti e autorizzazioni all’utilizzo
• Questo materiale è stato assemblato da informazioni raccolte dai seguenti testi di Biochimica:
– CHAMPE Pamela , HARVEY Richard , FERRIER Denise R. LE BASI DELLA BIOCHIMICA [ISBN 9788808-17030-9] – Zanichelli
– NELSON David L. , COX Michael M. I PRINCIPI DI BIOCHIMICA DI LEHNINGER - Zanichelli
– GARRETT Reginald H., GRISHAM Charles M. BIOCHIMICA con aspetti molecolari della Biologia
cellulare - Zanichelli
– VOET Donald , VOET Judith G , PRATT Charlotte W FONDAMENTI DI BIOCHIMICA [ISBN 9788808-06879-8] - Zanichelli
• E dalla
–
–
–
–
consultazione di svariate risorse in rete, tra le quali:
Kegg: Kyoto Encyclopedia of Genes and Genomes http://www.genome.ad.jp/kegg/
Brenda: http://www.brenda.uni-koeln.de/
Protein Data Bank: http://www.rcsb.org/pdb/
Rensselaer Polytechnic Institute:
http://www.rpi.edu/dept/bcbp/molbiochem/MBWeb/mb1/MB1index.html
• Il materiale è stato inoltre rivisto e corretto dalla Prof. Giancarla Orlandini dell’Università di Parma alla
quale va il mio sentito ringraziamento.
Questo ed altro materiale può essere reperito a partire da: http://www. gsartor.org/pro
• Il materiale di questa presentazione è di libero uso per didattica e ricerca e può essere usato senza
limitazione, purché venga riconosciuto l’autore usando questa frase:
Materiale ottenuto dal Prof. Giorgio Sartor
Università di Bologna
Giorgio Sartor
Ufficiale: [email protected]
Personale: [email protected]
Aggiornato il 11/04/2017 10:15:50
82