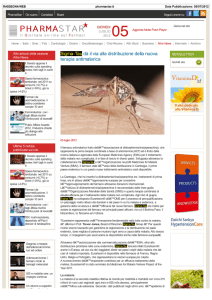
MEDIA COVERAGE
Eurartesim® (diidroartemisinina/piperachina):
dopo la distribuzione in Cambogia, al via l’autorizzazione
anche nei paesi africani: Ghana, Tanzania e Burkina Faso.
Comunicato stampa del 24 aprile 2013
Aggiornato al 29 aprile 2013
COMUNICATO STAMPA
GIORNATA MONDIALE CONTRO LA MALARIA
Eurartesim® (diidroartemisinina/piperachina):
dopo la distribuzione in Cambogia, al via l’autorizzazione
anche nei paesi africani: Ghana, Tanzania e Burkina Faso.
La Cambogia è il primo paese endemico in cui è stata avviata la distribuzione di Eurartesim®, la nuova terapia
antimalarica combinata a base di diidroartemisinina/piperachina.
Eurartesim® è stato da poco autorizzato anche in Ghana, primo paese africano a registrare il farmaco, in
Tanzania e in Burkina Faso.
Eurartesim® è frutto della collaborazione tra l’italiana Sigma-Tau e l’organizzazione no-profit Medicines for
Malaria Venture (MMV).
La malaria è la seconda malattia infettiva al mondo per morbilità e mortalità con circa 215 milioni di nuovi casi
registrati ogni anno e 655 mila decessi, principalmente nell’Africa sub-sahariana.
Roma, 24 aprile 2013 – Eurartesim® (diidroartemisinina/piperachina) terapia combinata a base di
artemisinina (ACT), frutto della ricerca italiana e già distribuito in Cambogia, primo paese endemico in
cui questo nuovo trattamento antimalarico è stato inserito tra i trattamenti di prima linea, è stato
recentemente autorizzato anche in altri Paesi endemici. Il Ghana è infatti il primo paese in Africa ad
aver approvato Eurartesim® per il trattamento della malaria non complicata.
La buona notizia arriva proprio in occasione della Giornata Mondiale contro la Malaria che si
celebrerà in tutto il mondo domani 25 aprile. Si tratta di una pietra miliare per il trattamento della
malaria in Africa. L’avvenuta registrazione in Ghana renderà ora il farmaco disponibile anche per i
pazienti africani. Sigma-Tau ha inoltre avviato e ottenuto la registrazione del farmaco anche in altri
paesi africani: Burkina Faso e Tanzania.
Eurartesim®, raccomandato dalle linee guida dell’Organizzazione Mondiale della Sanità (OMS) e
sviluppato attraverso la collaborazione tra Sigma-Tau e l’organizzazione no-profit Medicines for
Malaria Venture (MMV), è stato approvato dalla European Medicines Agency (EMA) nel 2011.
Questa registrazione ha permesso, inoltre, l'uso di Eurartesim® all'interno del programma INESS
Fase IV (di cui fanno parte il Ghana, il Burkina Faso, il Mozambico e la Tanzania), che raccoglie dati
sulla sicurezza ed efficacia di nuove ACT e condivide le informazioni con altri paesi in cui la malaria è
endemica. Questi dati indicheranno progressivamente come utilizzare al meglio il farmaco anche in
vista delle ulteriori registrazioni nei paesi INESS.
La malaria
La malaria è la seconda malattia infettiva al mondo per morbilità e mortalità con circa 215 milioni di nuovi casi
registrati ogni anno e 655 mila decessi, principalmente nell’Africa sub-sahariana. Secondo i dati pubblicati negli
ultimi anni, l’epidemia di malaria continua a espandersi in tutto il mondo, complici i cambiamenti climatici che
stanno facendo sviluppare le zone in cui la zanzara vettore può vivere e infettare le persone. Più del 40% della
popolazione mondiale rischia di essere contagiata dal morbo e, anche se il 90% dei casi si registra in Africa, la
nuova frontiera della patologia è il Sud Est Asiatico, dove l’83% della popolazione (oltre 1 miliardo e 300 milioni
di persone) è a rischio. Secondo i dati dell’Organizzazione Mondiale della Sanità, la malaria è una delle 3
malattie più diffuse in Africa insieme all’HIV/Aids e alla tubercolosi ed è la principale causa di morte nei bambini
sotto i 5 anni (si stima che, a causa di questa malattia, ogni 45 secondi muoia un bambino).
PRESS RELEASE
WORLD MALARIA DAY
Eurartesim® (diidroartemisinina/piperachina):
Following distribution accords in Cambodia, authorizations also in African
nations: Ghana, Tanzania & Burkina Faso.
Cambodia is the first endemic nation where distribution of Eurartesim®, the new dihydroartemisininpiperaquine based antimalarial therapy has begun.
Eurartesim® has been recently authorized in Ghana, the first African country to register the drug. Tanzania
and Burkina Faso have also registered.
Eurartesim® is the result of a collaboration between Italian Pharma company Sigma-Tau and the NGO,
Medicines for Malaria Venture (MMV).
Malaria is the second most infectious disease and cause of death globally with about 215 million new cases
registered every year and 655 thousand deaths, mainly in sub-Saharan Africa.
Rome, 24 April 2013 – The result of Italian research, Eurartesim® a high-quality, (dihydroartemisininpiperaquine) therapy based on artemisinin (ACT) is already being distributed in Cambodia, the first
endemic country to use Eurartesim® as a first line of defence and treatment. The drug has recently
been authorized also in other endemic countries. Ghana is the first African nation to have approved
Eurartesim® for the treatment of uncomplicated malaria.
The good news is to be announced on World Malaria day, that is celebrated across the world
tomorrow, the 25th of April. This is a historical landmark event for treatment of malaria in Africa. The
registration of Eurartesim® in Ghana will make it available also to African patients. Sigma-Tau has
also started and obtained registration of the drug in other African nations like Burkina Faso and
Tanzania.
Eurartesim®, is recommended in World Health organization guidelines (WHO) and developed in
collaboration between Sigma-Tau and the non-profit organization Medicines for Malaria Venture
(MMV). The drug has also been approved by the European Medicines Agency (EMA) in 2011.
The registration has allowed the use of the drug in the Phase IV INESS program (that includes Ghana,
Burkina Faso, Mozambique and Tanzania), that gathers data on the safety and effectiveness of new
ACTs and shares the information with other malaria-endemic countries. The data will gradually
indicate how to improve the use of the drug as it achieves endorsement and is registered among the
other INESS countries.
Malaria
Malaria is the second most infective disease in the world in terms of mortality and infection rates with over 215
million new cases registered annually and 655 thousand deaths, mainly in Sub-Saharan Africa. According to
data released in recent years the malaria epidemic is continuing to expand worldwide also as a result of climate
change which is leading to the expansion of areas where the vector mosquitoes can live and infect people. Over
40% of the world’s population is at risk of infection and, although 90% of cases occur in Africa, the new frontier
of the disease is South East Asia where 83% of the population (over 1.3 billion people) is at risk. According to
the World Health Organization, together with HIV/AIDS and tuberculosis, malaria is one of the 3 most
widespread diseases in Africa and the leading cause of death in children under 5 (the disease is estimated to kill
a young child every 45 seconds). In Europe autochthonous cases are rare. These are largely cases of people
accidentally bitten by infective mosquitoes carried by air carriers. Much larger is the number of cases of imported
malaria, i.e. of travelers infected in countries where malaria is endemic. In particular, since the year 2000,
France is the country most affected by malaria with 56,638 cases, followed by the United Kingdom with 20,809
cases, Italy with 5,881, Belgium with 2,882 and Portugal with 563 cases.1
Eurartesim®
Eurartesim® is a combined therapy drug (ACT - Artemisinin-based Combination Therapy) based on
dihydroartemisinin-piperaquine (DHA-PQP) that has proven its effectiveness in treating uncomplicated malaria
caused by Plasmodium Falciparum in adults and children. The molecule meets the standards of the WHO
recommendations, which endorse the concept of associating two active ingredients in a unique pill: the
derivative of Artemisinin with high antimalarial ability (Dihydroartemisinin) and a second anti-malarial ingredient
(Piperaquine) that guarantees protection against any eventual resistance. Clinical testing has shown that
Eurartesim® guarantees a high percentage of success rate and cure, higher than 95% and a better as well as
longer protection from new malaria infections. With a reduction of 50% of new infection rates in the two months
after treatment compared to other ACTs. Besides, Eurartesim® also allows a simpler dosage regimen (1 daily
dose for three days).
The approval of the drug by the EMA is based on the results of a series of large scale clinical trials carried out to
assess the security and effectiveness of the new ACT compared to artemether/lumefantrine
and
artesunate/mefloquine. The clinical studies involved 2.700 patients in Africa (Burkina Faso, Zambia, Kenya,
Mozambique & Uganda), in Asia (Thailand, India & Laos), including about 1.036 African children between the
age of 6 months and ten years of age, all having uncomplicated P. falciparum malaria and treated with the
dihydroartemisinin-piperaquine combination
Sigma-Tau
Sigma-Tau is a leading, all Italian capital, International pharmaceutical Group, founded in 1957, that invests in
the research, development and marketing of innovative and effective treatments to improve human well-being
and quality of life. Sigma-Tau Group has headquarters in Pomezia (Rome, Italy), and subsidiaries in France,
Switzerland, the Netherlands, Belgium, Portugal, Germany, UK, India, along with production plants in Italy, Spain
and US (Indianapolis); with about 2000 employees and an extensive network of licensees worldwide achieved a
global turnover of € 688 million in 2012.
The Sigma-Tau Group has invested and continues to invest a significant share of its revenues in R&D with a
view to identify innovative therapies and cures for those having to deal with rare diseases and/or diseases that
have high clinical or social impact. Sigma-Tau’s R&D efforts are mainly directed towards rare and neglected
diseases, oncology, immuno-oncology, and biotechnology, and more specifically towards the study and
development of technological platforms for specific, innovative therapies and radioimmunotherapy of tumors, as
well as product line extensions.
Web Site: www.sigma-tau.it
For more information:
Head of Communication and Information Sigma-Tau
Bruno Chiavazzo
Phone. 06 91394181
e-mail: bruno.chiavazzo@sigma-tau
1
World Health Organization (http://data.euro.who.int/CISID/), dati 2000-2011. Per la Francia i dati sono disponibili solo fino al
2010, per l’Italia solo fino al 2007 e per il Portogallo solo fino al 2009.
In Europa i casi autoctoni sono rari. Per lo più si tratta di persone punte accidentalmente da zanzare infette,
trasportate da vettori aerei. Molto più esteso è il numero di casi di malaria importata, ovvero di persone infettate
nel corso di viaggi nei paesi in cui la malaria è endemica. Nello specifico, dal 2000 ad oggi, la Francia è stata la
nazione più colpita con 56.638 casi, seguita dal Regno Unito con 20.809, dall’Italia con 5.881, dal Belgio con
2.882 e dal Portogallo con 562 casi1.
Eurartesim®
Eurartesim® è una terapia combinata (ACT - Artemisinin-based Combination Therapy) composta da
diidroartemisinina/piperachina, che si è dimostrata altamente efficace nel trattamento della malaria non
complicata causata da Plasmodium Falciparum negli adulti e nei bambini. La molecola risponde infatti alle
raccomandazioni dall’OMS, che promuovono l’associazione nella stessa compressa di due principi attivi: il
derivato dell’artemisinina ad altissima attività antimalarica (diidroartemisinina) e un secondo antimalarico
(piperachina) che garantisce la protezione da eventuali resistenze. Studi clinici hanno dimostrato che
Eurartesim® garantisce un'alta percentuale di guarigione, superiore al 95%, e una protezione migliore e di più
lunga durata nei confronti delle nuove infezioni, con una riduzione di circa il 50% del numero di nuove infezioni
nei due mesi dopo il trattamento rispetto alle altre ACT. Eurartesim® offre inoltre il vantaggio di un facile regime
di somministrazione (1 dose al giorno per 3 giorni).
L’approvazione del farmaco da parte dell’EMA si basa sui risultati di una serie di studi clinici su larga scala che
hanno avuto l’obiettivo di valutare la sicurezza e l’efficacia della nuova ACT rispetto all’artemeter/lumefantrina e
all’artesunato/meflochina. Gli studi hanno coinvolto più di 2.700 pazienti in Africa (Burkina Faso, Zambia, Kenya,
Mozambico e Uganda) e in Asia (Thailandia, India e Laos), compresi circa 1.036 bambini africani tra i 6 mesi e i
10 anni di età, tutti con malaria non complicata da P. falciparum e trattati con la combinazione
diidroartemisinina/piperachina.
Sigma-Tau
Il Gruppo Sigma-Tau, fondato nel 1957, rappresenta una delle più importanti realtà farmaceutiche internazionali
a capitale interamente italiano. È da sempre impegnato nella ricerca, nello sviluppo e nella commercializzazione
di farmaci innovativi per migliorare il benessere e la qualità della vita dell’uomo.
Il Gruppo Sigma-Tau ha sede centrale a Pomezia (Roma) e filiali in Francia, Svizzera, Belgio, Olanda,
Portogallo, Germania, Regno Unito, India, con stabilimenti produttivi oltre che in Italia, in Spagna e negli Stati
Uniti (Indianapolis); con oltre 2.000 dipendenti e un crescente network di licenziatari a livello mondiale nel 2012
ha raggiunto un fatturato di 688 milioni di euro. Il Gruppo Sigma-Tau ha investito e continua ad investire una
quota significativa del proprio fatturato nella Ricerca e Sviluppo al fine di identificare terapie innovative per offrire
un'opportunità di cura a chi deve affrontare malattie poco diffuse e/o ad elevato impatto clinico e sociale.
L’impegno della R&S Sigma-Tau è principalmente dedicato alle patologie rare e neglette e all’immunooncologia/biotech, in particolare allo studio e lo sviluppo di piattaforme tecnologiche proprietarie volte a terapie
mirate innovative e alla radioimmunoterapia dei tumori, nonché alle estensioni di linea.
Sito web: www.sigma-tau.it
Per maggiori informazioni:
Responsabile comunicazione e informazione Sigma-Tau
Bruno Chiavazzo
Tel. 06 91394181
e-mail: bruno.chiavazzo@sigma-tau
1
World Health Organization (http://data.euro.who.int/CISID/), dati 2000-2011. Per la Francia i dati sono disponibili solo fino al
2010, per l’Italia solo fino al 2007 e per il Portogallo solo fino al 2009.
Web
Data
Testata
Titolo
24/04/13
Il farmacista online.it
Malaria. Ok a Eurartesim in
Ghana, Tanzania e Burkina
Faso
24/04/13
Quotidiano Sanità.it
Malaria. Al via
autorizzazione di Eurartesim
in Ghana, Tanzania e
Burkina Faso
Data
Testata
Titolo
29/04/13
Adnkronos Salute
Anti-malaria Sigma Tau in
Ghana, Tanzania e Burkina
Faso
06/05/13
Panorama della Sanità
Eurartesim: al via
l'autorizzazione anche in
Ghana, Tanzania e Burkina
Faso.
01/06/13
About Pharma
Dagli stop giudizionari in
Europa e Italia alla farmacia
etica
Quotidiani/Periodici
Sigma Tau
033184
www.ecostampa.it
Sigma Tau
033184
www.ecostampa.it
Sigma Tau
033184
www.ecostampa.it
Lettori: n.d.
Panorama della Sanità
06-MAG-2013
da pag. 10
Diffusione: n.d.
SIGMATAU
1
033184
www.ecostampa.it
Mensile
Sigma Tau
033184
www.ecostampa.it
Mensile
Sigma Tau
033184
www.ecostampa.it
Mensile
Sigma Tau
033184
www.ecostampa.it
Mensile
Sigma Tau