Foglio di
informazione
professionale
Nr. 145
29 agosto 2005
Uso crescente di antidepressivi negli adolescenti: segno (allarmante) dei tempi?
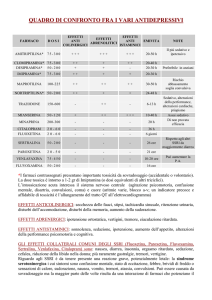
Il 21 aprile 2005, l’Agenzia Europea dei Medicinali (EMEA) ha controindicato nei minori di 18 anni l’uso
degli antidepressivi citalopram (es. Elopram), duloxetina (es. Yentreve), escitalopram (es. Cipralex),
fluoxetina (es. Prozac), fluvoxamina (es. Maveral), mianserina (Lantanon), mirtazapina (Remeron),
reboxetina (es. Edronax), sertralina (es. Zoloft) e venlafaxina (Efexor) per il rischio di comportamenti
correlati al suicidio e ostilità (aggressività, comportamento oppositivo e rabbia). Sono rimaste escluse le
indicazioni approvate in tali fasce di età (in Italia, il trattamento del disturbo ossessivo compulsivo per
sertralina e fluvoxamina, rispettivamente dai 6 e 8 anni in poi).
Con questo provvedimento si conclude (definitivamente?) una vicenda che ha avuto inizio 2 anni fa e che ha
suscitato preoccupazione e scalpore. Dalla metà del 2003, gli antidepressivi, soprattutto gli inibitori selettivi
della ricaptazione della serotonina (SSRI), sono al centro di un acceso dibattito che ha riguardato la loro
efficacia e i loro effetti indesiderati.
Per molto tempo, i problemi di tipo psichiatrico dei bambini e degli adolescenti sono stati gestiti con
interventi di tipo psicologico e sociale, facendo ricorso ai farmaci solo occasionalmente, nei casi più difficili.
Negli ultimi 5 anni le prescrizioni di antidepressivi in età pediatrica hanno fatto registrare un incremento
generalizzato: +100% in Canada, +150% in USA, +280% in Italia, con una prevalenza d’uso molto alta nei
primi due paesi (18 per mille), meno marcata in Italia (3 per mille). Ovunque, gli SSRI sono al vertice delle
classifiche. Durante il 2002, 1.600 ragazzi italiani hanno ricevuto un antidepressivo: il 71% un SSRI, in
particolare paroxetina, sertralina e citalopram, il 15% antidepressivi triciclici, il 4% triciclici più SSRI e il
10% trazodone o venlafaxina. Nei bambini dai 6 ai 13 anni, la prevalenza d’impiego è risultata più alta nei
maschi, nell’adolescenza maggiore nelle femmine; in più della metà dei casi, si è trattato di farmaci non
registrati per uso pediatrico o con limitazioni di età.
Efficacia
Tra i vari problemi di tipo psichiatrico del bambino nei quali gli SSRI sono stati impiegati (ansia, disturbo da
deficit di attenzione/iperattività, depressione) solo per il disturbo ossessivo compulsivo esistono adeguate
evidenze di beneficio. Per quanto riguarda, invece, il trattamento della depressione, ad oggi non è dimostrata
l’utilità di alcun antidepressivo, indipendentemente dalla classe terapeutica di appartenenza. Una revisione
sistematica della Cochrane non ha rilevato differenze significative tra antidepressivi triciclici e placebo,
mentre i 5 studi controllati, randomizzati, pubblicati, che hanno documentato una maggiore efficacia di
fluoxetina, paroxetina, sertralina e citalopram rispetto al placebo sono stati criticati per la metodologia, le
misure di esito adottate e la rilevanza clinica degli effetti misurati, e due studi sono stati considerati
arbitrariamente positivi dagli autori pur in assenza di dati indicanti una superiorità nei confronti del placebo.
La stima della reale efficacia di questi farmaci è stata, inoltre, viziata dal cosiddetto “bias di pubblicazione”,
il principio in base al quale chi è proprietario dei dati delle ricerche (le ditte produttrici) decide in piena
autonomia se pubblicarli o meno. Gli studi con esito negativo hanno, quindi, poche probabilità di essere
pubblicati: nel caso degli antidepressivi, ben 9 studi non “hanno visto la luce”. Dei 15 studi sul trattamento
della depressione valutati recentemente dalla Food and Drug Administration (FDA), l’ente regolatorio
americano, 12 non hanno evidenziato differenze statisticamente significative nell’efficacia
dell’antidepressivo rispetto al placebo. Di questi, solo 2 sono stati pubblicati: uno riguardante la venlafaxina
e uno la sertralina, ma “aggregando” i dati di un altro studio.
INTESA – Via Provina, 3 – 38040 Ravina (TN) – Tel. 0461 901111
Sicurezza
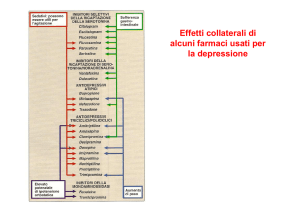
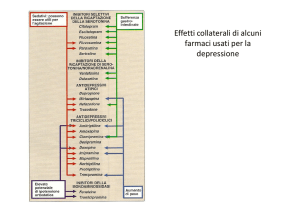
Sulla base di quanto era stato sinora pubblicato, gli effetti indesiderati più comuni degli SSRI non
sembravano diversi da quelli osservati negli adulti (cefalea, disturbi gastrointestinali, insonnia). Va detto,
però, che la breve durata degli studi (8-10 settimane) e il ridotto numero di pazienti arruolati non consentono
di rilevare gli eventi avversi gravi ma poco frequenti, come il suicidio; inoltre l’obiettivo principale degli
studi è la valutazione dell’efficacia e viene data scarsa importanza al monitoraggio e alla segnalazione delle
reazioni avverse. Per esempio, nello studio pubblicato sulla paroxetina, 11 adolescenti su 93 avevano sospeso
il farmaco per “gravi” effetti indesiderati di tipo psichiatrico, il più comune dei quali veniva descritto come
”labilità emotiva”. Questa reazione, successivamente definita “ideazione suicidaria, ostilità,
aggressività…..”, ha richiesto il ricovero in ospedale del 7,5% dei ragazzi con depressione lieve trattati con
paroxetina (contro nessuno trattato con placebo), ma è stata completamente ignorata nella discussione finale
dei risultati. Il protocollo dello studio sulla sertralina non prevedeva, addirittura, la registrazione dei possibili
eventi avversi e il farmaco è stato descritto come “ben tollerato”.
Nel dicembre dello scorso anno, il Committe on Safety of Medicines (CSM) inglese, in una revisione degli
studi sull’impiego di 8 antidepressivi di nuova generazione (citalopram, escitalopram, fluoxetina,
fluvoxamina, mirtazapina, paroxetina, sertralina e venlafaxina) nel trattamento della depressione in bambini
e adolescenti, aveva concluso che il bilancio rischi/benefici di questi farmaci era sfavorevole e ne aveva
controindicato l’uso sotto i 18 anni. Una valutazione dell’associazione tra uso di antidepressivi e rischio di
suicidio è stata effettuata in seguito anche dalla FDA, che ha analizzato i dati di 24 studi clinici condotti tra il
1983 e il 2001 sull’uso in bambini e adolescenti di 9 antidepressivi (quelli presi in considerazione dal CSM
più nefazodone), documentando un aumento del rischio di suicidio o di ideazioni suicide. In nessuno dei
singoli studi il rischio relativo di suicidio era aumentato in maniera statisticamente significativa, ma
aggregando i dati, è risultato pari a 1,78; ciò significa che i ragazzi che vengono trattati con questi
antidepressivi corrono un rischio quasi doppio di suicidio rispetto a quelli che non li assumono. La revisione
della FDA ha evidenziato anche un aumentato rischio di aggressività e agitazione psicomotoria. Un dato
coerente con quanto osservato in un’analisi delle cartelle cliniche di 82 bambini e adolescenti trattati con
SSRI che ha stimato nel 22% l’incidenza di effetti indesiderati di tipo psichiatrico.
Su questi farmaci ci sono, inoltre, scarse informazioni sugli esiti a lungo termine. Mancano, ad esempio, dati
di follow-up sullo sviluppo cognitivo e neurocomportamentale, mentre sia gli studi clinici che singole
segnalazioni indicano un rallentamento della crescita in bambini trattati con SSRI (presumibilmente dovuto a
una ridotta secrezione di ormone somatotropo), reversibile alla sospensione del trattamento. Risultano,
inoltre, poco indagati gli effetti a livello dell’attività sessuale: negli adulti che assumono SSRI, l’incidenza di
disturbi è del 30%-40%, mentre gli studi sull’impiego di questi farmaci nei bambini e adolescenti riportano
un solo caso. L’analisi retrospettiva delle cartelle cliniche di 22 adolescenti in terapia con SSRI ha, però,
evidenziato in 5 pazienti (23%) la comparsa di anorgasmia o diminuzione della libido. Non è possibile,
infine, valutare se l’assunzione di antidepressivi in soggetti prepuberi o durante l’adolescenza possa
interferire con l’attività sessuale da adulti.
Conclusioni
Ad oggi, il profilo beneficio/rischio degli antidepressivi impiegati nei bambini e negli adolescenti resta
ancora da definire. Il dibattito sull’uso degli antidepressivi in età pediatrica va al di là della loro efficacia e
sicurezza e tocca problemi che ci riguardano da vicino. La mancata pubblicazione degli studi negativi
sottolinea l’improrogabilità di creare dei registri di studi clinici e la necessità di rendere trasparenti i risultati
della sperimentazioni. Il fatto che i possibili rischi associati all’uso di paroxetina siano stati sollevati grazie
alle segnalazioni giunte alla trasmissione “Panorama” della BBC inglese sottolinea, inoltre, i limiti degli
attuali sistemi di farmacovigilanza e mette a nudo, ancora una volta, la scarsa attenzione e sensibilità delle
autorità regolatorie che si occupano (o dovrebbero occuparsi) di tutelare la salute pubblica.
A cura del dott. Mauro Miselli
Bibliografia
- Clavenna A. e Bonati M. Antidepressivi in età pediatrica: molte ombre, poche evidenze. Rivista Sperimentale di Freniatria 2004;
CXXVII:81-94.
- Hazel P. et al. Tricyclic drugs for depression in children and adolescent (Cochrane Review). Cochrane Library, Issue 2, 2004.
- Jureidini J.N. et al. Efficacy and safety of antidepressants for children and adolescents. BMJ 2004; 328:879-83.
- Whittington C.J. et al. SSRIs in childhood depression: systematic review of published versus unpublished data. Lancet 2004;
363:1335; 1341-5.
- Antidepressant medications in children and adolescents. Therapeutics Letter 2004; 52:1-4.
INTESA – Via Provina, 3 – 38040 Ravina (TN) – Tel. 0461 901111